Атлас по физиологии. В двух томах. Том 1: учеб. пособие / А. Г. Камкин, И. С. Киселева - 2010. - 408 с. : ил.
|
|
|
|
Глава 2. Вторичные мессенджеры
Общие представления о путях сигнальной трансдукции
Для большинства регуляторных молекул между их связыванием с мембранным рецептором и окончательной реакцией клетки, т.е. изменением ее работы, вклиниваются сложные серии событий - определенные пути передачи сигнала, иначе называемые путями сигнальной трансдукции.
Регуляторные вещества принято подразделять на эндокринные, нейрокринные и паракринные. Эндокринные регуляторы (гормоны) выделяются эндокринными клетками в кровь и переносятся ею к клеткам-мишеням, которые могут находиться в любом месте организма. Нейрокринные регуляторы выделяются нейронами в непосредственной близости от клеток-мишеней. Паракринные вещества освобождаются несколько дальше от мишеней, но все же достаточно близко к ним, чтобы достичь рецепторов. Паракринные вещества секретируются одним типом клеток, а действуют на другой, однако в некоторых случаях регуляторы предназначены тем клеткам, которые их выделили, или соседним клеткам, относящимся к тому же типу. Это называется аутокринной регуляцией.
В ряде случаев последний этап сигнальной трансдукции состоит в фосфорилировании определенных эффекторных белков, что ведет к усилению или угнетению их активности, а это, в свою очередь, определяет необходимую организму клеточную реакцию. Фосфорилирование белков осуществляют протеинкиназы, а дефосфорилирование - протеинфосфатазы.
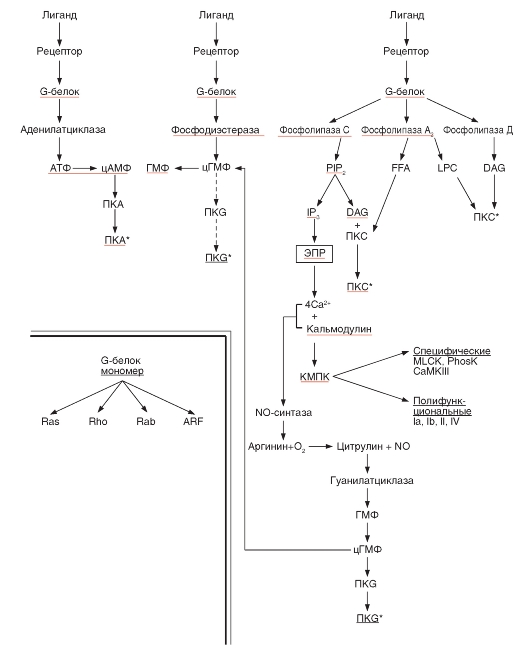
Изменения протеинкиназной активности происходят в результате связывания регуляторной молекулы (в общем случае называемой лигандом) с ее мембранным рецептором, что запускает каскады событий, некоторые из которых приведены на рисунке (рис. 2-1). Активность различных протеинкиназ регулируется рецептором не прямо, а через вторичные мессенджеры (вторичные посредники), в роли которых выступают, например, циклический АМФ (цAMФ), циклический ГМФ (цГMФ), Са2+, инозитол-1,4,5-три- фосфат (IP3) и диацилглицерол (DAG). При этом связывание лиганда с мембранным рецептором изменяет внутриклеточный уровень вторичного мессенджера, что, в свою очередь, отражается на активности протеинкиназы. Многие регулятор-
ные молекулы влияют на клеточные процессы через пути сигнальной трансдукции с участием гетеротримерных ГТФ-связывающих белков (гетеротримерных G-белков) или мономерных ГТФ-связывающих белков (мономерных G-белков).
Когда молекулы лиганда связываются с мембранными рецепторами, взаимодействующими с гетеротримерными G-белками, происходит переход G-белка в активное состояние путем связывания с ГТФ. Активированный G-белок может затем взаимодействовать со многими эффекторными белками, прежде всего ферментами, такими, как аденилатциклаза, фосфодиэстераза, фосфолипазы С, А2 и D. Это взаимодействие запускает цепи реакций (рис. 2-1), которые заканчиваются активацией различных протеинкиназ, таких, как протеинкиназа А (ПКА), протеинкиназа G (ПKG), протеинкиназа C (ПИС).
В общих чертах пути сигнальной трансдукции с участием G-белков - протеинкиназ включает следующие этапы.
1. Лиганд связывается с рецептором на мембране клетки.
2. Связанный с лигандом рецептор, взаимодействуя с G-белком, активирует его, и активированный G-белок связывает ГТФ.
3. Активированный G-белок взаимодействует с одним или несколькими следующими соединениями: аденилатциклазой, фосфодиэстеразой, фосфолипазами С, А2, D, активируея или ингибируя их.
4. Внутриклеточный уровень одного или нескольких вторичных мессенджеров, таких, как цАМФ, цГМФ, Са2+, IP3 или DAG, возрастает или снижается.
5. Увеличение или уменьшение концентрации вторичного мессенджера влияет на активность одной или нескольких зависимых от него протеинкиназ, таких, как цАМФ-зависимая протеинкиназа (протеинкиназа А), цГМФ-зависимая протеинкиназа (ПКG), кальмодулинзависимая протеинкиназа (КМПК), протеинкиназа С. Изменение концентрации вторичного мессенджера может активировать тот или иной ионный канал.
6. Уровень фосфорилирования фермента или ионного канала изменяется, что влияет на активность ионного канала, обуславливая конечный ответ клетки.
Рис. 2-1. Некоторые каскады событий, реализующиеся в клетке благодаря вторичным посредникам.
Обозначения: * - активированный фермент
Мембранные рецепторы, связанные с G-белками
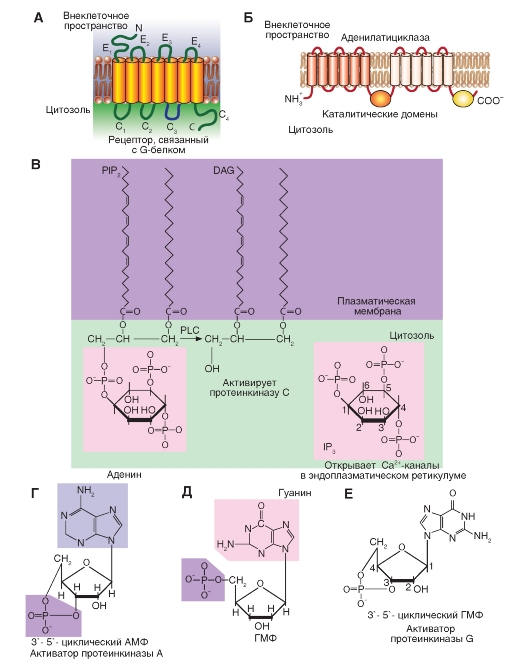
Мембранные рецепторы, опосредующие агонист-зависимую активацию G-белков, составляют особое семейство белков, в котором 500 с лишним представителей. К нему относятся α- и β-адренергические, мускариновые ацетилхолиновые, серотониновые, аденозиновые, обонятельные рецепторы, родопсин, а также рецепторы большинства пептидных гормонов. Представители семейства рецепторов, связанных с G-белками, имеют семь трансмембранных α-спиралей (рис. 2-2 А), каждая из которых содержит 22-28 преимущественно гидрофобных аминокислотных остатков.
Для некоторых лигандов, например, ацетилхолина, адреналина, норадреналина и серотонина, известны разные подтипы связанных с G-белками рецепторов. Зачастую они различаются сродством к конкурентным агонистам и антагонистам.
Далее представлена (рис. 2-2 Б) молекулярная организация аденилатциклазы - фермента, продуцирующего цАМФ (первый открытый вторичный мессенджер). Регуляторный путь аденилатциклазы считается классическим путем сигнальной трансдукции, обусловленной G-белками.
Аденилатциклаза служит основой позитивного или негативного контроля путей сигнальной трансдукции через G-белки. При позитивном контроле связывание стимулирующего лиганда, например, адреналина, действующего через β-адренергические рецепторы, ведет к активации гетеротримерных G-белков с α-субъединицей типа as («s» означает стимуляцию). Активация Gs-типа G-белков посредством связанного с лигандом рецептора приводит к тому, что его as-субъединица связывает ГТФ, и затем диссоциирует от βγ-димера.
На рисунке 2-2 В показано, как фосфолипаза С расщепляет фосфатидилинозитол-4,5-дифосфат на инозитол-1,4,5-трифосфат и диацилглицерол. Оба вещества, инозитол-1,4,5-трифосфат и диацилглицерол, относятся к вторичным мессенджерам. IP3, связываясь со специфическими лигандзависимыми Са2+-каналами эндоплазматического ретикулума, высвобождает из него Са2+, т.е. повышает концентрацию Са2+ в цитозоле. Диацилглицерол вместе с Са2+ активирует другой важный класс протеинкиназ - протеинкиназу С.
Затем показана структура некоторых вторичных мессенджеров (рис. 2-2 Г-Е): цАМФ, ГМФ,
цГМФ.
Рис. 2-2. Примеры молекулярной организации некоторых структур, участвующих в путях сигнальной трансдукции.
А - рецептор мембраны клетки, связывающий на внешней поверхности лиганд, а внутри - гетеротримерный G-белок. Б - молекулярная организация аденилатциклазы. В - структура фосфатидилинози- тол-4,5-дифосфата и образованных под действием фосфолипазы С инозитол-1,4,5-трифосфата и диацилглицерола. Г - структура 3',5'-циклического АМФ (активатора протеинкиназы А). Д - структура ГМФ. Е - структура 3',5'-циклического ГМФ (активатора протеинкиназы G)
Гетеротримерные G-белки
Гетеротримерный G-белок состоит из трех субъединиц: α (40 000-45 000 Да), β (около 37 000 Да) и γ (8000-10 000 Да). Сейчас известно около 20 различных генов, кодирующих эти субъединицы, в том числе не менее четырех генов β-субъединиц и примерно семь генов γ-субъединиц млекопитающих. Функция и специфичность G-белка обычно, хотя и не всегда, определяются его α-субъединицей. У большинства G-бел- ков субъединицы β и γ плотно связаны между собой. Некоторые гетеротримерные G-белки и пути трансдукции, в которых они задействованы, перечислены в табл. 2-1.
Гетеротримерные G-белки служат посредниками между рецепторами плазматической мембраны для более 100 внеклеточных регуляторных веществ и внутриклеточными процессами, которые они контролируют. В общих чертах, связывание регуляторного вещества с его рецептором активирует G-белок, а тот либо активирует, либо ингибирует фермент и/или вызывает цепь событий, приводящих к активации определенных ионных каналов.
На рис. 2-3 представлен общий принцип работы гетеротримерных G-белков. В большинстве G-белков α-субъединица представляет собой «рабочий элемент» гетеротримерных G-белков. Активация большинства G-белков приводит к конформационному изменению этой субъединицы. Неактивные G-белки существуют главным образом в форме αβγ-гетеротримеров,
с ГДФ в позициях, связывающих нуклеотид. Взаимодействие гетеротримерных G-белков с присоединившим лиганд рецептором ведет к преобразованию α-субъединицы в активную форму с повышенным сродством к ГТФ и пониженной афинностью его к βγ-комплексу. В результате активированная α-субъединица освобождает ГДФ, присоединяет ГТФ, а затем диссоциирует от βγ-димера. У большинства G-белков диссоциированная α-субъединица затем взаимодействует с эффекторными белками в пути сигнальной трансдукции. Однако у некоторых G-белков освободившийся βγ-димер может быть ответственным за все или некоторые эффекты рецептор-лигандного комплекса.
Работа некоторых ионных каналов модулируется G-белками непосредственно, т.е. без участия вторичных мессенджеров. Например, связывание ацетилхолина с мускариновыми М2-рецепторами сердца и некоторых нейронов ведет к активации особого класса К+-каналов. В этом случае связывание ацетилхолина с мускариновым рецептором ведет к активации G-белка. Его активированная α-субъединица затем отделяется от βγ-димера, а βγ-димер напрямую взаимодействует с особым классом К+-каналов, приводя их в открытое состояние. Связывание ацетилхолина с мускариновыми рецепторами, повышающее К+-проводимость пейсмекерных клеток в синоатриальном узле сердца - один из главных механизмов, посредством которого парасимпатические нервы вызывают уменьшение частоты сердечных сокращений.
Рис. 2-3. Принцип работы гетеротримерных ГТФ-связывающих белков (гетеротримерных G-белков).
Обозначения: R - рецептор, L - лиганд, Е - эффекторный белок
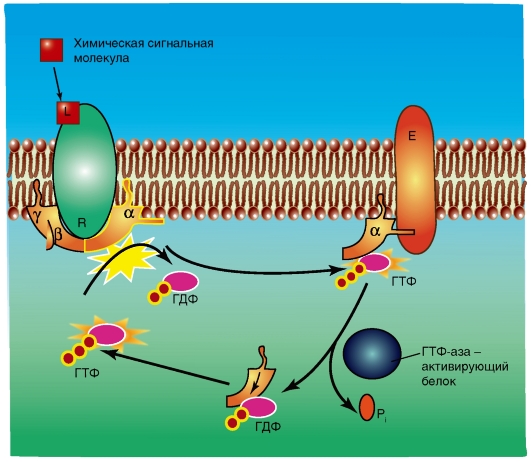
Таблица 2-1. Некоторые гетеротримерные ГТФ-связывающие белки млекопитающих, классифицированные на основе их α-субъединиц *

* В каждом классе α-субъединиц различают несколько изоформ. Идентифицировано более 20 α-субъединиц.
Мономерные G-белки
Клетки содержат еще одно семейство ГТФсвязывающих белков, которые называют мономерными ГТФ-связывающими белками. Они также известны как G-белки с низкой молекулярной массой или малые G-белки (молекулярная масса 20 000-35 000 Да). В таблице 2-2 перечислены основные подклассы мономерных ГТФсвязывающих белков и некоторые из их свойств. Ras-подобные и Rho-подобные мономерные ГТФ-связывающие белки участвуют в пути сигнальной трансдукции на этапе передачи сигнала от тирозинкиназы, рецептора фактора роста, на внутриклеточные эффекторы. Среди процессов, регулируемых путями сигнальной трансдукции, в которые вовлечены мономерные ГТФсвязывающие белки, можно назвать элонгацию полипептидной цепи в ходе белкового синтеза, пролиферацию и дифференцировку клеток, их злокачественное перерождение, контроль актинового цитоскелета, связь между цитоскелетом
и внеклеточным матриксом, транспорт везикул между различными органеллами и экзоцитозную секрецию.
Мономерные ГТФ-связывающие белки, как и их гетеротримерные аналоги, представляют собой молекулярные переключатели, существующие в двух формах - активированной «включенной» и инактивированной «выключенной» (рис. 2-4 Б). Однако активация и инактивация мономерных ГТФ-связывающих белков требует дополнительных регуляторных белков, которые, насколько известно, не требуются для работы гетеротримерных G-белков. Мономерные G-белки активируются гуанин-нуклеотид-освобождающими белками, а инактивируются ГТФаза-активирующими белками. Таким образом, активация и инактивация мономерных ГТФ-связывающих белков контролируется сигналами, которые изменяют активность гуанин-нуклеотид-освобождающих белков или ГТФаза-активирующих белков скорее, чем путем прямого воздействия на мономерные G-белки.
Рис. 2-4. Принцип работы мономерных ГТФ-связывающих белков (мономерных G-белков).
Обозначения: R - рецептор, L - лиганд
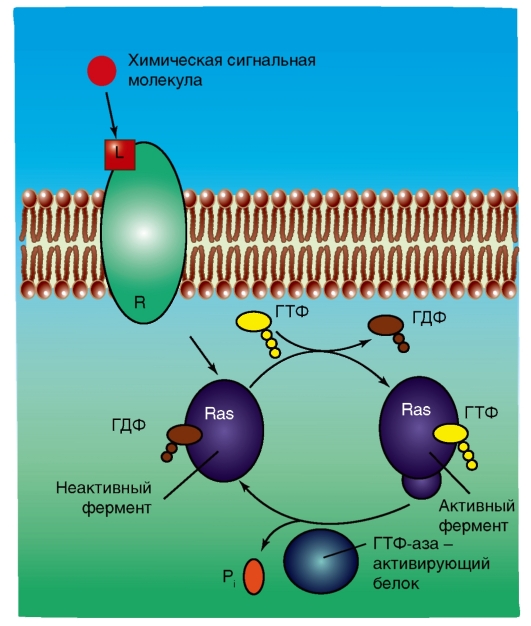
Таблица 2-2. Подсемейства мономерных ГТФ-связывающих белков и некоторые регулируемые ими внутриклеточные процессы

Механизм работы гетеротримерных G-белков
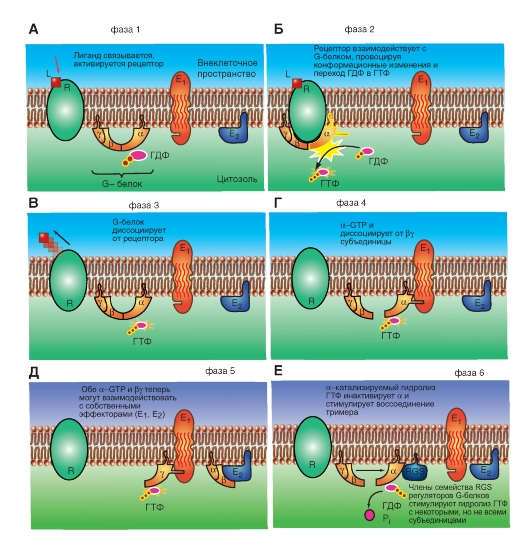
Неактивные G-белки существуют главным образом в форме αβγ-гетеротримеров, с ГДФ в их позициях, связывающих нуклеотид (рис. 2-5 А). Взаимодействие гетеротримерных G-белков с присоединившим лиганд рецептором ведет к преобразованию α-субъединицы в активную форму, которая имеет повышенное сродством к ГТФ и пониженную афинность его к βγ-комплексу (рис. 2-5 Б). В большинстве гетеротримерных G-белков именно α-субъединица представляет собой структуру, передающую информацию. Активация большинства G-белков приводит к конформационному изменению α-субъединицы.
В результате активированная α-субъединица освобождает ГДФ, присоединяет ГТФ (рис. 2-5 В), а затем диссоциирует от βγ-димера (рис. 2-5 Г). У большинства G-белков диссоциированная α-субъединица сразу взаимодействует с эффекторными белками (Е1) в пути сигнальной трансдукции (рис. 2-5 Г). Однако у некоторых G-белков освободившийся βγ-димер может быть ответственным за все или за некоторые эффекты рецептор-лигандного комплекса. Затем βγ-димер взаимодействует с эффекторным белком Е2 (рис. 2-5 Д). Далее показано, что члены RGS семьи G-белка стимулируют гидролиз ГТФ (рис. 2-5 Е). Это инактивирует α-субъединицу и объединяет все субъединицы в αβγ-гетеротример.
Рис. 2-5. Цикл работы гетеротримерного G-белка, запускающего дальнейшую цепь событий с помощью своей α-субъединицы.
Обозначения: R - рецептор, L - лиганд, Е - эффекторный белок
Пути сигнальной трансдукции через гетеротримерные G-белки
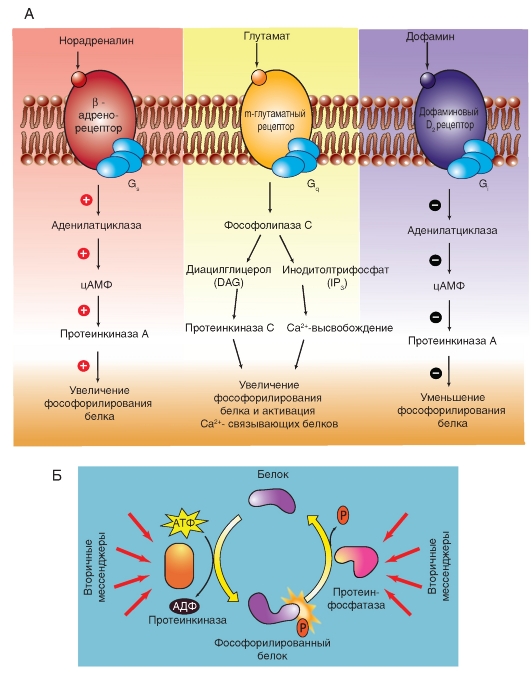
На рисунке 2-6 А показаны три лиганда, их рецепторы, связанные с разными G-белками, и их молекулярные мишени. Аденилатциклаза является основой для позитивного или негативного контроля путей сигнальной трансдукции, которые обусловлены G-белками. При позитивном контроле связывание стимулирующего лиганда, например норадреналина, действующего через β- адренергические рецепторы, ведет к активации гетеротримерных G-белков с α-субъединицей типа αS («s» означает стимуляцию). Поэтому такой G-белок называют G-белком GS-типа. Активация Gs-типа G-белков посредством связанного с лигандом рецептора приводит к тому, что его αs- субъединица связывает ГТФ и затем диссоциирует от βγ-димера.
Другие регуляторные вещества, такие, как адреналин, действующий через α2-рецепторы, или аденозин, действующий через α1-рецепторы, или дофамин, действующий через D2-рецепторы, участвуют в негативном или ингибирующем контроле аденилатциклазы. Эти регуляторные вещества активируют Gi-тип G-белков, которые имеют α-субъединицу типа αi («i» означает ингибирование). Связывание ингибирующего лиганда с его
рецептором активирует Gi-тип G-белков и вызывает диссоциацию его αi-субъединицы от βγ-димера. Активированная αi-субъединица связывается с аденилатциклазой и подавляет ее активность. Кроме того, βγ-димеры могут связывать свободные αs-субъединицы. Этим путем связывание βγ-димеров со свободной αs-субъединицей дополнительно подавляет стимуляцию аденилатциклазы, блокируя действие стимулирующих лигандов.
Еще один класс внеклеточных агонистов (рис. 2-6 А) связывается с рецепторами, которые активируют посредством G-белка, называемого Gq, β-изоформу фосфолипазы С. Она расщепляет фосфатидилинозитол-4,5-дифосфат (фосфолипид, в малых количествах присутствующий в плазматической мембране) на инозитол-1,4,5- трифосфат и диацилглицерол, которые относятся ко вторичным мессенджерам. IP3, связываясь со специфичными лигандзависимыми Са2+-каналами эндоплазматического ретикулума, высвобождает из него Са2+, т.е. повышает концентрацию Са2+ в цитозоле. Са2+-каналы эндоплазматического ретикулума вовлечены в электромеханическое сопряжение в скелетной и сердечной мышце. Диацилглицерол вместе с Са2+ активирует протеинкиназу С. К ее субстратам относятся, например, белки, участвующие в регуляции клеточного деления.
Рис. 2-6. Примеры путей сигнальной трансдукции через гетеротримерные G-белки.
А - в трех приведенных примерах связывание нейротрансмиттера с рецептором ведет к активации G-белка и последующему включению путей вторичных мессенджеров. Gs, Gq, и Gi подразумевают три различных типа гетеротримерных G-белков. Б - регуляция клеточных белков фосфорилированием ведет к усилению или угнетению их активности, а это, в свою очередь, определяет необходимую организму клеточную реакцию. Фосфорилирование белков осуществляют протеинкиназы, а дефосфорилирование - протеинфосфатазы. Протеинкиназа переносит фосфатную группу (Pi) от АТФ на сериновые, треониновые или тирозиновые остатки белков. Это фосфорилирование обратимо меняет структуру и функции клеточных белков. Оба типа ферментов - киназы и фосфатазы - регулируются различными внутриклеточными вторичными мессенджерами
Пути активации внутриклеточных протеинкиназ
Взаимодействие гетеротримерных G-белков с присоединившим лиганд рецептором ведет к преобразованию α-субъединицы в активную форму, которая имеет повышенное сродство к ГТФ и пониженную афинность его к βγ-комплексу. Активация большинства G-белков приводит к конформационному изменению α-субъединицы, которая освобождает ГДФ, присоединяет ГТФ, а затем диссоциирует от βγ-димера. Далее диссоциированная α-субъединица взаимодействует с эффекторными белками в пути сигнальной трансдукции.
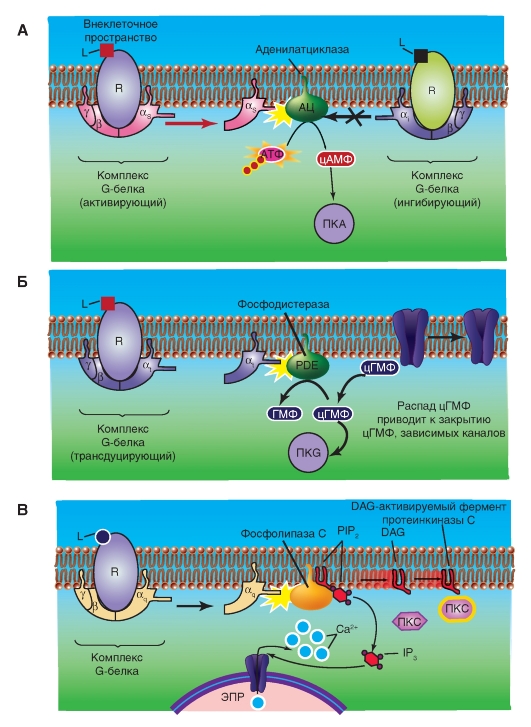
На рисунке 2-7 А продемонстрирована активация гетеротримерных G-белков Gs-типа с α-субъединицей типа αs, которая происходит благодаря связыванию с лигандом рецептора и приводит к тому, что αs-субъединица G-белков Gs-типа связывает ГТФ и затем диссоциирует от βγ-димера, а далее взаимодействует с аденилатциклазой. Это приводит к повышению уровня цАМФ и активации ПКА.
На рисунке 2-7 Б продемонстрирована активация гетеротримерных G-белков Gt-типа с α-субъединицей типа αt, которая происходит благодаря связыванию с лигандом рецептора и приводит к тому, что αt-субъединица G-белков Gt-типа активируется и затем диссоциирует от βγ-димера, а далее взаимодействует с фосфодиэстеразой. Это приводит к повышению уровня цГМФ и активации ПKG.
Рецептор катехоламинов α1 взаимодействует с Gαq -субъединицей, активирующей фосфолипазу С. На рисунке 2-7 В продемонстрирована активация гетеротримерных G-белков Gαq-типа с α-субъединицей типа αq, которая происходит благодаря связыванию лиганда с рецептором и приводит к тому, что αq-субъединица G-белков Gαq-типа активируется и затем диссоциирует от βγ-димера, а далее взаимодействует с фосфолипазой С. Она расщепляет фосфатидилинози- тол-4,5-дифосфат на IP3 и DAG. Это приводит к повышению уровня IP3 и DAG. IP3, связываясь со специфичными лигандзависимыми Са2+- каналами эндоплазматического ретикулума,
высвобождает из него Са2+. DAG вызывает активацию протеинкиназы С. В нестимулированной клетке значительное количество этого фермента находится в цитозоле в неактивной форме. Са2+ заставляет протеинкиназу С связываться с внутренней поверхностью плазматической мембраны. Здесь фермент может активироваться диацилглицеролом, который образуется при гидролизе фосфатидилинозитол-4,5-дифосфата. Мембранный фосфатидилсерин также может быть активатором протеинкиназы С, если фермент находится в мембране.
Описано около 10 изоформ протеинкиназы С. Хотя некоторые из них присутствуют во многих клетках млекопитающих, однако подтипы γ и ε обнаружены, главным образом, в клетках центральной нервной системы. Подтипы протеинкиназы С различаются не только распределением по организму, но, по-видимому, и механизмами регуляции своей активности. Некоторые из них в нестимулированных клетках связаны с плазматической мембраной, т.е. не требуют для активации увеличения концентрации Са2+. Некоторые изоформы протеинкиназы С активируются арахидоновой кислотой или другими ненасыщенными жирными кислотами.
Первоначальная кратковременная активация протеинкиназы С происходит под действием диацилглицерола, который освобождается, когда фосфолипаза Сβ активируется, а также под влиянием Са2+, освобожденного из внутриклеточных хранилищ с помощью IP3. Долго длящаяся активация протеинкиназы С запускается рецептор-зависимыми фосфолипазами А2 и D. Они действуют первично на фосфатидилхолин - основной мембранный фосфолипид. Фосфолипаза А2 отделяет от него жирную кислоту во втором положении (обычно ненасыщенную) и лизофосфатидилхолин. Оба эти продукта активируют определенные изоформы протеинкиназы С. Рецептор-зависимая фосфолипаза D расщепляет фосфатидилхолин таким образом, что образуется фосфатидная кислота и холин. Фосфатидная кислота далее расщепляется до диацилглицерола, участвующего в долговременной стимуляции протеинкиназы С.
Рис. 2-7. Основные принципы активации протеинкиназы А, протеинкиназы G и протеинкиназы С.
Обозначения: R - рецептор, L - лиганд
цAMФ-зависимая протеинкиназа (протеинкиназа А) и связанные с ней сигнальные пути
В отсутствии цАМФ, цАМФ-зависимая протеинкиназа (протеинкиназа А) состоят из четырех субъединиц: двух регуляторных и двух каталитических. У большинства типов клеток каталитическая субъединица одна и та же, а регуляторные субъединицы высокоспецифичны. Присутствие регуляторных субъединиц почти полностью подавляет ферментативную активность комплекса. Таким образом, активация ферментативной активности цАМФ-зависимой протеинкиназы должна вовлекать отделение регуляторных субъединиц от комплекса.
Активация происходит в присутствии микромолярных концентраций цАМФ. Каждая регуляторная субъединица связывает две его молекулы. Связывание цАМФ индуцирует конформационные изменения в регуляторных субъединицах и снижает аффинность их взаимодействия с каталитическими субъединицами. В результате этого регуляторные субъединицы отделяются от каталитических, и каталитические субъединицы становятся активированными. Активная каталитическая субъединица фосфорилирует белкимишени по определенным сериновым и треониновым остаткам.
Сравнение аминокислотных последовательностей цАМФ-зависимой и других классов протеинкиназ показывает, что, несмотря на сильные различия в их регуляторных свойствах, все эти ферменты высокогомологичны по первичной структуре срединной части. Эта часть содержит АТФ-связывающий домен и активный центр фермента, обеспечивающий перенос фосфата с АТФ на белок-акцептор. Участки киназ за пределами этой каталитической срединной части белка участвуют в регуляции киназной активности.
Определена также кристаллическая структура каталитической субъединицы цАМФ-зависимой протеинкиназы. Каталитическая средняя часть молекулы, имеющаяся у всех известных протеинкиназ, состоит из двух долей. Меньшая из них содержит необычный АТФ-связывающий участок, а большая доля содержит участок связывания пептида. Многие протеинкиназы содержат также регуляторный участок, известный как псевдосубстратный домен. По аминокислотной последовательности он напоминает фосфорилируемые участки субстратных белков. Псевдосубстратный домен, связываясь с активным центром протеинкиназы, ингибирует фосфорилирование истинных субстратов протеинкиназы. Активация киназы может включать фосфорилирование или нековалентную аллостерическую модификацию протеинкиназы для устранения ингибирующего действия псевдосубстратного домена.
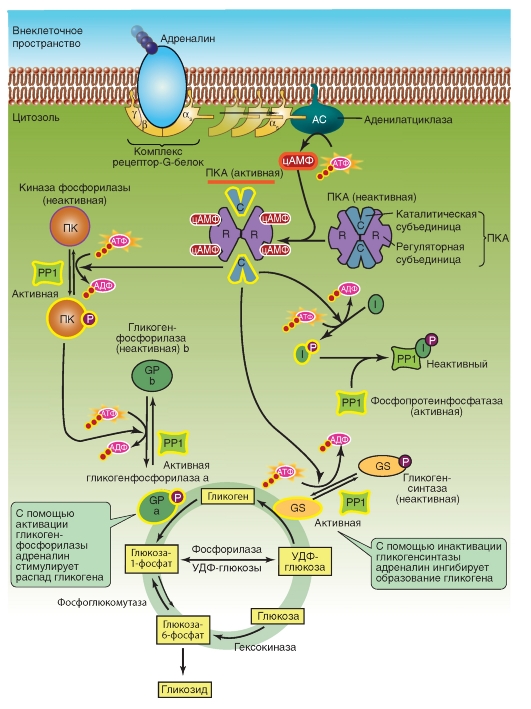
Рис. 2-8. цAMФ-зависимая протеинкиназа А и мишени.
Когда адреналин связывается с соответствующим рецептором, активация αs-субъединицы стимулирует аденилатциклазу с увеличением уровня цАМФ. цАМФ активирует протеинкиназу А, которая путем фосфорилирования дает три основных эффекта. (1) Протеинкиназа А активирует киназу фосфорилазы гликогена, которая фосфорилирует и активирует фосфорилазу гликогена. (2) Протеинкиназа А инактивирует гликогенсинтазу и таким образом уменьшает образование гликогена. (3) Протеинкиназа А активирует ингибитор фосфопротеин-фосфатазы-1 и тем самым ингибирует фосфатазу. Эффект в целом заключается в координации изменений уровня глюкозы.
Обозначения: УДФ-глюкоза - уридиндифосфатглюкоза
Гормональная регуляция активности аденилатциклазы
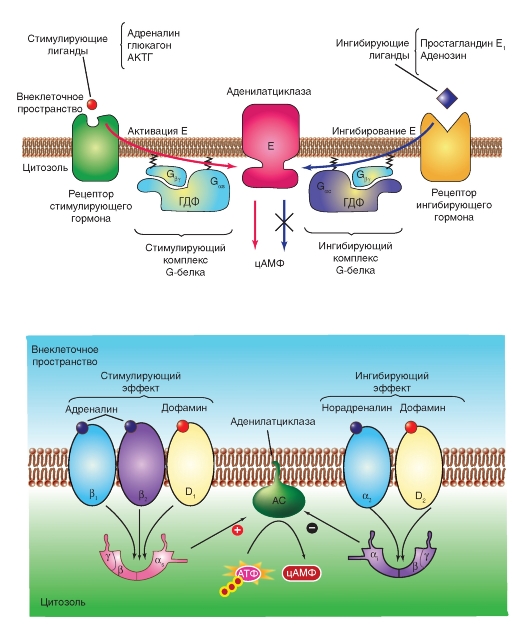
На рисунке 2-9 А представлен принципиальный механизм индуцированной гормонами стимуляции и ингибирования аденилатциклазы. Взаимодействие лиганда с рецептором, связанным с α-субъединицей типа αs (стимулирующая), вызывает активацию аденилатциклазы, тогда как взаимодействие лиганда с рецептором), связанным с α-субъединицей типа αi (ингибирующая), вызывает ингибирование фермента. Gβγ-субъединица и в стимулирующих, и в ингибирующих G-белках идентична. Gα-субъединицы и рецепторы различны. Лиганд-стимулирован-ное образование активных Gα•ГТФ комплексов происходит с помощью одинаковых механизмов в обоих Gαs,- и Gαi-протеинах. Однако Gαs•ГТФ и Gαi•ГТФ по-разному взаимодействуют с аденилатциклазой. Одна (Gαs•ГТФ) стимулирует, а другая Gαi•ГТФ) ингибирует ее каталитическую активность.
На рисунке 2-9 Б представлен механизм индуцированной определенными гормонами активации и ингибирования аденилатциклазы. β1-, β2- и D1-рецепторы взаимодействуют с субъединицами, которые активируют аденилатциклазу и повышают уровень цАМФ. α2-и D2-рецепторы взаимодействуют с Gαi субъединицами, которые ингибируют аденилатциклазу. (Что касается α1-рецептора, то он взаимодействует с G -субъединицей, которая активирует фосфолипазу С.) Рассмотрим один из примеров, представленных на рисунке. Адреналин связывается с β1-рецептором, что приводит к активации Gαs-белка, который стимулирует аденилатциклазу. Это приводит к увеличению внутриклеточного уровня цАМФ, и, таким образом, усиливает активность ПКА. С другой стороны, норадреналин связывается с α2-рецептором, что приводит к активации Gαi-белка, который ингибирует аденилатциклазу и тем самым снижает внутриклеточный уровень цАМФ, уменьшая активность ПКА.
Рис. 2-9. Индуцированная лигандами (гормонами) активация и ингибирование аденилатциклазы.
А - принципиальный механизм. Б - механизм применительно к конкретным гормонам
Протеинкиназа С и связанные с ней сигнальные пути
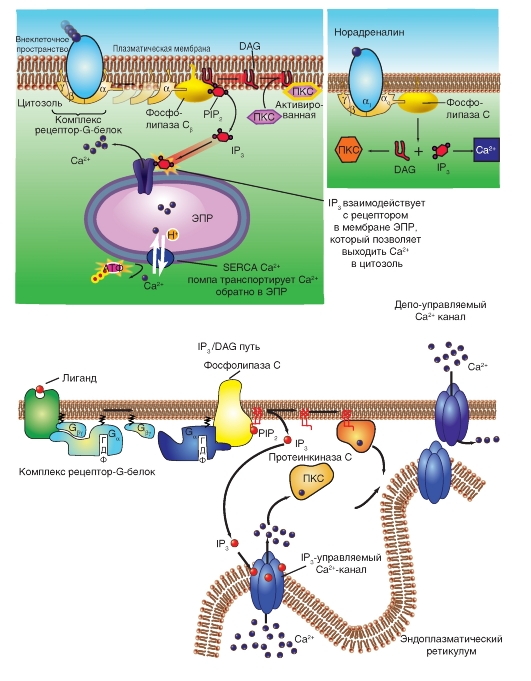
Рецептор α1 взаимодействует с Gαq-субъединицей G-белка, которая активирует фосфолипазу С. Фосфолипаза С расщепляет фосфатидилинози- тол-4,5-дифосфат на IP3 и DAG. IP3, связываясь со специфичными лиганд-зависимыми Са2+-каналами эндоплазматического ретикулума, высвобождает из него Са2+, т.е. повышает концентрацию Са2+ в цитозоле. DAG вызывает активацию протеинкиназы С. В нестимулированной клетке этот фермент находится в цитозоле в неактивной
форме. Если цитозольный уровень Са2+ повышается, происходит взаимодействие Са2+ с протеинкиназой С, что приводит к связыванию протеинкиназы С с внутренней поверхностью клеточной мембраны. В таком положении фермент активируется диацилглицеролом, образующимся при гидролизе фосфатидилинозитол-4,5-дифосфа- та. Мембранный фосфатидилсерин также может быть активатором протеинкиназы С, если фермент находится в мембране.
В таблице 2-3 приведены изоформы протеинкиназы С млекопитающих и свойства этих изоформ.
Таблица 2-3. Свойства изоформ протеинкиназы С млекопитающих
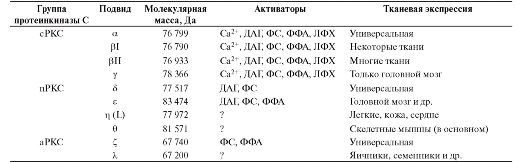
ДАГ - диацилглицерол; ФС - фосфатидилсерин; ФФА - цис-ненасыщенные жирные кислоты; ЛФХ - лизофосфатидилхолин.
Рис. 2-10. Сигнальные пути диацилглицерол / инозитол-1,4,5-трифосфат
Фосфолипазы и связанные с ними сигнальные пути на примере арахидоновой кислоты
Некоторые агонисты посредством G-белков активируют фосфолипазу А2, которая действует на мембранные фосфолипиды. Продукты их реакций могут активировать протеинкиназу С. В частности, фосфолипаза A2 отделяет от фосфолипидов находящуюся во втором положении жирную кислоту. Вследствие того, что некоторые фосфолипиды содержат в этом положении арахидоновую кислоту, вызванное фосфолипазой A2, расщепление этих фосфолипидов освобождает значительное ее количество.
Вышеописанный сигнальный путь арахидоновой кислоты, связанный с фосфолипазой А2, называют прямым. Непрямой путь активации арахидоновой кислоты связан с фосфолипазой Сβ.
Арахидоновая кислота сама по себе является эффекторной молекулой, а кроме того, служит предшественником для внутриклеточного синтеза простагландинов, простациклинов, тромбоксанов и лейкотриенов - важных классов регуляторных молекул. Арахидоновая кислота также образуется из продуктов расщепления диацил-глицеролов.
Простагландины, простациклины и тромбоксаны синтезируются из арахидоновой кислоты циклооксигеназно-зависимым путем, а лейкотриены - липоксигеназно-зависимым путем. Один из противовоспалительных эффектов глюкокортикоидов заключается как раз в ингибировании фосфолипазы A2, которая освобождает арахидоновую кислоту из фосфолипидов. Ацетилсалициловая кислота (аспирин) и другие нестероидные противовоспалительные средства ингибируют окисление арахидоновой кислоты циклооксигеназой.
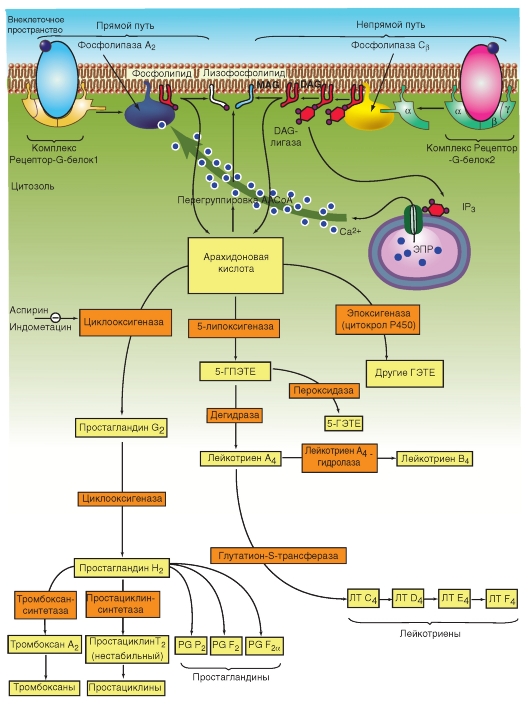
Рис. 2-11. Сигнальные пути арахидоновой кислоты.
Обозначения: ПГ - простагландин, ЛГ - лейкотриен, ГПЭТЕ - гидропероксиэйкозатетраеноат, ГЭТЕ - гидроксиэйкозатетраеноат, ЭПР - эндоплазматический ретикулум
Кальмодулин: строение и функции
Множество жизненно важных клеточных процессов, включая освобождение нейротрансмиттеров, секрецию гормонов и мышечное сокращение, регулируется цитозольным уровнем Са2+. Один из путей влияния этого иона на клеточные процессы заключается в его связывании с кальмодулином.
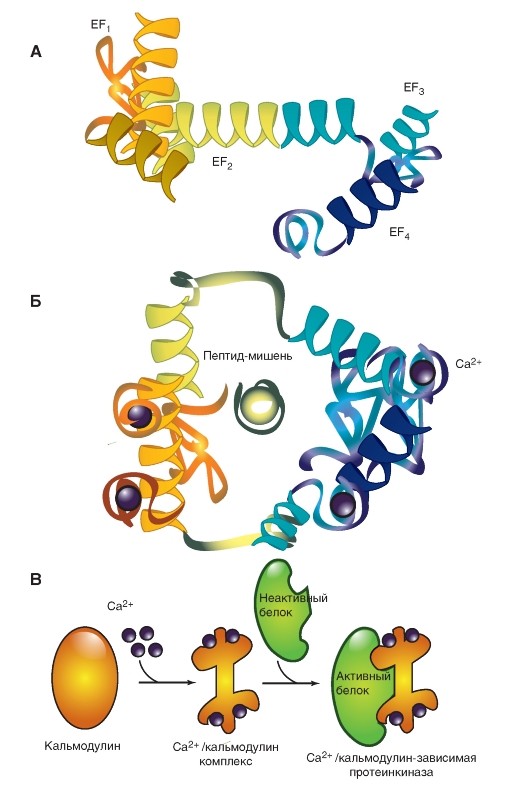
Кальмодулин - белок с молекулярным весом 16 700 (рис. 2-12 А). Он присутствует во всех клетках, иногда составляя до 1% их общего белкового содержимого. Кальмодулин связывает четыре иона кальция (рис. 2-12 Б и В), после чего этот комплекс регулирует активность различных внутриклеточных белков, многие из которых не относятся к протеинкиназам.
Комплекс Са2+ c кальмодулином активирует также кальмодулин-зависимые протеинкиназы. Специфический кальмодулин-зависимые протеинкиназы фосфорилируют специфические эффекторные белки, например, регуляторные легкие цепи миозина, фосфорилазу и фактор элонгации II. Мультифункциональные кальмодулин-зависимые протеинкиназы фосфорилируют многочисленные белки ядра, цитоскелета или мембранные белки. Некоторые кальмодулинзависимые протеинкиназы, такие, как киназа
легкой миозиновой цепи и киназа фосфорилазы, действуют только на один клеточный субстрат, тогда как другие полифункциональны и фосфорилируют более чем один субстратный белок.
Кальмодулин-зависимая протеинкиназа II относится к мажорным белкам нервной системы. В некоторых областях головного мозга на нее приходится до 2% общего белка. Эта киназа участвует в механизме, при котором увеличение концентрации Са2+ в нервном окончании вызывает освобождение нейротрансмиттера по типу экзоцитоза. Ее главным субстратом служит белок под названием синапсин I, присутствующий в нервных окончаниях и связывающийся с наружной поверхностью синаптических везикул. Когда синапсин I связан с везикулами, он предотвращает экзоцитоз. Фосфорилирование синапсина I вызывает его отделение от везикул, позволяя им выбросить нейротрансмиттер в синаптическую щель путем экзоцитоза.
Киназа легких цепей миозина играет важную роль в регуляции сокращения гладких мышц. Повышение цитозольной концентрации Са2+ в клетках гладких мышц активирует киназу легких цепей миозина. Фосфорилирование регуляторных легких цепей миозина приводит к длительному сокращению гладкомышечных клеток.
Рис. 2-12. Кальмодулин.
А - кальмодулин без кальция. Б - связывание кальция с кальмодулином и пептидной мишенью. В - схема связывания.
Обозначения: EF - Са2+-связывающие домены кальмодулина
Рецепторы с собственной ферметативной активностью (каталитические рецепторы)
Гормоны и факторы роста связываются с протеинами поверхности клетки, которые имеют ферментативную активность на цитоплазматической стороне мембраны. На рисунке 2-13 представлены пять классов каталитических рецепторов.
Один из характерных экземпляров трансмембранных рецепторов с гуанилатциклазной активностью, рецептор предсердного натрий-уретического пептида (ANP). Мембранный рецептор, с которым связывается ANP, не зависит от рассмотренных систем сигнальной трансдукции. Выше было описано действие внеклеточных агонистов, которые, связываясь с мембранными рецепторами, либо активируют аденилатциклазу через Gs-белки, либо угнетают ее через Gi. Мембранные рецепторы для ANP интересны тем, что сами рецепторы обладают гуанилатциклазной активностью, стимулирующейся связыванием ANP с рецептором.
ANP-рецепторы имеют внеклеточный ANP-свя- зывающий домен, единственную трансмембранную спираль и внутриклеточный гуанилатциклазный домен. Связывание ANP с рецептором повышает внутриклеточный уровень цГМФ , что стимулирует цГМФ-зависимую протеинкиназу. В противоположность цАМФ-зависимой протеинкиназе, имеющей регуляторную и каталитическую субъединицы, регуляторные и каталитические домены цГМФ-зависимой протеинкиназы находятся на одной полипептидной цепи. цГМФзависимая киназа затем фосфорилирует внутриклеточные белки, что приводит к различным клеточным ответам.
Рецепторы с серин-треонин-киназной активностью фосфорилируют белки только по остаткам серина и/или треонина.
Еще одно семейство мембранных рецепторов, не сопряженных с G-белками, состоит из белков с собственнойтирозин-протеинкиназнойактивностью. Рецепторами с собственной тирозин-протеинкиназной активностью служат белки с гликозилированным внеклеточным доменом, единственным
трансмембранным участком и внутриклеточным доменом с тирозин-протеинкиназной активностью. Связывание с ними агониста, например фактора роста нервов (NGF), стимулирует тирозин-протеинкиназную активность, что фосфорилирует специфичные белки-эффекторы по определенным тирозиновым остаткам. Большинство рецепторов для факторов роста димеризуются, когда с ними связывается NGF. Именно димеризация рецептора ведет к появлению у него тирозинпротеинкиназной активности. Активированные рецепторы часто фосфорилируют сами себя, что называется аутофосфорилированием.
К надсемейству пептидных рецепторов относят рецепторы инсулина. Это также тирозин-протеинкиназы. В подклассе рецепторов, относящихся к семейству инсулиновых рецепторов, нелигандный рецептор существует как дисульфид-связанный димер. Взаимодействие с инсулином приводит к конформационным изменениям обоих мономеров, что повышает связывание инсулина, активирует рецепторную тирозинкиназу и ведет к увеличению аутофосфорилирования рецептора.
Связывание гормона или фактора роста с его рецептором запускает разнообразные клеточные ответы, включая поступление в цитоплазму Са2+, увеличение Na+/H+ обмена, стимуляцию захвата аминокислот и сахара, стимуляцию фосфолипазы Сβ и гидролиз фосфатидилинозитолдифосфата.
Рецепторы гормона роста, пролактина и эритропоэтина, также как рецепторы интерферона и многих цитокинов, непосредственно не служат протеинкиназами. Однако после активации эти рецепторы образуют сигнальные комплексы с внутриклеточными тирозин-протеинкиназами, которые и запускают их внутриклеточные эффекты. Именно потому они не являются истинными рецепторами с собственной тирозин-протеинкиназной активностью, а просто связываются с ними.
На основе структуры можно полагать, что трансмембранные тирозин-протеинфосфатазы также представляют собой рецепторы, а их с тирозин-протеинфосфатазная активность модулируется внеклеточными лигандами.
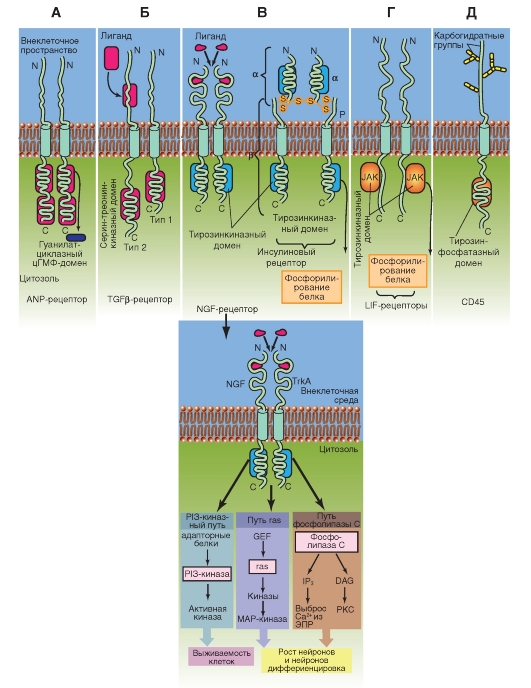
Рис. 2-13. Каталитические рецепторы.
А - рецептор гуанилциклазы, Б - рецептор с серин-треонин киназной активностью, В - рецептор с собственной тирозин-протеинкиназной активностью, Г - рецепторы, ассоциированные с тирозин-протеинкиназной активностью
Рецептор-связанные тирозинпротеинкиназы на примере рецепторов интерферона
Рецепторы интерферона непосредственно не являются протеинкиназами. После активации эти рецепторы образуют сигнальные комплексы с внутриклеточными тирозин-протеинкиназами, которые и запускают их внутриклеточные эффекты. То есть они не являются истинными рецепторами с собственной тирозин-протеинкиназной активностью, а просто связываются с ними таке рецепторы называются рецептор-связанными (рецептор-зависимыми) тирозин-протеинкиназами.
Механизмы, благодаря которому эти рецепторы оказывают действие, запускаются, когда гормон связывается с рецептором, что вызывает его димеризацию. Рецепторный димер связывает одну или несколько членов Janus-семейства тирозин-протеинкиназ (JAK). JAK затем перекрестно
фосфорилируют друг друга, а также рецептор. Члены семейства преобразователей сигнала и активаторов транскрипции (STAT) связывают фосфорилированные домены на комплексе рецептора и JAK. STAT-белки фосфорилируются JAK-киназами и затем отсоединяются от сигнального комплекса. В конечном итоге фосфорилированные STAT-белки образуют димеры, которые двигаются к ядру, чтобы активировать транскрипцию определенных генов.
Специфичность рецептора для каждого гормона отчасти зависит от специфики членов семейства JAK или STAT, объединяющихся для образования сигнального комплекса. В некоторых случаях сигнальный комплекс также активирует MAP-(митоген-активирующий протеин)-киназный каскад с помощью адапторных белков, используемых рецепторными тирозинкиназами. Некоторые из ответов рецепторных тирозинкиназных лигандов также вовлекают JAK и STAT пути.
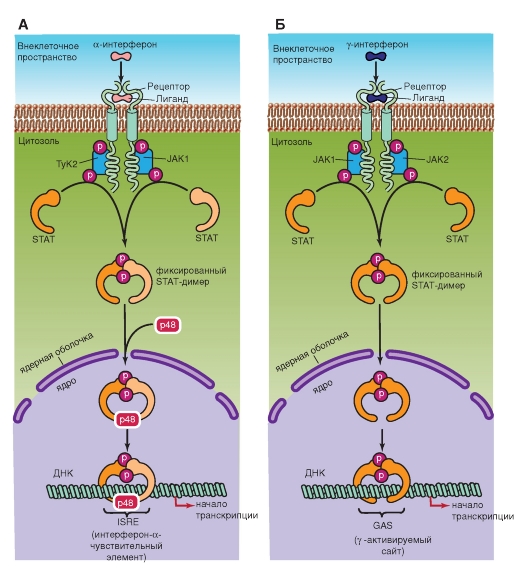
Рис. 2-14. Пример каталитических рецепторов, ассоциированных с тирозин-протеинкиназной активностью. Рецептор, активируемый α-интерфероном (А) и γ-интерфероном (Б)
Ras-подобные мономерные G-белки и опосредованные ими пути трансдукции
Лиганд, например фактор роста, связывается с рецептором, обладающим собственной тирозинпротеинкиназной активностью, что приводит к увеличению транскрипции в 10-ступенчатом процессе. Ras-подобные мономерные ГТФ-связывающие белки участвуют в пути сигнальной трансдукции на этапе передачи сигнала от рецепторов с собственной тирозин-протеинкиназной активностью (например, рецепторов фактора роста) на внутриклеточные эффекторы. Активация и инактивация мономерных ГТФ-связывающих белков требуют дополнительных регуляторных белков. Мономерные G-белки активируются гуанин-нуклеотид-освобождающими белками (GNRP), а инактивируются ГТФаза-активирующими белками (GAP).
Мономерные ГТФ-связывающие белки семейства Ras служат посредниками связывания митогенных лигандов и их тирозин-протеинкиназных рецепторов, что запускает внутриклеточные процессы, ведущие к пролиферации клеток. Когда Ras-белки неактивны, клетки не реагируют на факторы роста, действующие через тирозинкиназные рецепторы.
Aктивация Ras запускает путь сигнальной трансдукции, приводящий в конечном итоге к транскрипции определенных генов, способствующих клеточному росту. Каскад MAP-киназы (МАРК) вовлекается в ответы при активации Ras. Протеинкиназа С также активирует каскад MAP- киназы. Таким образом, каскад MAP-киназы оказывается важной точкой конвергенции для разнообразных эффектов, вызывающих клеточную пролиферацию. Более того, здесь наблюдается перекрест между протеинкиназой С и тирозинкиназами. Например γ-изоформа фосфолипазы С активируется путем связывания с активированным Ras-белком. Эта активация передается на протеинкиназу С в процессе стимуляции фосфолипидного гидролиза.
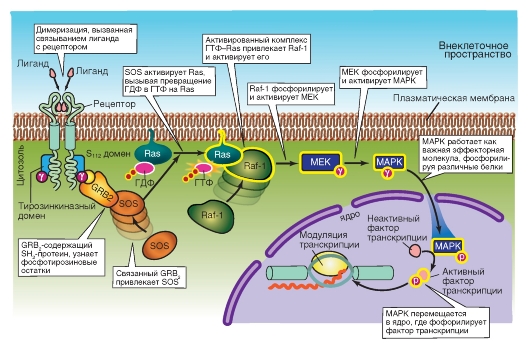
На рисунке 2-15 представлен механизм, включающий 10 ступеней.
1. Связывание лиганда приводит к димеризации рецептора.
2. Активированнаятирозин-протеинкиназа (RTK) фосфорилирует себя.
3. GRB2 (growth factor receptor-bound protein-2), SH2-содержащий протеин, узнает фосфотирозиновые остатки на активированном рецепторе.
4. Связывание GRB2 включает SOS (son of sevenless) обменный протеин гуаниннуклеотида.
5. SOS активирует Ras, формируя на Ras ГТФ вместо ГДФ.
6. Активный комплекс Ras-ГТФ активирует другие протеины физическим включением их в плазматическую мембрану. Активный комплекс Ras-ГТФ взаимодействует с N-терминальной частью серин-треонин киназы Raf-1 (известной как митоген-активирующий протеин, MAP) первой в серии последовательности активированных протеинкиназ, которые передают активационный сигнал в ядро клетки.
7. Raf-1 фосфорилирует и активирует протеинкиназу, названную MEK, которая известна как киназа МАP-киназы (МАРКК). MEK - это мультифункциональная протеинкиназа, фосфорилирующая субстраты остатков тирозина и серина / треонина.
8. MEK фосфорилирует МАP-киназу (МАРК), которая также вызывается внеклеточным сигналом - регуляторной киназой (ERK1, ERK2). Активация МАРК требует двойного фосфорилирования на соседних остатках серина и тирозина.
9. МАРК служит важнейшей эффекторной молекулой в Ras-зависимой сигнальной трансдукции, поскольку она фосфорилирует много клеточных протеинов после митогенной стимуляции.
10. Активированная МАРК переносится в ядро, где она фосфорилирует фактор транскрипции. В целом, активированный Ras активирует МАР
путем связывания с ней. Результатом этого каскада являются фосфорилирование и активация МАР-киназы, которая, в свою очередь, фосфорилирует факторы транскрипции, белковые субстраты и другие протеинкиназы, важные для деления и других ответов клеток. Активация Ras зависит от адаптерных белков, связывающихся с фосфотирозиновыми доменами на активированных факторами роста рецепторах. Эти адаптерные белки присоединяются и активируют GNRF (гуанин-нуклеотидобменный протеин), который активирует Ras.
Рис. 2-15. Регуляция транскрипции Ras-подобными мономерными G-белками, запускаемая с рецептора с собственной тирозин-протеинкиназной активностью
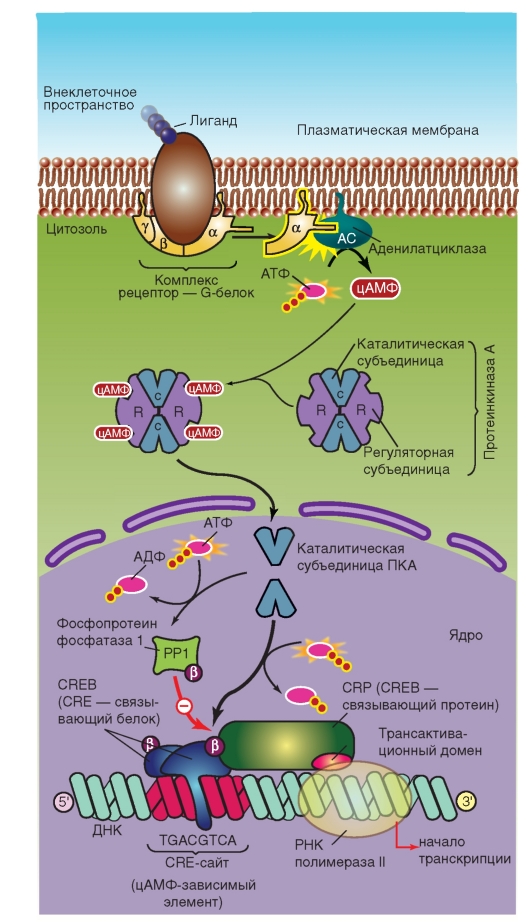
Регуляция транскрипции белком, взаимодействующим с цАМФзависимым элементом ДНК (CREB)
CREB -широко распространенный транскрипционный фактор - в норме связан с участком ДНК, названным CRE (сАМР response element). В отсутствии стимуляции CREB дефосфорилирован и не влияет на транскрипцию. Многочисленные пути сигнальной трансдукции посредством активации киназ (таких, как ПКА, Са2+/кальмо- дулин-киназа IV, МАР-киназа) приводят к фосфорилированию CREB. Фосфорилированный CREB связывается CBP (CREB-binding protein - CREB-связывающим протеином), который имеет домен, стимулирующий транскрипцию. Параллельно фосфорилирование активирует РР1
(фосфопротеинфосфатазу 1), которая дефосфорилирует CREB, что приводит к остановке транскрипции.
Показано, что активация CREB-опосредованно- го механизма важна для реализации таких высших когнитивных функций, как обучение и память.
На рисунке 2-15 показано также строение цАМФзависимой ПКА, которая в отсутствии цАМФ состоит из четырех субъединиц: двух регуляторных и двух каталитических. Присутствие регуляторных субъединиц подавляет ферментативную активность комплекса. Связывание цАМФ индуцирует конформационные изменения в регуляторных субъединицах, в результате чего регуляторные субъединицы отделяются от каталитических. Каталитические ПКА попадают в ядро клетки и запускают изложенный выше процесс.
Рис. 2-16. Регуляция генной транскрипции с помощью CREB (сАМР response element binding protein) через увеличение уровня циклического аденозинмонофосфата