Внутренние болезни: учебник. - 6-е изд., перераб. и доп. / В. И. Маколкин, С. И. Овчаренко, В. А. Сулимов. - 2012. - 768 с. : ил.
|
|
|
|
Глава 8. БОЛЕЗНИ СУСТАВОВ
БОЛЕЗНИ СУСТАВОВ
Поражения суставов различной этиологии в клинике внутренних болезней регистрируют достаточно часто. Заболевания суставов могут быть самостоятельной нозологической формой (РА, ОА, подагра), признаком патологических изменений других систем (артрит при СКВ, ССД) или реакцией на иной патологический процесс (реактивные артриты при каком-либо остром инфекционном заболевании).
Все многообразие заболеваний суставов можно свести к двум формам - артритам (воспалительные поражения суставов, не зависящие от непосредственной причины их возникновения, - инфекционного поражения, аутоиммунных процессов или выпадения микрокристаллов солей в синовиальной жидкости) и артрозам (дистрофически-дегенеративные поражения).
В этой главе будут рассмотрены наиболее частые заболевания суставов - РА, ОА, подагра и идиопатический анкилозирующий спондилоартрит (ББ).
РЕВМАТОИДНЫЙ АРТРИТ
Ревматоидный артрит (РА) - хроническое системное воспалительное заболевание соединительной ткани с преимущественным поражением суставов по типу эрозивно-деструктивного прогрессирующего полиартрита. Сущность заболевания состоит в поражении суставных тканей (синовиальная оболочка, суставной хрящ, капсула сустава) воспалительным процессом, развивающимся на иммунной основе и приводящим к эрозиям суставных поверхностей костей с последующим формированием выраженных деформаций и анкилозов. В основе нередко наблюдаемых внесуставных поражений лежит иммунокомплексный васкулит, вызывающий поражение внутренних органов и систем.
РА - одно из наиболее распространенных хронических воспалительных заболеваний суставов. Частота его возникновения в популяции составляет 1%. Заболевание может возникать у лиц любого возраста. Женщины болеют в 2,5 раза чаще, чем мужчины. В пожилом возрасте это различие менее очевидно.
Этиология
Причины развития РА неизвестны. Придают значение вирусным агентам (вирус Эпстайна-Барр), а также другим инфекционным возбудителям (стрептококки группы В, микоплазма). Молекулярные компоненты клеток микроорганизмов и продукты разрушения последних обладают тропизмом к суставным тканям, способны длительно персистировать в них и вызывать характерный иммунный ответ. Вирусы, встраиваясь в ДНК клеток хозяина, могут индуцировать синтез и секрецию неинфекционных белков, обладающих антигенной активностью, что служит стимулом к развитию иммунных реакций. Предполагают, что вирус Эпстайна-Барр может длительно существовать в организме лиц с генетической предрасположенностью к такому персистированию, что приводит к нарушению супрессорной функции Т-клеток и нарушению продукции иммуноглобулинов В-лимфоцитами.
В настоящее время в происхождении этого заболевания придают значение генетическим факторам. Так, риск заболеть РА в 16 раз выше у кровных родственников. РА чаще обнаруживают у носителей определенных антигенов класса II главного комплекса гистосовместимости (особенно HLA-DR1 и HLA- DR4). Так, носительство HLA DRW4 регистрируют у 52% больных РА и лишь у 13% лиц в популяции.
Имеют значение гормональные факторы: у мужчин в возрасте младше 50 лет РА диагностируют в 2-3 раза чаще, чем у лиц более старшего возраста. Прием контрацептивов и беременность снижают риск развития заболевания у женщин. Напротив, в период лактации (гиперпролактинемия) риск заболеть РА существенно повышается.
В целом, вклад генетических факторов в развитие РА составляет 15%, а факторов внешней среды - 85%.
Патогенез
На ранней стадии РА поражение суставов связано с неспецифической воспалительной реакцией, вызванной различными стимулами, которая, в свою очередь (у генетически предрасположенных лиц), приводит к патологическим изменениям клеток синовиальной оболочки. В дальнейшем в результате вовлечения в процесс иммунных клеток (Т-, В-лимфоциты и др.) в полости сустава происходит формирование эктопического лимфоидного органа, клетки которого начинают продуцировать аутоантитела к компонентам синовиальной оболочки. Аутоантитела (в первую очередь РФ - антитело к агрегированному IgG, а также антитела к ферменту Г-6-ФД и др.) и иммунные комплексы, активируя систему комплемента, еще более усиливают воспалительную реакцию, вызывающую прогрессирующее повреждение суставных тканей. Формируется ведущий морфологический признак ревматоидного воспаления - очаг гиперплазии соединительной ткани, так называемый паннус. Активированные
Т-лимфоциты стимулируют синтез макрофагами провоспалительных медиаторов (цитокинов), среди которых центральное место занимает ФНО-α, а также ИЛ-1. В развитии деструкции хряща и субхондральной кости при РА важную роль играют металлопротеиназы (коллагеназа, желатиназа), образующиеся в зоне паннуса.
На поздних стадиях в патогенезе РА преобладают процессы, обусловленные соматической мутацией синовиальных фибробластов и дефектами апоптоза. Это объясняет трудности противовоспалительного лечения, которое эффективно в рамках небольшого временного отрезка, после чего клетки-мишени начинают терять способность отвечать на регулирующие противовоспалительные стимулы и приобретают устойчивость к фармакологическим воздействиям.
Основная особенность РА состоит в том, что паннус постепенно разрушает хрящ и эпифизы костей с образованием узур (эрозий). Исчезновение хряща ведет к развитию фиброзного, а затем и костного анкилоза сустава. Деформацию суставов обусловливает и изменение периартикулярных тканей (капсулы сустава, сухожилий и мышц). Кроме поражений суставов, при РА практически всегда отмечают изменения соединительной ткани, различных органов и систем. Морфологическая основа их поражения - васкулиты и лимфоидная инфильтрация.
Классификация
В настоящее время в нашей стране принята рабочая классификация РА (Пленум Всесоюзного общества ревматологов, 1980), учитывающая клиникоанатомическую и клинико-иммунологическую характеристику процесса, характер течения, степень активности, рентгенологическую стадию артрита и функциональную активность больного.
Клинико-анатомическая характеристика:
• РА - полиартрит, олигоартрит;
• РА с системными проявлениями (висцеритами, поражением ретикулоэндотелиальной системы, серозных оболочек, легких, сердца, сосудов, глаз и почек, амилоидозом органов, псевдосептическим синдромом);
• особые синдромы (синдром Фелти, болезнь Стилла у взрослых);
• в сочетании с ОА, ревматизмом и другими ДЗСТ. Клинико-иммунологическая характеристика:
• серопозитивный;
• серонегативный. Течение болезни:
• медленно прогрессирующее (классическое);
• быстро прогрессирующее;
• без заметного прогрессирования (доброкачественное, малопрогрессирующее).
Степень активности:
• минимальная;
• средняя;
• высокая;
• ремиссия.
Рентгенологическая стадия:
• околосуставной остеопороз;
• остеопороз + сужение суставной щели (могут быть единичные узуры);
• остеопороз, сужение суставной щели, множественные узуры;
• то же + костный анкилоз. Функциональная активность:
• полностью сохранена;
• профессиональная трудоспособность ограничена;
• профессиональная трудоспособность утрачена;
• утрачена способность к самообслуживанию.
Клиническая картина
На первом этапе диагностического поиска выясняют основные жалобы больного, как правило, связанные с поражением суставов, а также особенности начала заболевания. Выделяют несколько вариантов начала.
• При постепенном начале заболевания (в течение нескольких месяцев) примерно в половине случаев отмечают медленное нарастание болей и скованности в мелких периферических суставах (лучезапястных, проксимальных межфаланговых, пястно-фаланговых, голеностопных и плюснефаланговых). Движения в суставах ограничены незначительно, температура тела остается нормальной. Характерна утренняя скованность суставов кисти - невозможность сжать пальцы в кулак (длительность скованности - от одного до нескольких часов).
• Моноартрит коленных или плечевых суставов с последующим быстрым вовлечением в патологический процесс мелких суставов кистей и стоп.
• Острый моноартрит крупных суставов, напоминающий септический артрит, который протекает с высокой температурой тела и сочетается с тендосиновитом, бурситом и подкожными (ревматоидными) узелками.
• Палиндромный ревматизм - множественные рецидивирующие атаки острого симметричного полиартрита суставов кистей, реже - коленных и локтевых суставов. Атаки продолжаются несколько дней и заканчиваются выздоровлением.
• Рецидивирующий бурсит и тендосиновит, особенно часто - в области лучезапястных суставов.
• Острый полиартрит с множественным поражением мелких и крупных суставов, выраженными болями, диффузным отеком и ограничением подвижности у лиц пожилого возраста. Этот вариант описывают как ремиттирующий серонегативный симметричный синовит с подушкообразным отеком.
• Генерализованная полиартралгия или симптомокомплекс, напоминающий ревматическую полимиалгию (обычно - у лиц пожилого возраста).
По мере течения РА больные отмечают развитие деформации пораженных суставов и ограничение их подвижности, которая в выраженных случаях приводит к полной потере функций сустава.
На первом этапе можно получить сведения о возможном поражении внутренних органов (возникновение жалоб соответственно вовлечению в патологический процесс различных органов), а также данные о ранее проводимом лечении. Применение препаратов золота, пеницилламина и цитостатиков указывает на развернутую клиническую картину болезни, тогда как эффективность назначения НПВС и аминохинолиновых производных свидетельствует о небольшом сроке заболевания и невысокой активности патологического процесса.
На втором этапе диагностического поиска существенную информацию дает исследование пораженных суставов: в начале заболевания или в период обострения отмечают клинические признаки артрита в виде сглаженности контуров сустава вследствие воспалительного внутрисуставного отека и отека периартикулярных тканей.
Характерно симметричное поражение мелких суставов кисти. По мере развития патологического процесса развиваются деформации суставов, обусловленные пролиферативными изменениями синовиальной оболочки и капсулы сустава, а также деструкцией суставного хряща и прилежащей костной ткани. Возникают подвывихи, усугубляющиеся развитием контрактур вследствие поражения сухожилий в местах их прикрепления к костям.
Некоторые из деформаций, наиболее типичные для РА, имеют самостоятельное значение: отклонение всей кисти в локтевую сторону («плавник моржа»), сгибательная контрактура проксимального межфалангового сустава при одновременном переразгибании в дистальном межфаланговом суставе (деформация пальца типа «пуговичной петли»), укорочение фаланг, сопровождающееся сморщиванием кожи над ними, в сочетании с ульнарной девиацией кисти (деформация кисти типа «рука с лорнетом»). Поражение других суставов не отличается от артритов иной этиологии. Изменения суставов кисти при РА служат «визитной карточкой» заболевания.
По мере прогрессирования РА развивается атрофия кожного покрова, который выглядит блестящим и как бы прозрачным. Наиболее отчетливо изменения кожи выражены в области пальцев и голеней. В некоторых случаях возникает изъязвление кожи голеней, которое может быть связано с васкулитом, обусловливающим формирование локальных некрозов. Иногда при длительном течении РА отмечают эритему в области ладоней.
У 20-30% больных обнаруживают так называемые ревматоидные узелки - безболезненные, достаточно плотные округлые образования диаметром от 2-3 мм до 2-3 см, обычно локализующиеся в местах, подвергающихся механическому давлению (разгибательная поверхность локтевой кости вблизи локтевого сустава, ахиллово сухожилие, седалищные бугры). Иногда узелки образуются в области мелких суставов кисти или стоп и в стенках синовиальной сумки, находящейся в области венечного отростка локтевой кости. Обычно узлы расположены подкожно, но могут формироваться внутрикожно и в сухожилиях. Размер узлов с течением времени меняется, а в период ремиссии они могут полностью исчезать. Их обнаруживают лишь у больных с серопозитивным РА.
Поражение суставов сопровождается развитием мышечной атрофии. Один из ранних симптомов РА при поражении суставов кисти - атрофия межкост-
ных мышц. При поражении других суставов развивается атрофия мышц, являющихся «моторными» для них. Со временем атрофия распространяется не только на мышцы, расположенные около пораженных суставов, но и на весь мышечный массив, что ведет к общему истощению. Также отмечают хруст в суставах при активных и пассивных движениях.
У больных РА можно обнаружить поражение сухожилий и синовиальных сумок. В синовиальной оболочке сухожильных влагалищ и синовиальных сумок также может развиваться воспаление, сопровождающееся образованием выпота. Наиболее часто отмечают поражение влагалищ сухожилий сгибателей и разгибателей пальцев, характеризующееся болезненностью и припухлостью в области кисти. Пальпаторно обнаруживают крепитацию при движениях. Сгибание пальцев может быть затруднено вследствие тендовагинита сухожилий сгибателей. В редких случаях формируются ревматоидные узелки в сухожилиях, что может послужить причиной их разрыва.
Аутоиммунный характер заболевания с преимущественным поражением суставов и других соединительнотканных элементов обусловливает распространение патологического процесса на внутренние органы. Как следует из рабочей классификации, при РА возможно поражение практически всех внутренних органов, но частота и степень его выраженности различны. Как правило, оно протекает субклинически, без выраженных симптомов.
Поражение сердца может манифестировать миокардитом (обычно очаговым и поэтому трудно диагностируемым), а также эндокардитом. В редких случаях при РА формируются клапанные пороки исключительно в виде недостаточности аортального или митрального клапана. Степень поражения клапана обычно невелика, и порок манифестирует клапанными (прямыми) симптомами, тогда как косвенные признаки, указывающие на тяжесть расстройств гемодинамики и компенсаторную гипертрофию различных отделов сердца, отсутствуют либо выражены крайне незначительно.
Перикардит, как правило, слипчивый, и его обнаруживают лишь при развитии застойных явлений в большом круге кровообращения, а также при рентгенологическом исследовании (на третьем этапе диагностического поиска). Выпотной перикардит, регистрируемый крайне редко, обычно сочетается с плевритом.
Ревматоидное поражение легких представлено диффузным фиброзирующим альвеолитом, узелковым поражением легочной ткани или легочным васкулитом. В связи с этим данные физикального обследования очень скудны: отмечают признаки синдрома легочной недостаточности, эмфиземы легких, реже - пневмосклероза с выслушиванием влажных звонких мелкопузырчатых хрипов в участках поражения.
При РА может развиваться плеврит, как правило, сухой с бессимптомным течением. Следы перенесенного плеврита обнаруживают лишь при рентгенологическом исследовании (на третьем этапе диагностического поиска). Исключительно редко отмечают экссудативный плеврит с образованием небольшого количества быстро рассасывающегося выпота.
Ревматоидное поражение почек диагностируют лишь на третьем этапе. Только при развитии амилоидоза почек и развитии нефротического синдрома
могут возникать массивные отеки. В протеинурической стадии амилоидоза почек типичные признаки можно обнаружить лишь при исследовании мочи.
Поражение нервной системы - полинейропатия - манифестирует нарушениями чувствительности в зоне пораженных нервов. Реже возникают двигательные расстройства. Характерно поражение дистальных нервных стволов, чаще всего - малоберцового нерва.
У 10-15% больных регистрируют вовлечение в патологический процесс слюнных и слезных желез, что диагностируют по сухости слизистой оболочки полости рта и конъюнктивы. Сочетание РА с поражением экзокринных желез носит название синдрома Шегрена. В отдельных случаях обнаруживают увеличение печени и селезенки, иногда - в сочетании с умеренным увеличением лимфатических узлов и лейкопенией. Такое сочетание носит название синдрома Фелти.
Поражение сосудов характерно для РА. Во время осмотра ногтей и дистальных фаланг можно обнаружить небольшие коричневатые очаги - следствие локальных микроинфарктов. Реже возникают васкулиты более крупных сосудов. При РА в результате артериита может развиться синдром Рейно.
Поражение глаз регистрируют нечасто. Обычно оно представлено двусторонним склеритом.
На третьем этапе диагностического поиска определяют степень активности воспалительного процесса и выраженность иммунологических изменений, а также уточняют степень поражения суставов и внутренних органов.
При лабораторном исследовании активность воспалительного процесса оценивают по существованию и выраженности острофазовых показателей (увеличение СОЭ, повышение концентрации фибриногена, СРБ и а2-глобулинов). Для тяжелого течения PA и поражения внутренних органов характерна гипохромная анемия. Ее выраженность коррелирует со степенью активности патологического процесса.
Число лейкоцитов и нейтрофилов в периферической крови при РА обычно соответствует норме. Лейкоцитоз обнаруживают при высокой лихорадке или лечении глюкокортикоидами, лейкопению - при синдроме Фелти - варианте течения РА.
Иммунные изменения при РА представлены обнаружением РФ (антитела к агрегированному IgG) в крови больных (в 70-90% случаев). Как было отмечено ранее, РФ синтезируется в плазматических клетках синовиальной оболочки, поэтому в начале болезни (в течение нескольких месяцев, реже - лет), особенно при доброкачественном течении, РФ определяют только в синовиальной жидкости. В крови его обнаруживают с помощью реакции Ваалера-Розе или латекс-теста. Величина титра РФ прямо пропорциональна активности патологического процесса, быстроте прогрессирования и развитию внесуставных симптомов болезни.
Титр РФ в реакции Ваалера-Розе около 1:160 считают высоким. В низком титре (1:10-1:20) его можно обнаружить в крови здоровых лиц молодого возраста, а также при ряде заболеваний с иммунным механизмом развития, СКВ, хроническом активном гепатите и циррозе печени. РФ появляется в различные сроки от начала болезни (обычно - в течение 1-2 лет), а иногда - с самого ее
начала. Отмечена положительная корреляция титра РФ и его обнаружения на ранней стадии болезни с тяжестью артрита и развитием системных проявлений. Примерно в 10-20% случаев РФ не обнаруживают ни в одном из периодов РА (серонегативные формы заболевания).
Другие признаки изменений иммунитета - LE-клетки, антиядерные антитела и антитела к гладким мышцам - обнаруживают в существенно более низком титре, чем при СКВ.
При рентгенологическом исследовании визуализируют изменения суставов. В зависимости от их выраженности выделяют четыре стадии:
• стадию I - остеопороз без деструктивных рентгенологических изменений;
• стадию II - незначительное разрушение хряща, небольшое сужение суставной щели, единичные узуры костей;
• стадию III - значительное разрушение хряща и кости, выраженное сужение суставной щели, подвывихи и девиации костей;
• стадию IV - симптомы III стадии + анкилоз.
Эта стадийность отражает временное течение заболевания: в ранней стадии изменения суставов могут отсутствовать или соответствуют I стадии, а при длительном течении болезни определяют изменения, соответствующие III-IV стадии.
Для уточнения диагноза артрита производят диагностическую пункцию сустава с последующим исследованием синовиального выпота. При РА в синовиальной жидкости за счет нейтрофилов увеличено число клеток и содержание белка, обнаруживают нейтрофилы, фагоцитирующие РФ, иммунные комплексы, содержащие РФ, а также собственно РФ.
В ряде случаев можно выполнить артроскопию в сочетании с биопсией синовиальной оболочки сустава и морфологическим исследованием. Типичный признак - пролиферация клеток синовиальной оболочки с их палисадообразным расположением по отношению к наложениям фибрина. Другие ее изменения в виде гиперплазии ворсин, лимфоидной инфильтрации, отложений фибрина и очагов некроза регистрируют при артритах иной этиологии. Артроскопия на ранней стадии болезни позволяет отдифференцировать РА от других воспалительных заболеваний суставов.
ЭКГ и рентгенологическое исследование органов грудной клетки используют для обнаружения поражения сердца и легких при висцеральных формах РА.
На основании комплексной оценки клинических и лабораторных признаков выделяют три степени активности ревматоидного процесса:
• I степень - минимальная;
• II степень - средняя;
• III степень - высокая (табл. 8-1).
На основании выраженности суставного синдрома и внесуставных поражений выделяют следующие клинические формы РА:
• преимущественно суставную;
• суставно-висцеральную;
• сочетание РА с другими диффузными заболеваниями соединительной ткани или поражением суставов;
• ювенильный РА.
Таблица 8-1. Клинико-лабораторные критерии активности ревматоидного артрита
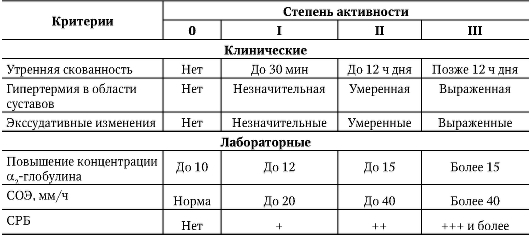
Преимущественно суставную форму регистрируют у 80% больных. У 66% пациентов она протекает в виде хронического прогрессирующего полиартрита, у 14% - в виде олиго- и моноартрита с подострым течением, поражением одного-двух крупных суставов (чаще - коленных) и небольшой их деформацией.
Суставно-висцеральную форму диагностируют в 12-13% случаев. Она протекает с поражением внутренних органов и выраженными общими реакциями в виде лихорадки, снижения массы тела, анемии и высокой активности лабораторных показателей (острофазовых и иммунологических).
РА может сочетаться с другими заболеваниями соединительной ткани, в том числе с ревматизмом, а также развиваться на фоне уже имеющегося деформирующего ОА.
Ювенильный РА (ЮРА) - форма РА, регистрируемая у детей в возрасте до 16 лет. При ЮРА отмечают острое начало заболевания с высокой лихорадкой, внесуставными нарушениями (васкулит с поражением внутренних органов), значительными иммунными изменениями. Отмечают поражение преимущественно крупных суставов (моно-, олигоартрит) с частым вовлечением в патологический процесс позвоночника. Часто обнаруживают поражение глаз (увеит). РФ определяют редко. Прогноз и течение более благоприятны, чем при РА у взрослых. Нередко отмечают трансформацию заболевания в РА взрослых или болезнь Бехтерева (ББ).
На основании темпа развития патологического процесса следует выделять медленно прогрессирующий, быстро прогрессирующий и малопрогрессирующий (доброкачественный) РА.
На основании динамического исследования активности РА условно выделяют следующие варианты заболевания.
• Легкие:
- артралгии;
- припухлость (болезненность) 3-5 суставов;
- внесуставные симптомы отсутствуют;
- РФ отсутствует или определяют в низком титре;
- СОЭ и (или) СРБ в пределах нормы или умеренно повышены;
- отсутствие патологических изменений при рентгенологическом исследовании.
• Умеренно тяжелые:
- артрит 6-20 суставов;
- отсутствие внесуставных симптомов (в большинстве случаев);
- РФ в высоком титре;
- СОЭ и (или) СРБ стойко изменены;
- при рентгенологическом исследовании - остеопения, умеренное сужение межсуставных щелей, небольшие единичные эрозии.
• Тяжелые:
- артрит более 20 суставов;
- быстрое развитие нарушений функций суставов;
- стойкое значительное увеличение СОЭ и СРБ;
- анемия, связанная с хроническим воспалением;
- гипоальбуминемия;
- РФ в высоком титре;
- при рентгенологическом исследовании определяют быстрое образование новых эрозий;
- экстраартикулярные симптомы отсутствуют.
Осложнения
Поражение внутренних органов (легкие, сердце), разрывы сухожилий, а также синдромы Шегрена и Фелти считают частью собственно РА. В качестве осложнений рассматривают амилоидоз почек и присоединение септического артрита.
Амилоидоз гистологически обнаруживают в 20-25% случаев РА. Клинически он манифестирует существенно реже и скорее связан с длительностью заболевания, чем с возрастом и полом. Наиболее характерный признак - протеинурия, которую можно определить случайно. Иногда на существование амилоидоза указывает высокая СОЭ и анемия при клинически неактивном РА. Также можно обнаружить спленомегалию и синдром нарушенного всасывания. Диагноз ставят после морфологического исследования (биопсия слизистой оболочки десны или прямой кишки). Высокой диагностической ценностью обладает биопсия почек.
Гломерулонефрит обнаруживают достаточно часто (35-60%), но он манифестирует незначительной протеинурией и микрогематурией (изолированный мочевой синдром) без повышения АД и отечного синдрома.
Септический артрит чаще всего регистрируют у лиц, получавших лечение глюкокортикоидами. Высокая температура тела, увеличение объема сустава и признаки воспалительного процесса (отек, гиперемия, резкая болезненность) указывают на необходимость проведения с диагностической целью немедленной аспирации экссудата. При микроскопическом исследовании экссудата обнаруживают большое количество нейтрофилов. При развитии септического артрита все острофазовые показатели значительно изменяются.
Диагностика
• Утренняя скованность продолжительностью не менее 1 ч.
• Припухлость трех суставов и более.
• Артрит суставов кисти - припухлость лучезапястных, пястно-фаланговых или проксимальных межфаланговых суставов.
• Симметричность артрита.
• Ревматоидные узелки.
• Обнаружение РФ в крови.
• Рентгенологические изменения, типичные для РА.
В соответствии с этими критериями диагноз РА достоверен при обнаружении не менее четырех критериев, при этом первые четыре из перечисленных признаков должны сохраняться не менее 6 нед (особенно важно в начальном периоде болезни).
Дифференциальная диагностика
РА следует дифференцировать от целого ряда заболеваний, сопровождающихся поражением суставов. Дифференциальная диагностика особенно сложна на ранней стадии болезни, когда отсутствует РФ, а также при суставновисцеральной форме заболевания.
РА следует дифференцировать от ревматического полиартрита, деформирующего ОА, суставного синдрома при СКВ, склеродермии, ББ, псориатического артрита и болезни Рейтера.
При ОРЛ (ревматизме) артрит отличается летучестью и поражением крупных суставов. Назначение противоревматических препаратов (ацетилсалициловая кислота, фенилбутазон, индометацин) быстро купирует суставные изменения. На первое место выступает поражение сердца: при первичной атаке порок еще не сформирован, но признаки ревмокардита отчетливо выражены. В дебюте РА суставной синдром не склонен к быстрому обратному развитию при лечении НПВС, сердце не поражено. При рецидивах ревматического полиартрита порок сердца обычно уже отчетливо сформирован, причем, если существует стеноз устья аорты или митрального клапана, то РА полностью исключают. Существование митральной или аортальной недостаточности не исключает РА, но гемодинамические изменения при пороке, развившемся при РА, весьма незначительны в отличие от порока сердца ревматического происхождения. Наконец, суставные изменения при ревматизме полностью обратимы, чего не бывает при РА.
При ОА преимущественно происходит поражение дистальных межфаланговых суставов с образованием около них костных разрастаний (узелки Гебердена), а также голеностопных и коленных суставов. В дальнейшем возможно поражение тазобедренных суставов и суставов позвоночника. Заболевание развивается у лиц среднего и пожилого возраста, часто - в сочетании с нарушением жирового обмена. Боли возникают при нагрузке и стихают в покое, утренней скованности нет. Острофазовые показатели отсутствуют. При рентгенологическом исследовании обнаруживают изменения, не свойственные РА (разрастание костной ткани - остеофиты, подхрящевой остеосклероз, сужение суставной щели и кистевидные просветления в эпифизах).
Суставной синдром при СКВ и ССД не считают основным признаком. В отличие от РА, при этих заболеваниях на первое место выступают изменение кожи, наиболее характерное для ССД, а также поражение внутренних органов (особенно при СКВ). При СКВ и ССД обычно выражен миозит, нередко возникает синдром Рейно (особенно при ССД) и мышечно-висцеральный синдром (нарушение акта глотания при ССД), чего обычно не бывает при РА. Рентгенологические изменения суставов при СКВ и ССД незначительны, но отличаются от таковых при РА.
Наконец, при СКВ существенно выражены иммунологические изменения, не выраженные в такой степени при РА. Динамическое наблюдение за больными позволяет обнаружить преимущественное поражение суставов при РА, висцериты и кожные поражения - при СКВ и ССД.
Анкилозирующий спондилоартрит характеризуется поражением мелких суставов позвоночника, распространяющимся снизу вверх в определенной последовательности: сакроилеальные суставы, поясничный, грудной и шейный отдел позвоночника. Заболевание манифестирует упорными болями в спине и ограничением подвижности позвоночника. Трудности дифференциальной диагностики возникают при так называемой периферической форме болезни, когда отмечают преимущественное поражение нижних конечностей (коленных, голеностопных и тазобедренных суставов). Островоспалительные признаки, как правило, выражены незначительно. Болезнь начинается постепенно, исподволь. При дифференциальной диагностике следует обратить внимание на поражение позвоночника, особенно илеосакрального отдела. ББ преимущественно страдают молодые мужчины. Заболевание генетически детерминировано: у 90-97% пациентов определяют антиген гистосовместимости HLA В-27, тогда как в популяции его обнаруживают у 5-10% лиц.
Псориатический артрит возникает примерно у 5% больных псориазом. Характерно поражение дистальных суставов кистей и стоп, но возможны изменения и других суставов (включая позвоночник). Обострение кожного процесса обычно сопровождается увеличением тяжести полиартрита. Трудность диагностики обусловлена тем, что кожное поражение может ограничиться образованием единичных бляшек, для обнаружения которых необходим тщательный осмотр волосистой части головы. Иногда артрит развивается раньше, чем кожное поражение. В крови РФ в основном отсутствует. Острофазовые показатели обычно выражены незначительно.
Синдром (болезнь) Рейтера - острое заболевание, характеризующееся сочетанием полиартрита, уретрита и конъюнктивита. В редких случаях отмечают кишечные расстройства и дерматит подошвенной поверхности стопы. Болезнь развивается как реакция на инфицирование хламидиями мочеполовой системы, в более редких случаях - в качестве ответа на сальмонеллезную инфекцию. Имеет значение наследственная предрасположенность к подобным реакциям. Трудность диагностики обусловлена тем, что у многих пациентов эпизод острого уретрита, конъюнктивита и кишечных расстройств бывает кратковременным или вообще отсутствует, а течение суставного синдрома стойкостью изменений, существованием достаточно выраженных местных, общих и лабораторных признаков воспаления, а также утренней скованностью напоминает таковое при РА. При проведении дифференциальной диагностики следует помнить, что
при болезни Рейтера возникает асимметричное поражение суставов нижних конечностей (коленных и голеностопных), распространяющееся снизу вверх. Артрит часто сочетается с сакроилеитом, поражением ахиллова сухожилия и подошвенным фасциитом. Изменения мелких суставов кисти практически отсутствуют. РФ в крови не обнаруживают.
Формулировка развернутого клинического диагноза должна соответствовать основным рубрикам, рабочей классификации РА и отражать:
• клинико-анатомическую характеристику (полиартрит, олиго-, моноартрит, сочетание поражения суставов с висцеритами или другими заболеваниями);
• клинико-иммунологическую характеристику (существование или отсутствие РФ);
• тяжесть болезни и характер течения (медленно или быстро прогрессирующий, малопрогрессирующий);
• степень активности;
• рентгенологическую характеристику (по стадиям);
• функциональную способность больного (сохранена, утрачена, степень утраты).
Лечение
Лечение больных РА следует начинать в специализированном стационаре, что позволяет избежать потери времени до назначения эффективного лечения. Чем раньше больной РА попадет в него, тем раньше он получит полноценное лечение.
При РА назначают комплексное лечение, направленное на ликвидацию воспалительного процесса в суставах, коррекцию иммунных нарушений, восстановление функций пораженных суставов и увеличение продолжительности жизни больных.
Современные рекомендации по лечению РА:
• базисное лечение начинают сразу после установления диагноза РА;
• его начинают с назначения наиболее эффективного препарата;
• базисную терапию продолжают неопределенно долго;
• при отсутствии эффекта от достаточного длительного применения базисного препарата следует заменить его;
• при отсутствии эффекта от монотерапии следует проводить комбинированное базисное лечение;
• базисную терапию следует начинать как можно раньше, особенно у больных с высоким титром РФ, выраженным увеличением СОЭ, поражением более 20 суставов и внесуставными нарушениями (ревматические узелки, поражение внутренних органов).
Метотрексат в настоящее время рассматривают в качестве препарата выбора. Его считают золотым стандартом лечения серопозитивного активного
РА.
Метотрексат сначала назначают в дозе 7,5 мг (пробная доза), а затем ее постепенно увеличивают до 15-25 мг/нед. Во время лечения категорически запрещают употребление алкоголя (даже малых доз) и пищевых продуктов,
содержащих кофеин. Метотрексат следует принимать в вечернее время 1 раз в неделю. Дробный прием вызывает токсические реакции в виде стоматита, поражения ЖКТ, редко - миелосупрессии. Для уменьшения выраженности побочных эффектов в день приема препарата отменяют применение НПВС (если больной их получает). Через 24 ч после приема метотрексата назначают фолиевую кислоту в дозе не менее 1 мг/сут (вплоть до следующего приема). Эффективность лечения оценивают спустя 4-8 нед. При повышении дозы метотрексата оценку токсичности проводят спустя шесть дней. Парентеральное введение используют в случае отсутствия эффекта от приема внутрь или при развитии токсических реакций.
Новый базисный препарат лефлуномид назначают в дозе 100 мг/сут в течение трех дней, а затем - по 20 мг/сут. Эффект наступает через 1-2 мес. Возможны осложнения в виде диареи, алопеции, кожной сыпи и зуда, а также в виде повышения АД.
Базисный препарат - соли золота - назначают в виде внутримышечных инъекций: пробная доза составляет 10 мг, а затем средство вводят в дозе 25- 50 мг. Ожидаемый эффект развивается через 3-6 мес. Поддерживающая доза составляет 50 мг 1 раз в 2-4 нед. Лечение солями золота рекомендовано всем больным с активным РА (как с ранним эрозивным артритом, так и в развернутой стадии заболевания) при отсутствии явных противопоказаний (поражение внутренних органов). Фактически терапию солями золота (кризотерапию) назначают пациентам, имеющим противопоказания к применению метотрексата.
Еще один базисный препарат - сульфасалазин - назначают в дозе 0,5 г/сут в два приема (после приема пищи). Дозу постепенно увеличивают до 2-3 г/сут. Ожидаемый результат лечения обычно получают через 1-2 мес. Сульфасалазин в основном применяют при низкой активности РА. Его также можно назначать больным, которым противопоказано лечение метотрексатом.
Такие цитостатические препараты, как азатиоприн, циклофосфамид, пеницилламин и циклоспорин, в настоящее время применяют редко, в первую очередь вследствие развития побочных эффектов и отсутствия достоверных данных об их влиянии на прогрессирование поражения суставов. Их назначают, главным образом, пациентам с РА, рефрактерным к метотрексату.
Аминохинолиновые препараты не назначают изолированно. Их назначением дополняют применение сульфасалазина при низкой активности РА: гидроксихлорохин назначают внутрь по 400 мг/сут в два приема (после приема пищи). Ожидаемый эффект наступает спустя 2-6 мес.
В настоящее время применяют генно-инженерный препарат, содержащий моноклональные антитела к ФНО-α, - инфликсимаб. Это средство выбора у пациентов, резистентных к лечению базисными препаратами. Инфликсимаб вызывает быструю положительную динамику клинических симптомов и лабораторных показателей (СОЭ, СРБ), а также замедляет прогрессирование деструкции суставов (независимо от пола и возраста). Разовая доза составляет 3 мг/кг. Препарат применяют повторно в той же дозе через 2 и 6 нед после первого введения, а затем - каждые 8 нед. Лечение инфликсимабом следует проводить одновременно с применением метотрексата. Другой препарат - ритуксимаб - содержит химерно-человеческие моноклональные антитела к антигену СД20+ В-лимфоцитов.
НПВС, оказывающие обезболивающее и противовоспалительное действие, назначают практически всем больным РА. Это особенно важно, так как лечебный эффект базисной терапии возникает не сразу после ее назначения. Действие этих препаратов обычно развивается в течение первых суток, но почти так же быстро прекращается после их отмены. Чаще всего используют напроксен (по 0,75-1 г/сут), диклофенак (по 100-150 мг/сут), ибупрофен (в дозе 1,2- 1,6 г), мелоксикам (по 7,5 мг 2 раза в сутки), кетопрофен (в дозе 100-300 мг/ сут в два приема), нимесулид (по 200-400 мг/сут в два приема) и целекоксиб (по 200-400 мг/сут в два приема). Существует индивидуальная чувствительность к НПВС, поэтому возможно различное лечебное действие отдельных лекарственных препаратов. НПВС не влияют на прогрессирование деструкции и прогноз заболевания.
Прием внутрь глюкокортикоидов в невысоких дозах при РА назначают исключительно редко: при выраженном воспалительном процессе в суставах, высокой лихорадке и висцеральных поражениях. Лечение прекращают, когда возникает эффект от применения длительно действующих лекарственных средств - метотрексата и препаратов золота.
Из сказанного следует, что глюкокортикоиды применяют не изолированно, а лишь в комбинации с базисными препаратами. Если воспалительный процесс в каком-либо суставе упорно сохраняется, то эффективно внутрисуставное введение глюкокортикоидов (депомедрол, метилпреднизолон, бетаметазон).
Физиотерапевтические методы (фонофорез гидрокортизона, электрофорез гиалуронидазы, тепловые процедуры) способствуют уменьшению местного воспалительного процесса в суставах. Положительный эффект при болях и признаках воспаления также оказывают аппликации диметилсульфоксида в сочетании с растворами НПВС на наиболее пораженные суставы.
Кроме медикаментозных и физиотерапевтических методов применяют так называемые нестандартные методы лечения, к которым относят:
• плазмаферез - удаление плазмы крови с целью снижения содержания ЦИК;
• лейкоцитоферез - удаление лимфоцитов;
• наружное или внутрисуставное облучение пораженных суставов лазерным лучом низкой мощности с целью воздействия на синовиальную оболочку;
• криотерапию (воздействие на суставы сверхнизких температур) с целью уменьшения выраженности воспалительного процесса в суставе;
• хирургические методы лечения (ранняя синовэктомия, реконструктивные операции, замена пораженного сустава протезом).
Прогноз
Ожидаемая продолжительность жизни больных РА на три года ниже средней у женщин, и на семь лет - у мужчин. Тем не менее, поскольку причины смерти больных РА не отличаются от таковых в общей популяции, этот диагноз в большинстве случаев не фигурирует среди причин смерти. Смертность больных РА выше, чем в общей популяции. Ее основные причины - инфекционные и респираторные заболевания, поражение почек и ЖКТ. Прогноз в отношении восстановления функций сустава делают неблагоприятным следующие факто-
ры: возникновение заболевания в молодом возрасте, сохранение активности процесса более одного года, высокий титр РФ и образование ревматоидных узелков.
Профилактика
Профилактика заключается в предупреждении обострений заболеваний и дальнейшего прогрессирования поражения суставов. В отношении родственников больного возможно проведение первичной профилактики, состоящей в предупреждении переохлаждений и тщательном лечении интеркуррентных инфекционных заболеваний.
ОСТЕОАРТРОЗ
Остеоартроз (ОА) - гетерогенная группа заболеваний различной этиологии со сходными биологическими, морфологическими и клиническими признаками и исходом, в основе которых лежит поражение всех компонентов сустава, в первую очередь хряща, субхондральной кости, синовиальной оболочки, связок, капсулы и периартикулярных мышц.
Дегенерация суставного хряща - нормальный физиологический процесс, возникающий у 100% лиц в возрасте старше 60 лет. Этапы возрастной дегенерации хрящевой ткани:
• уменьшение содержания хондроитинсульфата, приводящее к изменению гидродинамических свойств хряща и скорости диффузии питательных веществ;
• замещение основного вещества хряща соединительной тканью вследствие гибели хондроцитов;
• потеря эластичности и упругости хряща;
• разволокнение хрящевой ткани, образование изъязвлений с обнажением подлежащей кости в зоне наибольшей нагрузки (обычно - в середине суставной поверхности кости).
При ОА происходит подобная описанной, но более ранняя и быстрая дегенерация хряща, сопровождающаяся изменениями окружающих тканей.
ОА - самое распространенное заболевание суставов. Заболеваемость составляет 8,2 случая на 100 тыс. населения, распространенность - 20%. ОА не приводит к смертельному исходу. Заболевание обычно начинается в возрасте старше 40 лет. Его рентгенологические признаки обнаруживают у 50% лиц в возрасте 55 лет и у 80% - в возрасте старше 75 лет. Поражение коленного сустава (гонартроз) чаще регистрируют у женщин, а тазобедренного сустава (коксартроз) - у мужчин.
Этиология
Различают первичный и вторичный ОА. Первичный ОА - преждевременное старение хряща суставов, ранее не пораженных патологическим процессом. Вторичный ОА - поражение хряща суставов, ранее подвергавшихся патологическим воздействиям.
При первичном ОА имеют значение следующие факторы:
• генетические (в семьях, где есть больные ОА, заболевание регистрируют в 2 раза чаще, чем в контрольной группе), связанные с дефектами гена коллагена II типа;
• эндокринные (в климактерическом периоде ОА развивается более быстрыми темпами);
• постоянные микротравмы суставов в результате неадекватных физических нагрузок (в частности, спортивных).
При вторичном ОА отмечают снижение резистентности хряща к физиологической нагрузке вследствие:
• травм хряща;
• врожденных нарушений статики;
• слабости мышц и связок;
• ранее перенесенных артритов;
• нарушений конгруэнтности суставных поверхностей.
Патогенез
При ОА все этапы возрастной дегенерации хряща протекают быстрее и в более молодом возрасте. В патогенезе ОА играют роль три фактора:
• изменение суставных поверхностей кости (хряща и подлежащих отделов кости);
• воспаление синовиальной оболочки (реактивный синовит);
• фиброзно-склеротические изменения синовиальной оболочки.
В основе патогенеза ОА лежит нарушение нормального метаболизма хрящевой ткани с преобладанием катаболических процессов над анаболическими. Нарушение выработки медиаторов и ферментов при патологических изменениях хондроцитов включает синтез провоспалительных цитокинов, особенно ИЛ-1, под действием которого хондроциты синтезируют протеиназы, вызывающие деградацию коллагена и протеогликана хряща. Кроме того, синтезируются простагландины, принимающие участие в развитии неспецифического воспаления, и происходит избыточное образование оксида азота, также оказывающего токсическое действие на хрящ.
Основное вещество хряща (кислые и нейтральные мукополисахариды), покрывающего суставную поверхность, перерождается и местами исчезает, замещаясь плотной соединительной тканью. Хондроциты гибнут, хрящ становится тусклым, сухим, теряет эластичность, может растрескиваться и изъязвляться с обнажением подлежащей кости.
Этот процесс не тождествен эрозивному артриту при РА, при котором разрушение хряща осуществляет рыхлая соединительная ткань - паннус. При ОА субхондрально развивается остеосклероз, а на периферии суставных поверхностей возникают разрастания кости - остеофиты. Фиброзно-склеротические изменения захватывают капсулу сустава и синовиальную оболочку. Кроме того, возникают фиброзные изменения связочного аппарата, сопровождающиеся кальцификацией, что приводит к подвывихам сустава.
Реактивный синовит (воспаление синовиальной оболочки) возникает вследствие раздражения внутрисуставным детритом - кусочками некротизирован-
ного хряща. Иногда отмечают гипертрофию ворсин синовиальной оболочки с хрящевой или костной метаплазией. Отрыв таких измененных ворсин ведет к формированию суставных «мышей».
Клиническая картина
ОА регистрируют преимущественно у женщин в возрасте 40-60 лет. Основным признаком считают суставной синдром. Выделяют следующие основные формы поражения суставов при ОА:
• поражение тазобедренного сустава - коксартроз - наиболее тяжелая форма заболевания, обнаруживаемая в 40% всех случаев ОА;
• поражение коленного сустава - гонартроз - регистрируют в 33% случаев (первичная форма возникает преимущественно у женщин в климактерическом периоде, вторичная - в результате травмы сустава и нарушения статики);
• поражение дистальных межфаланговых суставов с образованием узелков Гебердена (костные разрастания в области суставов) обнаруживают у 1/3 всех больных ОА (регистрируют преимущественно у женщин в климактерическом периоде);
• поражение суставов позвоночника, межпозвоночных дисков (спондилез или остеохондроз позвоночника) и синовиальных межпозвоночных суставов (спондилоартроз).
На первом этапе диагностического поиска обнаруживают основную жалобу больного - боли в пораженном суставе и некоторое ограничение его подвижности. Боли связаны с нагрузкой на пораженный сустав, поэтому их называют механическими. Обычно они начинаются незаметно, и сначала пациенты жалуются лишь на неясные, неинтенсивные боли в пораженных суставах (одном суставе). Как правило, они возникают к концу дня и исчезают в покое. По мере развития патологических изменений в суставе боли становятся интенсивнее и длительнее, а для их возникновения достаточно небольшой физической нагрузки. Отмечают так называемые стартовые боли в начале ходьбы. Постепенно больной «врабатывается» и они стихают, но при продолжении нагрузки появляются вновь и исчезают (уменьшаются) лишь при ее прекращении. Боли в пораженных суставах (тазобедренном, позвоночнике) могут возникать при длительном пребывании в фиксированной позе - при работе сидя, длительном нахождении в вертикальном положении и др. Для уменьшения болевых ощущений пациент должен обязательно изменить позу. Причины развития болей не связаны с поражением собственно хряща, так как он лишен нервных окончаний. Их определяет поражение костей, суставов (растяжение измененной капсулы сустава и связочного аппарата, сдавление нервных окончаний фиброзной тканью капсулы сустава) и околосуставных тканей. Особое место занимает реактивный синовит (тендовагинит), обусловленный раздражением синовиальной оболочки детритом, а также воздействием неспецифических факторов - переохлаждением или чрезмерной физической нагрузкой. При развитии реактивного синовита больные отмечают отечность пораженного сустава, увеличение его объема и резкое усиление болей при движении. Иногда отмечают повышение температуры тела до субфебрильных значений.
Движения в суставе в начале развития патологического процесса слегка ограничены вследствие болей. В дальнейшем, по мере развития изменений капсулы сустава и связочного аппарата, амплитуда движений может значительно ограничиться (особенно при коксартрозе). В ряде случаев развивается так называемая блокада сустава, характеризующаяся внезапной резкой болью и практически полной невозможностью движений в суставе, что обусловлено ущемлением суставной «мыши» между суставными поверхностями. Характерный симптом ОА - крепитация (хруст, треск или скрип) в суставах при движении, возникающая вследствие нарушения конгруэнтности суставных поверхностей.
Своеобразны жалобы больных при поражении позвоночника. Они отмечают не только боли в пораженном отделе при пребывании в длительной фиксированной позе, но и болевые ощущения в других местах (например, в грудной клетке, что иногда имитирует стенокардию, а также в нижних конечностях, что сочетается со слабостью мышц бедер).
На втором этапе диагностического поиска можно обнаружить изменения в пораженных суставах. Так, дистальные межфаланговые суставы кистей становятся менее подвижными, в них развиваются анкилозы и возникают узловатые образования - узелки Гебердена, представленные костными разрастаниями. Такие же костные образования могут располагаться и в проксимальных межфаланговых суставах (узелки Бушара). Ногтевые фаланги пальцев кисти постепенно искривляются и заостряются.
В мелких суставах кисти, стопы, а также в голеностопном суставе в результате чрезмерных физических нагрузок и повторных травм могут возникать подвывихи.
В случае поражения межпозвоночных дисков и суставов позвоночника возможно возникновение болезненности при поколачивании по остистым отросткам позвонков, а также симптомов вторичного корешкового синдрома вследствие сдавления остеофитами нервных корешков.
Если поражен тазобедренный сустав, то в связи с укорочением конечности вследствие сплющивания головки бедра нарушается походка. Фиброзносклеротические изменения капсулы сустава нарушают отведение конечности. Постепенно развивается атрофия мышц бедра.
Можно обнаружить деформацию коленного сустава, вызванную утолщением и сморщиванием его капсулы и связанную с образованием остеофитов.
При пальпации определяют болезненность в медиальной части суставной щели и местах прикрепления сухожилий к костям. При развитии вторичного синовита возникает припухлость пораженного сустава, пальпация становится болезненной, а объем движений уменьшается. Снижается чувствительность кончиков пальцев, возникают парестезии и чувство онемения.
Физикальное обследование позволяет утвердиться в правильности диагноза.
На третьем этапе диагностического поиска необходимо отвергнуть ряд заболеваний, протекающих со сходным суставным синдромом, а также уточнить характер и выраженность поражения суставов.
При исследовании периферической крови не обнаруживают никаких патологических изменений. Лишь при реактивном синовите отмечают незначитель-
но выраженные острофазовые показатели (повышение СОЭ до 20-25 мм/ч и увеличение содержания СРБ).
При биохимическом и иммунологическом исследовании крови изменения отсутствуют: РФ, АНФ, LE-клеток, а также антител к гладкой мышечной ткани и ДНК нет.
При рентгенологическом исследовании суставов обнаруживают прогрессирующие изменения, нарастающие параллельно продолжительности заболевания и выраженности клинических симптомов. Выделяют четыре стадии рентгенологических изменений:
• стадия I - нормальная суставная щель, остеофиты выражены незначительно;
• стадия II - выраженные остеофиты, незначительное сужение суставной щели;
• стадия III - множественные остеофиты, явное сужение суставной щели, умеренная деформация суставных поверхностей кости, субхондральный остеосклероз;
• стадия IV - резко выраженные многочисленные остеофиты и сужение суставной щели, глубокий остеосклероз, значительная деформация суставных поверхностей.
При поражении позвоночника отмечают следующие варианты поражения:
• спондилез - по краям тел позвонков образуются шипы - так называемые остеофиты;
• спондилоартроз - поражение суставов позвоночника (как известно, каждый грудной позвонок имеет четыре межпозвоночных и два позвоночнореберных сустава);
• остеохондроз - поражение межпозвоночных дисков, нередко - с формированием грыж Шморля и пролабированием пульпарного ядра межпозвоночного диска в том или ином направлении.
Диагностика
ОА диагностируют на основании обнаружения характерных клинических признаков (боль, скорость развития болезни, характер поражения определенных суставов) и данных рентгенологического исследования. При установлении диагноза необходимо учитывать возраст больного, пол и факторы, способные стать причиной возникновения ОА.
Институтом ревматологии Российской Федерации (1993) предложены критерии ОА.
• Клинические критерии:
- боли в суставах, возникающие в конце дня и (или) в первой половине ночи;
- боли в суставах, возникающие при физической нагрузке и уменьшающиеся в покое;
- деформация сустава вследствие костных разрастаний (включая узелки Гебердена и Бушара).
• Рентгенологические критерии:
- сужение суставной щели;
- остеосклероз;
- остеофитоз.
Первые два критерия в каждой группе считают основными, а третьи - дополнительными. Для установления диагноза ОА обязательно обнаружение первых двух клинических и рентгенологических критериев.
Вместе с тем необходимо исключить ряд заболеваний, при которых поражение суставов напоминает клиническую картину ОА. В первую очередь необходимо исключить РА у лиц пожилого возраста. В основе дифференциальной диагностики лежат следующие признаки. Поражение крупных суставов при РА возникает после длительного периода болезни. Собственно РА дебютирует поражением мелких суставов кисти и стопы (проксимальных межфаланговых, но не дистальных, что типично для ОА). Узелки Гебердена иногда принимают за ревматоидные узелки, но для последних характерна другая локализация (под кожей локтевых суставов). Во время исследования синовиальной жидкости при ОА признаков воспаления, характерных для РА, не обнаруживают, а при биопсии синовиальной оболочки определяют фиброз и незначительную клеточную инфильтрацию.
Формулировка развернутого клинического диагноза должна учитывать:
• локализацию поражения;
• фазу заболевания (обострение, ремиссия);
• существование вторичных изменений в мышцах, нервных корешках и др. Лечение
Лечение ОА продолжает оставаться сложной и недостаточно решенной задачей .
Назначают комплексное лечение, преследующее цели:
• замедление прогрессирования патологического процесса;
• уменьшение выраженности боли - основной причины обращения больного к врачу;
• нормализация обменных процессов в суставном хряще;
• улучшение функций пораженных суставов.
Поскольку увеличенная масса тела и снижение тонуса мышц - факторы риска развития и прогрессирования ОА, нормализация массы и укрепление мышц - важные направления лечения заболевания.
Ликвидацию болевого синдрома обеспечивает назначение ненаркотических анальгетиков центрального действия (парацетамол), НПВС и так называемых хондропротекторов.
При умеренных болях без признаков воспаления (синовит) следует периодически назначать ненаркотический анальгетик центрального действия (парацетамол в дозе до 4 г/сут). Его преимущество перед НПВС состоит в меньшей вероятности развития побочных эффектов со стороны ЖКТ.
У больных с выраженными постоянными болями, часто связанными не только с механическими факторами, но и воспалением (синовит), препаратами выбора считают НПВС. Наиболее предпочтительно использование ибупрофена (по 1200-1400 мг/сут), кетопрофена (по 100 мг/сут) и диклофенака (по 100 мг/ сут). НПВС оказываются эффективными при использовании в меньших дозах,
чем при лечении РА. Рациональным считают начало лечение с назначения полной дозы. При достижении обезболивающего эффекта ее снижают до необходимой поддерживающей. При улучшении состояния прием НПВС отменяют, но при обострении их назначают повторно. Применение пироксикама и индометацина не рекомендовано в связи с тем, что они ослабляют действие других препаратов, которые может принимать пожилой пациент (например, антигипертензивных средств). Кроме того, индометацин оказывает хондродеструктивное действие, и его прием может способствовать прогессированию дегенерации хряща. У пожилых больных, принимающих НПВС, следует учитывать возможность развития эрозивного гастрита, поэтому рекомендовано назначение препаратов, вызывающих селективную блокаду циклооксигеназы-2 (ЦОГ-2), - мелоксикам (по 7,5 мг/сут) или целекоксиб (в дозе 100-200 мг/сут).
Трамадол (опиоидный анальгетик) применяют в течение короткого времени для купирования сильной боли при неэффективности парацетамола или НПВС, а также при невозможности назначения оптимальных доз этих лекарственных средств. Трамадол назначают в дозе 50 мг/сут с ее постепенным увеличением до 200-300 мг/сут.
Обезболивающий эффект оказывают аппликации диметилсульфоксида на пораженный сустав (особенно с добавлением раствора НПВС).
Кроме того, выполняют внутрисуставное введение различных препаратов:
Внутрисуставное введение глюкокортикоидов рекомендовано при ОА, сопровождающемся симптомами воспаления. Эффект лечения (уменьшение боли и симптомов воспаления) продолжается от 1 нед до 1 мес. Применяют метилпреднизолон (в дозе 20-40 мг) и триамцинолон (в дозе 20-40 мг). Частота введения не должна превышать 2-3 раз в год.
Производные гиалуроната для внутрисуставного введения (остеонил) уменьшают боли в коленных суставах. Эффект продолжается от 3 до 12 мес.
Весьма эффективными препаратами считают естественные компоненты суставного хряща (хондропротекторы) - хондроитина сульфат и глюкозамин.
Хондроитина сульфат применяют длительно (возможны повторные курсы) в дозе 1000-1500 мг/сут в 2-3 приема, что позволяет снизить дозу НПВС. Сходной эффективностью и переносимостью обладает глюкозамин, который назначают в дозе 1500 мг/сут однократно в течение не менее 6 мес (повторными курсами).
Хондропротектор афлетоп вводят в коленный сустав 2 раза в неделю (всего - пять введений). Его применение комбинируют с приемом внутрь 2-3 таблеток хондроитина сульфата + глюкозамина (в дозе 500 мг + 500 мг в сутки). Хондроитина сульфат + глюкозамин принимают в течение полугода. Такой комбинированный курс проводят до 2 раз в год.
Внутрь сустава 1 раз в неделю вводят препарат гиалуроновой кислоты суплазин (курс - три введения). Суплазин также комбинируют с приемом внутрь хондроитина сульфата + глюкозамина (не менее полугода).
Улучшения функций пораженных суставов достигают использованием физиотерапевтических методов лечения: ЛФК, тепловых (парафиновые аппликации, озокерит) и электропроцедур (токи УВЧ или ультразвук на область пораженных суставов). Также применяют электрофорез гиалуронидазы и ка-
лия йодида*, способствующий рассасыванию фиброзной ткани капсулы сустава и прикрепляющихся к суставу сухожилий.
После стихания обострения и уменьшения болей хороший эффект оказывает санаторно-курортное лечение (лечебные грязи, радиоактивные или сульфидные ванны).
Достаточно эффективным считают хирургическое лечение (артроскопические операции для удаления хрящевого детрита). Эндопротезирование тазобедренного или коленного сустава проводят только при тяжелом инвалидизирующем поражении этих сочленений.
Прогноз
ОА (особенно первичный) редко приводит к потере трудоспособности, но при локализации процесса в тазобедренном суставе вследствие быстро прогрессирующего ограничения движений больной становится инвалидом.
Профилактика
Первичная профилактика сводится к борьбе с внешними факторами, которые могут способствовать развитию дегенеративных изменений в суставном хряще (предупреждение постоянных микротравм суставов и длительной функциональной перегрузки, нормализация массы тела и др.).
ПОДАГРА
Подагра - заболевание, обусловленное нарушением обмена пуринов, характеризующееся гиперурикемией, рецидивирующим острым, а в дальнейшем и хроническим артритом и поражением почек.
Сущность заболевания состоит в нарушении обмена мочевой кислоты, в результате чего в суставах и околосуставной клетчатке откладываются кристаллы мононатриевых уратов, что приводит к развитию артрита. Кроме того, отмечают избыточное образование уратных камней в лоханках почек и мочевыводящих путях, а также развитие интерстициального нефрита.
Увеличение содержания в организме мочевой кислоты обусловлено тремя механизмами:
• метаболическим - увеличением синтеза мочевой кислоты;
• почечным - снижением экскреции мочевой кислоты почками;
• смешанным - умеренным увеличением синтеза мочевой кислоты в сочетании со снижением ее экскреции почками.
Все эти механизмы нарушения обмена мочевой кислоты принимают участие в развитии подагры.
Гиперурикемию обнаруживают у 4-12% населения, но подагрой страдает 0,1-1% населения. Частота развития подагрического артрита в различных популяциях колеблется и составляет от 5 до 50 случаев на 1000 мужчин и 1-9 случаев на 1000 женщин. Риск возникновения подагры нарастает по мере увеличения содержания мочевой кислоты. Пик заболеваемости приходится на возраст около 40-50 лет у мужчин и старше 60 лет - у женщин (до менопаузы женщины практически не болеют подагрой). Соотношение мужчин и женщин
среди пациентов составляет 2-7:1. Острый приступ подагры у подростков и у лиц молодого возраста возникает редко. Обычно он обусловлен первичным или вторичным дефектом синтеза мочевой кислоты.
Этиология
Различают первичную и вторичную подагру.
Первичная (идиопатическая) подагра - наследственное заболевание, детерминированное одновременным действием нескольких патологических генов. Кроме наследственной предрасположенности, в ее развитии играет роль алиментарный фактор - повышенное употребление с пищей продуктов с избыточным содержанием пуринов, жиров, углеводов и алкоголя.
Вторичная подагра - результат гиперурикемии, возникающей при некоторых заболеваниях: гемобластозах, новообразованиях, болезнях почек, сердечной недостаточности, некоторых обменных и эндокринных заболеваниях, а также при приеме лекарственных препаратов, способствующих повышению концентрации мочевой кислоты в крови (диуретики, салицилаты, цитостатические препараты, глюкокортикоиды).
Патогенез
При подагре отмечают нарушение соотношения синтеза и выделения мочевой кислоты из организма.
Вследствие генетически обусловленного нарушения функции ферментов, участвующих в метаболизме пуринов (снижение активности или отсутствие глюкозо-6-фосфатазы, гипоксантинфосфорибозилтрансферазы и др.), повышается синтез мочевой кислоты и возникает постоянная гиперурикемия. С другой стороны, снижается экскреция уратов почками. В результате этих процессов в организме происходят накопление и отложение уратов преимущественно в соединительной ткани суставов, почек и других тканей.
Под влиянием уратных кристаллов происходит стимуляция фагоцитами, синовиальными клетками и другими компонентами сустава провоспалительных медиаторов (ИЛ-1, ФНО-α, ИЛ-8, ИЛ-6, фосфолипаза А2, анафилотоксины и др.). В результате нейтрофилы проникают в полость сустава, где происходит фагоцитоз кристаллов. Уратные кристаллы повреждают лизосому нейтрофила, способствуя дальнейшему выходу лизосомальных ферментов и развитию воспаления. Основные звенья патогенеза подагры представлены на рис. 8-1.
Клиническая картина
Клиническая картина заболевания представлена различными синдромами.
• Рецидивирующие атаки острого подагрического артрита (чаще всего - моноартрита). В основе острого артрита лежит острая преципитация кристаллических уратов в синовиальной жидкости с их последующим фагоцитозом нейтрофилами. Фагоцитирующие лейкоциты в дальнейшем разрушаются, и в полость сустава проникает множество лизосомальных ферментов, вызывающих воспалительную реакцию синовиальной обо-
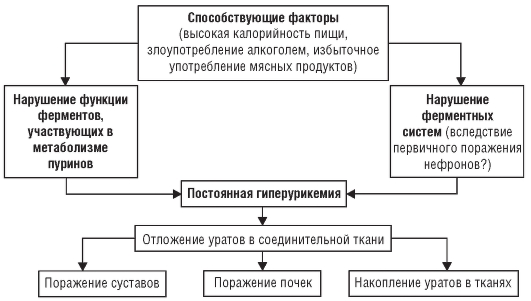
Рис. 8-1. Патогенез подагры
лочки и периартикулярных тканей - артрит. В развитии поражения суставов выделяют:
- межприступную (интервальную) подагру;
- хроническую тофусную подагру.
• Поражение почек в виде мочекаменной болезни и подагрической почки (интерстициальный нефрит, редко - диффузный гломерулонефрит). В основе подагрической почки лежит отложение уратов или мочевой кислоты в мозговом, реже - корковом веществе почки. Отложения носят очаговый характер и располагаются в межуточной ткани. Вокруг них развивается воспалительная реакция. Поражение клубочков обнаруживают редко. Оно характеризуется утолщением стенок капилляров, клеточной пролиферацией, гиалиновыми отложениями и склерозом клубочков.
• Поражение периферических тканей (отложение уратов, формирующих специфические для подагры подагрические узлы). Подагра достаточно часто сочетается с другими заболеваниями обмена веществ: сахарным диабетом, нарушением жирового обмена, а также атеросклерозом и ГБ.
Ha первом этапе диагностического поиска можно получить информацию о начале заболевания, характерных признаках острого подагрического артрита и о дальнейшем вовлечении суставов в патологический процесс, а также о существовании и выраженности почечного синдрома.
Подагра чаще всего манифестирует атаками острого подагрического артрита, часто возникающими на фоне полного здоровья у мужчин в возрасте старше 30 лет. Факторы, провоцирующие приступ: переохлаждение, легкая травма, длительная ходьба, злоупотребление алкоголем или обильной мясной жирной пищей, интеркуррентные инфекционные заболевания. Приступ начинается внезапно (чаще - ночью) и манифестирует резкими болями в плюснефаланговом суставе большого пальца (реже - в других суставах) стопы, голеностопном,
коленном, локтевом и крайне редко - в лучезапястном суставе. Сильные боли возникают в покое и усиливаются при опускании конечности. На высоте болей возможно повышение температуры тела до 38-39 °С. Сустав опухает, кожа над ним приобретает синевато-багровый цвет. Приступ продолжается от 3 до 10 дней, после чего боли полностью исчезают, функция сустава восстанавливается, а внешне он приобретает нормальную форму. С течением времени отмечают укорочение межприступных периодов с увеличением продолжительности суставных болей. В патологический процесс вовлекаются и другие суставы. С годами больные отмечают деформацию и ограничение подвижности суставов (преимущественно - нижних конечностей). При вовлечении в патологический процесс почек (развитие мочекаменной болезни) возникают приступы почечной колики, сопровождающиеся всеми характерными признаками; периодически происходит отхождение камней.
На втором этапе диагностического поиска во время приступа обнаруживают характерные признаки острого подагрического артрита: припухлость сустава, резкую болезненность при пальпации и изменение цвета кожи над суставом. В межприступном периоде все суставные изменения исчезают.
Со временем нарастают стойкие изменения в суставах конечностей (чаще - нижних) и возникают признаки хронического полиартрита: возникает дефигурация, ограничение подвижности сустава, деформация вследствие узелковых отложений и костных разрастаний, подвывихи пальцев, контрактуры и грубый хруст в коленных и голеностопных суставах. Больные утрачивают трудоспособность и с трудом передвигаются.
При длительности заболевания более 3-5 лет образуются тофусы - специфические для подагры узелки, представленные отложением уратов и окруженные соединительной тканью. Они локализуются преимущественно на ушных раковинах и локтях, реже - на пальцах кистей и стоп. Тофусы иногда размягчаются и самопроизвольно вскрываются с образованием свищей, через которые выделяется беловатая масса (кристаллы мочекислого натрия). Инфицирование свищей происходит редко. При развитии подагрической почки возникает АГ. Подагра располагает к развитию нарушений жирового обмена и атеросклероза, способствует прогрессированию ГБ и других заболеваний сердечно-сосудистой системы (например, ИБС).
На третьем этапе диагностического поиска можно:
• подтвердить характерное поражение суставов;
• обнаружить поражение почек;
• детализировать степень нарушений пуринового обмена.
При рентгенологическом исследовании пораженных суставов обнаруживают изменения, развивающиеся при тяжелом течении, большой длительности болезни и дебюте артрита в молодом возрасте. Наиболее значимые изменения:
• круглые («штампованные») дефекты эпифизов костей, окруженные склеротической каймой;
• кистовидные дефекты, разрушающие кортикальный слой кости;
• утолщение и расширение тени мягких тканей в связи с отложением в них уратов.
Поражение почек - подагрическая почка - манифестирует протеинурией и цилиндрурией (обычно - незначительной). В случае развития мочекаменной
болезни при умеренной протеинурии отмечают гематурию и большое количество кристаллов мочевой кислоты в осадке. После приступа почечной колики гематурия усиливается.
Почечная недостаточность при поражении почек развивается редко. Ее признаком служат повышение концентрации креатинина в крови, резкое снижение фильтрации и относительная плотность мочи ниже 1015.
Нарушение пуринового обмена представлено гиперурикемией (0,24- 0,50 ммоль/л или 4-8,5 мг в 100 мл мочи).
Во время приступа подагрического артрита отмечают присутствие в крови острофазовых показателей (нейтрофильный лейкоцитоз, увеличение СОЭ, повышение содержания фибриногена, α2-глобулина и СРБ), исчезающих после купирования приступа.
Диагностика
Диагностика заболевания основана на обнаружении характерных приступов суставных болей, подагрических тофусов, гиперурикемии, кристаллов солей мочевой кислоты в синовиальной жидкости и характерных рентгенологических изменений.
В настоящее время для установления диагноза применяют так называемые классификационные критерии:
• обнаружение характерных кристаллов в суставной жидкости;
• обнаружение тофусов, содержащих мочевую кислоту, что подтверждают химическим методом или с помощью поляризационной микроскопии;
• обнаружение шести из 12 нижеперечисленных признаков:
- более одной атаки острого артрита в анамнезе;
- воспаление сустава достигает максимума в первый день болезни;
- моноартрит;
- гиперемия кожи над пораженным суставом;
- припухание и боль в первом плюснефаланговом суставе;
- одностороннее поражение первого плюснефалангового сустава;
- одностороннее поражение суставов стопы;
- подозрение на тофусы;
- гиперурикемия;
- асимметричный отек суставов;
- субкортикальные кисты без эрозий (при рентгенографии);
- отрицательные результаты посева синовиальной жидкости.
Шесть клинических критериев и более обнаруживают у 88% больных подагрой, менее чем у 3% больных септическим артритом и у 11% пациентов с пирофосфатной артропатией.
Дифференциальная диагностика
Подагру необходимо дифференцировать от ряда заболеваний, манифестирующих как острым, так и хроническим поражением суставов. В основе дифференциальной диагностики лежат следующие особенности подагры и заболеваний со сходной клинической картиной.
Типичные для ОА узелки Гебердена иногда расценивают как подагрические тофусы, но при ОА узелки обнаруживают в области дистальных межфаланго-
вых суставов пальцев рук, где тофусы не локализуются. В отличие от тофусов, узелки Гебердена имеют плотную консистенцию. Кроме того, при ОА прежде всего происходит поражение крупных суставов (тазобедренного и коленного), тогда как при подагре - плюснефаланговых (97%) и голеностопных (50%). Изменение коленных суставов регистрируют реже (в 36% случаев). В анамнезе при ОА нет типичных приступов острого артрита.
От тофусов необходимо дифференцировать и ревматоидные узелки, особенно если РА протекает с поражением плюснефаланговых суставов больших пальцев стоп. Необходимость дифференциальной диагностики с РА также возникает при длительном течении подагры, вовлечении в патологический процесс множества суставов и развитии их деформации. Различие вполне очевидно: при подагре болезнь обычно дебютирует атаками острого артрита типичной локализации (первый плюснефаланговый или мелкие суставы стопы), отсутствует РФ и существуют типичные рентгенологические изменения. В то же время РА начинается с поражения суставов кисти, болезнь часто дебютирует в молодом возрасте, при длительном течении развивается мышечная атрофия, отсутствует гиперурикемия, а рентгенологические признаки имеют другие особенности. Ревматоидные узлы никогда не вскрываются, тогда как тофусы часто вскрываются с выделением беловатой крошковатой массы.
Острый приступ подагрического артрита нередко напоминает острый ревматический полиартрит, но отличить подагру от ревматизма сравнительно нетрудно. Ревматизм регистрируют преимущественно у детей и подростков (реже - у взрослых), а подагра дебютирует у лиц в возрасте около 40 лет. Для ревматизма характерны поражение сердца и высокий титр противострептококковых антител.
В ряде случаев возникает необходимость в дифференциальной диагностике подагрического артрита и артроза первого плюснефалангового сустава. Деформирующий ОА указанной локализации развивается часто, сочетаясь с плоскостопием, нарушением жирового обмена и варикозным расширением вен нижних конечностей. Он манифестирует болями при ходьбе, образованием остеофитов в области эпифиза плюсневой кости и постепенным искривлением большого пальца стопы. При повторном повреждении сустава (длительная ходьба, ношение узкой обуви) могут развиться реактивный синовит первого плюснефалангового сустава и воспаление периартикулярных тканей. В отличие от подагрического артрита, признаки воспаления возникают постепенно, выражены умеренно и представлены слабым отеком и небольшой гиперемией. Боли нерезкие, нет нарушения общего состояния, острофазовые признаки воспаления отсутствуют, температура тела не повышается. На рентгенограмме выражены признаки ОА.
Лечение
Назначают комплексное лечение, включающее:
• нормализацию пуринового обмена;
• купирование острого приступа подагрического артрита;
• восстановление функции пораженных суставов (лечение хронического полиартрита).
Нормализацию пуринового обмена осуществляют с помощью системы мероприятий, в число которых входят:
• нормализация питания;
• ликвидация факторов, способствующих гиперурикемии;
• длительный прием лекарственных препаратов, способствующих снижению синтеза мочевой кислоты в организме и ее повышенному выделению почками.
Тучным больным необходимо похудеть, так как ожирение закономерно сочетается с увеличением продукции уратов и одновременным уменьшением их выделения почками.
Больным категорически запрещено употреблять алкоголь, который при частом приеме вызывает гиперурикемию. Полагают, что молочная кислота - конечный продукт метаболизма этилового спирта - замедляет выделение уратов почками.
Необходимо ограничить употребление продуктов, богатых пуринами (мясо, рыба, печень, почки, бобовые), и принимать достаточное количество жидкости (более 1500 мл/сут), так как выделение менее 1 мл/мин (1400 мл/сут) мочи приводит к уменьшению выведения уратов.
Почти у 40% больных подагрой регистрируют АГ, поэтому следует помнить, что применение для нормализации АД тиазидных диуретиков у больных подагрой способствует повышению содержания в крови мочевой кислоты. Не следует назначать им ацетилсалициловую кислоту, так как при этом нарастает содержание мочевой кислоты в крови, что может спровоцировать приступ подагрического артрита.
В ряде случаев проведения указанных мероприятий бывает достаточно для профилактики приступов артрита и уменьшения выраженности урикемии, но отдельным больным приходится назначать лекарственные препараты, нормализующие пуриновый обмен. В противном случае возникает риск развития АГ и нарушений функций почек, а также риск развития мочекаменной болезни. Кроме того, нелеченая подагра способствует развитию атеросклероза.
При решении вопроса о выборе препарата для длительного антиподагрического лечения необходимо учитывать механизмы, обусловливающие повышение концентрации мочевой кислоты в крови. При гиперпродукции пуринов следует назначать антагонисты синтеза пуринов, при уменьшении их выделения - урикозурические препараты. Больным с нормальным выделением пуринов рекомендуют средства обоих механизмов действия.
Одно из урикозурических средств - сульфинпиразон8. Увеличения выделения мочевой кислоты достигают за счет подавления ее реабсорбции в почечных канальцах. Начальная доза составляет 50 мг 3 раза в сутки. Дозу постепенно увеличивают (обычно до 200-400 мг/сут) до нормализации концентрации уратов в крови. При лечении сульфинпиразоном8 для уменьшения риска образования камней в почках больному следует принимать сравнительно много жидкости (2-3 л/сут). Побочные явления: тошнота, рвота, кожные аллергические реакции, лейкопения. Применение препарата противопоказано при язвенной болезни желудка и двенадцатиперстной кишки. Сульфинпиразон8 нельзя назначать при гиперпродукции уратов, снижении клубочковой фильтрации, подагрической нефропатии и мочекаменной болезни.
Среди средств, уменьшающих синтез пуринов, лучшим считают аллопуринол. Его назначают в стартовой дозе 100 мг/сут с постепенным увеличением дозы до 300 мг/сут. Если клубочковая фильтрация снижена до 30-60 мл/мин, то доза аллопуринола не должна превышать 100 мг/сут, а при клубочковой фильтрации 60-90 мл/мин она не должна быть более 200 мг/сут.
Лечение аллопуринолом рекомендовано при выраженной гиперпродукции уратов (особенно у больных с урикемией более 0,6 ммоль/л), подагрических узелках, подагре, сопровождающейся почечной недостаточностью, вторичной подагре с избыточным образованием мочевой кислоты (у больных лейкозами, множественной миеломой, эритремией), острой нефропатии, вызванной отложением мочевой кислоты в результате лечения новообразований цитостатическими средствами, а также больным, страдающим образованием уратных камней.
При длительном лечении аллопуринолом возможны обратное развитие уратных отложений в тканях и улучшение функций почек. Больные хорошо переносят препарат, но у ряда из них могут возникать кожные изменения и симптомы раздражения ЖКТ.
Указанные препараты назначают лишь после полного купирования острого подагрического артрита, так как их применение на фоне затихающего воспаления суставов может вызвать серьезное обострение артрита.
При первичной подагре аллопуринол следует принимать пожизненно, при вторичной - в зависимости от устранения конкретной провоцирующей ситуации. Перерывы в лечении ведут к рецидиву заболевания.
Эффективность антигиперуремического лечения определяется нормализацией содержания мочевой кислоты в крови (менее 360 мкмоль/мл), уменьшением частоты приступов подагры, рассасыванием тофусов и отсутствием прогрессирования уролитиаза.
Острый приступ подагрического артрита купируют назначением колхицина, который принимают внутрь в дозе 0,5-0,6 мг каждый час до стихания признаков артрита или до возникновения побочных эффектов (рвота, понос), но не более 6 мг/сут, или в первый день в дозе 3 мг (по 1 мг 3 раза в день после приема пищи), во второй - в дозе 2 мг (по 1 мг утром и вечером), а затем - по 1 мг/сут.
При отсутствии противопоказаний препаратами выбора служат НПВС в полных терапевтических дозах: нимесулид (по 100 мг 2 раза в день), напроксен (по 500 мг 2 раза в день) и диклофенак (по 25-50 мг 4 раза в день).
Приступ подагрического артрита может начаться внезапно, без каких-либо предвестников, поэтому больной всегда должен иметь достаточное количество препарата, купирующего боль. Эффективность лечения тем выше, чем раньше начинают лечение.
Глюкокортикоиды для купирования приступа обычно не используют, лишь при особенно нестерпимых болях возможно внутрисуставное введение депомедрола, метилпреднизолона, бетаметазона и триамцинолона (в крупные суставы по 10-40 мг, в мелкие - по 5-20 мг).
Антигипертензивный препарат лозартан (блокатор рецепторов к ангиотензину II) обладает умеренным урикозурическим эффектом, что позволяет применять его у больных подагрой с АГ.
Восстановления функций пораженных суставов при хроническом течении подагрического артрита достигают с помощью ЛФК и санаторно-курортного лечения. На курорте больные принимают радиоактивные или сульфидные ванны, а также грязелечение (аппликации на пораженные суставы). В процессе бальнеотерапии возможно обострение артрита, в связи с чем в течение первых 8-10 дней рекомендован прием НПВС, ранее купировавших острый приступ артрита (индометацин, фенилбутазон, диклофенак).
Прогноз
Поражение суставов обычно не приводит к утрате трудоспособности, но подавляющее большинство больных подагрой погибают от сердечно-сосудистых заболеваний, связанных с атеросклерозом (инсульты, ИМ). Менее четверти больных погибают от ХПН.
Профилактика
Первичная профилактика подагры заключается, прежде всего, в нормализации питания и отказе от алкоголя. Это особенно необходимо при существовании наследственной отягощенности.
ИДИОПАТИЧЕСКИЙ АНКИЛОЗИРУЮЩИЙ СПОНДИЛОАРТРИТ (БОЛЕЗНЬ БЕХТЕРЕВА)
Болезнь Бехтерева (ББ) - хроническое системное воспалительное заболевание осевого скелета, характеризующееся преимущественным поражением крестцово-подвздошных сочленений и позвоночника. Помимо последнего в патологический процесс нередко вовлекаются периферические суставы и внутренние органы (сердце, почки, глаза).
ББ относят к группе спондилоартритов, в которую также включены реактивные артриты, псориатическая артропатия, спондилопатии при заболеваниях кишечника (НЯК и БК), а также недифференцированная спондилоартропатия. Этим заболеваниям свойственны общие черты: несимметричный олигоартрит, сакроилеит и поражение других отделов позвоночника, аортит, передний увеит, наследственная предрасположенность, частое существование HLA-27 и отсутствие РФ в крови.
Распространенность ББ среди взрослых составляет от 0,2 до 1,1%. Заболевание развивается, главным образом, у молодых мужчин. Соотношение заболеваемости среди мужчин и женщин колеблется от 5:1 до 9:1. Болеют обычно лица в возрасте 15-30 лет. После достижения возраста 45 лет ББ развивается крайне редко.
Воспалительный процесс начинается с крестцово-подвздошных сочленений. Вслед за этим возникает множественное поражение межпозвоночных и реберно-позвонковых суставов, реже - периферических суставов. Синдесмофиты (межпозвоночные скобы), очевидно, формируются в результате переноса кальция из костей позвоночника в связки и фиброзное кольцо. В результате окостенения фиброзного кольца межпозвоночных дисков и связочного аппара-
та позвоночник приобретает форму, напоминающую бамбуковую трость; движения в нем практически отсутствуют.
Этиология и патогенез
Этиология и патогенез заболевания окончательно не выяснены. Большое значение имеет наследственная предрасположенность, ассоциированная с носительством HLA-B27 (более чем у 90% больных, тогда как в популяции этот антиген обнаруживают лишь у 7% лиц). Частота существования ББ среди родителей больных составляет 3%, а у лиц контрольной группы - 0,5%. Склонность к более тяжелому течению заболевания у носителей HLА-В27 свидетельствует о том, что этот антиген не только служит иммуногенетическим маркером, но и имеет непосредственное патогенетическое значение.
Клиническая картина
Клиническая картина заболевания весьма разнообразна, поэтому принято выделять несколько ее форм.
• Центральная форма - поражение только позвоночника.
• Ризомелическая форма - поражение позвоночника и «корневых» суставов (тазобедренного и плечевого).
• Периферическая форма - поражение позвоночника и периферических суставов (коленных, стопы).
• Скандинавская форма - поражение позвоночника и мелких суставов кистей стоп. Эта форма имеет большое сходство с РА.
На первом этапе диагностического поиска (болезнь обычно начинается исподволь, незаметно) определяют жалобы пациентов на боли в поясничнокрестцовой области, возникающие при длительном пребывании в одном положении, чаще - в ночное время, особенно ближе к утру. Боли уменьшаются после нескольких движений или легкой гимнастики. У лиц физического труда боли могут возникать или усиливаться в конце рабочего дня. При поражении грудного отдела позвоночника возникают опоясывающие боли по типу межреберной невралгии, усиливающиеся при кашле и глубоком вдохе.
В развернутой стадии болезни пациенты жалуются на постоянные боли в позвоночнике, усиливающиеся в ночное время, при физической нагрузке и перемене погоды. Отмечают стреляющие боли в различных отделах позвоночника, мышцах спины, бедер и голеней.
В поздней стадии болезни боли приобретают характер радикулоалгий, резко усиливаются при физической нагрузке и движении. Трудоспособность больных значительно снижается.
Если в процесс вовлечены периферические суставы, то больные отмечают боли и ограничение подвижности в «корневых» суставах (особенно при поражении тазобедренного сустава). При артритах коленного, голеностопного и суставов стопы отмечают болезненность при движениях и ограничение амплитуды последних.
Последовательность вовлечения суставов в патологический процесс имеет свои особенности: чаще всего жалобы возникают при поражении крестцово-
подвздошного сочленения и суставов позвоночника. Если болезнь начинается в юношеском возрасте, то в дебюте чаще всего отмечают поражение периферических (крупных и мелких) суставов, обычно сопровождающееся повышением температуры тела, сердцебиениями и неприятными ощущениями в области сердца, что делает клиническую картину весьма схожей с атакой ревматизма. Жалобы, связанные с сакроилеитом, возникают позже.
Больные также жалуются на нарушение осанки и походки, ограничение физической активности и периодически возникающие обострения заболевания.
На втором этапе диагностического поиска можно получить много информации, ценной для установления диагноза (особенно в развернутой стадии болезни). В начальной стадии ББ данных меньше, тем не менее они оказываются чрезвычайно полезными.
В ранней стадии ББ осанка и походка больного не нарушены, но при пальпации определяют болезненность крестцово-подвздошных суставов. Также отмечают гипотрофию и напряжение прямых мышц спины.
В развернутой стадии болезни находки более существенны: уже существует нарушение осанки и походки, более выражены грудной кифоз, шейный лордоз и сглаживание поясничного лордоза. Развиваются резкие изменения прямых мышц спины, а затем и их атрофия. При постукивании по остистым отросткам позвоночника возникает болезненность, а при боковом сжатии грудной клетки - резкие боли.
В поздней стадии болезни отмечают выраженный кифоз грудного отдела позвоночника. Резко изменяется походка больного: он движется, широко расставляя ноги и совершая качательные движения головой. При пальпации обнаруживают атрофию мускулатуры спины, шеи и трапециевидных мышц. Позвоночник полностью неподвижен и, чтобы посмотреть в сторону, больному необходимо повернуть все тело.
Если наряду с поражением позвоночника отмечают изменение других суставов (крупных или мелких), то в период активности болезни определяют все признаки артрита: дефигурацию сустава различной степени выраженности, ограничение подвижности и боли при движениях.
При развитии внесуставных поражений (сердечно-сосудистой системы, почек, глаз) можно обнаружить изменения сердечной мышцы (миокардит) и клапанного аппарата сердца (незначительная недостаточность митрального или аортального клапана). Крайне редко может развиться перикардит, сопровождающийся соответствующими симптомами.
Поражение глаз при ББ протекает в виде ирита, увеита, иридоциклита и эписклерита (по данным разных авторов, регистрируют у 10-30% больных).
Поражение почек представлено амилоидозом, развивающимся при высокой активности воспалительного процесса и тяжелом прогрессирующем течении заболевания.
Редко регистрируемое поражение легких выражается в развитии фиброза, сопровождающемся соответствующими признаками.
На третьем этапе диагностического поиска подтверждают диагностическое предположение о ББ, степени активности процесса, поражении внутренних органов и их функциональном состоянии.
В период активности процесса обнаруживают острофазовые показатели (увеличение СОЭ, концентрации а2-глобулинов и СРБ). Возможно развитие умеренной гипохромной анемии, повышение содержания IgA и ЦИК. РФ и АНФ не обнаруживают.
HLA-27 определяют у 90-95% больных. Вследствие относительно высокой частоты экспрессии этого гена у здоровых лиц (в России - около 10%) самостоятельного диагностического значения определение этого маркера не имеет. Его обнаружение может иметь значение для ранней диагностики ББ у молодых мужчин, у которых есть определенные клинические предпосылки подозревать это заболевание (семейный анамнез, боли в позвоночнике), но явные рентгенологические признаки сакроилеита отсутствуют. При несомненной ББ его обнаружение имеет прогностическое значение.
Весьма существенны данные рентгенологического исследования. В ранней стадии на рентгенограмме костей таза можно обнаружить признаки сакроилеита: нечеткость суставных контуров, неровность суставных поверхностей и очаги субхондрального остеосклероза. В развернутой стадии отмечают выраженные признаки сакроилеита или анкилоз крестцово-подвздошных сочленений и поражение межпозвоночных суставов, в поздней стадии - типичные для ББ изменения: анкилоз межпозвоночных суставов, окостенение фиброзного кольца межпозвоночных дисков, передних и боковых связок.
Проведение КТ рекомендовано при сомнении в существовании сакроилеита по данным рентгенологического исследования.
При развитии амилоидоза почек обнаруживают протеинурию различной степени выраженности. Почечную недостаточность диагностируют по величине снижения почечной фильтрации и концентрации креатинина в крови.
Ограничение подвижности грудной клетки приводит к уменьшению легочной вентиляции, что определяют при исследовании функции внешнего дыхания.
Диагностика
В настоящее время оптимальными признаны модифицированные НьюЙоркские критерии.
Клинические критерии:
• указания в анамнезе на воспалительные боли в спине или поясничной области (боли с постепенным началом у больных в возрасте младше 40 лет, продолжающиеся не менее 3 мес, сопровождающиеся утренней скованностью, усиливающиеся в покое и уменьшающиеся при физических упражнениях);
• ограничение движений в поясничном отделе позвоночника в сагиттальной и фронтальной плоскости;
• ограничение подвижности грудной клетки (разница окружности грудной клетки на вдохе и выдохе менее 2,5 см на уровне четвертого межреберья) с поправкой на пол и возраст.
Рентгенологические критерии:
• двусторонний сакроилеит II-IV стадии;
• односторонний сакроилеит II-IV стадии.
Диагноз считают достоверным при обнаружении одного рентгенологического признака в сочетании с любым клиническим симптомом. Чувствительность критериев составляет 83%, специфичность - 98%. Тест на обнаружение HLA-B27 полезен только в качестве дополнения.
ББ у мужчин молодого возраста можно заподозрить уже на самой ранней стадии на основании существования следующих изменений:
• болей воспалительного типа в суставах или пояснице;
• симметричного моноили олигоартрита суставов ног;
• болезненности при пальпации пояснично-крестцового отдела позвоночника;
• ощущения скованности в пояснице;
• ранних признаков двустороннего сакроилеита на рентгенограмме (субхондральный остеопороз, неотчетливые контуры сочленений с ложным расширением суставной щели, очаговый периартикулярный остеосклероз крестца и подвздошных костей).
В раннем периоде болезни имеет значение обнаружение болей при нагрузке на крестцово-подвздошное сочленение. Для ранней диагностики важны и такие редкие симптомы, как артралгия или артрит в области грудиноключичных и грудинореберных сочленений, болей в пятках, напряжение мышц в области поясницы, сглаженность поясничного лордоза, а также затруднения при сгибании в пояснице.
В развернутой стадии болезнь диагностировать легче: возникают радикулярные боли, нарушение осанки («поза просителя» или прямая доскообразная спина), напряжение мышц спины (симптом «тетивы») или их атрофия, ограничение подвижности грудной клетки, характерные рентгенологические изменения, артрит тазобедренных и (или) коленных суставов.
Следует отметить, что эти признаки имеют диагностическое значение после исключения прочих заболеваний, протекающих с подобным воспалительным поражением позвоночника и суставов (вторичные спондилоартриты). При обнаружении выраженного периферического артрита проводят дифференциальную диагностику ББ с РА.
Лечение
Основные цели лечения - облегчение выраженности болей в позвоночнике и периферических суставах, а также поддержание подвижности в них; купирование увеита. Лечение должно быть систематическим, его проводят на протяжении всей жизни больного.
Основные лекарственные препараты - НПВС (индометацин, диклофенак). Диклофенак назначают в начальной дозе 100-150 мг/сут; в такой же дозе применяют индометацин. При достижении положительного эффекта дозу снижают до 50-75 мг/сут. Прием лекарственных средств продолжают неограниченно длительное время. В период обострения дозу НПВС вновь можно увеличить. При плохой переносимости или существовании факторов риска поражения ЖКТ целесообразно назначение селективных НПВС (целекоксиб, мелоксикам).
Эффективным, особенно при поражении периферических суставов, может быть длительное лечение сульфасалазином (по 2-3 г/сут на протяжении не менее 3-4 мес).
Глюкокортикоиды при плановом лечении обычно не используют. Преднизолон назначают лишь в определенных ситуациях - при неэффективности НПВС, высокой лихорадке и увеите. Их назначают в виде пульс-терапии: метилпреднизолон вводят внутривенно капельно в дозе 750-1000 мг ежедневно на протяжении трех дней подряд.
При артрите периферических суставов быстрый эффект наступает при внутрисуставном введении метилпреднизолона, депомедрола, бетаметазона и триамцинолона. Специальным показанием к их применению считают такие внесуставные нарушения, как воспалительные поражения глаз (ириты, иридоциклиты) и редко регистрируемые тяжелые лихорадочные формы болезни, сопровождающиеся системным васкулитом. В последнем случае доза преднизолона составляет 30-40 мг/сут.
Эффективность применения ингибиторов ФНО-α доказана у больных с тяжелым течением и высокой активностью патологического процесса, несмотря на применение НПВС, глюкокортикоидов и сульфасалазина. Инфликсимаб назначают в дозе 5 мг/кг, реже - по 3 мг/кг. У подавляющего большинства больных развивается быстрый эффект (часто - уже на следующий день после инъекции), сохраняющийся в течение 7 лет на фоне поддерживающего лечения.
Некоторым больным с выраженными мышечными болями вследствие повышения тонуса спинных мышц рекомендовано применение миорелаксанта скутамила-Св (сочетание изопротана в дозе 0,15 г и парацетамола в дозе 0,1 г) по одной таблетке 3 раза в день.
Для больных очень важны занятия ЛФК, препятствующие развитию тугоподвижности позвоночника и периферических суставов. Комплекс не должен быть слишком тяжелым, и его следует выполнять до 3 раз в день. Весьма полезны занятия ЛФК, проводимые в плавательном бассейне.
Важное место в лечении больных занимает ежегодное использование радоновых, сероводородных ванн и грязевых аппликаций на курортах или в специализированных стационарах.
Прогноз
Прогностически неблагоприятные факторы:
• поражение тазобедренного сустава и ранний шейный кифоз;
• «сосискообразное» поражение пальцев;
• низкая эффективность НПВС;
• СОЭ более 30 мм/ч;
• раннее ограничение подвижности позвоночника;
• стойкий олигоартрит;
• начало заболевания в возрасте младше 16 лет.
При отсутствии перечисленных факторов вероятен благоприятный исход (чувствительность - 92,5%, специфичность - 78%). При поражении тазобе-
дренного сустава или существовании трех факторов более вероятен неблагоприятный исход (чувствительность - 50%, специфичность - 97,5%).
Смертность при ББ в 1,5 раза выше, чем в популяции. Основные причины смерти больных - сердечно-сосудистые заболевания и амилоидоз.
У большинства больных постепенно снижается функциональная подвижность опорно-двигательного аппарата (особенно через десять лет с момента начала заболевания). При диспансерном наблюдении и длительном систематическом лечении в 70% случаев удается задержать прогрессирование болезни.