Фармакология : учебник. - 10-е изд., испр., перераб. и доп. - Харкевич Д. А. 2010. - 752 с.
|
|
|
|
ГЛАВА 10 ПРОТИВОПАРКИНСОНИЧЕСКИЕ СРЕДСТВА
Эту группу средств применяют для лечения болезни Паркинсона, а также при паркинсонизме различного происхождения.
Болезнь Паркинсона представляет собой хроническое нейродегенеративное заболевание, при котором поражаются ядра экстрапирамидной системы. Наиболее частыми проявлениями этой патологии являются ригидность1 (резко повышенный тонус мышц), тремор (постоянное непроизвольное дрожание), гипокинезия2 (скованность движений). Изменяются также походка и поза больного. Постепенно возникают психические нарушения, страдает умственная деятельность. Этиология болезни Паркинсона неизвестна3. Обнаружено, однако, что при этом заболевании в базальных ядрах4, а также в черной субстанции снижается со- держание дофамина, который оказывает преимущественно тормозное влияние на неостриатум. Последний, как известно, участвует в регуляции функций спинного мозга. По современным представлениям, недостаток дофамина, связанный с уменьшением количества дофаминергических нигростриатных нейронов, является основной причиной двигательных и психических нарушений, которые характеризуют синдром паркинсонизма.
За последние годы показано, что в развитии болезни Паркинсона ведущую роль играет возникающий дисбаланс между дофаминергической и глутаматергической системами головного мозга. Как уже было отмечено, при развитии болезни Паркинсона в нейронах черной субстанции снижается содержание дофамина, оказывающего тормозное влияние на нейроны неостриатума. На этом фоне превалирует стимулирующее влияние глутаматергических нейронов. Это приводит к нарушению двигательной и психической функций. Возникают гипокинезия, тремор, ригидность и брадифрения5. С учетом сказанного терапия болезни Паркинсона направлена на восстановление динамического равновесия между разными медиаторными системами, вовлеченными в регуляцию функций базальных ядер. Одна из основных задач фармакотерапии паркинсонизма - устранение дефицита дофамина в соответствующих ядрах. Воспользоваться для этой цели самим дофамином не представляется возможным, так как он практически не проникает через гематоэнцефалический барьер и, следовательно, не попадает при обычных путях введения в ткани мозга. Поэтому при паркинсонизме используют предшественник дофамина L-ДОФА, который проходит через тканевые барьеры и затем
1 От лат. rigidus - твердый, негибкий.
2 От греч. hypo - под, ниже, kinesis - движение.
3 В 80-х годах XX в. из препарата типа героина, применявшегося в США наркоманами, было выделено соединение МРТР (1-метил-4-фенил-1,2,3,6-тетрагидропиридин), вызывающее у людей и животных избирательное и необратимое разрушение дофаминовых нигростриатных нейронов. При этом возникают двигательные нарушения по типу болезни Паркинсона. Высказывается предположение, что это соединение может быть одной из причин возникновения паркинсонизма. Однако этот вопрос остается открытым, так как неизвестны источники образования этого вещества, а также возможности его попадания из окружающей среды в организм человека. В настоящее время МРТР используется в фармакологии для получения экспериментальной модели пар- кинсонизма.
4 В полосатом теле - corpus striatum (объединяет два ядра: хвостатое ядро - nucleus caudatus и скорлупу - putamen; это так называемый неостриатум) и бледном шаре - globus pallidus (палеостри- атум).
5 Брадифрения (от греч. bradys - медленный, phren - ум, разум) характеризуется замедленным течением психических процессов (мышления, эмоций, речи).
в нейронах под влиянием фермента ДОФА-декарбоксилазы превращается в дофамин. Повысить активность дофаминергической системы можно и за счет усиления выделения и(или) угнетения нейронального захвата дофамина нейронами черной субстанции. С этой же целью можно воспользоваться веществами, которые оказывают прямое стимулирующее влияние на дофаминовые рецепторы. Несомненный интерес представляют ингибиторы МАО-В, инактивирующей в тканях мозга дофамин.
Весьма перспективны также вещества, блокирующие глутаматергические влияния. К числу таких препаратов относятся антагонисты NMDA-рецепторов, устраняющие стимулирующие эффекты глутаматергических нейронов на базальные ядра и задерживающие дегенеративные изменения дофаминергических нейронов.
В функции ядер экстрапирамидной системы принимают участие также холинергические нейроны. При недостатке дофамина преобладают стимулирующие холинергические влияния. Для устранения создавшегося при этом дисбаланса между дофаминергическими и холинергическими влияниями можно использовать центральные холиноблокаторы. Препараты этой группы восстанавливают нарушенное равновесие за счет подавления холинергической передачи (рис. 10.1).
Исходя из принципов действия противопаркинсонических веществ, их подразделяют на следующие основные группы.
I. Вещества, активирующие дофаминергические влияния
1. Предшественник дофамина Леводопа
2. Средства, стимулирующие дофаминовые рецепторы (дофаминомиметики)
Бромокриптин Ропинирол
3. Ингибиторы моноаминоксидазы В Селегилин
II. Вещества, угнетающие глутаматергические влияния Мидантан
III. Вещества, угнетающие холинергические влияния Циклодол
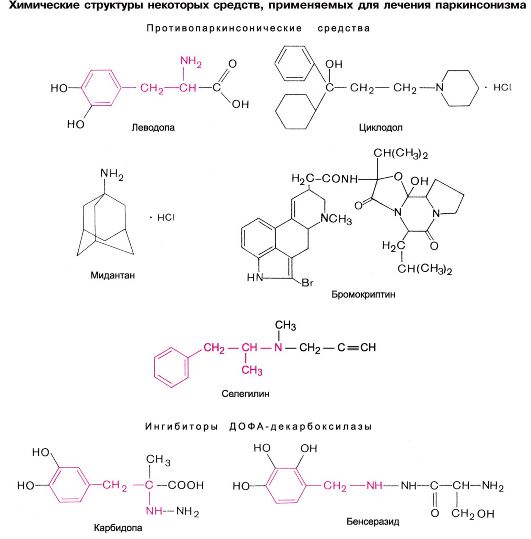
См. химические структуры
Леводопа (L-ДОФА, леводофа) представляет собой левовращающий изомер диоксифенилаланина, который является предшественником дофамина. Проникает через гематоэнцефалический барьер и затем в нейроны, где леводопа превращается в дофамин. Накапливаясь в базальных ганглиях, дофамин устраняет или ослабляет проявления паркинсонизма (см. рис. 10.1). Особенно выраженно влияет леводопа на гипокинезию, менее - на ригидность, еще меньше - на тремор.
Леводопа относится к наиболее эффективным средствам, применяемым при лечении болезни Паркинсона и симптоматического паркинсонизма (исключая паркинсонизм, вызванный некоторыми лекарственными препаратами, в частности антипсихотическими средствами). Действие леводопы развивается через 1 нед и более и достигает максимума примерно через 1 мес. Дозу увеличивают постепенно. Назначают препарат только после еды. Лечение проводят длительно, так как это по существу заместительная терапия (восполняется недостаток дофамина).
Из желудочно-кишечного тракта препарат всасывается быстро. Однако значительная его часть (70-90%) метаболизируется в слизистой оболочке кишечника. В организме превращается в дофамин и другие метаболиты. Это происходит под
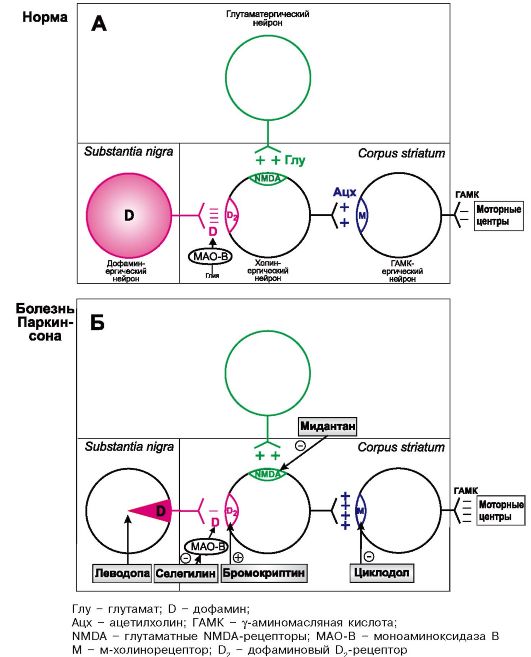
Рис. 10.1. Основная направленность действия противопаркинсонических средств (схема).
влиянием ДОФА-декарбоксилазы, КОМТ и МАО. В итоге в ЦНС поступает около 1% от введенной дозы леводопы. Метаболиты и незначительные количества неизмененной леводопы выделяются почками.
Довольно часто наблюдаются побочные эффекты: нарушение аппетита, тошнота, рвота, ортостатическая гипотензия, сердечные аритмии, психические расстройства, двигательные нарушения (у ряда больных возникают хореиформные движения).
Все эти осложнения обратимы и могут быть нивелированы снижением дозы леводопы. Многие побочные эффекты связаны с образованием дофамина из леводопы в периферических тканях. Последнее можно уменьшить, комбинируя леводопу с ингибиторами периферической ДОФА-декарбоксилазы, не проника-
ющими через гематоэнцефалический барьер (например, с карбидопой или бенсеразидом; рис. 10.2). Выпускают препараты, содержащие леводопу с карбидопой (синемет, наком) и леводопу с бенсеразидом (мадопар). Такие сочетания повышают количество леводопы, поступающей в ЦНС. Это связано с тем, что ингибируется декарбоксилирование леводопы в кишечнике и печени (повышается ее поступление в системное кровообращение), в периферических тканях, например в почках (что способствует поддержанию высоких концентраций вещества в крови), а также в эндотелии капилляров мозга (устраняется энзиматический барьер для проникновения леводопы в мозг).
Для повышения эффективности леводопы, устранения или уменьшения ее побочных эффектов, помимо использования ингибиторов периферической ДОФАдекарбоксилазы, применяют также ингибиторы КОМТ, например энтакапон (комтан1). Кроме того, при тошноте и рвоте назначают блокаторы дофамино-
1 Применение аналогичного препарата толкапона ограничено, так как у него выявлена выраженная гепатотоксичность.
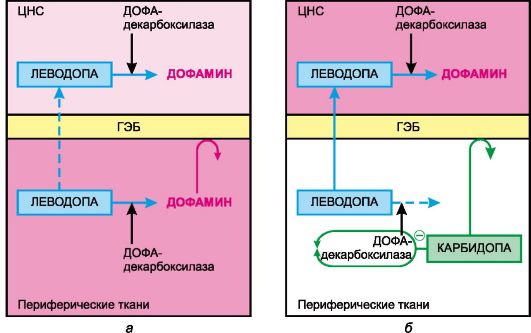
Рис. 10.2. Действие леводопы (а) и леводопы в сочетании с карбидопой (б) (схема). ГЭБ - гематоэнцефалический барьер; минус - угнетающее действие. Интенсивность красного цвета условно отражает концентрацию дофамина в ЦНС и периферических тканях.
вых рецепторов периферических тканей и пусковой зоны рвотного центра (например, домперидон; не проникает через гематоэнцефалический барьер). При развитии психозов используют блокатор дофаминовых рецепторов головного мозга клозапин (в 10 раз активнее в отношении D4-, чем D2-рецепторов).
Нельзя сочетать леводопу с неизбирательными ингибиторами МАО (последняя инактивирует норадреналин, дофамин; при угнетении МАО может возникнуть резкая гипертензия), а также с пиридоксином (витамином В6), который снижает активность леводопы.
Наиболее эффективна леводопа в течение 2-5 лет. Постепенно развивается привыкание, возникают дискинезия и другие побочные эффекты.
Препарат противопоказан при тяжелых заболеваниях сердечно-сосудистой системы, печени, почек, при психозах.
К стимуляторам дофаминовых рецепторов, используемым при лечении паркинсонизма, относится бромокриптин (парлодел). По химическому строению это полусинтетическое производное алкалоида спорыньи эргокриптина (производное лизергиновой кислоты). Является агонистом дофаминовых D2-рецепторов. Обладает отчетливой противопаркинсонической активностью. К типичным эффектам бромокриптина относится также торможение продукции пролактина и гормона роста (см. главу 20; 20.1). Принимается внутрь. Из желудочно-кишечного тракта всасывается около 30%. Бóльшая часть инактивируется при первом прохождении печеночного барьера. Максимальная концентрация в плазме накапливается через 1,5-3 ч; t1/2=3-6 ч. Значительная часть бромокриптина подвергается биотрансформации. Основной путь выведения - с желчью в кишечник. Бромокриптин, как правило, применяют в комбинации с леводопой.
Побочные эффекты на начальных стадиях лечения: тошнота, рвота, ортостатическая гипотензия. При длительном применении возможны психические нарушения, дискинезия, непереносимость этилового спирта, запор и др.
Одним из агонистов D2- и D3-дофаминовых рецепторов является ропинирол (реквип). Противопаркинсонический эффект связывают с его влиянием на постсинаптические D2-дофаминовые рецепторы в неостриатуме. Угнетает секрецию пролактина. По эффективности при паркинсонизме ропинирол превосходит бромокриптин.
Как отмечалось, один из путей усиления дофаминергических влияний заключается в подавлении процессов инактивации дофамина. По такому принципу действуют ингибиторы МАО-В. К избирательным необратимо действующим ингибиторам этого фермента относится селегилин (депренил). Обычно его применяют в сочетании с леводопой. Отличается от ингибиторов МАО неизбирательного действия тем, что при взаимодействии с симпатомиметиками не вызывает выраженных гипертензивных реакций (см. главу 11.2).
В эксперименте обнаружено, что, помимо ингибирования МАО-B, селегилин обладает нейропротекторным эффектом, уменьшая повреждение нейронов при ишемии и при воздействии ряда нейротоксических веществ. Частично это может быть связано с индукцией фактора роста нервов, продуцируемого глиальными астроцитами. Имеются предварительные клинические данные о благоприятном влиянии селегилина на состояние пациентов при таком нейродегенеративном заболевании, как болезнь Альцгеймера. Не исключено, что подобный эффект может проявляться и в отношении болезни Паркинсона, но это требует специального исследования.
К противопаркинсоническим веществам, устраняющим глутаматергические влияния, относится мидантан1 (амантадина гидрохлорид, симметрел). Согласно современным представлениям, мидантан блокирует глутаматные NMDA-рецеп- торы и тем самым снижает стимулирующее влияние кортикальных глутаматных нейронов на неостриатум, превалирующее на фоне недостаточности дофамина. Это уменьшает клинические проявления болезни Паркинсона - ригидность, тремор и гипокинезию. Кроме того, отмечено, что мидантан обладает нейропротекторным эффектом в отношении нейронов черной субстанции. Связывают это также с угнетением NMDA-рецепторов указанных нейронов и уменьшением поступления в клетки ионов кальция, что снижает возможность деструкции нейронов и замедляет прогрессирование заболевания. Мидантан обладает и некоторым м-холиноблокирующим эффектом.
Применяют мидантан при лечении болезни Паркинсона и симптоматическом паркинсонизме (постэнцефалитическом или цереброваскулярном), особенно в случаях, когда леводопа противопоказана. Мидантан устраняет или уменьшает гипокинезию, в меньшей степени - ригидность и тремор. Улучшение наступает через 1-2 сут и более; максимальный эффект наблюдается через несколько дней, иногда недель.
Переносится мидантан в большинстве случаев хорошо. Из побочных эффектов иногда наблюдаются бессонница, галлюцинации, ортостатическая гипотензия, диспепсические расстройства, головная боль.
Препарат следует с осторожностью применять при ряде заболеваний ЦНС, сопровождающихся галлюцинациями, эпилептиформными судорогами, а также при тяжелых заболеваниях печени и почек.
1 Первоначально был предложен как противовирусное средство для профилактики гриппа типа А2 под названием амантадин (см. главу 28).
Весьма целесообразно комбинированное применение с леводопой, что позволяет уменьшить ее дозу.
Последняя группа противопаркинсонических средств представлена так называемыми центральными холиноблокаторами. Они подавляют стимулирующие холинергические влияния в базальных ганглиях благодаря угнетению центральных холинорецепторов. На синтез, высвобождение и гидролиз ацетилхолина, по имеющимся данным, они не влияют. Из таких препаратов широкое применение получил циклодол (артан, тригексифенидила гидрохлорид). Он оказывает как центральное, так и периферическое м-холиноблокирующее действие. Влияние на ЦНС способствует уменьшению или устранению двигательных нарушений, связанных с поражением экстрапирамидной системы. Циклодол наиболее эффективно уменьшает тремор и в меньшей степени - ригидность, мало влияя на гипокинезию.
Применяют циклодол при болезни Паркинсона, паркинсонизме и других патологических состояниях, связанных с поражением экстрапирамидной системы. Циклодол эффективен также при явлениях паркинсонизма, вызванных антипсихотическими средствами. Назначают препарат внутрь. Он хорошо всасывается из тонкой кишки и быстро выводится. Кумуляции не наблюдается. При длительном применении развивается привыкание.
Угнетение периферических м-холинорецепторов является причиной ряда нежелательных эффектов (сухость слизистой оболочки полости рта, тахикардия, нарушение аккомодации, снижение тонуса мышц кишечника и др.). Спазмолитическое действие циклодола связано как с атропиноподобным, так и с прямым миотропным (папавериноподобным) действием. При передозировке циклодола могут возникать нарушения со стороны ЦНС (возбуждение, галлюцинации).
Циклодол противопоказан или его следует применять с осторожностью при глаукоме, нарушении мочеотделения, вызванном гипертрофией предстательной железы, при заболеваниях сердца, печени, почек. Не следует назначать циклодол пожилым людям (ухудшается память, нарушается мышление).
При лечении паркинсонизма иногда используют и другие центральные холиноблокаторы: тропацин (дифенилтропина гидрохлорид), бензтропина мезилат (когентин) и др.
Все перечисленные противопаркинсонические препараты не относятся к средствам этиотропной терапии. Они лишь устраняют или ослабляют синдром паркинсонизма, и поэтому лечебный эффект сохраняется только во время их применения.
Препараты
Название | Средняя терапевтическая доза для взрослых; путь введения | Форма выпуска |
Леводопа - Levodopa | Внутрь 0,25-1 г | Капсулы и таблетки по 0,25-0,5 г |
Мидантан - Midantanum | Внутрь 0,05-0,1 г | Таблетки, покрытые оболочкой, по |
Циклодол - Cyclodolum | Внутрь 0,001-0,005 г | Таблетки по 0,001; 0,002 и |
Селегилин - Selegiline | Внутрь 0,005-0,01 г | Таблетки по 0,005 и |
Бромокриптин - Bromocriptine | Внутрь 0,03-0,04 г | Таблетки по 0,005 и |