Биология: учебник / Пехов А.П., -, 2010. - 664 с.
|
|
|
|
ГЛАВА XV Генетическая инженерия
Генетическая инженерия
Современная биология коренным образом отличается от традиционной биологии не только большей глубиной разработки познавательных идей, но и более тесной связью с жизнью общества, с прак- тикой. Можно сказать, что в наше время биология стала средством преобразования живого мира с целью удовлетворения материальных потребностей общества. Это заключение иллюстрируется прежде всего тесной связью биологии с биотехнологией, которая стала важнейшей областью материального производства, равноправным партнером механической и химической технологий, созданных чело- веком, а также с медициной.
С момента своего возникновения биология и биотехнология всегда развивались совместно, причем с самого начала биология была научной основой биотехнологии. Однако длительное время недостаток собственных данных не позволял биологии оказывать очень большое влияние на биотехнологию. Положение резко изменилось с созданием во второй половине XX в. методологии генетической инженерии, под которой понимают генетическое манипулирование с целью конструкции новых и реконструкции существующих генотипов. Являясь по своей природе методическим достижением, генетическая инженерия не привела к ломке сложившихся представлений о биологических явлениях, не затронула основных положений биологии подобно тому, как радиоастрономия не поколебала основных положений астрофизики, установление «механического эквивалента тепла» не привело к изменению законов теплопроводности, а доказательство атомистической теории вещества не изме- нило соотношений термодинамики, гидродинамики и теории упругости (А.А. Баев).
Тем не менее генетическая инженерия открыла новую эру в биологии по той причине, что появились новые возможности для про- никновения в глубь биологических явлений с целью дальнейшей характеристики форм существования живой материи, более эффективного изучения структуры и функции генов на молекулярном уровне, понимания тонких механизмов работы генетического аппарата. Успехи генетической инженерии означают переворот в современном
естествознании. Они определяют критерии ценности современных представлений о структурно-функциональных особенностях молекулярного и клеточного уровней живой материи. Современные данные о живом имеют гигантское познавательное значение, ибо обеспечивают понимание одной из важнейших сторон органического мира и тем самым вносят неоценимый вклад в создание научной картины мира. Таким образом, резко расширив свою познавательную базу, биология через генетическую инженерию оказала также ведущее влияние на подъем биотехнологии.
Генетическая инженерия создает заделы на пути познания способов и путей «конструирования» новых или улучшения существующих организмов, придавая им большую хозяйственную ценность и способность резкого увеличения продуктивности биотехнологических процессов. Однако генетическая инженерия создала новые горизонты и для медицины по линии диагностики и лечения многих болезней, как ненаследственных, так и наследственных. Она открыла новые пути в поисках новых лекарств и материалов, используемых в медицине. Генетическая инженерия и биотехнология стимулировали разработку методов бионанотехнологии.
В рамках генетической инженерии различают генную и клеточную инженерию. Под генной инженерией понимают манипуляции с целью создания рекомбинантных молекул ДНК. Часто эту методологию называют молекулярным клонированием, клонированием генов, технологией рекомбинантных ДНК или просто генетическими манипуляциями. Важно подчеркнуть, что объектом генной инженерии являются молекулы ДНК, отдельные гены. Напротив, под клеточной инженерией понимают генетические манипуляции с изолированными отдельными клетками или группами клеток растений и животных.
ГЕННАЯ ИНЖЕНЕРИЯ И ЕЕ ИНСТРУМЕНТЫ
Генную инженерию составляет совокупность различных экспериментальных приемов (методик), обеспечивающих конструкцию (реконструкцию), клонирование молекул ДНК и генов с заданными целями.
Методы генной инженерии используют в определенной последовательности (рис. 127), причем различают несколько стадий в выпол-
нении типичного генно-инженерного эксперимента, направленного на клонирование какого-либо гена, а именно:
1. Выделение плазмидий ДНК из клеток интересующего организма (исходного) и выделение ДНК-вектора.
2. Разрезание (рестрикция) ДНК исходного организма на фрагменты, содержащие интересующие гены, с помощью одного из ферментов-рестриктаз и выделение этих генов из рестрикционной смеси. Одновременно разрезают (рестрицируют) векторную ДНК, превращая ее из кольцевой структуры в линейную.
3. Смыкание интересующего сегмента ДНК (гена) с ДНК вектора с целью получения гибридных молекул ДНК.
4. Введение рекомбинантных молекул ДНК путем трансформации в какой-либо другой организм, например в Е. coli или соматические клетки.
5. Высев бактерий, в которые вводили гибридные молекулы ДНК, на питательные среды, позволяющие рост только клеток, содержащих гибридные молекулы ДНК.
6. Идентификация колоний, состоящих из бактерий, содержащих гибридные молекулы ДНК.
7. Выделение клонированной ДНК (клонированных генов) и ее характеристика, включая секвентирование азотистых оснований в клонированном фрагменте ДНК.
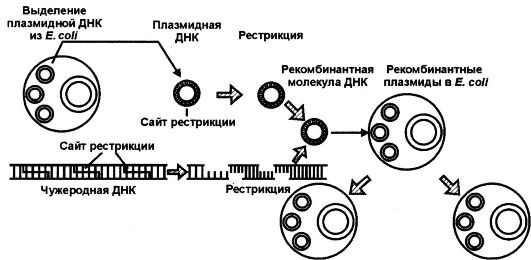
Рис. 127. Последовательные стадии генно-инженерного эксперимента
В ходе эволюции бактерии развили способность синтезировать так называемые рестрицирующие ферменты (эндонуклеазы), которые стали частью клеточной (бактериальной) системы рестрикциимодификации. У бактерий системы рестрикции-модификации являются внутриклеточной иммунной системой защиты от чужеродной ДНК. В отличие от высших организмов, у которых распознание и разрушение вирусов, бактерий и других патогенов происходит внеклеточно, у бактерий защита от чужеродной ДНК (ДНК растений и животных, в организме которых они обитают) происходит внутриклеточно, т.е. тогда, когда чужеродная ДНК проникает в цитоплазму бактерий. С целью защиты бактерии в ходе эволюции развили также способность «метить» собственную ДНК метилирующими основаниями на определенных последовательностях. По этой же причине чужеродная ДНК из-за отсутствия в ней метильных групп на тех же последовательностях плавится (разрезается) на фрагменты разными бактериальными рестриктазами, а затем деградируется бактериальными экзонуклеазами до нулеотидов. Можно сказать, что таким образом бактерии защи- щают себя от ДНК растений и животных, в организме которых они обитают временно (как патогены) или постоянно (как сапрофиты).
Рестриктазы впервые были выделены из Е. coli в
Действие системы рестрикции-модификации «рационализуется» так называемыми палиндромными (распознающими) последователь- ностями азотистых оснований, которые являются сайтами рестрикции ДНК. Палиндромные последовательности - это последовательности оснований, которые одинаково читаются вперед и назад, как, например, последовательность букв радар. Поскольку цепи ДНК обладают антипараллельным направлением, то считают, что последовательность является палиндромной, если она идентична, когда читается в направлении от 5' - к 3'-концу на верхней и на нижней цепи от 3' - к 5'-концу, а именно:
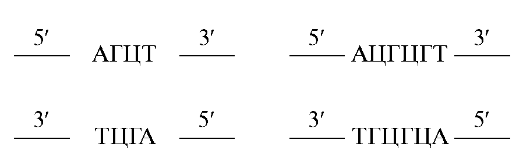
Палиндромы могут быть любых размеров, но большинство тех палиндромов, которые используют в качестве сайтов узнавания рестриктазами, состоят из 4, 5, 6 и реже 8 оснований.
Рестриктазы - это абсолютно необходимый инструмент в генной инженерии для вырезания интересующих фрагментов (генов) из больших молекул ДНК. Поскольку известно более 100 ферментов рестрикции, то это позволяет выбор рестриктаз и селективное вырезание фрагментов из исходной ДНК.
Замечательной особенностью рестриктаз является то, что они продуцируют разрезы молекул на несколько фрагментов (рестриктов) ДНК уступами, в результате чего в образующихся концах одна цепь длиннее другой, образуя своеобразный хвост. Такие концы (хвосты) получили название «липких» концов, так как они способны к самокомплементарности.
Рассмотрим результаты рестрикции на примере одной из наиболее известных рестриктаз Eco RI из системы рестрикция-модификация Е. соИ. Вместо того чтобы плавить ДНК в центре палиндромной последовательности узнавания, этот фермент плавит ДНК за преде- лами центра и продуцирует 4 самокомплементарных («липких») конца, состоящих из разного количества нуклеотидов, а именно:
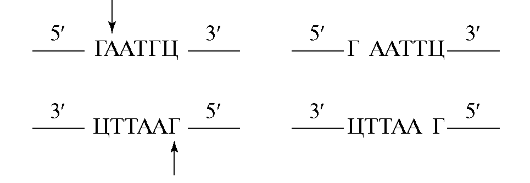
Эти «липкие» концы в генно-инженерных опытах полезны по той причине, что они могут быть воссоединены комплементарно при низких температурах, что позволяет эффективное смыкание ДНК-фрагментов.
Сайты распознавания и сайты плавления в случае других рестриктаз имеют другое содержание, а именно:
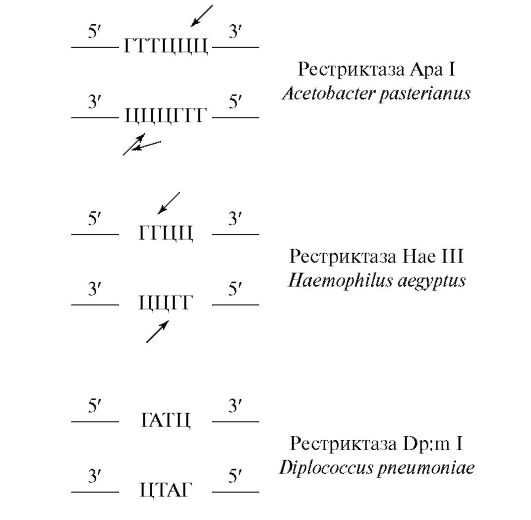
Вслед за рестрикцией ДНК из рестрикционной смеси выделяют рестрикционные ДНК-фрагменты (ДНК-рестрикты), которые необ- ходимы затем для объединения с вектором. Для выделения ДНКрестриктов прибегают к электрофорезу, поскольку с помощью этого метода рестрикцированную ДНК очень легко фракционировать благодаря размерам фрагментов-рестриктов и константным отношениям электрический заряд-масса. Фрагменты в электрическом поле мигрируют в ходе электрофореза при частоте, зависимой от их размеров (массы). Чем больше (длиннее) фрагмент, тем медленнее он мигрирует в электрическом поле. Материалом, в котором проводят электрофорез, являются незаряжающиеся агароза или полиакриламид. Для опознания фрагментов используют этидий бромид, который красит фрагменты, что ведет к их более легкому обнаружению.
Результативность электрофореза очень высока, поскольку с его помощью могут быть разделены фрагменты, размеры которых состав- ляют от 2 до 50 000 оснований.
После электрофореза фрагменты из агарозы выделяют с помощью разных методов. На основании результатов сравнения размеров
рестриктов одной и той же ДНК, полученных с помощью разных рестриктаз, строят рестрикционные карты, на которых показывают сайты рестрикции каждой из использованных рестриктаз. В практическом плане рестрикционные карты позволяют определять не только размеры рестриктов, но и выяснять расположение в молекулах ДНК локусов тех или иных генов.
Поскольку у высших организмов в ходе транскрипции синтезируется гетерогенная ДНК, корректируемая процессингом, то в генной инженерии обычно используют комплементарную ДНК (кДНК), которую получают при использовании в качестве матрицы мРНК, на которой обратная транскриптаза синтезирует одноцепочечную ДНК (кДНК), являющуюся копией мРНК. В последующем эти одноцепочечные ДНК превращают в двухцепочечные ДНК. Считают, что кДНК содержит непрерывные нуклеотидные последовательности (транскрибируемые и транслируемые). Именно кДНК используют для рестрикции.
Выделенные после электрофореза из агарозных гелей фрагменты ДНК (рестрикты) можно предварительно подвергнуть сек-вентированию, т.е. определить в них нуклеотидную последовательность. Для этого служат химический и ферментативный методы секвентирования. Химический метод основан на получении меченных радиоактивным фосфором (32Р) фрагментов и удалении из этих фрагментов одного из оснований с последующим учетом результатов радиоавтографии гелей, содержащих эти фрагменты. Ферментативный метод основан на том, что в конец анализируемого фрагмента вводят нуклеотид, используемый затем в синтезе разных фрагментов in vitro, анализируемых на нуклеотидную последовательность электрофоретически. Для изучения специфических последовательностей нуклеотидов в молекуле ДНК используют
также гибридизацию ДНК-ДНК, РНК-РНК, ДНК-РНК, Нозерн-
и Саузерен-блоттинги.
Генетические векторы. Сегмент ДНК (ген), который предназначен для молекулярного клонирования, должен обладать способностью к репликации при переносе его в бактериальную клетку, т.е. быть репликоном. Однако он такой способностью не обладает. Поэтому, чтобы обеспечить перенос и обнаружение клонируемых генов в клетках, их объединяют с так называемыми генетическими векторами. Последние должны обладать как минимум двумя свойствами. Во-первых, векторы должны быть способны к репликации
в клетках, причем в нескольких концах. Во-вторых, они должны обеспечивать возможность селекции клеток, содержащих вектор, т.е. обладать маркером, на который можно вести контрселекцию клеток, содержащих вектор вместе с клонируемым геном (рекомбинантные молекулы ДНК). Таким требованиям отвечают плазмиды и фаги. Плазмиды являются хорошими векторами по той причине, что они являются репликонами и могут содержать гены резистентности к какому-либо антибиотику, что позволяет вести селекцию бактерий на устойчивость к этому антибиотику и, следовательно, легкое обнаружение рекомбинантных молекул ДНК
(рис. 128).
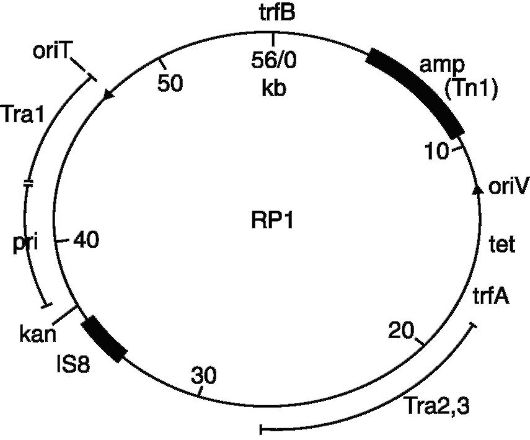
Рис. 128. Вектор pBRl
Поскольку не существует природных плазмидных векторов, то все известные к настоящему времени плазмидные векторы были сконструированы искусственно. Исходным материалом для создания ряда генетических векторов послужили R-плазмиды, в которых с помощью рестриктаз удаляли излишние последовательности ДНК, в том числе те, на которых располагались множественные сайты рестрикции. Это удаление определялось тем, что плазмидный вектор должен обладать только одним сайтом узнавания для одной рестриктазы, причем этот сайт должен лежать в функционально несущественном районе плазмидного генома. Например, плазмидый вектор pBR 322, который имеет гены резистентности к ампициллину и тетрациклину, что делает его очень удобным
для селекции бактерий, содержащих клонируемый сегмент ДНК, обладает одиночными сайтами рестрикции для более 20 ферментов- рестриктаз, включая такие известные рестриктазы, как Eco RI, Hind III, Pst I, Pva II и Sal I.
Фаговые векторы тоже обладают рядом преимуществ. Они могут включать в себя более крупные (более длинные) клонируемые фрагменты ДНК по сравнению с плазменными векторами. Далее, перенос фагами клонируемого фрагмента в клетки в результате инфицирования ими последних является более эффективным, чем трансформация ДНК. Наконец, фаговые векторы позволяют более эффективный скрининг (распознание) на поверхности агара колоний, содержащих клетки, несущие клонируемый ген. Многие фаговые векторы сконструированы на базе фага лямбда.
Кроме фаговых используют и другие вирусные векторы, сконструированные на базе вируса герпеса, а также векторы, сконструированные на базе дрожжевой ДНК.
Если клонирование генов проводят, используя клетки млекопитающих или растений, то требования к векторам те же, что и в случае клонирования в бактериальных клетках.
Конструирование рекомбинантных молекул ДНК. Непосредственное конструирование рекомбинантных молекул ДНК следует после того, как получены рестрикты исследуемой ДНК и векторной ДНК. Оно заключается в смыкании сегментов-рестриктов исследуемой ДНК с рестриктом векторной ДНК, которая в результате рестрикции превращается из кольцевой в линейную ДНК.
Чтобы сомкнуть фрагменты исследуемой ДНК с ДНК вектора, используют ДНК-лигазу (рис. 129). Лигирование будет успешным, если смыкаемые структуры обладают З'-гидроксильной и 5'-фос- фатной группами и если эти группы расположены соответствующим образом относительно одна другой. Фрагменты объединяются через их «липкие» концы в результате самокомплементарности. При высоких концентрациях фрагментов последние время от времени становятся в правильное положение (напротив друг друга). Многие рестриктазы, такие как Eco RI, продуцируют «липкие» концы, состоящие из четырех оснований. Процесс лигирования «липких» концов, состоящих из четырех оснований, происходит при пониженной температуре (до 12 ?С).
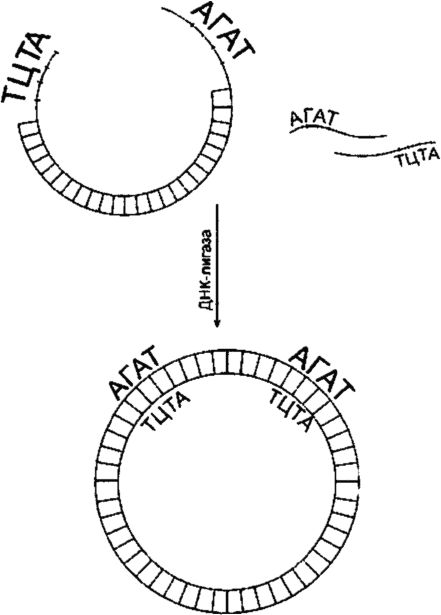
Рис. 129. ДНК-лигирование
Если при рестрикции образуются фрагменты без «липких» концов, то их «насильственно» конвертируют в молекулы с «липкими» концами, используя фермент трансферазу. Этот фермент добавляет нуклеотиды к 3'-концу ДНК. На одном фрагменте может быть добавлен поли-А-хвост, на другом - поли-Т-хвост. Для генерации любых желаемых концов ДНК используют также полимеразную цепную реакцию (ПЦР). Принцип ПЦР основан на денатурации выделенной из клеток ДНК и «отжиге» ее с добавлением к ренатурирующимся цепям ДНК-олигонуклеотидов, состоящих из 15-20 нуклеотидов каждый. Эти олигонуклеотиды должны быть комплементарны последовательностям в цепях, разделенных расстояниями в 50-2000 нуклеотидов. Будучи «затравкой» для синтеза ДНК in vitro, они позволяют ДНК-полимеразе копировать те участки, которые находятся между «затравками». Это копирование дает большое количество копий изучаемого фрагмента ДНК.
Введение рекомбинантных молекул ДНК в клетки. После смыкания интересующего фрагмента ДНК (гена) с генетическим вектором с помощью ДНК-лигазы образованные рекомбинантные молекулы вводят в клетки с целью добиться их репликации (за счет генетического вектора) и увеличения количества копий. Наиболее популярным способом введения в клетки рекомбинантных молекул ДНК, в которых вектором служит плазмида, является трансформация Е. coli. С этой целью бактериальные клетки предварительно обрабатывают кальцием или рубидием (ионами), для того
чтобы они стали «компетентными» в восприятии рекомбинатной ДНК. Чтобы повысить частоту проникновения ДНК в клетки, используют метод электропорации, заключающийся в кратком экспонировании клеток в интенсивном электрическом поле. Эта обработка создает полости в мембранах клеток, что способствует лучшему восприятию клетками ДНК. После введения рекомбинатных молекул ДНК в бактерии последние высевают на МПА (мясо-пептонный агар), обогащенный антибиотиками для селекции желаемых клеток, т.е. клеток, содержащих рекомбинантные молекулы ДНК. Частота трансформации является невысокой. Обычно один трансформант возникает на 105 высеянных клеток. Если же вектор является фаговым, то прибегают к трансфекции клеток (бактерий или дрожжей) фагом. Что касается соматических клеток животных, то их трансфекцию осуществляют ДНК в присутствии химических веществ, облегчающих прохождение ДНК через плазматические мембраны. Возможны также прямые микроинъекции ДНК в овоциты, в культивируемые соматические клетки и в эмбрионы млекопитающих.
Важнейшим моментом, связанным с молекулярным клонированием, является поиск способа, позволяющего установить, действитель- но ли клонируемый фрагмент включился в вектор и вместе с вектором, образовав рекомбинатную молекулу ДНК, вошел в клетки. Если речь идет о бактериальных клетках, то один из способов основан на учете инсерционной инактивации плазмидного (векторного) гена резистентности. Например, в плазмидном векторе pBR 322, детерминирующем резистентность к ампициллину и тетрациклину, един- ственный сайт для рестриктазы Pst I находится в локусе, занимаемом геном резистентности к ампициллину. Pst I-плавление на этом сайте генерирует «липкие» концы, позволяющие лигирование клонируемого фрагмента с векторной ДНК. Однако при этом плазмидный (векторный) ген ампициллинрезистентности инактивируется, тогда как ген тетрациклинрезистентности на векторе остается интактным. Именно ген тетрациклинрезистентности и используется для селекции клеток, трансформируемых рекомбинантными молекулами ДНК. Это позволяет убедиться, что клетки выросших колоний на среде с тетрациклином действительно содержат рекомбинантные молекулы ДНК, их проверяют с помощью так называемого «спот-теста» на паре чашек с плотной средой, одна из которых содержит ампициллин, тогда как другая лишена этого антибиотика. Клонируемые ДНК находятся
лишь в трансформантах, резистентных к тетрациклину. Что касается трансформантов, резистентных одновременно к ампициллину и тетрациклину (АрТс), то они содержат плазмидные (векторные) молекулы, которые спонтанно приобрели кольцевую форму без включения в них чужеродной (клонируемой) ДНК.
Другой способ обнаружения инсерции чужеродных (клонируемых) фрагментов в плазмидный вектор основан на использовании вектора, содержащего ген β-галактозидазы. Инсерция чужеродной ДНК в этот ген неизбежно инактивирует синтез β-галактозидазы, что может быть обнаружено посевом трансформированных клеток на среду, которая содержит субстраты β-галактозидазы. Эта среда позволяет селекцию окрашенных колоний клеток. Существуют и другие методы.
Как уже отмечено, рестрикционные линейные фрагменты векторной ДНК способны к восстановлению кольцевой структуры без включения в них клонируемых сегментов. Чтобы уменьшить частоту спонтанного образования таких кольцевых молекул векторной ДНК, рестрикты векторной ДНК обрабатывают фосфатазой. В результате этого образование кольцевых молекул ДНК становится невозможным, поскольку будут отсутствовать концы 5'-РО4, необходимые для действия лигазы.
Совокупность колоний-трансформантов, выросших на селективной среде, представляет собой совокупность клеток, содержащих клоны разных фрагментов (генов) клонируемой геномной или кДНК. Коллекции этих клонов формируют так называемые библиотеки ДНК, широко используемые в генно-инженерных работах.
Заключительной стадией клонирования генов является выделение и исследование клонированной ДНК, включая секвенирование. Перспективные штаммы бактерий или соматических клеток, содержащих рекомбинантные молекулы ДНК, которые контролируют синтез интересующих белков, имеющих коммерческую ценность, передают в промышленность.
КЛЕТОЧНАЯ ИНЖЕНЕРИЯ
Как отмечено в начале главы, клеточной инженерией называют генетические манипуляции с изолированными клетками животных и растений. Эти манипуляции часто осуществляют in vitro, а главной целью они имеют получение генотипов этих организмов с заданными свойствами, в первую очередь хозяйственно полезными. Что касает-
ся человека, то клеточная инженерия оказалась применимой к его половым клеткам.
Предпосылкой к развитию клеточной инженерии у человека и животных явилась разработка методов культивирования их сома- тических клеток на искусственных питательных средах, а также получение гибридов соматических клеток, включая межвидовые гибриды. В свою очередь успехи в культивировании соматических клеток оказали влияние на изучение половых клеток и оплодотворения у человека и животных. Начиная с 60-х гг. ХХ в. в нескольких лабораториях мира были выполнены многочисленные эксперименты по пересадке ядер соматических клеток в яйцеклетки, искусственно лишенные ядер. Результаты этих экспериментов часто были противоречивы, но в целом они привели к открытию способности клеточных ядер обеспечивать нормальное развитие яйцеклетки (см. гл. IV).
На основе
результатов изучения развития оплодотворенных яйцеклеток в 60-е гг. XX
в. были начаты также исследования по выяснению возможности
оплодотворения яйцеклеток вне организма матери. Очень быстро эти
исследования привели к открытию возможности оплодотворения яйцеклеток
сперматозоидами в пробирке и дальнейшего развития образованных таким
путем зародышей при имплантации в матку женщины. Дальнейшее
совершенствование разработанных в этой области методов привело к тому,
что рождение «пробирочных» детей стало реальностью. Уже к
В
Под влиянием результатов, связанных с получением «пробирочных» детей, у животных тоже была разработана технология, получившая название трансплантации эмбрионов. Она связана с разработкой способа индукции полиовуляции, способов искусственного оплодот- ворения яйцеклеток и имплантации зародышей в организм животных - приемных матерей. Суть этой технологии сводится к следую-
щему. Высокопродуктивной корове вводят гормоны, в результате чего наступает полиовуляция, заключающаяся в созревании сразу 10-20 клеток. Затем яйцеклетки искусственно оплодотворяются мужскими половыми клетками в яйцеводе. На 7-8-й день зародыши вымывают из матки и трансплантируют в матки другим коровам (приемным матерям), которые затем дают жизнь телятам-близнецам. Телята наследуют генетический статус своих подлинных родителей.

Рис. 130. «Пробирочные» дети
Другой областью клеточной инженерии у животных является создание трансгенных животных. Наиболее простой способ получения таких животных заключается во введении в яйцеклетки исходных животных линейных молекул ДНК. Животные, развившиеся из оплодотворенных таким образом яйцеклеток, будут содержать в одной из своих хромосом копию введенного гена и, кроме того, они будут передавать этот ген по наследству. Более сложный способ получения трансгенных животных разработан на мышах, различающихся по окраске шерстного покрова, и сводится к следующему. Вначале из организма беременной серой мыши извлекают четырехдневных зародышей и измельчают их на отдельные клетки. Затем из эмбриональных клеток извлекают ядра, переносят их в яйцеклетки черных мышей, предварительно лишенных ядер. Яйцеклетки черных мышей, содержащие чужие ядра, помещают в пробирки
с питательным раствором для дальнейшего развития. Развившиеся из яйцеклетки черных мышей зародыши имплантируют в матки белых мышей. Таким образом, в этих экспериментах удалось получить клон мышей с серой окраской шерстного покрова, т.е. клонировать эмбриональные клетки с заданными свойствами. В главе IV мы рассмотрели результаты оплодотворения искусственно лишенных ядер яйцеклеток овец ядерным материалом соматических клеток животных этого же вида. В частности, из яйцеклеток овец удаляли ядра, а затем в такие яйцеклетки вводили ядра соматических клеток (эмбриональных, плодовых или клеток взрослых животных), после чего оплодотворенные таким образом яйцеклетки вводили в матки взрослых овец. Рождающиеся ягнята оказались идентичными овцедонору. Пример - овца Долли. Получены также клоновые телята, мыши, кролики, кошки, мулы и другие животные. Такое конструирование трансгенных животных представляет собой прямой путь клонирования животных с хозяйственно полезными признаками, включая особей определенного пола.
Трансгенные животные получены также при использовании исходного материала, принадлежащего разным видам. В частности, известен способ передачи гена, контролирующего гормон роста, от крыс в яйцеклетки мышей, а также способ комбинирования бластомеров овцы с бластомерами козы, что привело к возникновению гибридных животных (ковец). Эти эксперименты указывают на воз- можность преодоления видовой несовместимости на самых ранних этапах развития. Особенно заманчивые перспективы открываются (если видовая несовместимость будет преодолена полностью) на пути оплодотворения яйцеклеток одного вида ядрами соматических клеток другого вида. Речь идет о реальной перспективе создания хозяйственно ценных гибридов животных, которых невозможно получить путем скрещиваний.
Следует отметить, что ядерно-трансплантационные работы еще не очень эффективны. Эксперименты, выполненные на земноводных и млекопитающих, в целом показали, что их результативность является небольшой, причем она зависит от несовместимости между донорскими ядрами и реципиентными овоцитами. Кроме того, препятствием на пути к успехам являются также образующиеся хромосомные аберрации в трансплантированных ядрах в ходе даль- нейшего развития, которые сопровождаются гибелью трансгенных животных.
На стыке работ по изучению гибридизации клеток и иммунологических исследований возникла проблема, связанная с получением и изучением так называемых моноклональных антител. Как отмечено выше, антитела, продуцируемые организмом в ответ на введение антигена (бактерии, вирусы, эритроциты и т.д.), представляют собой белки, называемые иммуноглобулинами и составляющие фундаментальную часть защитной системы организма против возбудителей болезней. Но любое чужеродное тело, вводимое в организм, представляет собой смесь разных антигенов, которые будут возбуждать продукцию разных антител. Например, эритроциты человека обладают антигенами не только для групп крови А (II) и В (III), но и многими другими антигенами, включая резус-фактор. Далее, белки клеточной стенки бактерий или капсида вирусов также могут действовать в качестве разных антигенов, вызывающих образование разных антител. В то же время лимфоидные клетки иммунной системы организма обычно представлены клонами. Значит, даже только по этой причине в сыворотке крови иммунизированных животных антитела всегда представляют собой смесь, состоящую из антител, продуцируемых клетками разных клонов. Между тем для практических потребностей необходимы антитела только одного типа, т.е. так называемые моноспецифические сыворотки, содержащие антитела только одного типа или, как их называют, моноклональные антитела.
В поисках методов получения моноклональных антител швейцарскими исследователями в
желаемым антигеном. Слияния клеток достигают смешиванием их в присутствии полиэтиленгликоля, который индуцирует слияние клеточных мембран, а затем в высеве их на питательную среду, позволяющую рост и размножение только гибридных клеток (гибридом). Размножение гибридом проводят в жидкой среде, где они растут далее и секретируют антитела в культуральную жидкость, причем только одного типа, к тому же в неограниченных количествах. Эти антитела получили название моноклональных. Чтобы повысить частоту образования антител, прибегают к клонированию гибридом, т.е. к селекции отдельных колоний гибридом, способных вызывать образование наибольшего количе- ства антител желаемого типа. Моноклональные антитела нашли широкое применение в медицине для диагностики и лечения ряда болезней. В то же время важнейшее преимущество моноклональной технологии заключается в том, что с ее помощью могут быть получены антитела против материалов, которые невозможно очистить. Напротив, можно получить моноклональные антитела против клеточных (плазматических) мембран нейронов животных. Для этого мышей иммунизируют выделенными мембранами нейронов, после чего их селезеночные лимфоциты объединяют с миеломными клетками, а дальше поступают, как описано выше.
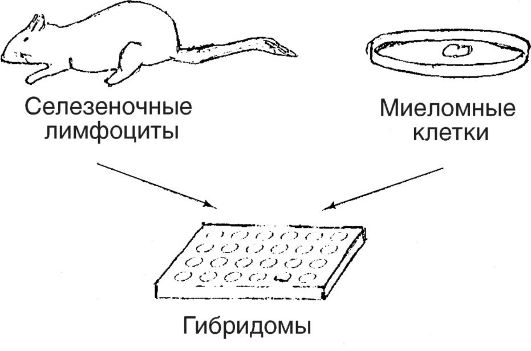
Рис. 131. Получение моноклональных антител
ГЕНЕТИЧЕСКАЯ ИНЖЕНЕРИЯ И МЕДИЦИНА
Генная инженерия оказалась очень перспективной для медицины, прежде всего в создании новых технологий получения физиологически активных белков, используемых в качестве лекарств (инсулин, соматостатин, интерфероны, соматотропин и др.).
Инсулин используют для лечения больных диабетом, который стоит на третьем месте (после болезней сердца и рака) по частоте вызываемых смертельных случаев. Мировая потребность инсулина составляет несколько десятков килограммов. Традиционно его получают из панкреатических желез свиней и коров, но гормоны этих животных слегка отличаются от инсулина человека. Инсулин свиней различается по одной аминокислоте, а коровий - по трем. Считают, что инсулин животных часто вызывает побочные эффекты. Хотя химический синтез инсулина осуществлен давно, но до сих пор промышленное производство гормонов оставалось очень дорогим. Сейчас получают дешевый инсулин с помощью генно-инженерного метода путем химико-ферментативного синтеза гена инсулина с последующим введением этого гена в кишечную палочку, которая затем синтезирует гормон. Такой инсулин более «биологичен», так как химически идентичен инсулину, вырабатываемому клетками поджелудочной железы человека.
Интерфероны - белки, синтезируемые клетками главным образом в ответ на заражение организма вирусами. Интерфероны характери- зуются видовой специфичностью. Например, у человека установлены три группы интерферонов, продуцируемых различными клетками под контролем соответствующих генов. Интерес к интерферонам определяется тем, что их широко используют в клинической практике для лечения многих болезней человека, особенно вирусных.
Имея крупные размеры, молекулы интерферона мало доступны для синтеза. Поэтому большинство интерферонов сейчас получают из крови человека, но выход при таком способе получения небольшой. Между тем потребности в интерфероне исключительно велики. Это поставило задачу изыскать эффективный метод производства интерферона в промышленных количествах. Генетическая инженерия лежит в основе современного производства «бактериального» интерферона.
Усилилось влияние генетической инженерии на технологию тех лекарственных веществ, которые уже давно создаются по био- логической технологии. Еще в 40-50-е гг. XX в. была создана
биологическая промышленность для производства антибиотиков, которые составляют наиболее эффективную часть лекарственного арсенала современной медицины. Однако в последние годы отмечается значительный рост лекарственной устойчивости бактерий, особенно к антибиотикам. Причина заключается в широком распространении в микробном мире плазмид, детерминирующих лекарственную устойчивость бактерий. Именно поэтому многие знаменитые ранее антибиотики утратили свою былую эффективность. Единственный пока путь преодоления резистентности бактерий к антибиотикам - это поиски новых антибиотиков. По оценкам специалистов, в мире ежегодно создают около 300 новых антибиотиков. Однако большинство из них либо неэффективно, либо токсично. В практику же каждый год вводится лишь несколько антибиотиков, что заставляет не только сохранять, но и увеличивать мощность антибиотической промышленности на основе генно-инженерных разработок.
Для лечения паразитарных и многих неинфекционных болезней в течение длительного времени используют лекарственные вещества, полученные в процессе химического синтеза, однако некоторые из них вредны для организма. Поэтому наметилась тенденция расширить производство микробных метаболитов (других, кроме антибиотиков), перспективных в качестве лекарственных веществ. Еще в начале XX в. В.Л. Омелянский разработал теоретические основы учения о трансформирующей активности микроорганизмов. Вызывая окисление, восстановление, гидратацию, дегидратацию, полимеризацию и другие реакции, микроорганизмы многих видов способны изменять субстрат, на который они воздействуют, трансформировать химические соединения. В настоящее время на трансформирующей способности микроорганизмов основан ряд производств, выпускающих из стероидного сырья растительного происхождения вещества с фармакологическими свойства. Например, с помощью микроскопических грибов трансформируют стероидные соединения в кортизон и гидрокортизон. Актиномицеты и бактерии используются для производства преднизолона, диакабола и т.д., имеющих большое значение в медицине.
Основные задачи генной инженерии в тех технологиях лекарственных веществ, в которых продуцентами лекарств являются микроорганизмы, определяются необходимостью генно-инженерной реконструкции последних с целью повышения их активности. В то же
время началась реализация идеи создания лекарств в виде малых молекул, что способствует их большей эффективности.
Иммунная биотехнология связана с производством прежде всего вакцин нового поколения для профилактики инфекционных болезней человека и животных. Первыми коммерческими продуктами, созданными с помощью генетической инженерии, стали вакцины против гепатита людей, ящура животных и некоторые другие. Исключительно важное направление в этой области связано с производством моноклональных антител, реагентов, необходимых для диа- гностики возбудителей болезни, а также для очистки гормонов, витаминов, белков различной природы (ферментов, токсинов и др.).
Значительный практический интерес представляет метод получения искусственного гемоглобина путем введения гемоглобиновых генов в растения табака, где под контролем этих генов продуциру- ются α- и β-цепи глобина, которые объединяются в гемоглобин. Синтезируемый в клетках табачных растений гемоглобин полностью функционален (связывает кислород). Клеточная инженерия в применении к человеку связана не только с решением фундаментальных проблем биологии человека, но и с преодолением прежде всего женского бесплодия. Поскольку частота положительных случаев имплантации в матку женщин эмбрионов, полученных in vitro, является небольшой, то получение монозиготных близнецовэмбрионов in vitro также имеет значение, так как увеличиваются возможности повторных имплантаций за счет «запасных» эмбрионов. Особый интерес представляют перспективы использования стволовых клеток в качестве источника замены клеток и тканей в лечении таких болезней, как диабет, повреждения спинного мозга, боли сердца, остиоартриты, болезнь Паркинсона. Но для реализации этих перспектив необходимо углубленное изучение биологии стволовых клеток.
В использовании генетической инженерии применительно к проблемам медицины особое значение приобрела задача разработки генно-инженерных методов радикального лечения наследственных болезней, которые, к сожалению, еще не поддаются лечению существующими методами. Содержание этой задачи заключается в разработке способов исправления (нормализации) мутаций, результатом которых являются наследственные болезни, и в обеспечении передачи «исправлений» по наследству. Считают, что успешной разработке генно-инженерных методов лечения наследственных болезней будут
способствовать данные о геноме человека, полученные в результате выполнения международной научной программы «Геном человека».
ЭКОЛОГИЧЕСКИЕ ПРОБЛЕМЫ ГЕНЕТИЧЕСКОЙ ИНЖЕНЕРИИ
Подняв на новый уровень биотехнологию, генетическая инженерия нашла также применение в разработке способов определения и устранения загрязнений окружающей среды. В частности, сконструированы штаммы бактерий, которые являются своеобразными индикаторами мутагенной активности химических загрязнений. С другой стороны, генно-инженерным способом сконструированы штаммы бактерий, содержащие плазмиды, под контролем которых происходит синтез ферментов, способных разрушать многие химические соединения- загрязнители среды обитания. В частности, некоторые плазмидосодержащие бактерии способны разлагать до безвредных соединений нефть и нефтепродукты, оказавшиеся в среде в результате различных аварий или других неблагоприятных причин.
Однако генетическая инженерия - это превращение генетического материала, которое в природе отсутствует. Следовательно, продукты генной инженерии - это абсолютно новые продукты, не существующие в природе. Поэтому она сама по себе из-за неизвестности ее продуктов таит опасность как для природы и среды обитания, так и для персонала, работающего в лабораториях, где используют методы генетической инженерии или работают со структурами, созданными в ходе генно-инженерных работ.
Поскольку возможности клонирования генов безграничны, то еще в самом начале этих исследований среди ученых возникли вопросы о природе создаваемых организмов. Одновременно были высказаны предположения о ряде нежелательных последствий этой методологии, причем эти предположения нашли поддержку и среди широкой общественности. В частности, появились раз- ногласия о свойствах бактерий, получивших в генно-инженерных экспериментах гены животных. Например, сохраняют ли бактерии Е. coli свою видовую принадлежность из-за содержания введенных в них генов животного происхождения (например, гена инсулина) или их следует считать новым видом? Далее, насколько долговечны такие бактерии, в каких экологических нишах они могут
существовать?
Но самое главное стало заключаться в появлении опасений, что в ходе
производства и манипуляций с рекомбинантными молекулами ДНК могут быть
созданы генетические структуры со свойствами, непредвиденными и
опасными для здоровья человека, для исторически сложившегося
экологического равновесия. Тогда же начались и призывы к мораторию на
генетическую инженерию. Эти призывы вызвали международный резонанс и
привели к международной конференции, которая состоялась в
Другой аспект нежелательных последствий генно-инженерных работ связан с опасностью для здоровья персонала, работающего в лабораториях, где применяют методы генетической инженерии, поскольку в таких лабораториях используют фенол, этидий бромид, УФ-излучения, которые являются вредными для здоровья факторами. Кроме того, в этих лабораториях существует возможность заражения бактериями, содержащими рекомбинантные молекулы ДНК, контролирующие нежелательные свойства, например лекарственную резистентность бактерий. Эти и другие моменты определяют необходимость повышения уровня техники безопасности в генноинженерных работах.
Наконец, широко обсуждаются в обществе проблемы опасности генетически модифицированных продуктов (генетически изме- ненных томатов, картофеля, кукурузы, сои), а также таких продуктов, как хлеб, пасты, конфеты, мороженое, сыр, растительное масло, мясные продукты, которые в ряде стран, особенно в США, приобрели широкое распространение. На протяжении 12 000 лет сельского хозяйства человек употреблял продукты естественного происхождения. Поэтому предполагают, что с генетически модифицированной пищей в организм человека попадут новые токсины, аллергены, бактерии, канцерогены, что приведет к совершенно новым болезням будущих поколений. В связи с этим возникает вопрос о подлинно научной оценке генетически модифицированной пищи.
ВОПРОСЫ ДЛЯ ОБСУЖДЕНИЯ
1. Что понимают под генной, клеточной и генетической инженерией? Есть ли разница между этими понятиями и молекулярном клонировании?
2. В чем заключается прогрессивность генетической инженерии по сравнению с другими методами, используемыми в биологии?
3. Перечислите основные «инструменты» генной инженерии.
4. Что представляют собой ферменты-рестриктазы, каковы их свойства и их роль в генной инженерии?
5. Все ли рестриктазы образуют «липкие» концы исследуемых ДНК и зависит ли структура «липких» концов от вида рестриктазы?
6. Дайте определение генетическим векторам. Существуют ли природные векторы?
7. Как получают генетические векторы в лабораторных условиях? Какие биологические объекты являются исходным материалом для получения векторов?
8. Какова предельная длина последовательностей азотистых оснований ДНК, которые еще могут включиться в генетический вектор? Различаются ли векторы по «мощности»?
9. Охарактеризуйте свойства ДНК-лигазы и определите ее роль в генной инженерии.
10. Как смыкают клонируемый сегмент ДНК (ген) с генетическим вектором?
11. Какова частота введения рекомбинантных молекул ДНК в бактериальные клетки?
12. На каком принципе основана селекция бактериальных клеток, содержащих рекомбинантные молекулы ДНК? Приведите один из примеров такой селекции.
13. Можно ли считать штамм Е. coli, содержащий ген инсулина человека, новым видом бактерий?
14. Многие штаммы бактерий обладают одинаковыми ферментами, практически одинаково обеспечивающими их метаболизм. Между тем нуклеотидная специфичность систем рестрикции-модификации бактерий различна. Можете ли вы объяснить это явление?
15. Почему последовательности ДНК, представляющие сайты распознавания рестриктазами, не могут содержать более восьми пар оснований?
16. Сколько раз последовательность ГГЦЦ, распознаваемая рестриктазой Нае III, будет встречаться в сегменте ДНК длиной в 50 000 пар оснований с 30-, 50- и 70-процентным содержанием ГЦ?
17. Рестриктазы Bam HI и Bgl I плавят последовательности Г ГАТЦЦ и Т ГАТЦА соответственно. Можно ли включить в сайт Bam HI фрагменты ДНК, продуцированные Bgl I-рестрикцией? Если да, то почему? Если используемая плазмида (вектор) содержит один сайт для рестрикции Bgl I, то на какой питательной среде можно осуществить селекцию бактерий, эту плазмиду?
18. Вычислите частоту трансформации бактерий на одну молекулу ДНК, если на 5000 плазмидных пар оснований образуется 5-105 трансформантов?
19. Можно ли клонировать 0-пункт репликации ДНК Е. coli и если да, то каким образом?
20. Можно ли определить, сколько необходимо молекул ДНК для трансформации одной клетки Е. coli?
21. Можно ли с помощью полимеразной цепной реакции определить сайт сплайсинга на мРНК?
22. Каким образом можно использовать полимеразную цепную реакцию для того, чтобы ввести желаемый сайт рестрикции в интересующее место на фрагменте ДНК, предназначенном для клонирования?
23. Назовите методы клеточной инженерии в применении к животным. Какова хозяйственная ценность животных, получаемых этими методами?
24. Дайте определение понятиям «трансгенные растения» и «трансгенные животные». Сохраняют ли трансгенные организмы свою видовую принадлежность или их можно считать организмами новых видов?
25. Что такое гибридомы и моноклональные антитела? Как их получают?
26. Применима ли клеточная инженерия к человеку?
27. Допустим, что инъекция чужеродной ДНК в яйцеклетку мыши и имплантация оплодотворенной таким путем яйцеклетки в организм мыши закончились ее беременностью и рождением мышат, содержащих в геноме копии инъецированной ДНК. Однако мышата оказались мозаиками, т.е. одни их клетки содержат копии инъецированной ДНК, другие лишены этой ДНК. Можете ли вы объяснить природу этого явления?
28. Считаете ли вы генетически опасной пищу, приготовленную из генетически измененных продуктов?
29. Необходима ли научная экспертиза генетически измененных продуктов питания?
Познание определяется тем, что утверждается нами как Истина.
П.А. Флоренский, 1923