Общее обезболивание и седация в детской стоматологии: Руководство/ В.И. Стош, С.А. Рабинович и др. 2007 - 184 с.
|
|
|
|
ГЛАВА 4 ОСОБЕННОСТИ ЛЕКАРСТВЕННОЙ ТЕРАПИИ У ДЕТЕЙ
Несмотря на кажущуюся «не очень большую» значимость данного вопроса для врачей-стоматологов, наш педагогический опыт показал, что знаний курсантов ФПКС, участвующих в циклах «Обезболивание и неотложная помощь в стоматологии», недостаточно, но и у врачейанестезиологов некоторые позиции связанные с ним нуждаются в уточнении.
Лекарственная терапия в детском возрасте существенным образом отличается от таковой у взрослых не только в количественном, но и качественном отношении.
При назначении лекарств в детском возрасте имеют значение как моменты индивидуального характера, так и специфические особенности разных периодов детства. У взрослых существует тесная корреляция между дозой лекарства и массой тела, а во многих случаях возраст не имеет значения. У детей необходимо учитывать типичные особенности разных возрастных периодов.
Период новорожденности характеризуется функциональной и морфологической незрелостью, и это обязывает врача проявлять особую осторожность и даже отказываться от некоторых лекарственных средств. Ребенок грудного возраста отличается быстрым нарастанием массы и роста, повышенным содержанием воды в организме, переходным синдромом недостаточности антител и усиленным обменом веществ. В препубертатном и пубертатном периодах наступают значительные колебания гормонального гомеостаза в организме.
Все это вызывает даже при точном определении доз лекарства в разные периоды детского возраста весьма разнообразные, а в некоторых случаях и неожиданные реакции. Гораздо больше у детей, чем у взрослых, лекарственная терапия находится под контролем генотипа. Например, отсутствие или недостаточность некоторых ферментов (эритроцитарная глутатионредуктаза, ацетилтрансфераза печени, недостаточность глюкозо-6-фосфатдегидрогеназы и др.) могут вызвать неожиданные побочные явления даже при самой осторожной и точной дозировке лекарства [10, 20, 41].
4.1. ПЕРИОД НОВОРОЖДЕННОСТИ
Первые 28 дней жизни - это период адаптации после внутриутробной к самостоятельной жизни, характеризующийся повышенными требованиями к организму. Почти все принятые вещества (ксенобиотики) превращаются в другие соединения, а в этом важную роль играют процессы конъюгации и очищения. Центральный орган в метаболизме лекарственных средств - печень. Среди множества ферментов, образующихся в печени, для медикаментозной терапии особое значение имеет глюкуронилтрансфераза, принимающая активное участие в обмене билирубина, который во время новорожденности образуется в резко повышенных количествах. Ввиду низкого содержания глюкуронилтрансферазы в печени (около 1/100 количества взрослых) у новорожденного развивается физиологическая желтуха. Разные вещества могут вытеснять этот фермент из его соединений с билирубином, в результате чего развивается желтуха. В организме новорожденного отсутствуют или имеются в минимальных количествах и другие ферменты, которые прямо или косвенно принимают участие в расщеплении лекарственных средств. Так, например, нет фермента, расщепляющего молекулу кортизола. Побочные явления у детей старшего возраста при назначении им гексобарбитала и аминопирина связаны с недостаточным окислением, вызванным отсутствием соответствующих ферментов. Жизнь эритроцитов новорожденного на 25% короче, чем у взрослого из-за преходящей недостаточности глюкозо-6-фосфат-дегидрогеназы. Этим объясняются нежелательные побочные явления, которые наблюдаются при назначении некоторых лекарственных препаратов. У новорожденных нарушена также и редукционная способность эритроцитов. Вследствие отсутствия или снижения содержания метгемоглобинредуктазы и каталазы, а также и из-за более быстрого окисления фетального гемоглобина (HbF) новорожденные гораздо более чувствительны к веществам, образующим метгемоглобин.
Процесс ацетилирования, играющий важную роль в биологической трансформации некоторых веществ, также недостаточен у новорожденных и недоношенных вследствие незрелости печени. Это надо иметь в виду при назначении лекарственных средств (например, римицида). Опасность возникновения нежелательных побочных явлений в периоде новорожденности обусловлена недостаточным выделением и обезвреживанием токсичных веществ почками, при этом экскреция почечны-
ми канальцами более ограничена, чем клубочковая фильтрация. Исследование уровня разных лекарственных средств в крови новорожденных и недоношенных детей показали, что он не только выше, но и медленнее снижается.
Это касается в первую очередь антибиотиков, но и особо токсичные, как например хлорамфеникол и стрептомицин, а также сульфаниламидные препараты в этом возрасте не назначают. С другой стороны, медленное выведение имеет то преимущество, что позволяет уменьшить число приемов препарата.
В период новорожденности резко повышена проницаемость слизистой оболочки органов пищеварения в отношении разных лекарственных средств, обусловленная недостаточной секрецией соляной кислоты и пепсиногена желудком, а также низким содержанием ферментов поджелудочной железы липазы и амилазы. В этот период жизни также низко количество дисахаридазы. Усиленная и ускоренная резорбция в желудочно-кишечном тракте для некоторых веществ может оказаться и преимуществом.
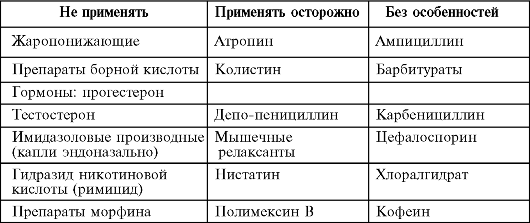
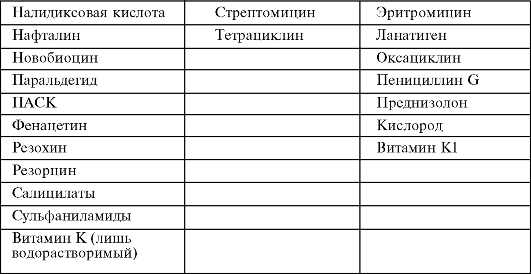
Ввиду функциональной незрелости новорожденного следует избегать тех лекарственных препаратов, которые ингибируют или вызывают поражение дыхательного центра, и в первую очередь соединений морфина. Таким образом, очевидно, что в период новорожденности и у недоношенных детей следует проявлять особую осторожность при назначении лекарственных средств (табл. 11).
Таблица 11.
Применение лекарственных средств у новорожденных и недоношенных детей
 4.2. НЕДОНОШЕННЫЕ ДЕТИ
4.2. НЕДОНОШЕННЫЕ ДЕТИ
Все особенности неонатального периода еще в большей мере относятся к недоношенным детям, у которых функциональная и морфологическая незрелость ферментных систем, печени и почек выражены еще сильнее, а приспособление к внеутробной жизни длится гораздо дольше. В этом возрасте играют важную роль выраженная незрелость дыхательного центра и неполноценность терморегуляции. Ввиду огромной относительной поверхности тела недоношенных дозу лекарственных препаратов определяют из расчета на килограмм массы тела. Необходимо обратить внимание на обстоятельство, что с молоком матери выделяется большая часть принятых ею лекарств, что может привести к побочным явлениям и даже отравлению ребенка.
4.3. ДОШКОЛЬНЫЙ ВОЗРАСТ
Особенностью этого возраста является высокое содержание воды в тканях и относительно большая поверхность тела, что также надо иметь в виду при определении доз лекарственных средств. В этом возрасте важно найти способ ввести его в виде не отвергаемом ребенком.
4.4. ШКОЛЬНЫЙ ВОЗРАСТ
Этот период характеризуется усиленным ростом и гормональной адаптацией. Что касается массы тела и роста, многие дети «догоняют» взрослых, но полной зрелости еще не достигают, поэтому дозирование лекарственных средств должно быть индивидуализированным, в зависимости от их переносимости, физического развития ребенка и тяжести заболевания.
4.5. ПРОБЛЕМЫ ДОЗИРОВАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Оптимальное дозирование лекарственных препаратов в детском возрасте определяют множество факторов: период детства (возраст), масса и поверхность тела, характер и тяжесть заболевания, способ применения, всасывание и выведение, вкусовые качества лекарства, цель медикаментозной терапии (ударные дозы, поддерживающие дозы, профилактика), наличие побочных явлений.
Особое значение при дозировании лекарств имеет структура организма детей, который в значительной мере отличается от организма взрослых. Внеклеточная жидкость у новорожденных представляет 45%, а у взрослых - 15% массы тела. Внутриклеточная жидкость и твердые составные части (белки, жиры и микроэлементы) в первые дни новорожденности представляют лишь 29%, а у взрослых - 54% общей массы тела.
В зависимости от химических, физических и физиологических свойств, разные лекарственные средства распределяются в экстра- и интрацеллюлярных пространствах. Поэтому эффективного лечения не следует ожидать лишь на основании определения абсолютного содержания в крови, так как результат зависит от концентрации действующего вещества в очаге болезни. Так, например, некоторые антибиотики достигают очень различных концентраций в крови, тканях, полостях тела, и именно это определяет эффективность их терапевтического воздействия. Они, и в особенности пенициллиновые соединения и тетрациклиновые препараты, распределяются главным образом в экстравазальных пространствах, вот почему грудным детям назначают в 2 раза большие дозы, чем взрослым. Что касается конкретного дозирования лекарств в детском возрасте, то существуют несколько возможностей: дозирование, связанное с дозой
для взрослых; дозирование в зависимости от возраста ребенка; определение дозы эмпирическим путем; дозирование в зависимости от массы и определение дозы в зависимости от поверхности тела [10].
Определение дозы лекарственного средства для детей как той или иной части дозы взрослого, необходимой в данном возрасте ребенку, уже практически не используют (табл. 12). Данный способ дозирования неточен, основан только на возрасте ребенка и не учитывает его индивидуальных особенностей. Для некоторых препаратов доза определяется эмпирическим путем. Это касается главным образом лекарственных средств, для которых, имея в виду особенности организма детей, невозможно использовать определенные расчетные формулы.
Таблица 12.
Дозировка лекарственных препаратов у детей
Возраст | Часть дозы для взрослого | Дозис-фактор по Harnack |
1 мес | 1/10 | 1,8 / от 0 до 1 года/ |
6 мес | 1/5 | 1,8 / от 0 до 1 года/ |
1 год | 1/4 | 1,8 / от 0 до 1 года/ |
3 года | 1/3 | 1,6 / от 1 до 6 лет/ |
7 лет | 1/2 | 1,4 /от 6 до 10 лет/ |
12 лет | 2/3 | 1,2 /от 10 до 12 лет/ |
Взрослый | 1 | 1,0 |
В детском возрасте преобладающее значение имеет определение дозы в зависимости от массы и поверхности тела. Оба метода взаимно дополняются в зависимости от вида лекарства. Они позволяют легко вычислить необходимую дозу в зависимости от массы, а для определения площади поверхности тела существуют номограммы или таблицы (табл. 13). Расчет дозы с применением дозис-фактора Харнака проводится по формуле:
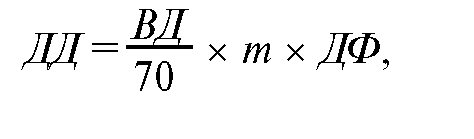 в которой ДД - детская доза; ВД - взрослая доза; m - масса тела ребенка, кг; ДФ - дозис-фактор. Расчет по данной формуле позво-
в которой ДД - детская доза; ВД - взрослая доза; m - масса тела ребенка, кг; ДФ - дозис-фактор. Расчет по данной формуле позво-
ляет более точно определить необходимые для конкретного ребенка дозировки лекарственных препаратов, поскольку учитывается конкретная масса тела ребенка и возрастные особенности обменных процессов [39].
Однако существует возможность еще более точно вычислить необходимую данному конкретному ребенку дозировку лекарственных препаратов на основании площади поверхности его тела. В данном случае применяют следующую формулу:
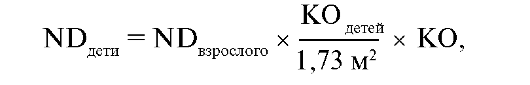 где ND - нормальная доза; КО - поверхность тела.
где ND - нормальная доза; КО - поверхность тела.
Таблица 13.
Соотношение поверхности тела в зависимости от возраста, роста и массы тела ребенка
Возраст | Масса, кг | Рост, см | Поверхность тела, м2 | Процентное отношение к взрослым | |
% массы | % поверхности | ||||
Новорожденные | 3,5 | 50 | 0,25 | 5 | 14 |
2-3 мес | 5 | 60 | 0,28 | 8 | 16 |
6 мес | 7,5 | 65 | 0,35 | 11 | 20 |
1 год | 10 | 75 | 0,43 | 15 | 25 |
3 года | 15 | 97 | 0,6 | 23 | 35 |
6 лет | 20 | 115 | 0,85 | 30 | 46 |
7 лет | 23 | 123 | 0,9 | 35 | 50 |
9 лет | 28 | 135 | 1,0 | 42 | 50 |
10 лет | 30 | 140 | 1,05 | 46 | 60 |
12 лет | 40 | 142 | 1,2 | 62 | 70 |
14 лет | 50 | 150 | 1,43 | 77 | 86 |
Взрослые | 70 | 162 | 1,73 | 100 | 100 |
4.6. СПОСОБЫ ПРИМЕНЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Способы применения лекарственных средств в детском возрасте зависят от возраста ребенка, характера заболевания, резорбции лекарства, места проведения лечения (на дому, в стационаре).
Пероральное применение предпочитают в детском возрасте за исключением тех случаев, когда имеются резко выраженное отсутствие аппетита, тошнота или рвота. Детям младше 5 лет предпочитают давать жидкую форму лекарства: капли, микстуры и др., которые должны иметь приятный вкус (с этой целью добавляют соответствующие средства). Препараты, выпускаемые лишь в форме таблеток, необходимо заранее измельчать и давать вместе со сладкими жидкостями или фруктовыми соками. Не следует давать лекарства вместе с пищей, так как и по прекращении лечения, ребенок может отказываться от приема пищи без приятного лекарственного сопровождения. Не рекомендуется давать детям лекарства в форме таблеток для разжевывания, так как существует риск, что при недостаточном присмотре за ребенком он может поглотить большое количество таблеток и получить отравление. Чаще всего такие отравления вызываются именно лекарствами в форме таблеток, которые дети поглощают незаметно от родителей. Капсулы также следует растворять заранее и давать вместе с жидкостями. Если на это нет особых предписаний, лекарства для перорального приема лучше всего давать до еды во избежание рвоты принятой пищей.
В некоторых случаях дети отказываются принимать лекарства, поэтому необходимо расспрашивать подробно о проведенном лечении в прошлом. Следует учитывать, что не всегда рвота после приема лекарства - признак его непереносимости, так как у некоторых детей рвота начинается при одном лишь виде лекарства [20].
Ректальное применение. Очень часто детям, находящимся в лихорадочном состоянии и склонным к рвоте, а также капризным детям назначают лекарственные препараты per rectum, в виде свечей. Имеется немало жаропонижающих и обезболивающих средств, выпускаемых в форме, подходящей для ректального применения. Однако всасывание через слизистую прямой кишки не всегда адекватно, в особенности, если ампула прямой кишки заполнена фекалиями. Кроме того, применение свечей может вызвать раздражение и дефекацию с выбрасыванием лекарства, вот почему в некоторых случаях необходимо заранее сделать очиститель-
ную клизму. Доза лекарства при ректальном применении должна быть на 50% выше, чем при пероральном.
Парентеральное применение. При тяжелых заболеваниях, рвотах и отказе принимать лекарство очень часто необходимо прибегать к парентеральному, главным образом внутримышечному, пути введения. Недостатки внутримышечного введения - резкая болезненность и образование инфильтратов, асептических или микробных, а преимущества сводятся к более медленному рассасыванию и более продолжительному действию препарата. При внутримышечном введении необходимо соблюдать некоторые технические правила, а именно производить инъекцию в передневерхнюю часть бедра или наружный верхний квадрант ягодицы.
Внутривенное введение рекомендуют при самых тяжелых формах заболеваний, когда необходимо быстро получить высокую концентрацию лекарства в крови. Некоторые лекарственные средства выпускают лишь в форме, пригодной для внутривенного введения. Последнее, в особенности у грудных детей, сопряжено со значительными техническими трудностями.
Следует иметь в виду и другие способы введения лекарств детям: подкожное, внутрикожное, интраназальное, однако применение их ограничено. Внутрисердечное впрыскивание адреналина используют только по жизненным показаниям.
При назначении лекарственных средств маленьким детям следует учитывать, что при нормальном артериальном давлении и неизмененной периферической циркуляции препараты, введенные внутримышечно, оказывают действие быстрее, чем при подкожном введении [41].
При ухудшении циркуляции (шок, анемия, ацидоз) препараты, введенные как подкожно, так и в мышцу, почти не поступают в кровеносное русло, однако при улучшении циркуляции ранее введенные препараты могут быстро всосаться и вызвать передозировку. Поэтому при всех состояниях с нарушенной циркуляцией препараты следует вводить только в вену, а их дозу следует уменьшить на 20-25%.
В современной педиатрической анестезиологии, особенно амбулаторной, уделяют большое внимание относительно новым способам введения лекарств; главным образом это касается способов введения препаратов для премедикации. В течение последних 15 лет в научной литературе появилось большое количество сообщений о применении перорального, сублингвального (буккального), интраназального,
транскутанного (чрескожного) способов введения как альтернативных внутривенному и внутримышечному [55].
В табл. 14 приведены дозировки лекарственных средств, часто применяемых для премедикации у детей.
Таблица 14.
Фармакологические средства, используемые для премедикации у детей
Препарат | Дозировка, мг/кг | Препарат | Дозировка, мг/кг |
Промедол | 0,15-0,3 | Мидазолам | 0,15-0,2 |
Омнопон | 0,04-0,1 | Димедрол | 0,8-1,2 |
Фентанил | 0,008-0,0025 | Пипольфен | 0,8-1,2 |
Атропин | 0,012-0,018 | Супрастин | 0,4-0,7 |
Метацин | 0,01-0,02 | Кетамин | 2,5-3,0 |
Седуксен | 0,3-0,5 | Дроперидол | 0,3-0,5 |
* * *
Один из вариантов общей анестезии, применяемый в детской амбулаторной практике. Комбинированный наркоз смесью севорана, закиси азота и кислорода и внутривенной инфузией пропофола и мидазолама.
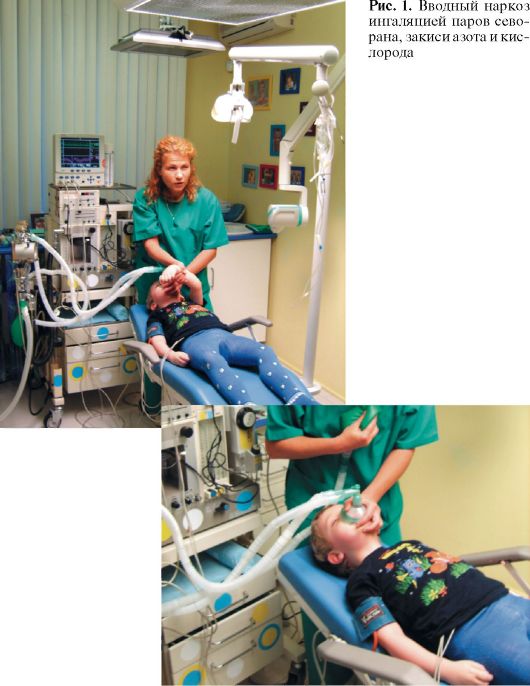 Рис. 2. Вводный наркоз - ингаляция севорана, закиси азота и кислорода
Рис. 2. Вводный наркоз - ингаляция севорана, закиси азота и кислорода
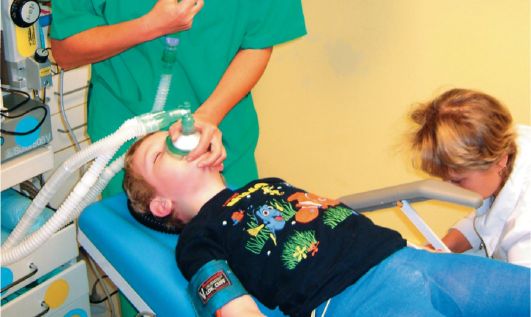 Рис. 3. Вводный наркоз продолжается, обеспечивается венозный доступ
Рис. 3. Вводный наркоз продолжается, обеспечивается венозный доступ
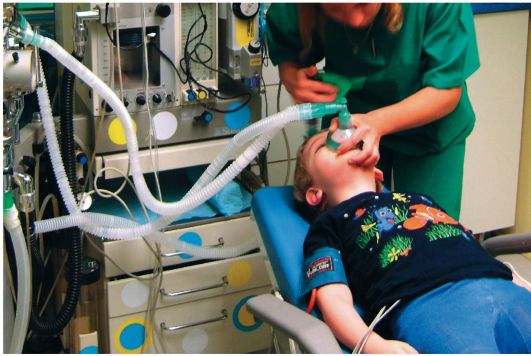 Рис. 4. Искусственная вентиляция легких после внутривенного введения миорелаксанта Цисатрикурия (Нимбекс)
Рис. 4. Искусственная вентиляция легких после внутривенного введения миорелаксанта Цисатрикурия (Нимбекс)
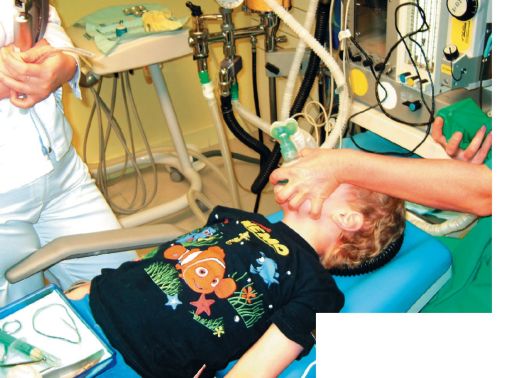 Рис. 5. Все готово к интубации трахеи. Трубка - термопластик с манжетой
Рис. 5. Все готово к интубации трахеи. Трубка - термопластик с манжетой
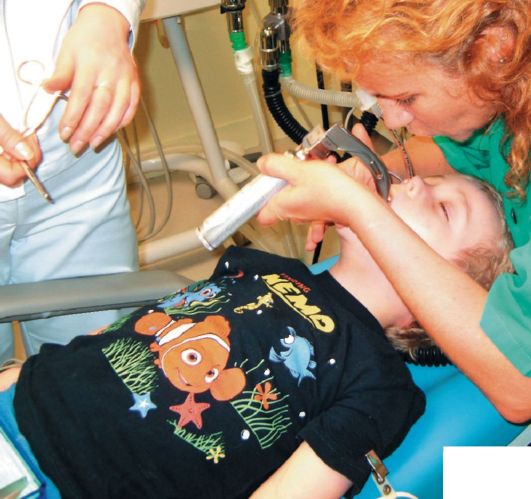 Рис. 6. Интубация трахеи
Рис. 6. Интубация трахеи
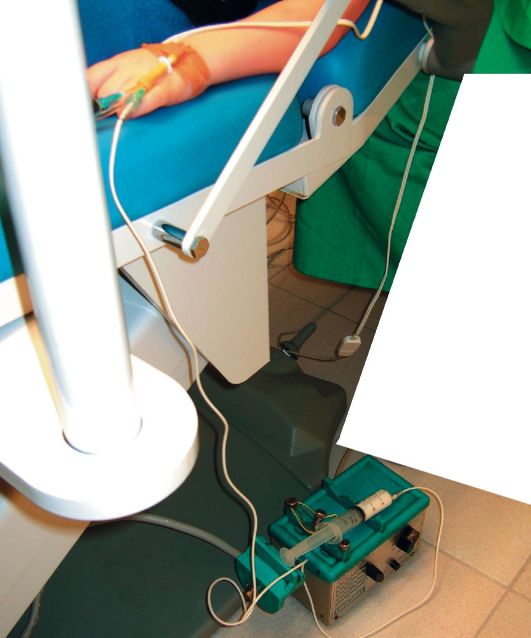 Рис. 7. Основной наркоз поддерживается внутривенной инфузией пропофола и мидазолама
Рис. 7. Основной наркоз поддерживается внутривенной инфузией пропофола и мидазолама
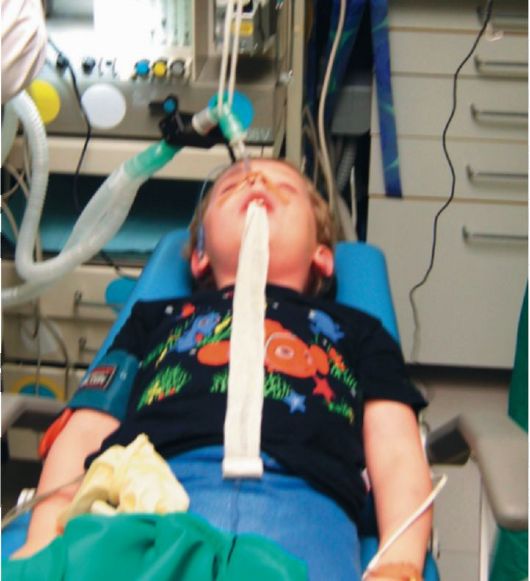 Рис.
8. Положение ребенка после интубации трахеи, интубации трахеи. Фиксация
коннектора интубационной трубки. Тампонада ротоглотки
Рис.
8. Положение ребенка после интубации трахеи, интубации трахеи. Фиксация
коннектора интубационной трубки. Тампонада ротоглотки
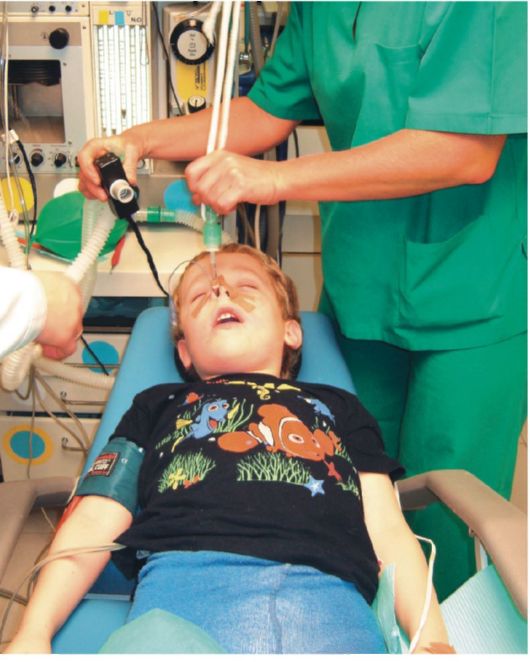 Рис. 9. Подключение датчика наркозного аппарата, определяющего концентрацию наркотизирующих агентов в дыхательной смеси
Рис. 9. Подключение датчика наркозного аппарата, определяющего концентрацию наркотизирующих агентов в дыхательной смеси
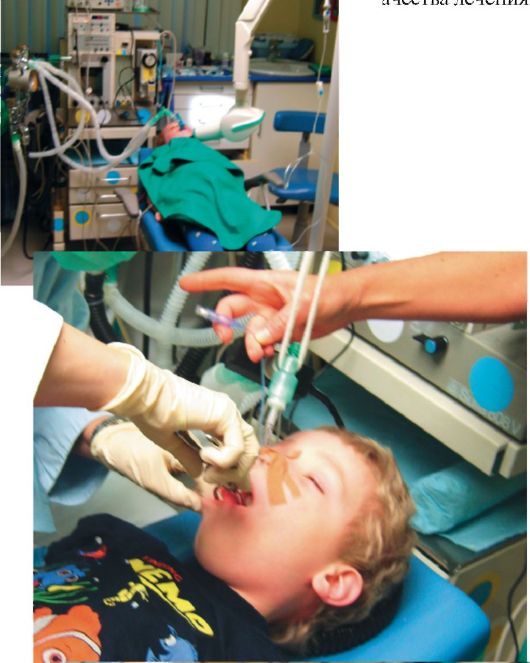 Рис. 10. Рентгенологический контроль
Рис. 10. Рентгенологический контроль
качества лечения зубов в ходе стоматологического вмешательства и наркоза
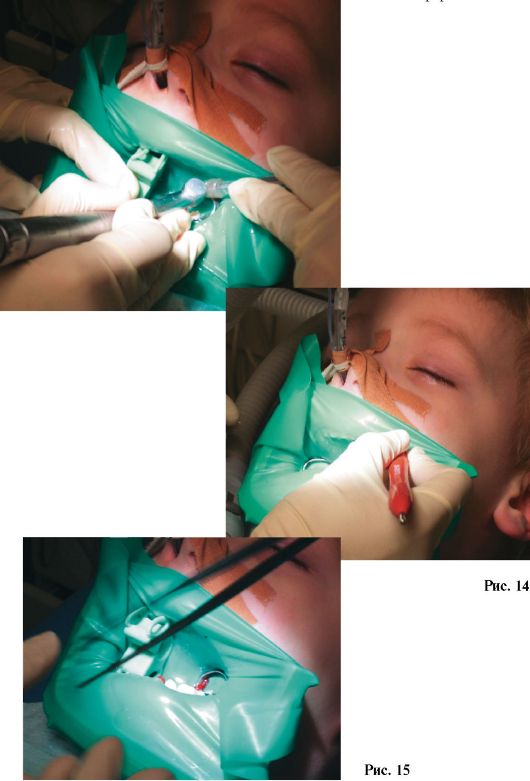
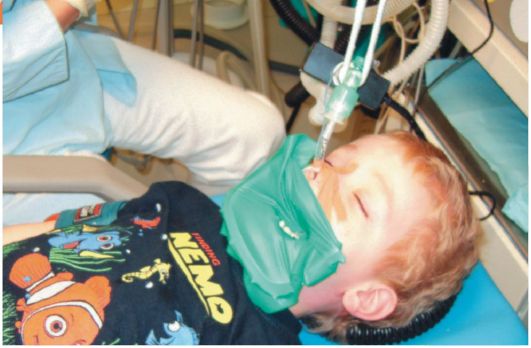 Рис. 11, 12. Наложение коффердама
Рис. 11, 12. Наложение коффердама
Рис. 13. Работа стоматолога комфортна
 Комментарии к фотографиям 1-15
Комментарии к фотографиям 1-15
Наше мнение по поводу продемонстрированной методики комбинированного наркоза ингаляцией смеси севорана, закиси азота и кислорода и внутривенной инфузией пропофола и мидазолама.
• Применена сложная методика общего обезболивания, включающая комбинацию ингаляционных и внутривенных методов и средств наркоза. Вводный наркоз ингаляционный смесью севорана, закиси азота и кислорода - масочный.
• После обеспечения венозного доступа и введения недеполяризующего миорелаксанта цисатракурия (Нимбекс) средней длительности действия (до 60 мин) проведена интубация трахеи трубкой с манжетой, и переход к основному наркозу. Основной наркоз: эндотрахеальная ингаляция севорана, закиси азота и кислорода; контур, замкнутый с абсорбером; низкий поток - 1 л/мин; испаритель севорана вне контура дыхания; вентиляция легких искусственная и внутривенная инфузия пропофола с мидазоламом.
• Данный вариант создает комфортные условия для работы врачастоматолога, позволяет пользоваться кофердамом, работать турбиной с водяным охлаждением, пломбировать зубы, применяя эстетические материалы и т.д. Длительность продемонстрированного наркоза составила 1 ч 20 мин.
Спорные моменты
Мы считаем, что амбулаторное общее обезболивание при стоматологических вмешательствах у детей не должно продолжаться дольше 1- 1,5 ч. При необходимости более длительных вмешательств рекомендуется выполнять их в 2-3 посещения. Наркоз со спонтанной вентиляцией легких у детей длительностью до 2 ч, как правило, не вызывает дыхательных нарушений.
Эндотрахеальный наркоз с ИВЛ, проводимый низким потоком свежих газов (Low Flow-анестезия), требует определенной квалификации анестезиолога и соответствующего оборудования, что не всегда возможно.
• Применение эндотрахеальных трубок с манжетой у детей до 10 лет не всегда оправдано, так как может сопровождаться известными посленаркозными осложнениями.
• При проведении данного наркоза использовано неоправданно большое количество анестезирующих препаратов, взаимодействие которых в каждом конкретном случае не всегда можно предсказать.
• Проведение подобной анестезии сегодня допустимо в условиях стационара.