Неврология и нейрохирургия / под ред. А.Н. Коновалова, А.В. Козлова ; Е.И. Гусев, А.Н. Коновалов, В.И. Скворцова : учебник : - т. 1. - 2009. - 624 с.
|
|
|
|
ГЛАВА 8. МЕТОДЫ ИССЛЕДОВАНИЯ В КЛИНИЧЕСКОЙ НЕВРОЛОГИИ И НЕЙРОХИРУРГИИ
Диагностическое заключение, основанное на жалобах, анамнезе и результатах неврологического и общеклинического обследования больного, нуждается в подтверждении с помощью дополнительных методов исследования. Эти вспомогательные методы могут способствовать уточнению диагноза. Все дополнительные исследования должны быть обоснованы, по возможности согласованы с больным или его родственниками. Следует принимать во внимание также их экономическую целесообразность.
8.1. Электроэнцефалография
Электроэнцефалография - метод исследования функционального состояния головного мозга путем регистрации его биоэлектрической активности через неповрежденные покровы головы. Регистрация биотоков непосредственно с обнаженного мозга называется электрокортикографией. Электроэнцефалограмма (ЭЭГ) представляет собой суммарную активность большого числа клеток мозга и состоит из различных компонентов. ЭЭГ регистрируют при помощи электроэнцефалографа. Применяют как монополярный, так и биполярный способ отведения биопотенциалов.
Основными компонентами ЭЭГ здорового взрослого человека в состоянии бодрствования являются альфа- и бета-ритмы (рис. 8.1). Альфа-волны - правильные ритмичные колебания с частотой 8-12 в секунду и амплитудой 30-70 мкВ. Альфаритм регистрируется преимущественно в затылочных областях, при
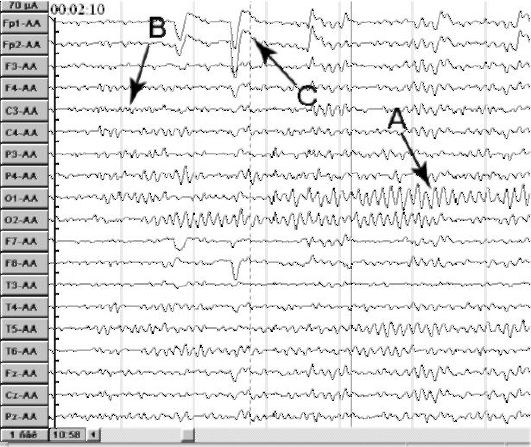 Рис. 8.1. Показатели
электрической активности головного мозга в фоновой записи в норме. А -
альфа-ритм; В - бета-ритм; С - глазодвигательный артефакт
Рис. 8.1. Показатели
электрической активности головного мозга в фоновой записи в норме. А -
альфа-ритм; В - бета-ритм; С - глазодвигательный артефакт
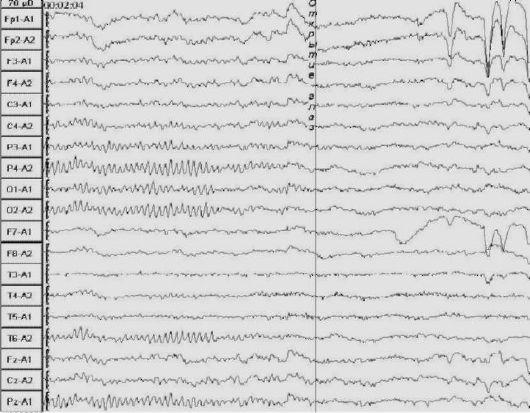 Рис. 8.2. Реакция активации
Рис. 8.2. Реакция активации
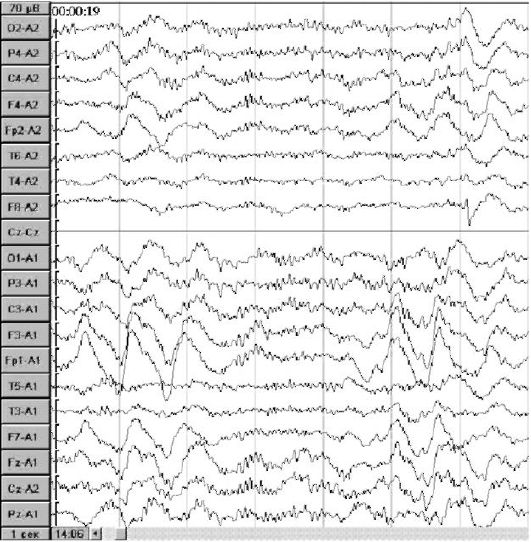 Рис. 8.3. ЭЭГ
больной с карциномой левой лобной доли. Высокоамплитудные дельта волны
преимущественно в передних отведениях левого полушария мозга
Рис. 8.3. ЭЭГ
больной с карциномой левой лобной доли. Высокоамплитудные дельта волны
преимущественно в передних отведениях левого полушария мозга
открывании глаз возникает его депрессия (реакция активации) (рис. 8.2). Бета-волны выражены преимущественно в передних отделах мозга (лобных и височных). На ЭЭГ здорового человека нередко регистрируются колебания в пределах 1-7 в секунду, но их амплитуда не превышает 20-30 мкВ. В некоторых случаях альфа-ритм может отсутствовать или, наоборот, альфа-активность может быть усилена.
При патологических состояниях на ЭЭГ регистрируются дельтаволны частотой 1-3 в секунду, тета-волны частотой 4-7 в секунду (рис. 8.3). Признаком патологической активности считаются острые волны, пики, комплексы спайк-волна, пароксизмальная активность - внезапно появляющиеся изменения ритмической активности. Эти изменения наблюдаются у больных эпилепсией
(рис. 8.4).
Введение в клиническую практику математических методов анализа ЭЭГ позволяет количественно оценить процессы электрогенеза в мозге. К таким методам относятся компрессированный спектральный анализ ЭЭГ и топоселективное картирование электрической активности мозга, позволяющие проводить количественную оценку частотно-энергетического распределения мощности этой активности; когерентный анализ, используемый для выявления взаимосвязи между различными областями мозга; корреляционный анализ, позволяющий оценить устойчивость биоэлектрических ритмов во времени, их стационарность.
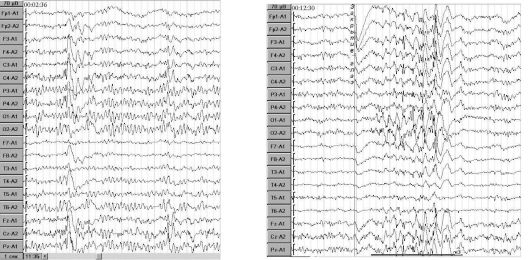 Рис. 8.4. ЭЭГ больной с эпилепсией
Рис. 8.4. ЭЭГ больной с эпилепсией
Компрессированный спектральный анализ (КСА) ЭЭГ
Сущность метода заключается в компьютеризированной трансформации первичной ЭЭГ в спектр мощности в соответствии с быстрым преобразованием Фурье. Преимуществом КСА является возможность мониторного наблюдения за динамикой электрогенеза коры полушарий большого мозга у постели больного на протяжении нескольких часов и даже суток (рис. 8.5).
Топоселективное картирование электрической активности мозга
Это вариант математической обработки электроэнцефалографического сигнала. Исходная многоканальная ЭЭГ трансформируется компьютером в числовую форму, представленную в виде спектра мощности ЭЭГ (рис. 8.6). На основании полученных данных строят карты пространственного распределения мощности различных видов электрической активности мозга. Метод позволяет объективно оценить выраженность межполушарной асимметрии ЭЭГ, наличие и локализацию очагов патологической активности, а также другие изменения ЭЭГ непосредственно в момент исследования.
Изменения ЭЭГ при патологическом процессе могут быть диффузными и локальными. Диффузные поражения мозга чаще всего регистрируются при менингитах, токсических поражениях, энцефалопатиях различ-
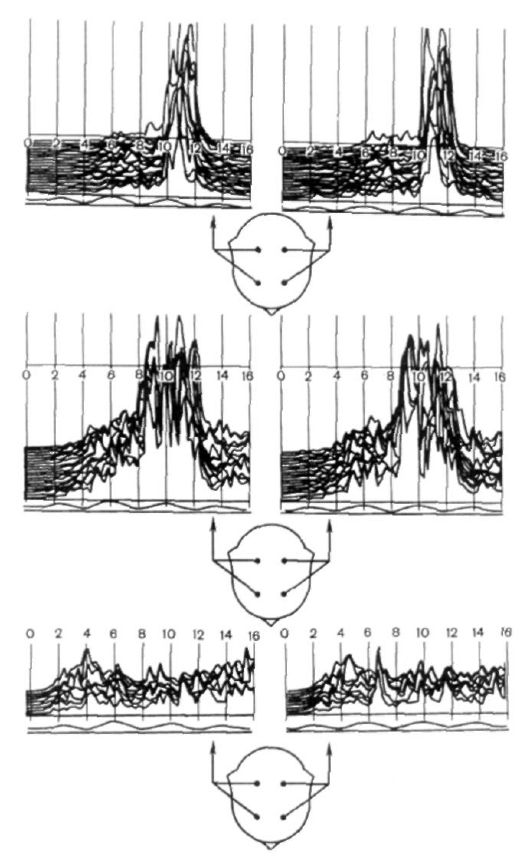 Рис. 8.5. Варианты компрессированных спектрограмм ЭЭГ (цифрами обозначена частота в герцах)
Рис. 8.5. Варианты компрессированных спектрограмм ЭЭГ (цифрами обозначена частота в герцах)
ного генеза и заключаются в отсутствии регулярной доминирующей активности, нарушении нормального топического распределения альфа- и бета-ритма, появлении диффузных патологических колебаний в виде высокоамплитудных тета-, дельта-волн. Локальные изменения на ЭЭГ возникают при очаговых поражениях головного мозга (опухоль, абсцесс, гематома, инфаркт, травма).
В настоящее время в клинической практике стала актуальной локализация источника электрической активности - так называемая обратная задача электроэнцефалографии. Поскольку ЭЭГ регистрируют через неповрежденные кожные покровы, большое значение имеют адекватная математическая обработка и анализ сигналов. При помощи специализированных компьютерных программ обнаруживаются дипольные источники электрических сигналов, поле которых с максимальным приближением описывает реальное распределение потенциалов биоэлектрической активности мозга, регистрируемое на ЭЭГ (рис. 8.7, 8.8).
8.2. Вызванные потенциалы мозга
Вызванные потенциалы мозга представляют собой его ответ на внешние раздражения. Амплитуда этих потенциалов ниже, чем амплитуда спонтанной электрической активности, их не удается выявить обычным визуальным анализом. Регистрация ВП производится с помощью специализированных цифровых усредняющих устройств. ВП исследуют с целью оценки функционального состояния систем афферентации различной модальнос-
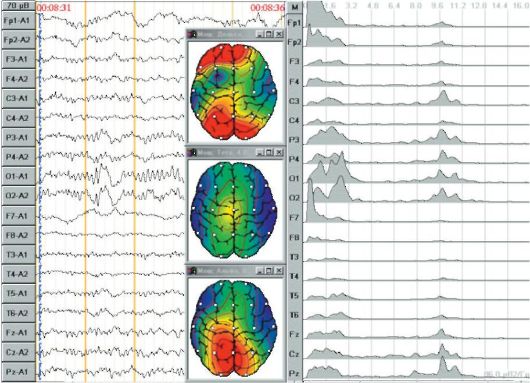 Рис. 8.6. Спектральный анализ в картирование ЭЭГ
Рис. 8.6. Спектральный анализ в картирование ЭЭГ
ти (зрительный, слуховой и др.), уровня их поражения. ВП можно использовать для объективной оценки состояния сенсорных функций (при дифференциации функциональных и органических расстройств), при органических поражениях ЦНС и ПНС, травме спинного мозга.
Метод ВП применяется для регистрации электрических ответов мозга на внешние раздражители (зрительный, слуховой стимул) или эндогенные события (например, принятие решения).
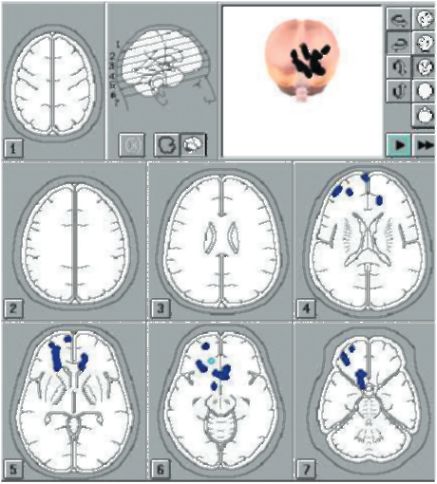 Рис. 8.7. Пример трехмерной локализации дельта-активности в проекции левой лобной доли у больной с карциномой на формализованных МР срезах
Рис. 8.7. Пример трехмерной локализации дельта-активности в проекции левой лобной доли у больной с карциномой на формализованных МР срезах
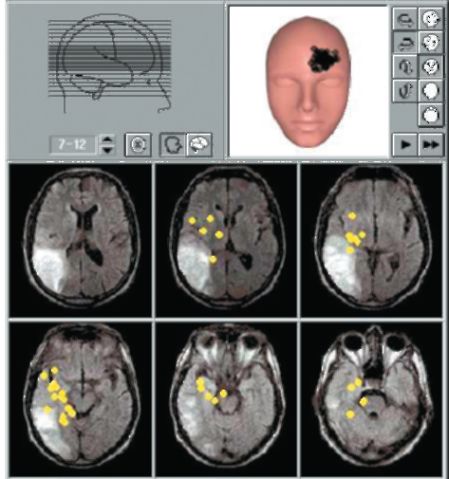 Рис. 8.8. Совмещение
данных МР-исследования и трехмерной локализации дипольных источников у
больного с ишемическим инсультом. Фокус дельта-активности в проекции
ишемических изменений, по данным МРТ
Рис. 8.8. Совмещение
данных МР-исследования и трехмерной локализации дипольных источников у
больного с ишемическим инсультом. Фокус дельта-активности в проекции
ишемических изменений, по данным МРТ
В слуховых ВП выделяют коротколатентные (ранние) и длиннолатентные (поздние) компоненты. Регистрацию коротколатентных стволовых ВП (КСВП) на акустическую стимуляцию в основном используют для диагностики поражений слухового нерва и мозгового ствола. Соматосенсорные ВП (ССВП) представляют собой электрические ответы нервных структур при стимуляции (обычно электрической) различных нервов (рис. 8.9). В клинической практике исследуют ССВП с периферических нервов (срединного, большеберцового), спинного и головного мозга. Используется стимуляция прямоугольными импульсами тока длительностью 100-300 мкс. Регистрирующий электрод записывает ВП, полученные при стимуляции, подаваемой через стимулирующий электрод. При повреждении периферических нервов и сплетений ССВП изменяются вплоть до полного исчезновения при перерыве проводящих путей. Компоненты ССВП изменяются также при эпилепсии, рассеянном склерозе, инсульте, прочих органических поражениях мозга.
8.3. Электромиография
Электромиография - метод регистрации биоэлектрической активности мышц, позволяющий определить функциональное состояние
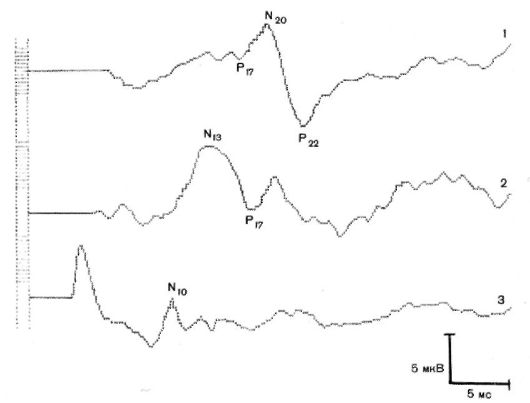 Рис. 8.9. Соматосенсорные вызванные потенциалы. Стимуляция правого срединного нерва.
Рис. 8.9. Соматосенсорные вызванные потенциалы. Стимуляция правого срединного нерва.
Регистрация: 1 - в области сенсорной проекции правой руки (средняя треть левой задней центральной извилины); 2 - на уровне СVII; 3 - в точке Эрба справа. Усреднение 250 потенциалов. N - негативный пик; P - позитивный пик (цифрами обозначены латентные периоды в миллисекундах)
нервно-мышечной системы. Электромиография применяется для определения места, степени и распространенности поражения у больных с нарушениями нервно-мышечной системы. Возможно отведение биопотенциалов мышц накожными (глобальная электромиография) и игольчатыми (локальная электромиография) электродами.
Электромиографию проводят для уточнения локализации, характера и тяжести поражения нервной системы. Метод помогает топической диагностике поражения корешка, сплетения или периферического нерва, выявлению типа поражения (единичный - мононевропатия или множественный - полиневропатия; аксональный или демиелинизирующий; уровень компрессии нерва при туннельных синдромах, а также состояние нервномышечной передачи). Полученные результаты позволяют сформулировать топический синдромологический электромиографический диагноз.
В норме регистрируются ЭМГ 1-го типа (рис. 8.10) с частыми, быстрыми колебаниями потенциалов с изменчивыми амплитудами. ЭМГ этого же типа со снижением биоэлектрических параметров (частоты, формы, длительности осцилляций) регистрируются у больных с миопатиями, пирамидными парезами и радикулоневритами. О корешковом поражении свидетельствуют гиперсинхронная ЭМГ, появление нестойких потенциалов фибрилляций и фасцикуляций при проведении тонических проб.
Основная форма нарушений биоэлектрических процессов, развивающихся в нейромоторном аппарате при поражениях нервной системы, проявляется ЭМГ 2-го типа с урежением колебаний потенциалов. ЭМГ 2-го типа преобладают при нейрональной и невральной локализации процесса. ЭМГ 3-го типа регистрируются при экстрапирамидных изменениях тонуса и гиперкинезах. Полное «биоэлектрическое молчание» - ЭМГ 4-го типа - отмечается при вялых параличах мышцы в случае гибели всех или большей части иннервирующих их мотонейронов. Компьютерная обработка ЭМГ обеспечивает более широкие диагностические возможности (рис. 8.11).
8.4. Электронейромиография
Электронейромиография - комплексный метод, в основе которого лежит применение электрической стимуляции периферического нерва с последующим изучением ВП иннервируемой мышцы (стимуляционная электро-нейромиография) или нерва (стимуляционная электронейрография).
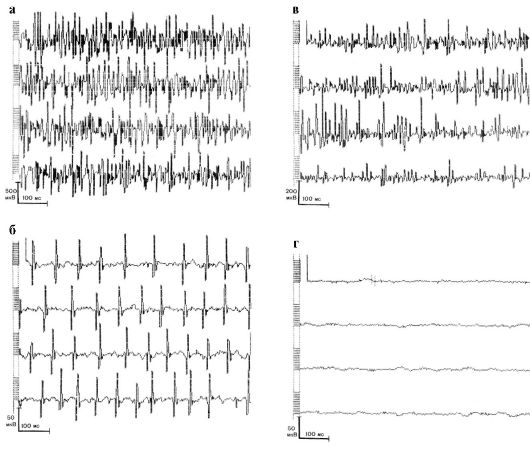 Рис. 8.10. Типы электромиографических кривых (глобальная регистрация ЭМГ; спонтанная активность): а - интерференционный тип кривой; двуглавая мышца плеча; максимальное усилие; б - денервационный тип кривой, характерный для переднерогового поражения; мышцы тенара; режим покоя; в - денервационный тип кривой, характерный для неврального поражения; мышцы тенара; максимальное усилие; г - кривая «биоэлектрического молчания»; мышцы гипотенара; максимальное усилие
Рис. 8.10. Типы электромиографических кривых (глобальная регистрация ЭМГ; спонтанная активность): а - интерференционный тип кривой; двуглавая мышца плеча; максимальное усилие; б - денервационный тип кривой, характерный для переднерогового поражения; мышцы тенара; режим покоя; в - денервационный тип кривой, характерный для неврального поражения; мышцы тенара; максимальное усилие; г - кривая «биоэлектрического молчания»; мышцы гипотенара; максимальное усилие
Вызванные потенциалы мышцы. М-ответ- суммарный синхронный разряд двигательных единиц мышцы в ответ на электрическое раздражение периферического двигательного нерва (рис. 8.12). Оценивают форму, фазность, амплитуду, длительность, дистальную и резидуальную латентность. В норме при регистрации с помощью поверхностного биполярного электрода М-ответ имеет две фазы (негативную и позитивную) длительностью от 15 до 25 мс с максимальной амплитудой до 7-15 мВ. При денервационном (невральном) поражении М-ответ становится полифазным, его длительность увеличивается, максимальная амплитуда снижается, удлиняется латентный период, повышается порог раздражения.
Н-ответ-рефлекторный ответ мышцы при электрическом раздражении чувствительных волокон нерва с использованием подпорогового для двигательных аксонов стимула (рис. 8.13). Представляет собой моносинаптический рефлекс, по механизму возникновения сходный с ахилловым. Отношение максимальных амплитуд Н- и М-ответов соответствует уровню рефлекторной возбудимости альфа-мотонейронов данной мышцы и в норме колеблется от 11 до 17%.
F-волна - потенциал, механизм возникновения которого аналогичен таковому Н-рефлекса, с той разницей, что стимулируются двигательные волокна. По латентному периоду и длительности сопоставим с Н-рефлексом.
Возвратный потенциал действия (ПД) нерва - суммарный ответ нервного ствола на электрическую стимуляцию. Вычленение из суммарного ПД смешанного нерва потенциала ответа чувствительных волокон имеет важное значение, так как именно благодаря ему возможно исследование параметров возбуждения и проведения по чувствительным волокнам.
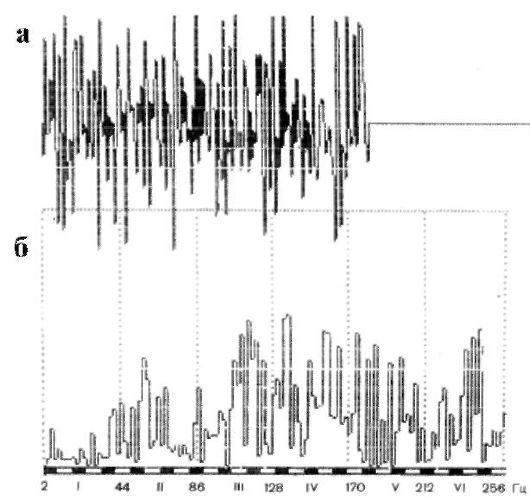 Рис. 8.11. Спектральный анализ частотного распределения электромиографической кривой: а - спонтанная активность (интерференционный тип кривой); б - гистограмма распределения мощности в частотных диапазонах: I - 146; II - 382; III - 609; IV - 776; V - 505; VI - 482
Рис. 8.11. Спектральный анализ частотного распределения электромиографической кривой: а - спонтанная активность (интерференционный тип кривой); б - гистограмма распределения мощности в частотных диапазонах: I - 146; II - 382; III - 609; IV - 776; V - 505; VI - 482
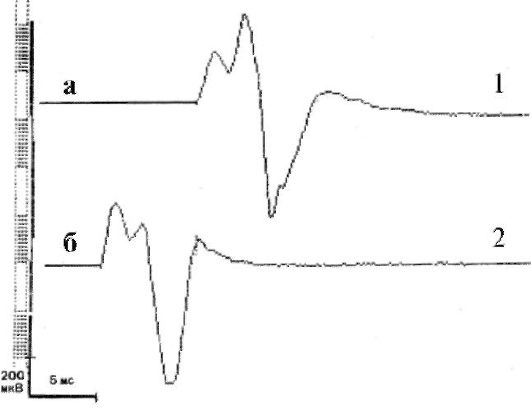 Рис. 8.12. Электронейромиография.
Определение скорости проведения импульса по двигательным волокнам
малоберцового нерва. Регистрация М- ответа в проксимальной (1) и
дистальной (2) точках: а - латентный период М-ответа в проксимальной точке; б -
то же в дистальной точке. Разность латентных периодов 8,1 мс;
расстояние между точками стимуляции 405 мм; скорость проведения импульса
50 м/с
Рис. 8.12. Электронейромиография.
Определение скорости проведения импульса по двигательным волокнам
малоберцового нерва. Регистрация М- ответа в проксимальной (1) и
дистальной (2) точках: а - латентный период М-ответа в проксимальной точке; б -
то же в дистальной точке. Разность латентных периодов 8,1 мс;
расстояние между точками стимуляции 405 мм; скорость проведения импульса
50 м/с
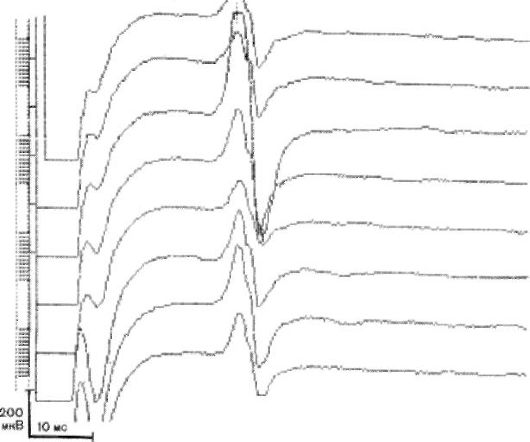 Рис. 8.13. Регистрация Н-ответа с икроножной мышцы. Вариабельность потенциалов по амплитуде
Рис. 8.13. Регистрация Н-ответа с икроножной мышцы. Вариабельность потенциалов по амплитуде
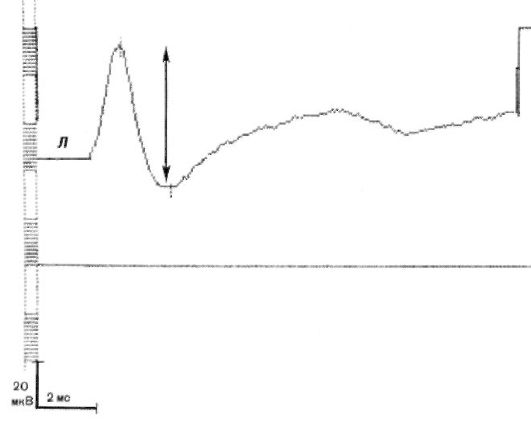 Рис. 8.14. Определение
скорости проведения импульса по чувствительным волокнам срединного
нерва. Регистрация потенциала действия нерва пальцевыми кольцевыми
электродами при стимуляции нерва в области запястья. Латентный период
потенциала; расстояние между точками стимуляции и регистрации 161 мм;
скорость проведения импульса 68,2 м/с; амплитуда потенциала действия
нерва 60 мкВ (указана стрелкой)
Рис. 8.14. Определение
скорости проведения импульса по чувствительным волокнам срединного
нерва. Регистрация потенциала действия нерва пальцевыми кольцевыми
электродами при стимуляции нерва в области запястья. Латентный период
потенциала; расстояние между точками стимуляции и регистрации 161 мм;
скорость проведения импульса 68,2 м/с; амплитуда потенциала действия
нерва 60 мкВ (указана стрелкой)
Определение скорости проведения импульса (СПИ) по периферическому нерву. Стимуляция нерва в двух точках позволяет определить время прохождения импульса между ними (рис. 8.14). Зная расстояние между точками, можно вычислить скорость проведения импульса по нерву по формуле:
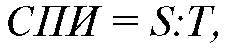 где
S - расстояние между проксимальной и дистальной точками раздражения
(мм), Т - разность латентных периодов М-ответов - для двигательных
волокон, ПД нерва - для чувствительных волокон (мс). В норме для
двигательных волокон периферических нервов конечностей СПИ колеблется от
49 до 65 м/с, для чувствительных волокон - от 55 до 68 м/с.
где
S - расстояние между проксимальной и дистальной точками раздражения
(мм), Т - разность латентных периодов М-ответов - для двигательных
волокон, ПД нерва - для чувствительных волокон (мс). В норме для
двигательных волокон периферических нервов конечностей СПИ колеблется от
49 до 65 м/с, для чувствительных волокон - от 55 до 68 м/с.
Ритмическая стимуляция периферического нерва проводится для выявления нарушения нервно-мышечной проводимости, миастенической реакции. Исследование нервно-мышечной проводимости с помощью ритмической стимуляции можно сочетать с фармакологическими пробами (прозериновой и др.).
Метод игольчатой миографии позволяет изучить активность двигательных единиц во время произвольного движения и в покое. При сокращении мышцы регистрируются потенциалы двигательных единиц (ПДЕ); потенциалы, регистрируемые в покое, называются потенциалами спонтанной активности и в
норме не встречаются. Они могут являться самостоятельным диагностическим признаком (миотонические разряды при миотонии) или указывать на активность патологического процесса (потенциалы фибрилляций и положительные острые волны при полимиозите). При анализе ПДЕ учитывают значения амплитуды, длительность и количество фаз. Различные сочетания значений этих параметров позволяют уточнить уровень поражения двигательной единицы (нейрональный, невральный, первично-мышечный).
8.5. Метод транскраниальной магнитной стимуляции
Магнитная стимуляция головного мозга - неинвазивный метод оценки функционального состояния пирамидного пути - проводится с помощью магнитного стимулятора при интенсивности магнитного поля порядка 2 Т импульсами длительностью 500-800 мкс. Магнитная катушка помещается в области проекции моторных зон коры и остистых отростков CVI-CVII и LI-LII. Моторный ответ регистрируют с помощью контралатерально расположенных накожных отводящих электродов с m. abductorpolicis brevis и m. tibialis anterior.
Образуемое магнитное поле стимулирует пирамидные клетки посредством возбуждения интернейронов коры большого мозга, при этом активируются наиболее быстропроводящие пирамидные волокна. Основным параметром функционального состояния пирамидного пути является время центрального проведения по нему, которое представляет собой разность латентных периодов М-ответов, полученных при магнитной стимуляции области верхушки свода черепа (vertex) и области проекции выхода корешков спинного мозга на уровне шейного (остистые отростки СVII-СVIII) или поясничного (остистые отростки LIV-Lv) утолщений. С помощью этого метода получены новые данные о состоянии пирамидного пути при ишемическом инсульте, боковом амиотрофическом склерозе, дегенеративных заболеваниях нервной системы, цервикальной миелопатии, рассеянном склерозе, травматических поражениях спинного мозга.
8.6. Эхоэнцефалоскопия
Метод основан на способности ультразвука отражаться от границы раздела двух сред (применительно к головному мозгу - его паренхимы
и ликвора, содержащегося в желудочковой системе). На ЭхоЭГ первый импульс - начальный комплекс - представляет собой возбуждающий генераторный импульс в сочетании с сигналами, отраженными от прилегающих к ультразвуковому зонду кожно-костных покровов головы (рис. 8.15). В центре располагается стабильный сигнал, отраженный от срединных структур головного мозга, расположенных в сагиттальной плоскости: III желудочек, шишковидная железа, прозрачная перегородка, большой серповидный отросток (М-эхо). Последний импульс на ЭхоЭГ является отражением ультразвукового сигнала от костно-кожных покровов противоположной стороны. Между импульсом начального комплекса и М-эхо располагаются сигналы, отраженные от других структур мозга, через которые проходят ультразвуковые волны в процессе исследования. В норме структуры, образующие М-эхо, расположены строго в сагиттальной плоскости и находятся на одинаковом расстоянии от симметричных точек правой и левой поверхностей головы, поэтому при отсутствии патологии М-эхо равно отстоит от начального комплекса при исследовании как правого, так и левого полушария большого мозга (рис. 8.16).
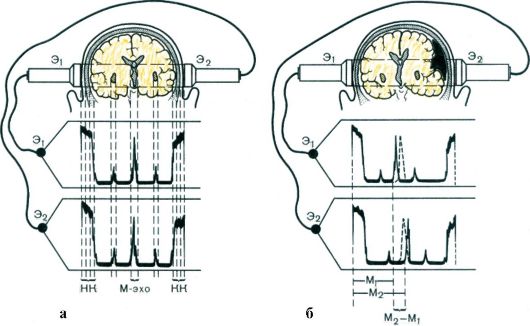 Рис. 8.15. Эхоэнцефалограммы. а -
эхоэнцефалограмма здорового человека; смещение срединных структур
головного мозга отсутствует: НК - начальный комплекс; М-эхо срединный
комплекс; КК - конечный комплекс; б - смещение срединных структур головного мозга: М1 и М2 - расстояние до срединных структур головного мозга слева и справа; Э - электроды
Рис. 8.15. Эхоэнцефалограммы. а -
эхоэнцефалограмма здорового человека; смещение срединных структур
головного мозга отсутствует: НК - начальный комплекс; М-эхо срединный
комплекс; КК - конечный комплекс; б - смещение срединных структур головного мозга: М1 и М2 - расстояние до срединных структур головного мозга слева и справа; Э - электроды
Объемное супратенториальное (расположенное выше намета мозжечка) образование (опухоль, гематома, область инфаркта с перифокальным отеком) вызывает смещение срединных структур мозга (М-эхо) в противоположную сторону. Отклонение срединного М- эхо более чем на 2 мм в одну из сторон должно рассматриваться как признак патологии. Наиболее информативным показателем объемного поражения полушария большого мозга следует считать смещение срединного М-эхо в сторону здорового полушария. Метод имеет большое значение для распознавания тяжелого поражения головного мозга, особенно на догоспитальном этапе.
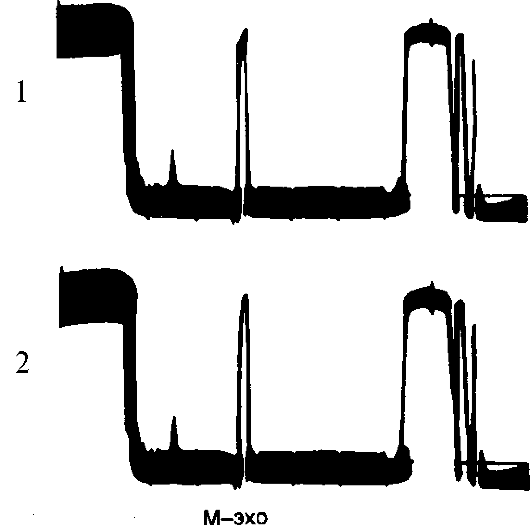 Рис. 8.16. Эхоэнцефалограмма
здорового человека. 1 - ультразвуковая локация справа; 2 -
ультразвуковая локация слева. Комплекс М-эхо расположен на одинаковом
расстоянии от зонда с двух сторон, ультразвуковые признаки смещения
срединных структур головного мозга отсутствуют
Рис. 8.16. Эхоэнцефалограмма
здорового человека. 1 - ультразвуковая локация справа; 2 -
ультразвуковая локация слева. Комплекс М-эхо расположен на одинаковом
расстоянии от зонда с двух сторон, ультразвуковые признаки смещения
срединных структур головного мозга отсутствуют
8.7. Ультразвуковая допплерография
Метод ультразвуковой допплерографии (УЗДГ) основан на эффекте Допплера, который состоит в изменении частоты волны (в данном случае ультразвукового сигнала), отраженной от движущегося объекта, в том числе от движущихся эритроцитов крови. Сдвиг частоты (допплеровская частота) пропорционален скорости движения крови в сосудах и углу между осями сосуда и датчика. УЗДГ позволяет измерять скорость и направление кровотока в артериальных и венозных сосудах, в том числе в экстракраниальных отделах сонных и позвоночных артерий (рис. 8.17, 8.18). Исключительное значение при этом имеет оценка направления и скорости кровотока по глазной артерии - одном из анастомозов, соединяющих системы наружной и внутренней сонных артерий. Для оценки функционирования анастомозов виллизиева круга используют компрессионные пробы с поочередным пережатием внутренних сонных артерий (эффективное функционирование анастомозов обеспечивает постоянство кровотока при выполнении пробы). Современная допллеровская техника позволяет оценить кровоток и по крупным внутричерепным артериям.
Исключительно ценную информацию обеспечивает дуплексное сканирование, позволяющее получить информацию о направлении, объемной скорости, ламинарности кровотока, а также о состоянии сосудистой стенки, толщине комплекса интима-медиа, наличии атеросклеротических бляшек, их структуре, физических характеристиках (рис. 8.19). Дуплексное сканирование используется для оценки состояния крупных внечерепных (сонных, позвоночных, подключичных артерий и плечеголовного ствола), а также интракраниальных артерий. Помимо изучения кровотока по артериальным сосудам, УЗДГ позволяет оценить скорость кровотока по внутричерепным венам и венозным синусам (прямой, поперечный, сигмовидный), а также по яремным венам.
Возможно использование функциональных проб, позволяющих оценить реактивность церебральных артерий (гипо- и гипервентиляция, применение вазодилататоров и пр.). Мониторирование УЗДГ - длительная запись показателей кровотока (1ч и более) применяется для выявления так называемых атипичных сигналов, отражающих прохождение по сосуду микроэмболов.
8.8. Нейрорентгенологические методы исследования
Краниография. Рентгенография остается ведущим способом выявления травматических поражений костей черепа (переломы, трещины).
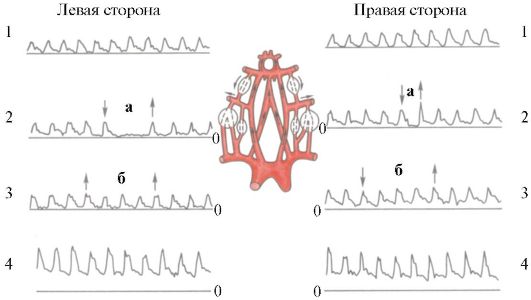 Рис. 8.17. Ультразвуковая допплерограмма сонных артерий в норме. 1-3 - надблоковая артерия; 4 - общая сонная артерия: а - компрессия общей сонной артерии; б - компрессия ветвей наружной сонной артерии
Рис. 8.17. Ультразвуковая допплерограмма сонных артерий в норме. 1-3 - надблоковая артерия; 4 - общая сонная артерия: а - компрессия общей сонной артерии; б - компрессия ветвей наружной сонной артерии
Краниография эффективна при распознавании врожденных и приобретенных деформаций черепа, первичных и вторичных опухолевых процессов в костной ткани, некоторых воспалительных изменений (остеомиелит). Новообразования гипофиза часто сопровождаются изменениями размеров и конфигурации турецкого седла. У детей и подростков важное диагностическое значение имеют рентгенологические признаки ликворной гипертензии (расхождение швов, пальцевые вдавления).
Череп имеет сложное анатомическое строение, поэтому, кроме обзорных снимков в прямой и боковой проекциях, делают специальные прицельные снимки. Краниографию можно использовать в качестве предварительного (скринингового) метода перед проведением КТ или МРТ.
Спондилография. Рентгенологическое исследование позволяет обнаружить проявления дегенеративных заболеваний позвоночника (остеохондроз, деформирующий спондилез и пр.). Спондилография может помочь выявить изменения в самих позвонках (остеофиты, унковертебральный артроз), межпозвонковых дисках (снижение высоты). Исключительно ценна информация о статических особенностях позвоночника (сколиоз, кифоз,
ротация по оси, состояние физио- логических лордозов). Рентгеноло-
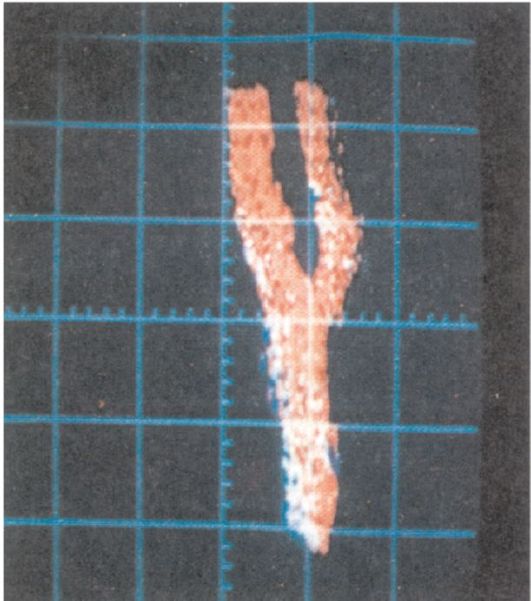 Рис. 8.18. Ультразвуковая допплерограмма общей сонной артерии в норме
Рис. 8.18. Ультразвуковая допплерограмма общей сонной артерии в норме
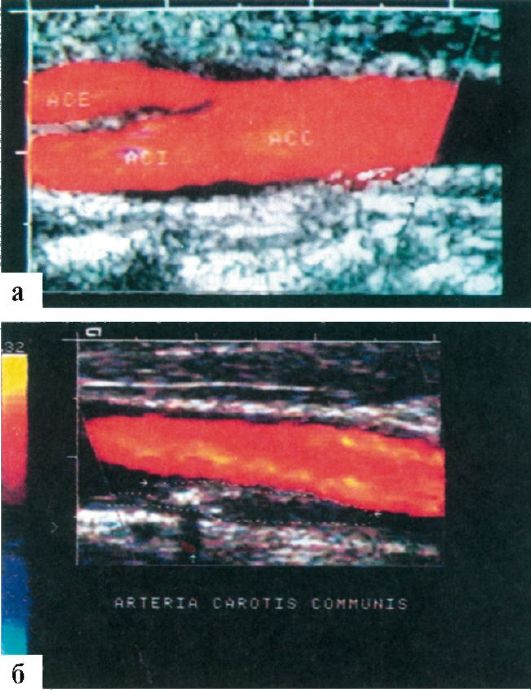 Рис. 8.19. Ультразвуковое изображение в режиме цветового допплеровского картирования бифуркации общей сонной артерии в норме (а) и атеросклеротической бляшки в общей сонной артерии (б)
Рис. 8.19. Ультразвуковое изображение в режиме цветового допплеровского картирования бифуркации общей сонной артерии в норме (а) и атеросклеротической бляшки в общей сонной артерии (б)
гическое исследование с функциональными пробами (сгибание-разгибаниие) позволяет диагностировать смещение позвонков относительно друг друга (спондилолистез). Спондилография является методом диагностики травматических повреждений позвоночника, неспецифических и специфических воспалительных (туберкулез) поражений, аномалий развития (незаращение дужек, сакрализация или люмбализация).
Рентгенологическое исследование позвоночника обычно производится в боковой и прямой проекциях. При необходимости делают прицельные рентгенограммы и снимки в специальных проекциях.
Миелография - рентгеноконтрастное исследование ликворопроводящих путей спинного мозга. Миелография применяется при диагностике опухолей спинного мозга, грыж межпозвонковых дисков, хронических спинальных арахноидитах и других патологических процессах, ограничивающих просвет позвоночного канала.
В настоящее время, как правило, используется восходящая миелография с введением йодсодержащего препарата через поясничный прокол. Исследование выполняют при опущенном головном конце стола, что позволяет обнаружить нижнюю границу препятствия ликворотоку. В качестве контрастного вещества можно использовать воздух (пневмомиелография).
Церебральная ангиография. Это рентгеноконтрастное исследование кровеносных сосудов позволяет уточнить характер и локализацию патологического процесса и применяется в диагностике пороков развития сосудистой системы (аневризмы артериальные и артериовенозные, артериовенозные соустья), стенозирующих поражений магистральных артерий головы для уточнения показаний к хирургическому вмешательству. Ангиографические методы можно подразделить на прямые, при которых производится пункция сонной или позвоночной артерии, и катетеризационные, когда контрастное вещество вводят в магистральные сосуды головы путем их катетеризации через бедренную, подмышечную или плечевую артерию.
Ангиография важна для исследования состояния сосудистого русла, коллатерального кровоснабжения и определения скорости мозгового кровотока. Выделяют артериальную, капиллярную и венозную фазы прохождения контрастного вещества по сосудам мозга. В норме контраст покидает сосудистое русло мозга за 8-9 с, но при резком повышении внутричерепного давления, обусловленном опухолью, гематомой, гидроцефалией, отеком мозга, время мозгового кровообращения может удлиняться до 15-20 с. При крайней степени внутричерепной гипер-
тензии и смерти мозга наблюдается остановка мозгового кровообращения: контрастное вещество не поступает в сосуды мозга. Ускорение мозгового кровотока отмечается при артериовенозных аневризмах и соустьях. У некоторых больных с подозрением на артериовенозную мальформацию спинного мозга, а также при некоторых спинальных опухолях для установления диагноза требуется спинальная ангиография. Исследование выполняют путем катетеризации артерий, кровоснабжающих спинной мозг.
8.9. Компьютерная томография
Метод основан на измерении и последующей компьютерной обработке степени поглощения рентгеновского излучения различными тканями. На основании полученных данных реконструируется изображение (томограмма), в котором ткани с высокой рентгеновской плотностью (костная ткань, кровь) представлены высоким сигналом (светлые участки), а структуры, имеющие низкую плотность (спинномозговая жидкость, жировая ткань, - низким сигналом (темные участки).
При анализе компьютерных томограмм мозга оцениваются наличие очагов измененной рентгеновской плотности, их характеристики, расположение, форма и количество, наличие перифокального отека, смещение мозговых структур, изменение величины и конфигурациии ликворных пространств, в частности сдавления желудочков мозга (рис. 8.20).
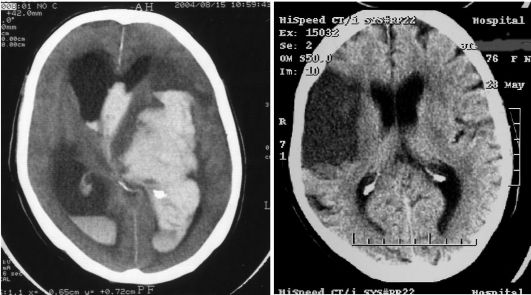 Рис. 8.20. КТ изменения при геморрагическом (слева) и ишемическом (справа) инсультах
Рис. 8.20. КТ изменения при геморрагическом (слева) и ишемическом (справа) инсультах
Компьютерная томография (КТ) является методом выбора при диагностике острых нарушений мозгового кровообращения и при острой черепно-мозговой травме. Высокая чувствительность КТ к присутствию крови позволяет выявлять очаги кровоизлияния в веществе мозга, наличие крови в желудочковой систем и в подоболочечных пространствах. Высока роль КТ в выявлении опухолей головного и спинного мозга. КТ может также использоваться для выявления и дифференциальной диагностики заболеваний позвоночника, спинного мозга и его корешков (новообразования, грыжи межпозвонковых дисков).
К числу несомненных достоинств КТ относятся относительно невысокая стоимость исследования и быстрота получения результата. Диагностические возможности КТ расширяются при использовании контрастного усиления, обычно используются неионные йодсодержащие препараты, которые вводятся внутривенно, при этом наблюдается поступление контрастного препарата в участки мозга и образования с нарушенным гематоэнцефалическим барьером (опухоль, участки воспаления).
Помимо КТ с пошаговым режимом сканирования, в настоящее время разработана методика спиральной КТ. Данный метод обеспечивает высокую разрешающую способность и позволяет воссоздавать объемное (трехмерное) изображение изучаемых структур. Возможно также выполнение ангиографии церебральных сосудов при болюсном введении определенной дозы контрастного прапарата внутривенно (рис. 8.21).
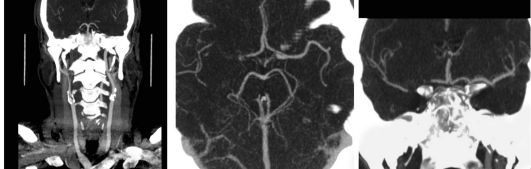 Рис. 8.21. КТ ангиография магистральных сосудов шеи (слева) и сосудов мозга (в центре и справа).
Рис. 8.21. КТ ангиография магистральных сосудов шеи (слева) и сосудов мозга (в центре и справа).
Окклюзия правой средней мозговой артерии на отрезке М1, кальцифицированные атеросклеротические бляшки в месте бифуркации сонных артерий на шее
8.10. Магнитно-резонансная томография
Метод магнитно-резонансной томографии (МРТ) основан на регистрации электромагнитного излучения, испускаемого протонами после воздействия на них электромагнитного поля радиочастотного диапазона. Излучение протонами энергии в виде разночастотных электромагнитных колебаний происходит параллельно с процессом релаксации - возвращением протонов в исходное состояние на нижний энергетический уровень после их предварительного возбуждения. Контрастность изображения тканей на томограммах зависит от времени, необходимого для релаксации протонов, а точнее от двух его компонентов: Т1 - времени продольной и Т2 - времени поперечной релаксации. Выбирая параметры сканирования, в частности частоту подачи радиочастотных импульсов (импульсная последовательность), можно влиять на контрастность изображения. Использование различных режимов подачи импульсов позволяет добиться увеличения контрастности при исследовании различных тканей и структур организма (белое и серое вещество мозга, костная ткань, ликвор, кровь), что обеспечивает большие диагностические возможности МРТ по сравнению с КТ. Особенности получаемого изображения во многом зависят от силы используемого в приборе магнитного поля.
Исследование в режиме Т1 дает более точное представление об анатомических структурах головного мозга, в то время как изображение, полученное при исследовании в режиме Т2, в большей степени отражает состояние воды в тканях. МРТ получила широкое распространение в клинической практике при многих формах поражения нервной системы: сосудистых заболеваниях, воспалительных, травматических и иных поражениях головного и спинного мозга (рис. 8.22).
Дополнительная информация может быть получена при введении контрастных агентов, способных накапливаться в патологически измененных участках мозга и образованиях при нарушении гематоэнцефалического барьера или усилении васкуляризации. В качестве контрастных агентов при используются соединения парамагнетиков, в частности гадолиния (магневист, омнискан).
Имеется целый ряд специализированных МРТ исследований, отличающихся физическими характеристиками процесса и алгоритмами оценки полученных сигналов. Существует возможность выполнения МР ангиографии, позволяющей получать изображения сосудов мозга без введения каких либо препаратов в организм (рис. 8.23). Диффузионно-
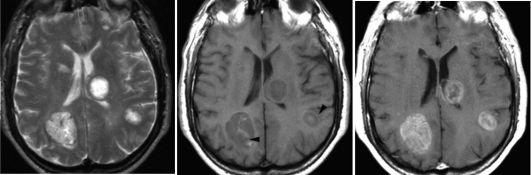 Рис. 8.22. Метастазы в головной мозг (указаны стрелками на среднем изображении). Тип МРТ изображений: слева - Т2-взвешенное изображение; в центре - Т1 взвешенное изображение; справа - Т2-взвешенное изображение с подавлением сигнала от жидкости (ликвора)
Рис. 8.22. Метастазы в головной мозг (указаны стрелками на среднем изображении). Тип МРТ изображений: слева - Т2-взвешенное изображение; в центре - Т1 взвешенное изображение; справа - Т2-взвешенное изображение с подавлением сигнала от жидкости (ликвора)
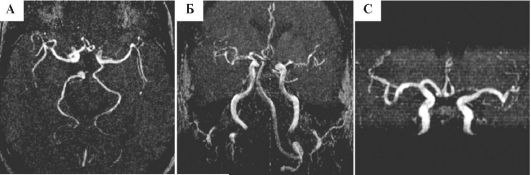 Рис. 8.23. Трехмерная времяпролетная ангиография (3D-TOF) церебральных сосудов в аксиальной (А), косой коронарной (В) и коронарной (С) проекциях.
Разобщенный виллизиев круг, задняя трифуркация левой внутренней сонной
артерии, гипоплазия правой вертебральной артерии, стеноз (или
гипоплазия) левой передней мозговой артерии на участке А1
Рис. 8.23. Трехмерная времяпролетная ангиография (3D-TOF) церебральных сосудов в аксиальной (А), косой коронарной (В) и коронарной (С) проекциях.
Разобщенный виллизиев круг, задняя трифуркация левой внутренней сонной
артерии, гипоплазия правой вертебральной артерии, стеноз (или
гипоплазия) левой передней мозговой артерии на участке А1
взвешенная МРТ позволяет выявлять ишемическое повреждение мозгового вещества на максимально ранних стадиях. Перфузионная МРТ обеспечивает возможность оценки локального кровотока в различных отделах мозга. Функциональная МРТ на основании оценки изменений локального кровотока при активации определенных церебральных структур (например, при выполнении заданного движения), позволяет картировать изменения функциональной активности мозга. Помимо получения анатомических изображений, возможно определение концентрации отдельных метаболитов в мозге (МР-спектроскопия), что позволяет изучать протекание биохимических процессов в центральной
нервной системе. С помощью МРТ могут быть получены трехмерные изображения исследуемого органа.
Важным преимуществом МРТ является ее безопасность для обследуемого и персонала. Ограничениями к ее применению является наличие металлических имплантатов и электронных устройств в организме, в частности искусственного водителя сердечного ритма.
8.11. Позитронная эмиссионная томография
Метод позитронной эмиссионной томографии основан на применении короткоживущих изотопов, которыми метятся вводимые в организм вещества, участвующие в обменных процессах мозга (глюкоза, аминокислоты, предшественники нейромедиаторов). Метод позволяет судить о состоянии обмена этих веществ в различных областях мозга и выявлять особенности их метаболизма в мозге, а также оценивать функциональную активность различных его отделов.
8.12. Диагностические манипуляции
Люмбальная пункция
Люмбальная пункция производится с целью получения цереброспинальной жидкости для ее анализа, определения внутричерепного давления и проходимости субарахноидальных пространств, выполнения миелографии, введения лекарственных препаратов. Показаниями к люмбальной пункции являются менингеальный синдром, подозрение на воспалительное поражение мозговых оболочек, подоболочечное кровоизлияние. Люмбальную пункцию не следует проводить при локальных гнойных процессах (пролежни, фурункулез), выраженном угнетении сознания с явлениями вторичного стволового синдрома (во избежание вклинения мозга). Пункцию обычно делают специальной иглой диаметром 0,5-1 мм и длиной 9-12 см между остистыми отростками позвонков LIII-LIV-LV. Больного укладывают на бок с согнутыми и приведенными к животу ногами. Голова больного согнута и располагается в одной горизонтальной плоскости с туловищем. Промежуток между остистыми отростками позвонков LIV-LV располагается на уровне линии, соединя- ющей гребни подвздошных костей (рис. 8.24). После обработки кожи в
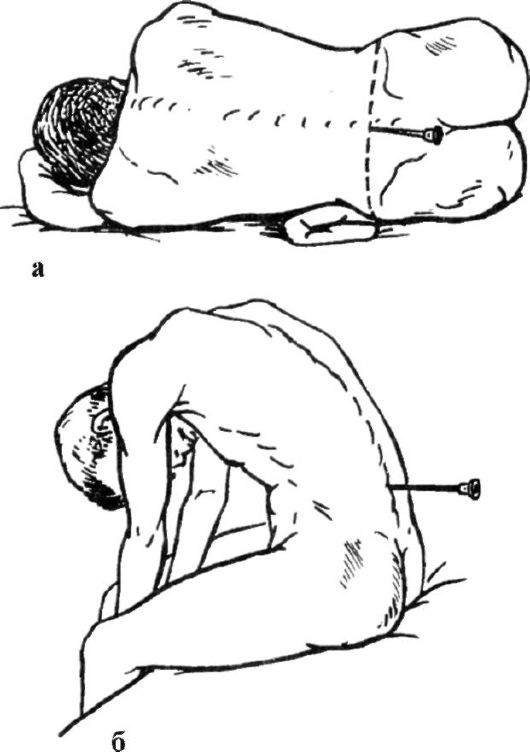 Рис. 8.24. Люмбальная пункция в положении больного на боку (а) и сидя (б)
Рис. 8.24. Люмбальная пункция в положении больного на боку (а) и сидя (б)
месте пункции дезинфцирующим раствором производят анестезию кожи и мягких тканей (2-3 мл 0,5% раствора новокаина).
Иглу со вставленным в нее мандреном продвигают строго в сагиттальной плоскости и несколько кверху соответственно промежутку между остистыми отростками. Момент прокола твердой мозговой оболочки определяется по ощущению «проваливания» иглы. Иглу продвигают на несколько миллиметров глубже, затем извлекают мандрен, и из иглы вытекает цереброспинальная жидкость. При продвижении иглы в субарахноидальное пространство может возникнуть резкая боль, если игла касается конского хвоста. В этом случае
надо осторожно изменить положение иглы. К игле подсоединяют трубку для измерения давления. По показаниям проводят ликвородинамические пробы. После этого извлекают 2-3 мл цереброспинальной жидкости для лабораторных исследований (определение количества белка, клеточного состава, присутствия флоры и определения ее чувствительности к антибактериальным препаратам и др.).
Ликвородинамические пробы делают для определения проходимости субарахноидального пространства спинного мозга. Проба Квекенштедта заключается в сдавлении вен шеи, вследствие чего повышается внутричерепное давление. При проходимости ликворных пространств выше уровня пункции одновременно повышается давление в манометрической трубке, подсоединенной к пункционной игле (отрицательная проба Квекенштедта).
При затруднении в циркуляции цереброспинальной жидкости отмечается медленный незначительный подъем давления на люмбальном уровне. При полном блоке субарахноидального пространства изменения давления в манометрической трубке в ответ на сдавление вен шеи вообще не происходит (положительная проба Квекенштедта). Анало-
гичный результат можно получить при сгибании головы больного, что также приводит к затруднению ликворного оттока из полости черепа и повышению интракраниального давления.
Дополнительную информацию о проходимости субарахноидального пространства спинного мозга можно получить при надавливании на брюшную стенку больного (проба Стуккея), что также приводит к повышению ликворного давления вследствие затруднения оттока из вен брюшной полости и спинномозгового канала. При блоке ликворного пространства на шейном или грудном уровне при пробе Стуккея ликворное давление на поясничном уровне будет повышаться, а при сдавлении вен шеи (проба Квекенштедта) оно будет неизменным.
Субокципитальная пункция
Субокципитальная пункция (пункция большой цистерны мозга) производится с диагностической целью (анализ цереброспинальной жидкости), для введения лекарственных средств и выполнения миелографии. Пункцию можно выполнять как в лежачем, так и в сидячем положении больного. Субокципитальную пункцию выполняют следующим образом. Выбривают волосы в шейно-затылочной области, кожу дезинфицируют. При резко согнутой голове больного определяют наружный затылочный бугор и остистый отросток CII. Посередине расстояния между ними производят анестезию кожи. Иглу вводят строго в сагиттальной плоскости до тех пор, пока ее конец не упрется в затылочную кость. По мере погружения иглы производят анестезию мягких тканей раствором новокаина. После того как игла упрется в кость, ее надо несколько извлечь и ее конец сместить вниз в направлении затылочной цистерны. Такое перемещение иглы производится до тех пор, пока ее конец не опустится ниже края затылочной кости (рис. 8.25). При продвижении иглы внутрь хирург испытывает эластическое сопротивление в момент прокола атлантоокципитальной мембраны. При попадании конца иглы в большую цистерну после извлечения мандрена из иглы начинает вытекать цереброспинальная жидкость.
Выполнение субокципитальной пункции требует очень большой осторожности и определенного навыка. При неправильной технике возможны серьезные осложнения, в первую очередь ранение задней нижней мозжечковой артерии и повреждение продолговатого мозга.
Вентрикулярная пункция
Пункция боковых желудочков мозга осуществляется с диагностической целью (получение цереброспинальной жидкости для исследования, измерение интракраниального давления); для выполнения вентрикулографии (контрастирование желудочков мозга с помощью рентгеноконтрастных веществ); выполнения некоторых операций на желудочковой системе с помощью вентрикулоскопа. Иногда приходится прибегать к вентрикулярной пункции с лечебной целью, чтобы путем извлечения цереброспинальной жидкости снизить внутричерепное давление при нарушении оттока ликвора из желудочков мозга. Вентрикулярная пункция производится также при установке системы наружного дренирования желудочков мозга или выполнении шунтирующих операций на ликворной системе мозга.
Чаще производится пункция переднего или заднего рога бокового желудочка. При пункции переднего рога бокового желудочка делают линейный разрез мягких тканей длиной около 4 см. Края кожи разводят с помощью ранорасширителя Янсена (рис. 8.26). Накладывают фрезевое отверстие, которое должно располагаться на 2 см кпереди от коронарного шва и на 2 см латеральнее средней линии сагиттального шва. Твердую мозговую оболочку вскрывают крестообразно и в мозг вводят канюлю для вентрикулопункции.
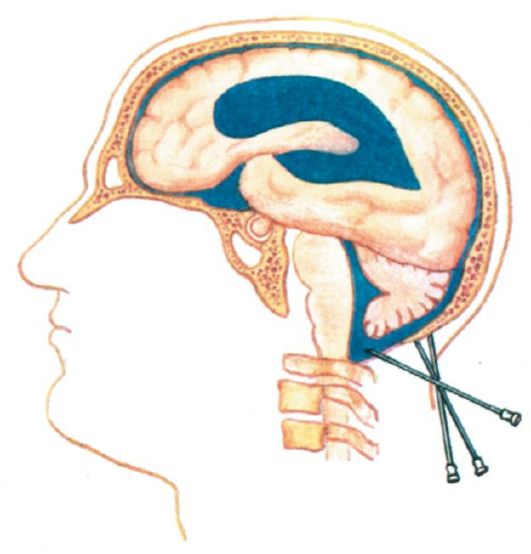 Рис. 8.25. Субокципитальная пункция
Рис. 8.25. Субокципитальная пункция
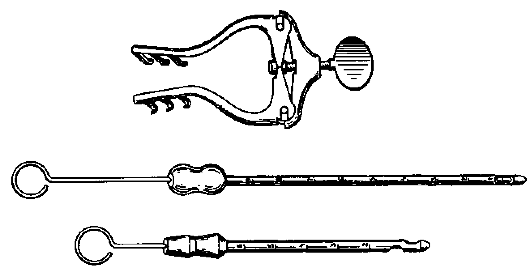 Рис. 8.26. Расширитель Янсена для разведения кожных краев при вентрикулярной пункции, вентрикулярные канюли
Рис. 8.26. Расширитель Янсена для разведения кожных краев при вентрикулярной пункции, вентрикулярные канюли
Канюлю продвигают параллельно сагиттальной плоскости в направлении внутреннего слухового прохода. В норме у взрослых передний рог располагается на глубине 5-5,5 см. При гидроцефалии это расстояние может существенно сокращаться.
Для пункции заднего рога фрезевое отверстие накладывают на 3 см латеральнее и на 3 см выше наружного затылочного бугра. Канюли погружают в мозг в направлении верхненаружного края глазницы. В норме задний рог располагается на глубине 6-7 см (рис. 8.27).
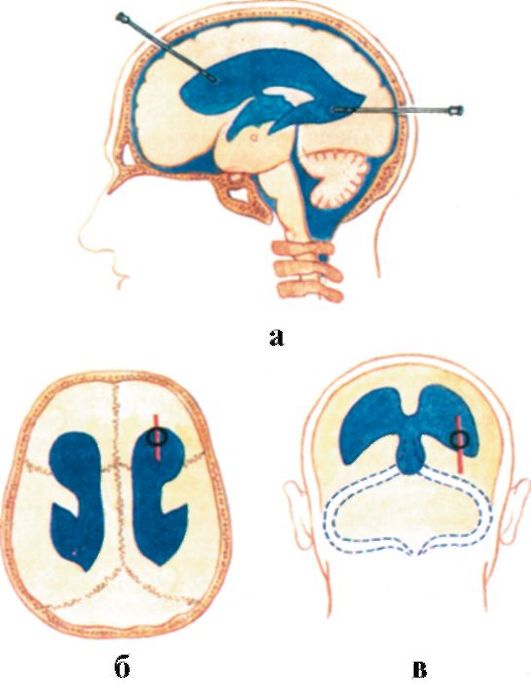 Рис. 8.27. Пункция переднего и заднего рогов бокового желудочка (а-в)
Рис. 8.27. Пункция переднего и заднего рогов бокового желудочка (а-в)