Урология : учебник / [С. Х. Аль-Шукри, В. Н. Ткачук] ; под ред. С. Х. Аль-Шукри и В. Н. Ткачука. - 2011. - 480 с. : ил.
|
|
|
|
Глава 16. ДРУГИЕ УРОЛОГИЧЕСКИЕ БОЛЕЗНИ
16.1. НОЧНОЕ НЕДЕРЖАНИЕ МОЧИ (ЭНУРЕЗ)
Ночное недержание мочи (энурез) - это непроизвольное подтекание мочи в ночное время. Это одно из самых частых функциональных расстройств у детей. Диагностировать энурез можно только в том возрасте, когда у детей уже сформировался контроль над мочевым пузырем, т. е. в возрасте старше 3 лет.
Эпидемиология. Частота энуреза наибольшая у маленьких детей и постепенно уменьшается с возрастом. Чаще энурез наблюдается у мальчиков, чем у девочек, соотношение составляет примерно 3 : 2.
Обследования нескольких тысяч детей показали, что в 5-летнем возрасте энурезом страдают 18 % мальчиков и 15 % девочек, в 7-летнем - 16 и 14 %, в 9-летнем - 8 и 8,5 %, в 11-летнем - 8 и 4 %, в 13-летнем - 4 и 2,5 % соответственно.
Приблизительно у 15 % детей с энурезом в течение одного года наблюдается спонтанная ремиссия, т. е. исчезновение ночного недержания мочи даже при отсутствии лечения. При этом вероятность спонтанного излечения в течение одного года составляет примерно 14 % в возрасте от 5 до 9 лет, 16 % - от 10 до 14 лет и 16 % - от 15 до 19 лет. К 15-летнему возрасту частота энуреза составляет только 1-2 %, ак 18-летнему - менее 1 %. У взрослых частота энуреза не превышает 0,5 %.
Как отмечено, с большой вероятностью энурез бесследно исчезает у большинства детей к подростковому возрасту. Однако, став взрослыми, такие люди имеют несколько бульшую вероятность развития проблем с мочеиспусканием.
В многочисленных исследованиях показано, что энурез в детском возрасте является существенным фактором риска возникновения дисфункций мочевого пузыря.
Классификация. Энурез подразделяют на первичный и вторичный. Под первичным энурезом понимается состояние, при котором ночное недержание мочи наблюдается с самого детства, без «светлых» промежутков. Если у ребенка в какой-либо период, по крайней мере, в течение 6 месяцев, ночное подтекание мочи отсутствовало, а затем
появилось, то говорят о вторичном энурезе. Первичной формой заболевания страдают примерно 75-80 % всех больных с энурезом.
Выделяют также неосложненный и осложненный энурез. При неос-ложненном энурезе ночное подтекание мочи служит единственным проявлением заболевания, при осложненном имеются и другие симптомы: учащение мочеиспускания, императивные позывы и недержание мочи в дневное время. Осложненной формой страдают около 15 % больных с энурезом.
Этиология и патогенез. Причины развития энуреза до конца не ясны. Однако известно, что к этому состоянию может приводить сочетание разных факторов: замедление созревания центральной нервной системы у детей, нарушение суточного ритма выработки антидиуретического гормона, отягощенная наследственность, нарушения поведения ребенка, пороки развития спинного мозга, инфекции мочевых путей.
Основная теория развития энуреза - нарушение своевременного развития рефлекторного контроля мочеиспускания. В норме у детей к 3-4 годам формируется произвольный контроль мочеиспускания, и они получают возможность сознательно начинать мочеиспускание или тормозить начавшийся позыв. Однако у некоторых функциональное созревание центральной нервной системы и формирование нормального контроля мочеиспускания затягиваются. Из-за этого может наблюдаться достаточно длительно ночное, реже дневное, непроизвольное мочеиспускание. Наличие так называемой спонтанной ремиссии, т. е. исчезновение энуреза даже в отсутствие лечения, свидетельствует о завершении формирования неврологического контроля мочеиспускания. Важный довод в поддержку теории развития энуреза - то, что нарушение произвольного мочеиспускания очень часто сочетается с другими проявлениями задержки развития ребенка, например, более медленным формированием контроля над опорожнением кишечника, поздним развитием речи и ходьбы.
Вероятность наличия энуреза значительно выше у детей с нарушением гормональной регуляции водного обмена - отсутствием суточного ритма выделения антидиуретического гормона. Если у детей не имеется ночных и дневных различий в уровне антидиуретического гормона, то объем образующейся ночью мочи значительно больше нормы. Следствием этого является значительное растяжение мочевого пузыря ночью, что в сочетании с нарушением нервной регуляции нижних мочевых путей часто приводит к непроизвольному истечению мочи.
В развитии энуреза большую роль играет отягощенная наследственность. Вероятность энуреза у детей, чьи родители им не страдали,
составляет 15 %. Установлено, что риск появления энуреза у ребенка значительно выше, если хотя бы у одного из родителей в детстве был энурез. В таких семьях вероятность энуреза у ребенка оценивается в 44 %. Если же у обоих родителей в детстве был энурез, то она составляет уже 77 %. При этом у таких детей отмечается задержка установления нормального ночного контроля мочеиспускания в среднем на 1,5 года по сравнению с обычными детьми. Проведенные в последние годы генетические исследования показали, что ген, ответственный за наследуемый энурез, может быть локализован на хромосоме 13q.
Установлено, что энурезу способствует нарушение поведения ребенка. Энурез у детей часто сочетается с различными психологическими отклонениями, проявляющимися в раздражительности, невнимательности, плаксивости, иногда агрессивности. Возможно, само наличие энуреза, а особенно неправильная реакция на недержание мочи со стороны окружающих, могут приводить к каким-либо эмоциональным расстройствам.
Отмечено, что энурез, особенно вторичный, чаще встречается у детей с инфекционно-воспалительными заболеваниями нижних мочевых путей, например циститом. Важность этого фактора подтверждается также тем, что иногда ночное недержание мочи исчезает только после назначения адекватной антибактериальной терапии.
Известна связь между энурезом и пороками развития спинного мозга, наиболее часто spina bifida и менингомиелоцеле. Однако какие-либо неврологические отклонения отмечаются у очень незначительного числа детей с энурезом, приблизительно у каждого десятого. Кроме того, эффективность лечения энуреза практически не зависит от наличия каких-либо врожденных отклонений, поэтому, хотя пороки развития и являются фактором риска развития энуреза, их значение, по-видимому, невелико.
Симптоматика и клиническое течение. Ночное подтекание мочи во сне - единственный симптом при неосложненной форме энуреза. Частота подтекания может быть разной: от нескольких раз в месяц до нескольких раз за ночь. При осложненном энурезе, наряду с ночным недержанием мочи, у пациента отмечаются учащение мочеиспускания, императивные позывы и дневное недержание мочи. Характерные особенности больных с энурезом - наличие неврозов и эмоциональная лабильность. Выраженность невротических реакций напрямую связана с тяжестью энуреза.
Диагностика. Тщательно собранный анамнез может помочь в установлении причин развития энуреза. При осмотре больного необходимо
обратить внимание на состояние кожи внутренних поверхностей бедер, наружных половых органов. Из лабораторных методов исследования выполняют общий анализ мочи, клинический и биохимический анализы крови, пробу Зимницкого. Необходимо подсчитать количество мочеиспусканий и императивных позывов за сутки (дневник мочеиспускания). Неврологическое обследование поможет выявить изменения органического или функционального характера со стороны нервной системы.
При цистоскопии у больных с энурезом в некоторых случаях выявляют уменьшение емкости мочевого пузыря, трабекулярность стенки, положительный симптом Алексеева-Шрамма (зияние шейки мочевого пузыря). Цистометрия иногда позволяет обнаружить снижение максимального цистометрического объема и непроизвольную активность детрузора. Это особенно характерно для осложненного энуреза. Рентгенография области турецкого седла позволяет выявить патологические изменения гипофиза. На обзорной рентгенограмме пояснич-но-крестцового отдела позвоночника можно обнаружить незаращение дужек поясничных или крестцовых позвонков (spina bifida).
Лечение. Существуют два важнейших взаимодополняющих направления в лечении энуреза - мотивационная психотерапия и фармакотерапия. В лечении детей с энурезом чрезвычайно важна роль родителей. Их отношение к проблеме может иметь решающее влияние на эффективность терапии. Крайне отрицательно сказываются как на течении энуреза, так и на психике ребенка попытки родителей наказывать его за неспособность удержать мочу. Подобные «воспитательные» меры могут свести к нулю весь эффект проводимого лечения.
Мотивационная психотерапия имеет особенно большое значение при лечении детей, поскольку психологическое состояние ребенка существенно влияет на успех лечения. Мотивационная психотерапия - комплекс мероприятий, направленный на привлечение ребенка к процессу лечения. Наиболее простой и эффективный метод мотивационной терапии заключается в поощрении ребенка за каждую «сухую» ночь.
Медикаментозная терапия - второе основное направление лечения энуреза. Наиболее эффективны антихолинергические препараты - оксибутинин (дриптан), солифенацин и трициклические антидепрессанты (имипрамин). Эти лекарственные средства способствуют повышению функциональной емкости мочевого пузыря и снижению его спонтанной активности ночью. Дозы препаратов выбирают с учетом возраста ребенка. В случаях, когда применение указанных препаратов недостаточно эффективно, а это наблюдается примерно у одной трети
больных, в комплексную терапию необходимо включать синтетический аналог антидиуретического гормона (десмопрессин), способствующий снижению объема образующейся ночью мочи, что может уменьшить и выраженность энуреза.
Эффективность лечения энуреза достаточно высока. Методами терапии можно добиться полного прекращения ночного недержания мочи у девяти из десяти детей с энурезом. Длительность лечения и количество курсов терапии может существенно различаться. Рекомендуется продолжать терапию до тех пор, пока проявления энуреза будут отсутствовать не менее четырех недель. В конце курса лечения при отсутствии ночного недержания мочи в качестве провокации можно использовать преднамеренное увеличенное потребление жидкости вечером. Если при этом проявления энуреза не возобновились, дозы препаратов можно постепенно снижать и затем полностью их отменить. О полном успехе лечения можно говорить только в тех случаях, когда в течение двух лет после его окончания не было ни одного эпизода ночного недержания мочи.
16.2. НЕДЕРЖАНИЕ МОЧИ
Общепринято определение недержания мочи как состояния, при котором происходит непроизвольное подтекание мочи, являющееся социальной или гигиенической проблемой для больного.
Классификация. Недержание мочи можно разделить на уретральное и экстрауретральное (внеуретральное). При уретральной форме моча непроизвольно подтекает естественным путем, т. е. через мочеиспускательный канал. При второй форме недержания моча подтекает каким-либо иным путем, например через пузырно-влагалищный свищ. Основными причинами экстрауретральной формы недержания мочи служат пороки развития мочевых путей и их травматические повреждения. Экстрауретральное недержание мочи характеризуется отсутствием позывов на мочеиспускание и связи с какими-либо внешними факторами, например физической нагрузкой. Полное избавление от такой формы недержания мочи возможно только оперативным путем.
Значительно чаще встречается уретральное недержание мочи. Его можно разделить на следующие типы: стрессовое, ургентное, смешанное и недержание переполнения.
Стрессовое недержание мочи представляет собой непроизвольное подтекание мочи во время кашля, смеха, бега и других физических действий, приводящих к повышению внутрибрюшного и, следователь-
но, внутрипузырного давления в отсутствие сокращения или сверхрастяжения мочевого пузыря. Последняя часть определения указывает на то, что нарушения со стороны собственно мочевого пузыря не вовлечены в развитие этого типа недержания мочи. Характерная особенность стрессового недержания мочи - отсутствие позыва на мочеиспускание. Под стрессом в данном определении понимается не сильное нервное потрясение, а какая-либо физическая нагрузка, приводящая к повышению внутрибрюшного давления.
Наиболее частая причина стрессового недержания мочи - гиперподвижность или значительное смещение мочеиспускательного канала и шейки мочевого пузыря во время напряжения, которое наблюдается у женщин с ослаблением мышц тазового дна. Вторая по частоте причина стрессового недержания мочи - недостаточность наружного уретрального сфинктера. Уретральная недостаточность может быть врожденной или приобретенной, например, после травм. У мужчин стрессовое недержание мочи чаще всего возникает после операции на предстательной железе.
Наряду со стрессовым, часто наблюдается ургентное недержание мочи, характеризующееся непроизвольным ее подтеканием, связанным с сильным, неудержимым позывом на мочеиспускание. Такой позыв обозначают как императивный. Причина возникновения этой формы недержания мочи - гиперактивность мочевого пузыря.
Наличие у одного и того же больного нескольких типов недержания мочи обозначают термином смешанное недержание мочи. Чаще всего наблюдается сочетание симптомов стрессового и ургентного недержания мочи, что особенно характерно для женщин старшего возраста. Менее частой формой недержания мочи, которое обнаруживается обычно у пожилых мужчин с заболеваниями предстательной железы, является недержание переполнения, связанное с переполнением и перерастяжением мочевого пузыря, чаще всего из-за нарушения оттока мочи из него.
Диагностика. Основные задачи, решаемые при диагностике причин недержания мочи: объективное подтверждение недержания, определение типа недержания, выявление факторов, способствующих недержанию или вызывающих его. При обследовании больных с недержанием мочи необходимо придерживаться некоторых правил. Во-первых, должна применяться активная тактика, т. е. врач должен выяснить у пациента, есть ли у него проблемы с мочеиспусканием, так как зачастую больные из-за ложной стыдливости и психологических особенностей могут не предъявлять жалоб. Во-вторых, кроме обычного, проводят уродинамическое обследование пациентов с недержанием
мочи, оценивают состояние и функцию почек и верхних мочевых путей. Для выявления причины заболевания часто требуется привлечение гинеколога и невропатолога.
При оценке жалоб больного и сборе анамнеза заболевания необходимы тщательная детализация симптомов, связанных с дисфункциями нижних мочевых путей, и подробный анализ перенесенных заболеваний и проводимого лечения. При опросе необходимо выяснить, сопровождается ли недержание мочи ощущением позыва на мочеиспускание, какие факторы провоцируют подтекание мочи (физическая нагрузка, звук падающей воды и др.), время суток (например, вечер). Помимо этого, выясняют наличие учащения мочеиспускания и императивных позывов, давность проблем с мочеиспусканием, наличие энуреза в прошлом, наличие других нарушений мочеиспускания (например, ослабление струи мочи). Важную роль играют наличие, характер и локализация болевых ощущений во время или вне акта мочеиспускания; была ли или имеется гематурия. Для определения причины недержания мочи надо выяснить объем потребляемой пациентом жидкости, наличие нарушений функции кишечника, расстройств сексуальной функции, характер предыдущего лечения недержания мочи, его эффективность и переносимость.
При первом общении с больным необходимо просить его заполнить дневник мочеиспускания, по крайней мере, в течение трех дней, что позволяет объективно оценить частоту мочеиспускания и императивных позывов, количество эпизодов недержания мочи.
Физикальное обследование при недержании мочи имеет большое значение. Необходимо проводить пальпацию и перкуссию передней брюшной стенки для выявления образований, чувствительности и напряженности в надлобковой области, а также оценки количества остаточной мочи. Осмотр и пальпацию наружных половых органов у мужчин выполняют для выявления пороков их развития, а также мацерации кожи полового члена. Ректальное пальцевое исследование необходимо для определения чувствительности кожи промежности и области анального сфинктера, тонуса анального сфинктера, а у мужчин также для оценки состояния предстательной железы. Оценивают сохранность тазовых рефлексов: анального (усиление сокращения анального сфинктера при введении пальца в прямую кишку), бульбока-вернозного (усиление сокращения анального сфинктера при сжимании головки полового члена или клитора) и кожно-анального (усиление сокращения анального сфинктера при прикосновении к коже в пери-анальной области).
У женщин особое значение имеет исследование тазового дна: оценивают состояние и чувствительность кожи промежности, наличие опущения тазовых органов (цистоцеле, ректоцеле, пролапс матки, опущение передней стенки влагалища), тонус перинеальных и периваги-нальных мышц. Пальпируют уретру через переднюю стенку влагалища для выявления образований в мочеиспускательном канале (дивертикула, кисты, опухоли уретры). Для оценки гиперподвижности уретры во время исследования тазового дна больную просят напрячься и покашлять - при стрессовом недержании возможно подтекание мочи. Исследования проводят при умеренно наполненном мочевом пузыре.
Всем больным с недержанием необходимо выполнять общий анализ мочи, клинический и биохимический анализ крови. С помощью УЗИ оценивают количество остаточной мочи.
Цистоскопию проводят для выявления органических причин дизурии (например, опухоли и камней мочевого пузыря). УЗИ почек проводят для оценки сохранности ее паренхимы и выявления расширения чашечно-лоханочной системы. При УЗИ мочевого пузыря можно обнаружить камни, дивертикул, опухоль мочевого пузыря.
Экскреторную урографию проводят пациентам, у которых при УЗИ выявлена пиелоэктазия. Для оценки состояния мочевого пузыря применяют восходящую или нисходящую цистографию, причем рекомендуется выполнять снимок как в покое, так и при напряжении передней брюшной стенки. При этом можно выявить подвижность или фиксиро-ванность шейки мочевого пузыря, воронкообразность шейки мочевого пузыря и проксимального отдела мочеиспускательного канала, наличие и степень цистоцеле. При выполнении микционной цистоуретрогра-фии можно выявить дивертикул уретры, препятствия оттоку мочи по уретре, пузырно-мочеточниковый рефлюкс.
Уродинамические методы исследования наиболее важны при выявлении причин недержания мочи. Цистометрия - наиболее точный метод оценки функционального состояния мочевого пузыря. При цистометрии оцениваются чувствительность, емкость и растяжимость мочевого пузыря, а также наличие и амплитуда как произвольных, так и непроизвольных сокращений детрузора. На основании данных цистометрии устанавливают диагноз гиперактивности мочевого пузыря. Профиль уретрального давления измеряют в покое и при стресс-провокации (кашле). Уретральное давление в покое определяют для выявления недостаточности уретрального сфинктера. Динамическую оценку уретрального и внутрипузырного давления используют для выявления признаков стрессового недержания мочи. Высока информа-
тивность видеоуродинамического исследования, в котором сочетаются уродинамический и рентгенологический методы. Электромиографию уретрального сфинктера используют для диагностики его повреждения и нарушения иннервации.
Лечение. Выбор метода лечения недержания мочи зависит от многих факторов. К ним относят тип недержания мочи, его тяжесть, пол и возраст больного, сопутствующие заболевания. Необходимо учитывать также результаты использованных ранее методик лечения. Все методы лечения недержания мочи можно разделить на три направления: медикаментозное, немедикаментозное и оперативное.
У больных с ургентным недержанием мочи чаще всего используют медикаментозное лечение самостоятельно или в сочетании с немедикаментозными методиками. Основную группу лекарственных средств, применяемых при ургентном недержании мочи, составляют антихолинергические препараты: оксибутинин (дриптан), соли-фенацин (везикар), троспия хлорид (спазмекс) и др. Длительность лечения обычно составляет три месяца, иногда возникает необходимость в повторных курсах терапии. Для повышения эффективности медикаментозную терапию сочетают с немедикаментозным лечением. К последнему относят тренировку мочевого пузыря и выполнение специальных упражнений для мышц тазового дна. Тренировка мочевого пузыря заключается в соблюдении больным заранее установленного и согласованного с врачом плана мочеиспусканий, т. е. пациент должен мочиться через определенный интервал времени. Программа тренировки мочевого пузыря направлена на постепенное увеличение этого интервала. Другая немедикаментозная методика лечения больных с ургентным недержанием мочи предусматривает упражнения для мышц тазового дна. Эффективность этого вида лечения основана на наличии анально-детрузорного и уретрально-детрузорного рефлексов - рефлекторного торможения сократительной активности детру-зора при произвольных сокращениях соответственно наружных анального и уретрального сфинктеров.
Лечение стрессового недержания мочи может быть как консервативным, так и оперативным. Последнее преобладает. Консервативное лечение назначают в основном больным молодого возраста при легкой степени недержания мочи. Оно заключается в проведении курса упражнений для мышц тазового дна. Оперативные методы можно разделить на несколько типов: слинговые операции, пластика влагалища, подвешивающие операции. Слинговые (петлевые) операции выполняют у женщин, причиной стрессового недержания мочи у кото-
рых является уретральная недостаточность. Проведением под уретрой «петли» из собственных или синтетических тканей и ее фиксацией достигается увеличение внутриуретрального давления после операции и прекращение недержания мочи. Так называемые подвешивающие операции проводят при опущении тазовых органов из-за ослабления тазового дна. Восстановление нормального положения тазовых органов способствует удержанию мочи. Пластику влагалища применяют для укрепления стенки влагалища, ее часто применяют при цистоцеле и ректоцеле. Мужчинам с поврежденным уретральным сфинктером и возникшим вследствие этого недержанием мочи также выполняют слинговые операции или устанавливают искусственный уретральный сфинктер.
16.3. ГИПЕРАКТИВНОСТЬ МОЧЕВОГО ПУЗЫРЯ
Гиперактивностью мочевого пузыря (синдромом гиперактивного мочевого пузыря) называют симптомокомплекс, проявляющийся императивными позывами на мочеиспускание, с ургентным недержанием мочи или без него, обычно сопровождающийся учащением мочеиспускания и ноктурией.
В основе гиперактивности мочевого пузыря лежит повышение чувствительности его рецепторов к растяжению и увеличение сократительной активности детрузора. Во время цистометрии у таких больных можно выявить гиперактивность детрузора. Под этим термином понимают уродинамический феномен, проявляющийся наличием непроизвольных сокращений детрузора, спонтанных или после провокации, которые не могут быть подавлены волевым усилием.
Если причиной гиперактивности мочевого пузыря является какое-либо неврологическое заболевание, то она обозначается как нейроген-ная гиперактивность мочевого пузыря. При отсутствии неврологической патологии используют термин «идиопатическая гиперактивность мочевого пузыря».
Частоту гиперактивности мочевого пузыря определить достаточно сложно, так как такие больные зачастую не обращаются за медицинской помощью или обращаются только при развитии недержания мочи. Однако полагают, что данная дисфункция имеет место у 10-15 % взрослых мужчин и женщин. Частота выявления гиперактивности мочевого пузыря повышается с возрастом.
Причины идиопатической гиперактивности мочевого пузыря до конца не выяснены. Однако установлены факторы, играющие важную
роль в ее развитии. К ним относятся инфравезикальная обструкция, воспаление мочевого пузыря, ишемия стенки мочевого пузыря. В последние годы значительное внимание уделяется генетическим факторам развития гиперактивности мочевого пузыря. Установлена связь между энурезом в детстве и появлением симптомов гиперактивности мочевого пузыря во взрослом возрасте.
К развитию нейрогенной гиперактивности мочевого пузыря приводят поражения центральной нервной системы выше крестцового центра мочеиспускания (S2-S4). Наиболее частыми причинами таких поражений являются рассеянный склероз, черепно-мозговые и спи-нальные травмы, миеломенингоцеле, spina bifida.
Клиническими симптомами гиперактивности мочевого пузыря являются поллакиурия, императивные позывы и ургентное недержание мочи. Боли в надлобковой области, вне или во время акта мочеиспускания, не характерны для данного заболевания.
Методы обследования, применяемые у больных с гиперактивностью мочевого пузыря, можно разделить на основные (базовые), дополнительные и уродинамические. Основное (базовое) обследование включает сбор анамнеза и опрос больного, физикальное обследование, лабораторное исследование. При оценке жалоб больного и сборе анамнеза заболевания необходимы тщательная детализация симптомов (поллакиурия, императивные позывы, недержание мочи) и подробный анализ перенесенных пациентом заболеваний и проводимого лечения. При первом общении с больным необходимо просить его заполнить дневник мочеиспускания, что позволяет объективно оценить выраженность симптоматики. Пациенты должны заполнять дневник мочеиспускания по крайней мере в течение 3 дней. Данные дневника мочеиспускания важны также для оценки эффективности последующего лечения.
К дополнительным относят эндоскопические, рентгенологические и ультразвуковые методы обследования. Цистоуретроскопия проводится для выявления органических причин дизурии, таких как камни и опухоли мочевого пузыря. При наличии гиперактивности детрузора, особенно нейрогенной природы, часто наблюдают умеренную или выраженную трабекулярность мочевого пузыря. УЗИ проводят для оценки сохранности паренхимы почки и выявления расширения ее чашечно-лоханочной системы. При УЗИ мочевого пузыря можно также обнаружить камни, дивертикулы, опухоли. Экскреторную урографию выполняют пациентам, у которых при УЗИ выявлено расширение чашечно-лоханочной системы почек. При экскретор-
ной урографии можно выявить уретерогидронефроз, особенно часто осложняющий нейрогенные дисфункции нижних мочевых путей.
Уродинамические исследования наиболее информативны при диагностике дисфункций нижних мочевых путей. Показатели урофло-уметрии у больных с гиперактивностью мочевого пузыря в отсутствие инфравезикальной обструкции в норме. Иногда у таких пациентов наблюдаются трудности при проведении урофлоуметрии в связи с малой емкостью мочевого пузыря и невозможностью накопления необходимого для проведения исследования объема мочи. Цистометрия наполнения позволяет выявить непроизвольную активность детрузора, повышение чувствительности мочевого пузыря и снижение его растяжимости. Видеоуродинамическое исследование используется для комплексной оценки состояния нижних мочевых путей. Особенно полезно его выполнение для выявления сложных дисфункций нижних мочевых путей, например гиперактивности детрузора в сочетании с детрузорно-сфинктерной диссинергией.
Лечение. Лечебные мероприятия при гиперактивности мочевого пузыря можно разделить на немедикаментозные, медикаментозные и хирургические. Главный принцип - начинать лечение с применения наименее травматичных методов, дающих наименьшее число побочных эффектов. Для большинства больных с гиперактивностью мочевого пузыря этому принципу соответствует комбинация немедикаментозных и медикаментозных методов. Хирургическое лечение должно применяться только при безуспешности консервативной терапии.
Немедикаментозное лечение включает тренировку мочевого пузыря, упражнения для тазовых мышц, физиотерапевтические методы. Преимущества немедикаментозных методов - практически полное отсутствие побочных эффектов и ограничений к применению в последующем других видов лечения, а также возможность использования наряду с медикаментозной терапией.
Тренировка мочевого пузыря заключается в соблюдении больным заранее установленного и согласованного с врачом плана мочеиспусканий, т. е. пациент должен мочиться через определенные интервалы времени и тем самым стараться изменить сформировавшийся патологический стереотип мочеиспускания.
Лечебный эффект упражнений для тазовых мышц определяется наличием анально-детрузорного и уретрально-детрузорного рефлексов - торможением сократительной активности детрузора при произвольных сокращениях наружных анального и уретрального сфинкте-
ров. Эффективность упражнений для тазовых мышц повышается при использовании метода биологической обратной связи.
Физиотерапевтические методы лечения заключаются в электрической стимуляции сакральных дерматомов и периферической тибиаль-ной электрической стимуляции. Электрическая стимуляция указанных структур способствует снижению сократительной активности и чувствительности мочевого пузыря.
Медикаментозное лечение - основной метод лечения гиперактивности мочевого пузыря. В задачи медикаментозного лечения у таких больных входят снижение сократительной активности детрузора и увеличение функциональной емкости мочевого пузыря. Клинически это выражается в урежении мочеиспусканий и интенсивности императивных позывов, исчезновении ургентного недержания мочи.
Для лечения гиперактивности мочевого пузыря рекомендуются антихолинергические препараты (толтеродин, солифенацин), спазмолитики с антихолинергической активностью (оксибутинин) и трицик-лические антидепрессанты (имипрамин). Препараты других групп из-за недостаточной эффективности или выраженных побочных эффектов не рекомендованы к широкому применению.
Продолжительность лечения гиперактивности мочевого пузыря обычно составляет 3 месяца. После окончания лечения его эффект сохраняется несколько месяцев, реже дольше. При недостаточной эффективности первого курса лечения или развитии клинических рецидивов возможно проведение одного или нескольких повторных курсов терапии.
Если у больного имеется инфравезикальная обструкция, то препараты с антихолинергическими свойствами назначают с осторожностью, поскольку они снижают сократительную активность детрузора и вследствие этого могут еще более снизить скорость мочеиспускания. При наличии выраженной инфравезикальной обструкции в первую очередь необходимо восстановить отток мочи из мочевого пузыря, а затем уже проводить медикаментозное лечение гиперактивности мочевого пузыря.
Хирургическое лечение гиперактивности мочевого пузыря применяется редко и только в тех случаях, когда остальные методы лечения оказались неэффективными. Основные хирургические методы лечения - миэкто-мия детрузора и энтероцистопластика. Миэктомия детрузора заключается в иссечении детрузора из свода мочевого пузыря при сохранении интактного слизистого слоя. Цель операции - уменьшение сократимости детрузора. Показание к энтероцистопластике - резкое снижение
растяжимости и значительное уменьшение емкости мочевого пузыря при неэффективности консервативной терапии, особенно при риске развития уретерогидронефроза. Чаще всего используется цистопластика с замещением мочевого пузыря участком подвздошной кишки.
16.4. ВОДЯНКА ОБОЛОЧЕК ЯИЧКА
Водянка оболочек яичка (гидроцеле) - скопление серозной жидкости между париетальным и висцеральным листками собственной оболочки яичка.
Этиология и патогенез. Водянка оболочек яичка может быть врожденной и приобретенной. Врожденная водянка оболочек яичка наблюдается в основном у детей и возникает вследствие незаращения влагалищного отростка брюшины при эмбриональном развитии и накопления в нем жидкости (сообщающаяся водянка). Если влагалищный отросток облитерируется не на всем протяжении, а на отдельных участках, то возникают замкнутые полости, располагающиеся по ходу семенного канатика (фуникулоцеле). Приобретенная водянка оболочек яичка чаще встречается у взрослых.
«Симптоматическая» (реактивная) водянка яичка возникает как следствие острого воспалительного процесса в яичке, травмы и опухоли яичка, при выраженной сердечной недостаточности. Склеротические изменения влагалищной оболочки, облитерация лимфатических сосудов приводят к затруднению оттока жидкости и ее скоплению между париетальной и висцеральной оболочками яичка при идиопатической водянке оболочек яичка. Эти явления могут быть как следствием воспаления, так и возрастных изменений.
Симптоматология и клиническое течение. По клиническому течению различают острую и хроническую водянки оболочек яичка.
Острые водянки оболочек яичка почти всегда являются симптоматическими и часто наблюдаются при остром орхите, эпидидимите, простудных заболеваниях. При этом происходит быстрое увеличение мошонки в объеме. Пальпаторно определяется жидкостное образование плотноэластической консистенции. Острая водянка оболочек яичка сопровождается симптомами, характерными для острого воспалительного процесса мошонки: высокой температурой тела, болями в яичке и придатке, гиперемией и отечностью мошонки.
Хроническая водянка оболочек яичка часто протекает бессимптомно. При увеличении объема мошонки появляются тянущие боли по ходу семенного канатика, дискомфорт при ходьбе, половом акте. При
очень больших размерах водянки половой член втягивается под растянутую над ней кожу мошонки. При мочеиспускании моча попадает на кожу мошонки, что приводит к мацерации кожи.
Диагностика. При гидроцеле соответствующая половина мошонки увеличена, верхняя часть водяночного мешка отграничена от наружного отверстия пахового канала, кожа над водяночным мешком подвижна, с гладкой поверхностью; водяночный мешок плотноили мягкоэлас-тичной консистенции, определяется симптом флюктуации.
При перкуссии выявляется притупление. Водяночный мешок не вправляется в паховый канал (за исключением сообщающейся водянки, при которой жидкость при горизонтальном положении больного уходит в брюшную полость и перемещается обратно в вертикальном положении). Важный диагностический метод при обследовании больных с водянкой оболочек яичка - диафаноскопия - просвечивание мошонки интенсивным и направленным световым пучком. При водянке оболочек яичка световой пучок проходит через жидкость водяночного мешка, и мошонка приобретает равномерную интенсивную розовую окраску. При наличии опухоли или грыжи свет не будет проходить через мошонку.
Всем больным с гидроцеле необходимо проводить УЗИ мошонки, так как это позволяет выявить опухоль яичка при наличии симптоматической водянки оболочек яичка. Хирургические вмешательства на мошонке, в том числе и в связи с гидроцеле, при не распознанном до операции раке яичка резко ухудшают прогноз и выживаемость, поэтому противопоказаны. При гидроцеле на эхограммах яичко определяется в виде эхопозитивного образования однородной структуры, окруженного эхонегативной зоной (водяночной жидкостью).
При небольших опухолях в яичке появляется небольшой участок, несколько отличающийся по акустическим характеристикам от нормальной паренхимы. При больших опухолях яичко увеличено, отмечаются неровность контура, неоднородность внутренней структуры, появляются эхонегативные включения.
Дифференциальную диагностику необходимо проводить также и с пахово-мошоночной грыжей. В последнем случае содержимое увеличенной мошонки достаточно легко вправляется в брюшную полость, при пальпации ощущается урчание кишки, при перкуссии - тимпанит.
Лечение. При симптоматических водянках необходимо лечение основного заболевания: орхита, эпидидимита, опухоли и др.
Пункция водяночного мешка, даже с последующим введением скле-розирующих веществ, не является радикальным методом лечения и
в настоящее время используется редко. При этом методе велик риск возникновения осложнений и рецидива заболевания. Пункция показана только в том случае, когда тяжесть общего состояния пациента не позволяет выполнить оперативное лечение.
Основной и радикальный метод при хронических формах гидроце-ле - оперативное лечение.
Наиболее часто применяется операция Винкельмана: после вскрытия водяночной полости оболочки выворачивают и их края сшивают позади придатка яичка. Таким образом ликвидируется замкнутая полость, в которой накапливается жидкость, и внутренняя поверхность собственной оболочки яичка соприкасается с его мясистой оболочкой, которая может всасывать транссудат. При склерозированных, утолщенных оболочках выполняют их резекцию (операция Бергмана).
У детей при сообщающейся водянке проводят иссечение и перевязку влагалищного отростка брюшины. Прогноз при гидроцеле благоприятный, однако при больших размерах водяночного мешка и длительном течении заболевания возможны атрофия яичка и нарушение сперматогенеза.
16.5. ИНОРОДНЫЕ ТЕЛА В МОЧЕВОМ ПУЗЫРЕ И МОЧЕИСПУСКАТЕЛЬНОМ КАНАЛЕ
Инородные тела в мочевом пузыре. Инородные тела могут попасть в мочевой пузырь из уретры, мочеточников или из окружающих тканей, например из вскрывшихся в мочевой пузырь абсцессов или свищей. Большинство инородных тел попадает в пузырь через уретру.
Этиология и патогенез. Инородные тела в мочевой пузырь попадают по разным причинам, чаще всего в результате необдуманных действий пациентов или медицинских работников. Чаще всего пациенты с психическими расстройствами вводят в уретру предметы с целью мастурбации и, не удержав их, упускают в мочевой пузырь. Иногда детская шалость приводит к попаданию через уретру в мочевой пузырь инородных тел.
Известны случаи попадания в мочевой пузырь инородных тел в результате проникающих пулевых или осколочных ранений, осколков стекла. В мочевом пузыре могут оказаться лигатуры из нерастворимого шовного материала, мигрировавшие в его полость после хирургической или гинекологической операции. Описаны случаи удаления из мочевого пузыря марлевых шариков, пинцетов и хирургических игл, оставленных после операций на мочевых путях.
Любое инородное тело, попавшее в мочевой пузырь, инкрустируется мочевыми солями и со временем превращается в камень мочевого пузыря. Даже на гладкой поверхности градусника, находящегося в мочевом пузыре, спустя 2-3 месяца образуется мочевой камень. Катетеры Пеццера и Фолея, устанавливаемые в мочевой пузырь, несмотря на ежедневное промывание, спустя 1,5-2 месяца покрываются солями, нарушающими их проходимость. Инкрустируются и мочеточниковые стенты, которые спустя 3-4 месяца превращаются в трудноудалимые предметы, нарушающие отток мочи из почки.
Симптоматика. Любое инородное тело в мочевом пузыре приводит к воспалительной реакции, сопровождающейся дизурией, пол-лакиурией, иногда возникает терминальная или тотальная гематурия. При попадании предметов, находящихся в мочевом пузыре, в задний отдел уретры возникают боли спастического характера, наблюдается прерывание струи мочи.
Пациенты, которые ввели инородный предмет в уретру и мочевой пузырь, длительное время не обращаются за медицинской помощью из чувства стыда, надеясь на спонтанное его отхождение, однако присоединившийся цистит и гематурия вынуждают их обратиться к врачу.
Диагностика инородных тел мочевого пузыря не представляет трудности, если пациент расскажет о том, что произошло. Однако большинство обратившихся за помощью людей предпочитают умалчивать об инциденте, поэтому нередко лишь инструментальные и рентгенологические методы исследования позволяют поставить правильный диагноз. Иногда пациенты рассказывают об имевшем место происшествии, а чаще, ссылаясь на алкогольное опьянение и амнезию, умалчивают о случившемся. В таких случаях без должного обследования диагностируется острый цистит и пациенту назначают терапию с применением уроантисептиков, которая даст временный эффект или не улучшит состояние больного.
Наиболее информативное исследование при диагностике инородного тела в мочевом пузыре - цистоскопия, которая позволяет не только увидеть и идентифицировать предмет, но и с помощью операционного цистоскопа попытаться его удалить. Нередко инородное тело полностью петрифицируется и имеет вид камня мочевого пузыря. Поэтому следует выполнить обзорную рентгенографию мочевого пузыря, которая позволит распознать предмет, оценить структуру и ядро камня.
Наличие хронического цистита, при котором уменьшается емкость мочевого пузыря, не всегда позволяет достаточным образом наполнить пузырь или создать в нем прозрачную среду. В этих случаях цистоско-
пию заменяют обзорной рентгенографией или УЗИ мочевого пузыря. На обзорной рентгенограмме можно увидеть тень самого инородного тела и его солевую оболочку.
Лечение. Наличие инородного тела в мочевом пузыре любого происхождения - показание к его удалению. Пребывание в мочевом пузыре инородного предмета поддерживает воспаление его стенки, создает условия для пузырно-мочеточникового рефлюкса и пиелонефрита. Преимущество в удалении инородных тел мочевого пузыря принадлежит эндоскопическим манипуляциям, при которых вначале разрушают инкрустирующую оболочку, а затем экстрактором захватывают и извлекают инородный предмет.
При наличии в мочевом пузыре объектов, мигрировавших из околопузырной клетчатки (пули, осколки), которые (из-за их размеров) не проходят через уретру или могут вызвать серьезные ее повреждения, пациенту показано оперативное лечение. Обычно выполняют высокое сечение мочевого пузыря, ревизию его полости, удаление инородного тела с последующим ушиванием стенки наглухо. После операции мочевой пузырь дренируют по уретре трехходовым катетером для постоянного орошения его полости антисептическим раствором для подавления воспалительной реакции, обычной при инородных телах.
Прогноз при своевременном лечении благоприятный, но длительное механическое раздражение переходного эпителия мочевого пузыря может вызывать его метаплазию и злокачественное перерождение.
Инородные тела в мочеиспускательном канале. Это состояние возможно только у лиц мужского пола ввиду того, что сравнительно широкая и короткая уретра женщин не способна фиксировать в своем просвете инородное тело.
Этиология и патогенез. Инородные тела в мочеиспускательный канал попадают так же, как и в мочевой пузырь. Через наружное отверстие в уретру вводят инородные тела дети, оставленные без присмотра, психические больные с целью мастурбации, половые партнеры в состоянии алкогольного опьянения. Иногда инородные тела могут оказаться в мочеиспускательном канале после лечебных процедур и диагностических манипуляций.
Симптоматика. Инородное тело вызывает раздражение слизистой оболочки мочеиспускательного канала и приводит к хроническому уретриту, имеющему типичную клиническую картину. При длительном нахождении инородного предмета в уретре происходит его инкрустация, в стенке уретры возникают пролежни, возможно образование мочевых затеков и уретральных свищей.
При попадании инородного тела в уретру возникают болевые ощущения, усиливающиеся при мочеиспускании и эрекции. Спустя сутки появляются гнойные выделения, инициальная гематурия, сопровождающиеся странгурией, а иногда и острой задержкой мочеиспускания.
Диагностика. Инородное тело в мочеиспускательном канале легко пропальпировать, особенно если оно расположено в его висячей или промежностной части. При пальцевом исследовании через прямую кишку можно прощупать предмет, расположенный в перепончатой части мочеиспускательного канала. Уретру исследуют металлическим бужом, выполняют уретроскопию и уретрографию.
Слизистая оболочка мочеиспускательного канала весьма чувствительна к прикосновению и болезненна, поэтому любую манипуляцию на уретре следует проводить с применением местной анестезии или кратковременного наркоза. На фоне анестезии следует особенно аккуратно выполнять исследования, чтобы не перфорировать стенку мочеиспускательного канала и не протолкнуть инородный предмет в мочевой пузырь.
Лечение. Существуют некоторые приемы, позволяющие помочь пациенту самостоятельно избавиться от инородного тела. Для этого при наполненном мочевом пузыре в мочеиспускательный канал следует ввести анестетик с глицерином (катеджель с лидокаином), зажать уретру, поместить пациента в теплую ванну и затем предложить ему помочиться, сильно натуживаясь. При этом уретра, растянутая введенным глицерином, и интенсивный поток мочи из пузыря выталкивают инородное тело. Если этот прием не приносит успеха, предпринимают попытку извлечь инородное тело инструментами.
Удаляют инородное тело из мочеиспускательного канала в стационаре обычно с помощью операционного уретроцистоскопа. Под визуальным контролем захватывают инородное тело экстрактором «птичья лапа», в уретру вводят глицерин или вазелиновое масло и извлекают предмет. В редких случаях выполняют оперативное вмешательство - наружную уретеротомию.
Прогноз благоприятный.
16.6. МУЖСКОЕ БЕСПЛОДИЕ
Общие сведения. Согласно определению ВОЗ, бесплодной следует считать супружескую пару, которая не может добиться наступления беременности в течение года регулярной половой жизни без применения контрацепции.
Бесплодие в браке - распространенная проблема, которая отмечается примерно у 25 % супружеских пар, при этом нарушение мужской репродуктивной функции наблюдается примерно в половине случаев.
Существует несколько методов классификации бесплодия у мужчин. При абсолютном бесплодии зачатие невозможно вследствие необратимости изменений в организме мужчины, при относительном бесплодии его причины устранимы. Если мужчина никогда не был способен к оплодотворению, бесплодие называют первичным, в тех случаях, когда от него раньше наступали беременности, - вторичным. Секреторным бесплодием называют прекращение образования сперматозоидов, экскреторным (обструктивным) - бесплодие вследствие нарушения проходимости семявыносящих путей. Кроме того, принято рассматривать виды бесплодия в зависимости от причины его развития: гипотала-мо-гипофизарное (синдром Каллмана, конституциональная задержка полового развития, гиперпролактинемия и т. д.), тестикулярное (анор-хия, крипторхизм, варикоцеле, синдром клеток Сертоли, карцинома яичка и т. д.), семявыносящих путей (инфекции, врожденная и приобретенная обструкция, аутоиммунное), нарушение доставки спермы (аномальное расположение наружного отверстия уретры, деформации полового члена, эректильная дисфункция, ретроградная эякуляция и т. д.). Кроме того, если бесплодие является осложнением эндокринного заболевания, говорят об эндокринном бесплодии (нарушение секреции фолликулостимулирующего гормона - ФСГ, лютеинизирующего гормона - ЛГ, тестостерона), при врожденных генетических дефектах - о генетическом бесплодии (синдром Клайнфелтера, Шерешевского- Тернера и т. д.). Бесплодие после перенесенного воспаления половых органов называют поствоспалительным, вследствие действия токсинов - токсическим (лекарственные препараты, курение, алкоголь), и т. д. Наиболее распространено бесплодие при варикоцеле (12-13 %), после инфекций, передающихся половым путем (6-7 %), а также вследствие аутоиммунных реакций (3-4 %). Однако у большинства (60-75 %) мужчин не удается обнаружить причину, приводящую к бесплодию, в этих случаях его называют идиопатическим. Немаловажным фактором, от которого зависит вероятность наступления беременности, является возраст женщины. Так, если фертильный потенциал 25-летней женщины принять за 100 %, то, когда ей исполнится 35, 38 и 40 лет, он составит 50, 25 и 5 % соответственно. Этот фактор в последнее время играет все большую роль в связи с тем, что в индустриально развитых странах многие женщины предпочитают откладывать деторождение для обеспечения карьерного роста.
Варикоцеле - это варикозное расширение вен гроздьевидного сплетения, которое наблюдают примерно у 20-24 % мужчин вследствие нарушения оттока крови из-за несостоятельности клапанов, дренирующих сплетения яичковых вен. До настоящего времени нет единой точки зрения о влиянии варикоцеле на сперматогенез и фертильность мужчин. Наиболее распространена гипотеза, согласно которой варико-целе приводит к повышению температуры и гипоксии яичка, что может способствовать увеличению степени олигоастенотератозооспермии. Кроме того, у детей варикоцеле может приводить к снижению объема яичка и нарушению функции клеток Лейдига. Противоречивыми оказались результаты исследований, проведенных для доказательства целесообразности выполнения оперативного лечения - лигирования или эмболизации внутренней яичковой вены - у мужчин с варикоцеле и снижением показателей сперматогенеза для ликвидации бесплодия в браке. Мета-анализ этих работ, основанный на принципах доказательной медицины, в настоящее время не позволяет рекомендовать хирургическое лечение мужчин по поводу варикоцеле для восстановления их фертильного потенциала.
Бесплодие после воспаления половых органов (эпидидимита, орхита, простатита) чаще всего обусловлено обструкцией вследствие рубцовых изменений придатка яичка, семявыносящего протока или предстательной железы. Возможность восстановления проходимости семявыносящих путей у этих пациентов зависит от локализации и протяженности сужений. Альтернативой реконструкции может быть хирургическая экстракция сперматозоидов и использование их в программе вспомогательных репродуктивных технологий (ВРТ).
Эндокринное бесплодие обусловлено нарушением связей в гипо-таламо-гипофизарно-гонадной оси. Различают первичный и вторичный гипогонадизм. При первичном гипогонадизме происходит непосредственное повреждение ткани яичек под действием различных врожденных (анорхизм, синдром клеток Сертоли) или приобретенных (травма, рост новообразования) факторов, что сопровождается повышенной секрецией гонадропных гормонов гипофиза - ФСГ и ЛГ (гиперго-надотропный гипогонадизм). Прогноз у таких пациентов полностью зависит от наличия в яичках зон с сохраненным сперматогенезом, отсутствие которых свидетельствует о стерильности и отсутствии возможности излечения.
При вторичном гипогонадизме нарушение сперматогенеза является следствием недостаточной секреции гонадотропных гормонов гипофиза (гипогонадотропный гипогонадизм). Это состояние также может
быть врожденным (первичный дефицит гонадотропинов) или приобретенным (дефицит гонадотропинов вследствие заболеваний гипоталамо-гипофизарной области и др.). Реже встречается нормогонадотропный гипогонадизм, при котором отмечается низкая продукция тестостерона при нормальном уровне гонадотропинов. Считается, что в его основе лежат смешанные нарушения репродуктивной системы - сочетание повреждения ткани яичек и недостаточности гипоталамо-гипофи-зарной регуляции. При сохраненном сперматогенном эпителии прогноз у этой категории пациентов благоприятный.
Иммунное бесплодие может быть изоиммунным и аутоиммунным. При изоиммунном бесплодии синтез антиспермальных антител происходит в женском организме и препятствует продвижению сперматозоидов. При аутоиммунной форме в организме мужчины нарушается целостность образованного оболочкой семенных канальцев и клетками Сертоли гематотестикулярного барьера, вследствие чего формируются антитела, разрушающие сперматозоиды. К этому может привести множество причин, среди которых термическое или механическое повреждение, нарушение кровоснабжения, воспаление половых органов и т. д.
В настоящее время установлено большое число факторов, способных приводить к нарушениям фертильности мужчин. К ним относятся физические и эмоциональные перегрузки, злоупотребление алкогольными напитками и курением табака, пребывание в условиях с высокой температурой окружающей среды; заболевания, сопровождающиеся повышением температуры тела. Кроме того, угнетать сперматогенез могут и некоторые лекарственные препараты (ацетилсалициловая кислота, кофеин, циметидин, колхицин, ингибиторы моноаминоксигена-зы, нитрофураны, тестостерон и др.). Тяжелые сопутствующие болезни (сахарный диабет, атеросклероз, печеночная и почечная недостаточность) могут приводить к бесплодию вследствие нарушения метаболизма гормонов и развития копулятивных расстройств. Вероятность зачатия зависит от режима половой активности, применения контрацептивов, спермицидов. Все эти факторы следует принимать во внимание при обследовании бесплодных пар и при выборе метода лечения.
Диагностика. Ее начинают со сбора анамнеза, что у многих больных позволяет предположить основную причину бесплодия. Опрос обычно начинают с уточнения продолжительности периода, в течение которого супруги пытаются зачать ребенка. Необходимо расспросить мужчину о режиме половой жизни, применении контрацепции, а также перенесенных и сопутствующих заболеваниях (аномалии развития, воспа-
лительные заболевания и травмы мужских половых органов, сахарный диабет, болезни нервной системы, органов дыхания), оперативных вмешательствах, эпизодах повышения температуры тела, а также о наличии профессиональных и бытовых вредностей - высокой температуры окружающей среды, радиоактивных и токсичных соединений, курении табака, употреблении алкоголя и наркотиков, приеме лекарственных средств, которые могут повлиять на фертильность.
Объективное обследование проводят в помещении при температуре 20-22°С наедине с больным. При осмотре выявляют аномалии развития, оценивая рост и массу тела, определяют пропорциональность телосложения, обращают внимание на распределение волосяного покрова, соотношение мышечной массы и жировой клетчатки, а также осматривают область соска для исключения гинекомастии.
При осмотре и пальпации полового члена следует обратить внимание на наличие аномалий расположения наружного отверстия уретры, рубцов вследствие хирургических вмешательств и травм, уплотнений белочной оболочки, а также на возможность свободного смещения крайней плоти и обнажения головки полового члена. Гипоспадия, эписпадия, искривление полового члена, сужение уретры и фимоз могут препятствовать нормальному транспорту спермы при половом акте. При обнаружении выделений из уретры, эрозий на коже головки полового члена и крайней плоти следует провести обследование для исключения заболеваний, передающихся половым путем.
Органы мошонки осматривают в положении стоя. Яички в норме располагаются вертикально в нижней части мошонки, имеют объем около 15 см3 и плотноэластическую консистенцию. Отсутствие сперматозоидов в эякуляте мужчин с яичками нормальных размеров может свидетельствовать о наличии обструкции семявыносящих путей. Уменьшение объема яичка может указывать на недостаточное развитие сперматогенного эпителия, которое, в частности, наблюдают при синдроме Клайнфелтера и при гипогонадотропном гипогонадизме. Увеличение объема яичка может быть признаком новообразования, его следует дифференцировать от гидроцеле и кисты придатка яичка и семенного канатика. Для этого чаще всего используют ультразвуковое сканирование. Придатки яичек располагаются позади и несколько медиальнее яичек, при пальпации оценивают четко очерченные и безболезненные головку, тело и хвост, из которого выходит и определяется далее по ходу семенного канатика семявыносящий проток. Болезненность или уплотнение придатков характерны для воспаления, причинами которого могут быть инфекции: гонококки, хламидии,
кишечная палочка, протей, клебсиелла. Кистозные деформации придатка характерны для обструкции семявыносящих путей, отсутствие семявыносящего протока нередко наблюдается при муковисцидозе. В положении стоя в покое и при натуживании (проба Вальсальвы) также определяют состояние вен гроздьевидного сплетения, их варикозное расширение называется варикоцеле.
При проведении пальпации в области мошонки и пахового канала также можно обнаружить паховые грыжи, рубцовые изменения тканей вследствие ранее произведенных операций, которые могут быть причиной сдавливания семенного канатика и нарушения кровоснабжения яичка. Завершают объективное обследование пальцевым ректальным исследованием, для чего пациент ложится на бок и прижимает колени к животу или принимает коленно-локтевое положение. Предстательная железа в норме имеет плотноэластическую консистенцию, гладкую безболезненную поверхность, отчетливо выраженную срединную борозду. Болезненность железы при пальпации характерна для простатита, а при выявлении участков уплотнения требуется исключить рак предстательной железы.
Ведущим при проведении лабораторной диагностики у мужчины, состоящего в бесплодном браке, является исследование эякулята - спермограммы. Интерпретацию показателей спермограммы, выполненной с соблюдением стандартных требований руководства Всемирной Организации Здравоохранения (ВОЗ), проводят в соответствии референтными значениями (табл. 16.1).
Таблица 16.1. Референтные значения спермограммы в соответствии с требованиями ВОЗ
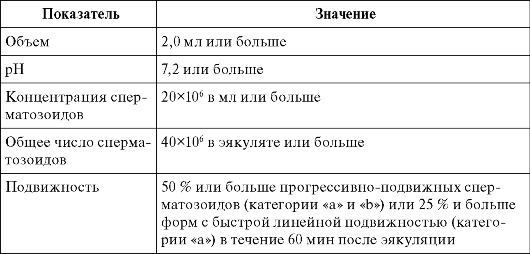
Окончание табл. 16.1.

При этом используют следующие термины:
- нормозооспермия - все параметры эякулята соответствуют референтным значениям;
- олигозооспермия - концентрация сперматозоидов меньше соответствующего референтного значения;
- астенозооспермия - подвижность сперматозоидов меньше соответствующего референтного значения;
- тератозооспермия - количество нормальных форм сперматозоидов меньше соответствующего референтного значения;
- олигоастенотератозооспермия - снижение количества и подвижности сперматозоидов в сочетании с уменьшением доли сперматозоидов, имеющих нормальное строение (ОАТ-синдром);
- криптозооспермия - в нативном препарате сперматозоиды отсутствуют, несколько сперматозоидов обнаружены в осадке после центрифугирования;
- азооспермия - отсутствие сперматозоидов в эякуляте, подтверждено анализом осадка после центрифугирования;
- аспермия - отсутствие эякулята.
Если показатели спермограммы нормальные, то последующего обследования не требуется, при отклонениях от референтных значений показано повторное исследование эякулята. При астенозооспермии целесообразно определение в семенной жидкости антиспермальных антител, присутствие которых может указывать на иммунологическую причину бесплодия.
Для уточнения диагноза выполняют и другие лабораторные исследования: клинический анализ крови, функциональные пробы, позволяющие характеризовать функцию печени и почек, анализ мочи. У мужчин, испытывающих оргазм при аспермии, обнаружение сперматозоидов
в моче после полового акта свидетельствует о ретроградной эякуляции. При подозрении на воспаление уретры и предстательной железы проводят трехстаканную пробу мочи.
Для дифференциальной диагностики при гипогонадизме производят определение содержания гормонов в крови: ФСГ, ЛГ, тестостерона и пролактина. При первичном гипогонадизме и недостаточном развитии герминогенных клеток и клеток Лейдига в яичках сперматозоидов нет или они представлены скудно, уровень тестостерона снижен, а содержание гонадотропных гормонов гипофиза - ФСГ и ЛГ - повышено. Пониженный уровень гонадотропинов - это признак вторичного гипогонадизма. Увеличение концентрации пролактина наблюдают при пролактин-секретирующих новообразованиях гипофиза.
Азооспермия служит показанием к проведению биопсии яичка. При этом можно обнаружить синдром клеток Сертоли, гипосперма-тогенез или остановку сперматогенеза, которые являются основными причинами секреторного бесплодия. Иногда (0,5-1 %) при гистологическом исследовании полученного материала оказывается, что азооспермия была следствием карциномы in situ яичка, при этом требуется соответствующее лечение. Сохранность сперматогенеза, как правило, свидетельствует об обструктивном бесплодии, при котором в ряде случаев возможна хирургическая реконструкция семявыносящих путей. При невозможности восстановления их проходимости сперматозоиды, полученные хирургическим путем, могут быть применены в программах ВРТ - при экстракорпоральном оплодотворении (ЭКО) с интрацитоплазматической инъекцией сперматозоида в яйцеклетку (ИКСИ). Эти методы также применяют у мужчин с азооспермией при секреторном бесплодии, если при биопсии у них удается выявить зоны сперматогенеза в яичках.
Азооспермия и олигозооспермия могут быть следствиями аномалии хромосомного набора или микроделеции Y-хромосомы, поэтому являются основаниями для проведения генетического обследования мужчин. Диагностика этих нарушений позволяет уточнить вероятность их наследственной передачи и риск развития генетически обусловленных заболеваний у потомства.
Ультразвуковое исследование органов мошонки позволяет визуализировать их внутреннюю структуру, проводить дифференциальную диагностику между жидкостными образованиями (водянка оболочек яичка, кисты придатков яичек, кисты семенного канатика) и тканевыми (рак яичка, опухоль придатка яичка, эпидидимит), а также выявить расширение вен гроздьевидного сплетения и ретроградный кровоток
при пробе Вальсальвы, характерные для варикоцеле. При трансректальном ультразвуковом сканировании у мужчин с обструкцией на уровне эякуляторных протоков можно отметить расширение семенных пузырьков, а также патологические изменения предстательной железы - кисты, рубцы, камни и т. д.
Лечение. Тактика лечения при бесплодии в браке зависит от вида бесплодия и характера изменений эякулята. Если показатели спер-мограммы не изменены, рекомендуется исключить женский фактор как причину бесплодного брака и в случае необходимости применять ВРТ - внутриматочные инсеминации, ЭКО, ИКСИ.
Соблюдение режима, при котором снижается воздействие факторов, угнетающих сперматогенез - снижение употребления алкоголя, отказ от курения, коррекция медикаментозной терапии, ликвидация воспалительных процессов и т. д. позволяет добиться улучшения показателей эякулята. В тех случаях, когда причиной бесплодия в браке является нарушение доставки спермы, проводят соответствующую фармакологическую или хирургическую коррекцию. При вторичном гипогонадизме эффективна гормональная заместительная терапия гонадотропными препаратами. При обструктивном бесплодии в ряде случаев может быть произведена реконструктивная операция и восстановление проходимости семявыносящих путей при помощи микрохирургической техники.
При аутоиммунном бесплодии, а также при идиопатическом ОАТ-синдроме или при отсутствии эффекта от проведенного лечения целесообразно применение ВРТ. При этом может потребоваться хирургическая экстракция и криоконсервация сперматозоидов. В тех случаях, когда у мужчин отсутствуют сперматозоиды, проблему бесплодия в браке можно решить при помощи донорства или усыновления.
16.7. ПОЛОВЫЕ РАССТРОЙСТВА У МУЖЧИН
Общие сведения. В конце ХХ в. был достигнут значительный прогресс в понимании механизмов, формирующих половое поведение мужчин: детально исследованы анатомические особенности мужской половой системы, существенно дополнены знания о физиологических и биохимических основах ее работы, описаны пути и медиаторы нейро-эндокринной регуляции. Эти знания в значительной мере способствовали совершенствованию методов диагностики половых расстройств, а также послужили основой для создания высокоэффективных подходов к лечению больных. При обследовании пациентов с копулятивными расстройствами при необходимости могут применяться основанные
на передовых медицинских технологиях новые диагностические методики - селективная ангиография, динамическая кавернозометрия, дуплексное сканирование с цветовым допплеровским картированием. В лечении используют высокоэффективные синтезированные лекарственные препараты и оперативные вмешательства, основанные на имплантации протезов полового члена и микрохирургических способах его реваскуляризации.
Эти подходы способствовали изменению господствующих ранее представлений о преимущественной роли психогенных факторов в развитии нарушений копулятивной функции. Сегодня считается, что более 80 % половых расстройств обусловлены органической патологией, при этом наиболее распространенными являются васкулогенные механизмы нарушений. В связи с этим на современном этапе возрастает понимание взаимосвязи различных аспектов полового поведения мужчин и общего состояния организма, наличия сопутствующих заболеваний: атеросклероза, гипертонической болезни, сахарного диабета, ожирения и др. Установлено, что копулятивные расстройства могут указывать на наличие или риск развития патологических изменений сердечно-сосудистой, эндокринной и нервной систем. Следовательно, анализ аспектов половой жизни мужчин должен быть включен в алгоритм обследования пациентов широким кругом специалистов. С развитием представления о патофизиологических основах сексуальных расстройств у мужчин совершенствовались представления об особенностях половых расстройств у женщин. Перечисленные факторы способствовали превращению этой области медицинской науки и практики в крупный междисциплинарный раздел, составляющие которого относятся не только к урологии и андрологии, но и к сексологии, терапии, эндокринологии, неврологии, гинекологии и т. д. Кроме того, стало ясно, что подавляющему большинству пациентов с копулятивными расстройствами не требуется проведение специального обследования, а при назначении современных высокоэффективных таблетированных лекарственных средств для устранения эректильной дисфункции достаточно компетенции врачей общей практики.
Половое поведение обеспечивает репродуктивную функцию, однако, в отличие от животных, у человека естественная, поставленная природой цель половой жизни - продолжение рода - не является единственной в реализации сексуальных потребностей. Согласно представлениям современной сексологии, модель полового поведения обусловлена взаимным дополнением различных компонентов - формированием половой дифференцировки, контролем личного опыта
и развития социальных навыков. У мальчиков она закладывается в момент рождения и постоянно совершенствуется, достигая зрелости после прохождения периода полового созревания. Таким образом, половая роль является не только выражением половой идентичности, но также представляет собой совокупность индивидуально-личностных и социально-нормативных аспектов деятельности.
Количественная оценка сексуальности может быть дана при анализе половой конституции человека, определяющей силу, длительность и частоту сексуальных реакций. При этом характер реального полового поведения мужчин в значительной степени модулируется большим количеством психофизиологических и социальных факторов, которые в настоящее время изучены недостаточно полно. В середине ХХ в. было сформировано представление о цикличном характере сексуальной активности мужчин и женщин, описаны основные фазы копулятивного цикла: возбуждения, «плато», оргазма и «разрешения». Кроме того, у мужчин были выделены основные компоненты полового акта: половое влечение, эрекция, эмиссия, эякуляция и оргазм. После завершения каждого цикла наступает период рефрактерности, в течение которого сексуальная активность невозможна.
Несмотря на то, что об угасании половой функции у мужчин с возрастом известно давно, широкомасштабные эпидемиологические исследования в этой области были проведены лишь в последнее время. При этом оказалось, что копулятивные расстройства встречаются часто - в среднем ими страдает около трети мужчин от 18 до 60 лет и более половины мужчин старше 40 лет. Вероятность развития дисфункций значительно увеличивается при наличии факторов риска (курение, ожирение) и сопутствующих заболеваний (атеросклероза, артериальной гипертензии, сахарного диабета и т. д.), способствующих нарушению кровоснабжения половых органов. Наряду с этим, нормальной работе физиологических механизмов может препятствовать недостаток мужского полового гормона тестостерона в крови, постепенное снижение уровня которого наблюдается у всех мужчин, начиная с 30-летнего возраста. Несмотря на то, что тестостерон не является прямым стимулятором регуляции компонентов копулятивного цикла, доказано, что этот гормон играет важную роль в формировании полового влечения, увеличивает синтез медиаторов эрекции в нервных окончаниях, поддерживает метаболизм гладкой мускулатуры, кавернозных нервов, эндотелия и соединительной ткани полового члена.
Выделяют первичные (врожденные) и вторичные (приобретенные), а также психогенные и органические (обусловленные нарушением функ-
ции внутренних органов) половые расстройства, однако наибольшее распространение получила классификация копулятивных расстройств у мужчин в соответствии с компонентами полового акта.
Половое влечение (либидо). Нейрогуморальная регуляция полового влечения производится лимбической областью и височной частью коры головного мозга и в основном обеспечивается активностью тестостерона, который вырабатывается в яичках под влиянием гормонов гипоталамо-гипофизарно-гонадной системы. Психическая составляющая либидо формируется под действием широкого спектра стимулирующих и тормозящих физиологических, психологических и социальных факторов и отличается индивидуальной вариабельностью. Принято рассматривать половое влечение как совокупность побуждения, имеющего биологическую природу, мотива - основанного на психологических факторах индивидуальности и взаимоотношений, и желания - связанного с культурными компонентами. Нормальные физиологические или патологические процессы, изменяющие нейрогуморальную или психическую составляющую либидо, могут привести как к усилению, так и к ослаблению полового влечения у мужчин. Наиболее распространено снижение полового влечения, которым, по современным данным, страдают от 12 до 28 % мужчин в возрасте от 40 до 80 лет. Факторами риска снижения либидо считают пожилой возраст и сопутствующие заболевания (гипого-надизм, гиперпролактинемию, депрессию, почечную недостаточность), злоупотребление алкоголем, негативный сексуальный опыт. Это патологическое состояние нередко сочетается с другими копулятивными расстройствами, в частности с эректильной дисфункцией.
Диагностика снижения полового влечения обычно не представляет затруднений и основана на анализе жалоб больного и сборе анамнеза. Нет единого мнения о нижней границе нормальных значений для величины либидо. Большинство мужчин, ведущих нормальную, с их точки зрения, половую жизнь, испытывают влечение и имеют половые акты от одного до четырех раз в неделю. Следовательно, проявление сексуальной активности реже, чем один раз в две недели, следует считать признаком, характерным для снижения либидо. При этом необходимо учитывать тесную взаимосвязь компонентов полового акта и возможное снижение полового влечения вследствие эректильной дисфункции, болезненного или преждевременного семяизвержения и т. д.
В дополнение к стандартным методам общеклинического обследования у больных, предъявляющих жалобы на снижение либидо, целесообразно анализировать уровень тестостерона и пролактина в крови и при необходимости рекомендовать консультацию эндокринолога.
При лечении пациентов со снижением полового влечения первоочередной задачей должно быть выявление и устранение основного заболевания, следствием которого является нарушение либидо. В настоящее время не создано эффективных лекарственных препаратов для симптоматической терапии. У многих пациентов с комплексными копулятивными расстройствами улучшение качества эрекции или нормализация эякуляции приводит к усилению полового влечения. У больных со снижением либидо вследствие гипогонадизма эффективна заместительная гормональная терапия препаратами тестостерона. При наличии проблем в отношениях между партнерами может потребоваться консультация психотерапевта или сексолога.
Эрекция. Накопление знаний об анатомическом строении полового члена, особенностях его кровоснабжения и биохимических механизмах стимуляции и торможения артериального притока к кавернозным телам позволило разработать современные рекомендации по диагностике и лечению больных с эректильной дисфункцией.
Половой член состоит из двух пещеристых (кавернозных) тел, расположенных дорсолатерально, и губчатого (спонгиозного) тела, расположенного вентрально. Кавернозные тела снаружи ограничены толстой неэластичной белочной оболочкой, волокна которой формируют межкавернозную перегородку, проницаемую для крови. Вокруг спонгиозного тела располагается более тонкая белочная оболочка. Все тела полового члена окружены фиброзной тканью - фасцией Бака, а более поверхностно - подкожной клетчаткой и кожей. Через губчатое тело проходит мочеиспускательный канал, в заднем отделе оно образует луковицу, а в переднем - головку полового члена.
Внутри кавернозных тел находится пещеристая ткань. Она представлена трехмерной сетью трабекул, состоящих из гладких мышц и фиброзных эластичных волокон. Трабекулы покрыты эндотелием и окружают заполненные кровью лакунарные (синусоидальные) пространства.
Кровоснабжение полового члена осуществляется через ветви внутренней половой артерии: артерию луковицы полового члена, глубокую (кавернозную) и дорсальную артерии полового члена и уретральную аретрию. Глубокая артерия следует через кавернозные тела по всей их длине, при этом от нее отходят множественные мелкие извитые ветви - хелициновые артерии, которые открываются в лакунарные пространства. Кровь из лакунарных пространств попадает в систему промежуточных дренирующих вен и проходит сквозь белочную оболочку через эмиссарные вены, а затем дренируется в глубокую дорсальную вену напрямую или через обвивающие вены.
Половой член иннервируется вегетативной и соматической нервной системой. Парасимпатические волокна выходят из сакрального эрек-тильного центра (S2-S4). Симпатические волокна берут начало в тора-колюмбальной зоне (ThXII-LII) и проходят вдоль периаортального сплетения в подчревное сплетение. Преганглионарные парасимпатические волокна сакрального эректильного центра объединяются с симпатическими волокнами гипогастрального сплетения в тазовом сплетении и формируют кавернозные нервы, осуществляющие автономную иннервацию кавернозных тел. Они сопровождают внутреннюю половую артерию и попадают в кавернозные тела латерокаудально от верхушки предстательной железы.
Соматическая иннервация представлена конечной ветвью полового нерва - дорсальным нервом полового члена. Сенсорная афферентная иннервация проходит через задние корешки сакральных сегментов SII-SIV и далее - через переднелатеральные собственные пучки в головной мозг. Половой нерв имеет и эфферентные двигательные волокна, которые направлены к мышцам тазового дна: луковично-губчатым и седалищно-пещеристым мышцам. Во время эрекции мышцы сдавливают луковицу, пещеристые тела и дорсальную вену полового члена, способствуя повышению интракавернозного давления.
Физиология эpекции. Эрекция полового члена происходит под влиянием центральной и периферической нервной системы и состоит из трех основных гемодинамических компонентов: снижения интра-кавернозного сопротивления вследствие расслабления гладких мышц пещеристой ткани; усиления кровоснабжения кавернозных тел за счет расширения глубоких артерий полового члена и уменьшения оттока крови за счет сдавления венозных сплетений пещеристых тел между стенками расширяющихся лакунарных пространств и ригидной белочной оболочкой (веноокклюзивный механизм).
Различают пять фаз эрекции.
I. Латентная фаза. Удлинение тела полового члена, интракавер-нозное давление не изменяется, гемодинамическое сопротивление пещеристой ткани уменьшается.
II. Фаза тумесценции. Постепенное нарастание тумесценции и ригидности, связанное с повышением артериального притока, увеличением кавернозного объема и повышение интракорпорального давления.
III. Фаза эрекции. Половой член имеет максимальную длину, давление в пещеристых телах достигает значений на 10-20 мм рт. ст. ниже уровня систолического артериального давления и стабилизируется,
происходит снижение притока крови до базальных значений, объем полового члена не изменяется.
IV. Фаза ригидности. Полная тумесценция и ригидность. Интра-корпоральное давление может превышать систолическое артериальное давление за счет действия мышц мочеполовой диафрагмы. Минимальный артериальный приток крови, полная венозная окклюзия.
V. Фаза детумесценции. Потеря ригидности; объем полового члена и интракавернозное давление постепенно уменьшаются, артериальный приток и венозный отток достигают базальных значений, половой член возвращается во флаццидное состояние.
В отсутствие эрекции преобладает влияние симпатической иннервации, которая приводит к тоническому сокращению гладких мышц артерий и кавернозных тел и ограничивает кровоток в пещеристой ткани. Развитию латентной фазы предшествует центральная психогенная и/или сенсорная стимуляция кавернозных нервов, способствующая повышению парасимпатического и снижению симпатического влияний с последующим расслаблением гладкомышечных элементов пещеристой ткани и артерий полового члена. Это приводит к его удлинению, снижению интракавернозного давления и значительному усилению артериального кровоснабжения. Для фазы тумесценции характерны увеличение объема полового члена и постепенное уменьшение оттока крови из пещеристых тел за счет веноокклюзивного механизма. В фазе эрекции интракавернозное давление приближается к систолическому, при этом устанавливается гемодинамическое равновесие между постоянным артериальным притоком и минимальным венозным оттоком. Максимальная ригидность появляется при сокращении мышц тазового дна, во время которого давление внутри кавернозных тел может существенно превышать систолическое давление (фаза ригидности). Фаза детумесценции наступает после прекращения стимулирующего воздействия кавернозных нервов, при этом повышается тонус хелицино-вых артерий и происходит сокращение гладкой мускулатуры трабекул. Кровоток и интракавернозное давление снижаются до первоначальных значений, исчезает ригидность, уменьшается тумесценция.
Биохимические механизмы эpекции. Согласно современным представлениям, расслабление гладких мышц кавернозных тел, необходимое для появления эрекции полового члена, происходит преимущественно под влиянием неадренергического-нехолинергического механизма, медиатором которого является оксид азота. Он образуется из L-аргинина и выделяется преимущественно нейронами и клетками эндотелия в ответ на сексуальную стимуляцию. Оксид азота прони-
кает в гладкомышечные клетки и стимулирует гуанилатциклазу, под действием которой синтезируется блокирующий кальциевые каналы и вызывающий миорелаксацию внутриклеточный медиатор эрекции - циклический гуанозинмонофосфат.
Патофизиологические механизмы эpектильной дисфункции. Эректильная дисфункция может быть вызвана как психогенными причинами, так и сосудистыми, нейрогенными, гормональными или мио-генными нарушениями. Эти факторы оказывают независимое влияние и могут сочетаться в разнообразных комбинациях.
Психогенная эpектильная дисфункция. Психогенная сенсорная или ментальная стимуляция является мощным промотором эрекции. Противоположные реакции, особенно страх, волнение, а также эмоции, связанные с полученным ранее негативным сексуальным опытом, могут значительно нарушить эректильные механизмы. Первичная психогенная эректильная дисфункция в большинстве случаев обусловлена социальным положением пациентов или последствиями их воспитания. Вторичные нарушения обычно развиваются остро и часто вызваны определенной ситуацией в жизни или в отношениях с партнером. Нередко они сопровождаются другими сексуальными расстройствами.
Сосудистая эpектильная дисфункция. Полноценная эрекция развивается при высокой объемной скорости кровотока в кавернозных артериях и адекватной работе веноокклюзивного механизма. Соответственно, сосудистая эректильная дисфункция является следствием уменьшения артериального притока к пещеристой ткани и нарушения венозного оттока из кавернозных тел. Иедостаточное кровоснабжение - причина эректильной дисфункции примерно у 50-80 % пациентов. У большинства из них можно выявить один или несколько факторов риска развития эндотелиальной дисфункции - атеросклероз, артериальную гипертензию, сахарный диабет, нарушения обмена липидов, курение. При этом расстройства эрекции усиливаются постепенно и обычно не зависят от партнерских отношений. Значительно реже вас-кулогенная эректильная дисфункция является следствием перенесенной травмы промежности или хирургического вмешательства на органах таза. Клинически недостаточность артериального кровоснабжения характеризуется замедленной индукцией эрекции после назначения вазоактивных препаратов.
Иарушение работы веноокклюзивного механизма может быть обусловлено разнообразными причинами: врожденными изменениями венозного дренажа (наличием эктопических вен), морфологическими повреждениями гладкомышечных клеток кавернозных тел, приводя-
щими к стойкому снижению или утрате их способности к релаксации, функциональными изменениями активности гладкомышечных клеток кавернозных тел (нарушениями обмена нейротрансмиттеров или стимуляции рецепторов), морфологическими изменениями белочной оболочки (возрастными особенностями, последствиями болезни Пейрони, перелома полового члена и т. д.), патологическими анастомозами между кавернозным телом и головкой полового члена (губчатым телом).
Hейpогенная эpектильная дисфункция. Травматические повреждения спинного мозга, нейропатии и другие патологические состояния, сопровождающиеся нарушением проведения нервных импульсов к половому члену, могут привести к эректильной дисфункции.
Эндокринная эpектильная дисфункция. В настоящее время имеются убедительные доказательства значительной роли андрогенов в регуляции эрекции. Несмотря на то, что молекула тестостерона не относится к непосредственным медиаторам эрекции, тестостерон-зависимые механизмы обеспечивают метаболизм и нормальную работу гладких мышц кавернозных тел, кавернозных нервов и белочной оболочки. В связи с этим снижение уровня тестостерона в крови проявляется не только ослаблением либидо, но и другими копулятивными расстройствами. Наиболее распространен возрастной андрогенный дефицит, обусловленный постепенным снижением выработки тестостерона у мужчин старше 30 лет. Копулятивные расстройства при гипогонадизме обычно успешно корригируют заместительной гормональной терапией.
Эpектильная дисфункция, вызванная лекарственными пpепаpатами. Различные медикаментозные средства могут играть существенную роль в патогенезе эректильной дисфункции. Наиболее отчетливо прослеживается эффект лекарственных препаратов, действующих на центральную и периферическую нервную систему, а также влияющих на гипоталамо-гипофизарно-гонадную ось. О возможном развитии копулятивных расстройств следует предупреждать пациентов, которым планируется проводить терапию центральными и периферическими α- и β-адреноблокаторами, психотропными средствами - транквилизаторами и антидепрессантами, а также И2-блокаторами.
Диагностика эpектильной дисфункции. Принято выделять основные (сбор анамнеза, объективное обследование, лабораторная диагностика) и специальные методы диагностики эректильной дисфункции. В подавляющем большинстве случаев представление о наиболее вероятном патофизиологическом механизме развития эректильной дисфункции можно получить при помощи основных методов исследования. Специальные методы требуются в сложных случаях, при желании
пациента установить этиологию заболевания, а также при необходимости документального подтверждения дисфункции при выборе пациентом инвазивных методов лечения.
Сбоp анамнеза. Тщательный сбор анамнеза в большинстве случаев позволяет установить природу эректильной дисфункции. Особое внимание следует обратить на выявление специфических факторов риска развития эректильной дисфункции - поражения сосудов (артериальная гипертензия, сахарный диабет, атеросклероз, курение), гормонального дисбаланса (гипогонадизм), нейрогенных расстройств (рассеянный склероз, травмы спинного мозга), урологических заболеваний (болезнь Пейрони, простатит, приапизм в анамнезе, расстройства мочеиспускания), ранее перенесенных хирургических вмешательств на половых органах или органах таза, курения, пристрастия к алкоголю и наркотическим средствам и медикаментозной терапии, способствующей нарушению эректильной функции. Кроме того, важно собрать семейно-бытовой анамнез, уточнить социальный статус больного и характер его взаимоотношений с партнером, а также оценить психологическое состояние пациента и ознакомиться с результатами предыдущих обследований и лечебных мероприятий в связи с копулятивными расстройствами.
На этапе сбора анамнеза необходимо провести дифференциальную диагностику сексуальных расстройств; эректильную дисфункцию следует отличать от снижения либидо, нарушения эякуляции или оргазма. При этом существенную помощь может оказать методика анкетирования вопросниками МИЭФ (Международный индекс эректильной функции), AMS (Симптомы старения мужчины), ADAM (Возрастной андрогенный дефицит у мужчин), IPSS (Международная шкала симптомов предстательной железы).
Объективное обследование. При проведении объективного обследования обращают особое внимание на развитие вторичных половых признаков и наружных половых органов. Аномальное распределение волосяного покрова и подкожной жировой клетчатки, а также небольшие размеры яичек являются признаками андрогенной недостаточности. При пальпации полового члена можно выявить уплотнения, характерные для болезни Пейрони. Измерение артериального давления и оценка пульсации периферических артерий стоп позволяют определить системные нарушения артериального кровоснабжения. Иа неврологическую причину эректильной дисфункции могут указывать изменения чувствительности половых органов и перианальной области, снижение тонуса анального сфинктера или ослабление бульбокавернозного рефлекса.
Лабоpатоpная диагностика. При подозрении на эндокринную природу эректильной дисфункции показано определение уровня тестостерона и, в некоторых случаях, пролактина, ЛГ, эстрадиола и белка, связывающий половой гормон. При подозрении на нарушение обмена липидов и сахарный диабет требуется проведение контрольных анализов состояния метаболизма с последующей коррекцией. Исследование функции печени проводят больным, злоупотребляющим алкоголем, это особенно важно в тех случаях, когда планируется интракавернозная терапия папаверином.
Специальные методы
Интpакавеpнозный тест с вазоактивными пpепаpатами. В настоящее время в диагностике эректильной дисфункции интракавернозное введение вазоактивных препаратов применяют редко. В основе действия этого метода лежит принудительное фармакологически индуцированное расслабление гладких мышц кавернозных тел и пенильных артерий. Обычно с этой целью используют папаверин в комбинации с фентоламином или простагландин Е1 При этом у здоровых мужчин усиливается приток артериальной крови и развивается эрекция. У больных с эректильной дисфункцией интракавернозный тест позволяет оценить функциональные характеристики кавернозной ткани, а также сохранность адекватного артериального притока и эффективность работы веноокклюзивного механизма. Быстрое развитие ригидной эрекции в ответ на введение небольших доз вазоактив-ных препаратов позволяет сделать предположение о нейрогенной или психогенной причине развития эректильной дисфункции, медленное развитие эрекции свидетельствует о слабом артериальном притоке, а быстрый спад кровенаполнения - о недостаточности веноокклюзив-ного механизма.
Результат интракавернозного теста определяют через 15 мин в вертикальном положении пациента. В большинстве случаев для его оценки пользуются следующей шкалой:
Э0 - нет видимой реакции;
Э1 - легкая тумесценция, нет ригидности;
Э2 - средняя тумесценция, нет ригидности;
Э3 - полная тумесценция, нет ригидности;
Э4 - полная тумесценция, средняя ригидность (достаточная для проведения полового акта);
Э5 - полная тумесценция, полная ригидность.
Дуплексное сканирование. Дуплексное сканирование (допплерогра-фия + УЗИ) - один из наиболее информативных методов диагностики. Оно позволяет произвести анализ структуры кавернозных тел, визуализировать сосуды полового члена и в сочетании с интракавернозным тестом дает возможность количественно оценить скорость пенильного артериального кровотока и эффективность работы веноокклюзивного механизма.
Пенильная ангиография. В недалеком прошлом пенильная артерио-графия в сочетании с введением вазоактивных препаратов считалась «золотым стандартом» диагностики эректильной дисфункции, однако в настоящее время она уступила место менее инвазивному и более информативному тесту - дуплексному сканированию. Артериография применяется в основном у больных с посттравматической эректильной дисфункцией перед реконструктивными операциями для визуализации внутренней половой и нижней эпигастральной артерий, которые используют для формирования анастомозов с сосудами полового члена.
Оценка веноокклюзивного механизма. Для оценки эффективности веноокклюзивного механизма применяют две взаимодополняющие методики - кавернозометрию и кавернозографию. Во время каверно-зометрии измеряют внутрикавернозное давление в условиях искусственной эрекции, полученной путем инфузии в пещеристые тела изотонического раствора натрия хлорида с заданной постояной скоростью. Если давление быстро спадает или если для появления ригидности потребовалась повышенная скорость притока, то следует заподозрить венозную утечку. В этом случае введение контрастного вещества в кавернозные тела (кавернозография) позволяет выявить локализацию патологических дренирующих вен.
Регистpация тумесценции и pигидности полового члена в ночное вpемя. У здоровых мужчин во время сна развивается от трех до пяти эпизодов эрекции (так называемые ночные эрекции). Истинная их природа неясна, они соответствуют фазам быстрых движений глаз, продолжаются в течение 20-30 мин и, вероятно, способствуют поддержанию нормального метаболизма в кавернозной ткани. Считается, что психогенная эректильная дисфункция не оказывает влияния на ночные эрекции, поэтому регистрация ночной тумесценции и ригидности полового члена может использоваться для дифференциальной диагностики. Наличие ночных эрекций можно установить при помощи теста почтовых марок и специальных приспособлений, однако, наиболее полную информацию дают приборы, оценивающие размеры и ригидность полового члена в режиме постоянного мониторирования.
Лечение. Иа основании анализа жалоб, анамнеза, результатов обследования больного врач должен получить представление о ведущем механизме нарушения эрекции и совместно с пациентом обсудить возможные варианты лечения. В настоящее время при эректильной дисфункции применяют:
- консеpвативное лечение: психотерапию, гормональную терапию, пероральную терапию, терапию с применением аппаратов, создающих локальное отрицательное давление;
- минимально инвазивное лечение - интрауретральную терапию и интракавернозные инъекции;
- опеpативное лечение - реваскуляризирующие вмешательства на половом члене, операции, направленные на усиление сопротивления венозному оттоку, вмешательства, позволяющие корригировать форму полового члена, и протезирование полового члена.
В соответствии с принципом целенаправленного подхода при беседе с пациентами обсуждают все методы коррекции имеющихся нарушений и необходимый для их реализации объем обследования.
Иередко эректильная дисфункция является следствием других, ранее не диагностированных заболеваний. В этих случаях лечение основного заболевания может сопровождаться улучшением эректильной функции. В соответствии с современными представлениями любой больной, обратившийся с жалобами на эректильную дисфункцию, должен быть направлен к врачу общей практики для оценки состояния здоровья, выявления и коррекции соматических заболеваний, которые могут быть причиной копулятивных расстройств. Это особенно важно для мужчин с признаками артериальной эректильной дисфункции, являющейся фактором риска развития острого инфаркта миокарда и нарушения мозгового кровообращения. Нередко своевременная коррекция сопутствующих заболеваний способствует нормализации копулятивной функции, а при нарушениях, обусловленных действием лекарственных средств, удается произвести замену на препарат с аналогичным эффектом без ущерба для качества эрекции. Кроме того, необходимо стремиться уменьшить влияние факторов риска развития эректиль-ной дисфункции - курения, злоупотребления алкоголем, избыточной массы тела, недостаточной физической активности.
Психотеpапия. Этот метод эффективен у больных с психогенной эректильной дисфункцией, причиной которой могут быть стрессовые ситуации, конфликты, депрессии, проблемы общения партнеров, недостаток сексуального опыта или чувство неловкости в интимной обстановке. Психотерапия требует участия обоих партнеров и заключается
в формировании новой системы их сексуальных взаимоотношений. В основном лечение направлено на снижение волнения, связанного с сексуальными действиями, и способствует избавлению от страха неудачной попытки полового акта. Следует отметить, что подходы к подобной сексуальной дисфункции сложно стандартизировать, так как степень и характер обеспокоенности индивидуальны у каждого пациента.
Γоpмональная теpапия при эректильной дисфункции носит преимущественно заместительный характер и применяется в основном у пациентов пожилого возраста со снижением полового влечения и ослаблением эрекции вследствие выраженной андрогенной недостаточности. Лечение направлено на сохранение полового поведения и вторичных половых признаков и требует поддержания физиологических концентраций гормона и его активных метаболитов в сыворотке крови. В настоящее время появились лекарственные препараты в форме геля и пластыря для накожного применения, а также депо-препараты для внутримышечного введения, позволяющие осуществлять заместительную гормональную терапию с поддержанием уровня тестостерона в пределах границ физиологически нормальных значений. Теоретически терапия андрогенами может способствовать опухолевой прогрессии при раке предстательной железы, поэтому до начала лечения следует проводить соответствующее обследование пациента, а в ходе лечения - динамическое наблюдение.
Пеpоpальная теpаnия. Наиболее эффективные препараты для перо-рального приема - ингибиторы фосфодиэстразы-5: силденафил, варде-нафил, тадалафил. Они способствуют усилению расслабления гладких мышц кавернозных тел и артерий полового члена, так как тормозят внутри клетки распад активного циклического гуанозинмонофосфата. Препараты быстро всасываются, поэтому рекомендуется принимать их за небольшой промежуток времени до предполагаемой половой активности. Без соответствующей сексуальной стимуляции препарат не приводит к появлению эрекции, так как он лишь усиливает эффект действия основных медиаторов - оксида азота и циклического гуано-зинмонофосфата. В настоящее время ингибиторы фосфодиэстразы-5 успешно используют подавляющее большинство больных с эректильной дисфункцией. В зависимости от этиологии дисфункции эффективность этих препаратов варьирует от 40 до 80 %, при этом частота побочных эффектов невелика, обычно они выражены слабо и быстро проходят. К ним относят головную боль, «приливы» к голове, диспепсию, повышенную чувствительность к свету и изменение цветоощущения.
Вакуумный эpектоp. Принцип действия вакуумного эректора - создание локального отрицательного давления в области полового члена, способствующего пассивному притоку крови к кавернозным телам. Этот аппарат представляет собой прозрачную пластмассовую или стеклянную камеру, которую надевают на половой член и плотно прижимают к поверхности кожи у его основания для создания герметичного пространства. Камера соединена с насосом, работа которого приводит к уменьшению давления внутри камеры и притоку крови к половому члену. После появления достаточного увеличения и уплотнения пещеристых тел процедуру прекращают, на половой член надевают специальное констрикторное кольцо, позволяющее сохранить кровенаполнение в течение полового акта. К преимуществам вакуумных эректоров относят малую инвазивность и возможность применения вне зависимости от этиологии эректильной дисфункции, к недостаткам - необходимость выполнять определенные манипуляции с аппаратом перед половым актом и дискомфорт, связанный с давлением констрикторного кольца.
Тpансуpетpальная терапия. В конце 1990-х гг. для лечения больных с эректильной дисфункцией было сконструировано устройство, позволяющее производить трансуретральное введение медикаментозных средств для достижения эрекции - MUSE (Medicated Urethral System for Erection). Оно дает возможность вводить препарат в просвет мочеиспускательного канала на глубину около 3 см от наружного отверстия. Перед применением MUSE пациент должен помочиться, а непосредственно после введения препарата - слегка помассировать уретру в течение нескольких минут. В настоящее время применяется трансуретральное введение альпростадила - синтетического аналога медиатора эрекции простагландина Е1. Альпростадил быстро проходит через эпителий мочеиспускательного канала, попадает в спонгиозное тело и через анастомозы достигает кавернозных тел. При этом он стимулирует аденилат-циклазу, что приводит к появлению циклического аденозинмонофосфа-та и способствует расслаблению гладкой мускулатуры кавернозных тел и артерий полового члена. В отличие от силденафила, местное действие препарата вне зависимости от сексуальной стимуляции способствует эрекции. Примерно 30 % пациентов, применяющих MUSE, отмечают боль в мочеиспускательном канале; уретроррагия встречается в 5 %, снижение артериального давления - в 2-8 % случаев.
Интpакавеpнозная теpаnuя. До появления силденафила в 1998 г. наиболее эффективным нехирургическим методом лечения эректиль-ной дисфункции считали интракавернозную терапию вазоактивными
препаратами. Этот способ широко применяется с 1982 г., к его преимуществам относят высокую эффективность, отсутствие системных побочных эффектов и сравнительно низкий риск местных осложнений. Иаиболее грозное осложнение интракавернозных инъекций - приапизм. Частота его развития зависит от вида и дозы вводимого препарата. Кроме того, при многолетнем применении у ряда больных появляются фиброзные изменения белочной оболочки, которые могут усугубить эректильную дисфункцию и сопровождаться искривлением полового члена во время эрекции.
В настоящее время фармацевтическая промышленность производит несколько средств для интракавернозной терапии. Наибольшую популярность в нашей стране завоевал препарат альпростадил. Он представляет собой простагландин Е1 - естественный медиатор эрекции, циклический эндопероксид, конечный продукт метаболизма арахидоновой кислоты. Впервые он был выделен в 1935 г., а в 1989 г. - синтезирован и предложен для лечения больных с эректильной дисфункцией. Взаимодействие альпростадила с протеином G способствует активизации аденилатциклазы, приводит к увеличению содержания активного циклического аденозинмонофосфата и расслаблению гладкомышечных клеток кавернозных тел и артерий полового члена.
Хupуpгuческое лечение. Несмотря на то что пероральная терапия, вакуумные эректоры и интракавернозная терапия в большинстве случаев позволяют ликвидировать эректильную дисфункцию, некоторые пациенты выбирают хирургическое лечение, так как предпочитают состояние, при котором появление эрекции не требует дополнительных подготовительных мероприятий. Кроме того, у ряда больных с нарушениями артериального и венозного кровообращения или выраженным фиброзом кавернозных тел консервативное лечение оказывается неэффективным.
Имплантация пенильного протеза. Протезы полового члена бывают полужесткими (гибкими и механическими) и гидравлическими (1-, 2- и 3-компонентными). После введения в кавернозные тела они обеспечивают ригидность и длину полового члена, достаточную для проведения полового акта. Полужесткие протезы состоят из двух стержней или цилиндров, которые содержат центральную плетеную гибкую металлическую проволоку, позволяющую поднимать и опускать протез, а также сохранять заданную кривизну. Механические модификации включают специальные шарниры для повышения гибкости и надежности фиксации в необходимом положении. Во время операции дорсальным субвенечным или пеноскротальным доступом вскрывают и в соответствии
с размерами протезов дилатируют кавернозные тела, имплантируют протезы и ушивают операционную рану.
Основное преимущество гuдpавлuческuх протезов - способность имитировать не только ригидность полового члена, но и состояние детумесценции. Однокомпонентный протез по внешнему виду соответствует полужесткому протезу, однако внутри он содержит гидравлическую систему, состоящую из надувной камеры, помпы и резервуара. При сдавлении дистального участка цилиндра, прилежащего к головке полового члена, из проксимального резервуара в цилиндр поступает изотонический раствор натрия хлорида, обеспечивающий необходимую ригидность. После окончания полового акта пациент сгибает половой член, при этом в механизме помпы открывается клапан, раствор перетекает обратно в резервуар, и протез возвращается в исходное положение. Однокомпонентные протезы имплантируют аналогично полужестким протезам.
Двухкомпонентные протезы состоят из двух полых цилиндров и помпы-резервуара. По сравнению с однокомпонентными протезами они содержат больший объем жидкости, а следовательно, лучше обеспечивают ригидность при половом акте и флаццидность (детумесцен-цию) в неактивном состоянии.
Трехкомпонентный протез является наиболее сложным, но в то же время наиболее совершенным устройством. Во время имплантации два полых цилиндра вводят внутрь кавернозных тел и соединяют с небольшой надувной помпой, расположенной в мошонке латеральнее яичка. Помпа позволяет производить наполнение и опорожнение цилиндров, аналогично фазам эрекции и детумесценции. Изотонический раствор натрия хлорида поступает в цилиндры из резервуара, размещенного в надлобковой области позади прямых мышц живота. Значительный объем жидкости внутри гидравлической системы протеза позволяет получить артифициальные ригидность и флаццидность, близкие к естественным, что облегчает адаптацию пациентов и способствует улучшению качества их жизни.
Иесмотря на то что частота послеоперационных осложнений в течение последних 10 лет существенно снизилась, после имплантации протезов любого типа может возникнуть неисправность, связанная с их конструктивными особенностями. Полужесткие протезы могут потерять способность сохранять заданную форму из-за перелома металлического стержня. Иеисправности гидравлических протезов происходят чаще, они, в основном, связаны с нарушением их герметичности. Во всех случаях нарушение функции протеза требует хирургического
вмешательства и замещения поврежденной части. Другое возможное осложнение - инфицирование протеза, которое развивается у 3-5 % пациентов (чаще всего с аутоиммунными заболеваниями, сахарным диабетом, а также оперированных по поводу повреждения протезов). При инфицировании протез удаляют, производят заживление раны и затем выполняют повторное протезирование. К другим, более редким осложнениям относят боли в половом члене, уменьшение его длины и снижение чувствительности.
Лигирование вен венозной недостаточности. Этот метод лечения в настоящее время в основном применяют при врожденных аномалиях вен полового члена, которые приводят к недостаточности веноокклю-зивного механизма. Пациенты обычно жалуются на малую продолжительность ригидной фазы эрекции. Диагноз можно поставить при кавернозографии и кавернозометрии, а хирургическое лечение заключается в прекращении патологической венозной утечки путем пликации ножек полового члена, эксцизии или лигирования глубокой дорсальной вены. Результаты операций при эректильной дисфункции, вызванной венозной недостаточностью, в целом, неудовлетворительные, успех достигается менее чем у 40 % пациентов, часто развиваются рецидивы. Послеоперационные осложнения включают укорочение полового члена и снижение его чувствительности, а также инфицирование раны.
Реваскуляpuзацuя при аpтеpuальной недостаточности. Восста-
новление артериального кровотока в половом члене в настоящее время, в основном, применяют после травматических повреждений тазовых артерий у молодых мужчин без сопутствующих сосудистых заболеваний. Диагноз следует подтвердить при селективной ангиографии, которая также позволяет визуализировать нижнюю эпигастральную артерию. В ходе операции выполняют ее мобилизацию и накладывают анастомоз с дорсальной пенальной артерией по типу конец в конец или конец в бок с дистальным лигированием. Иесмотря на то, что эта операция редко сопровождается осложнениями, в области анастомоза может образоваться тромб, а избыточный артериальный кровоток у ряда больных вызывает приапизм и гиперемию головки полового члена. При правильном определении показаний результаты реваскуляризации удовлетворительные, однако после операции до 65 % пациентов могут испытывать эректильную дисфункцию различной степени.
При врожденном искривлении полового члена, а также при изменении его формы вследствие травмы или фибропластической индурации (болезнь Пейрони) также может возникнуть потребность в оперативной коррекции. При этом используют методики гофрирования или иссече-
ния белочной оболочки со стороны, противоположной направлению изгиба полового члена, или иссекают измененный участок с последующим закрытием дефекта методом лоскутной пластики.
Эмиссия - это предшествующее семяизвержению физиологическое явление, во время которого закрывается шейка мочевого пузыря и в мочеиспускательный канал выделяется секрет парауретральных желез, предстательной железы, семенных пузырьков и содержимого ампул семявыносящих протоков. Эфферентный контроль эмиссии обеспечивается симпатической нервной системой (Th10-L5). Нарушения эмиссии могут наблюдаться у больных, перенесших симпатэктомию, а также при приеме лекарственных средств, снижающих тонус гладкомышеч-ных структур шейки мочевого пузыря.
Эякуляция (семяизвержение) и оргазм - это сложные феномены, заключающиеся в ритмичных сокращениях мышц тазового дна, при которых происходит выброс семенной жидкости из наружного отверстия мочеиспускательного канала, что сопровождается чувством глубокого удовлетворения. Физиологические механизмы контроля семяизвержения действуют через симпатическую нервную систему и соматические нервы и приводят к закрытию шейки мочевого пузыря, ритмичным расслаблениям наружного сфинктера в сочетании с активизацией поперечнополосатой мускулатуры тазового дна.
Принято выделять преждевременную эякуляцию, замедленную эякуляцию и анэякуляцию, ретроградную эякуляцию и болезненную эякуляцию.
Преждевременное семяизвержение - это отсутствие способности мужчины задерживать момент семяизвержения для собственного удовлетворения и удовлетворения партнерши. Чаще всего оно имеет психогенную природу и преимущественно наблюдается у молодых мужчин, еще не научившихся контролировать быстроту наступления эякуляции. Кроме того, это состояние может быть следствием высокой скорости срабатывания эякуляторного рефлекса, которое, в частности, наблюдается у мужчин с повышенной чувствительностью полового члена. Преждевременное семяизвержение часто приводит к развитию эректильной дисфункции.
В тех случаях, когда у мужчин появляются затруднения в завершении полового акта семяизвержением, говорят о задержке эякуляции, а при ее полном отсутствии - об анэякуляции. Чаще всего причинами этих патологических состояний являются различные заболевания, при которых нарушается образование компонентов семенной жидкости или их накопление в простатическом отделе мочеиспускательного канала при половом акте. К ним относятся сахарный диабет, нейрогенные расстройства,
травма спинного мозга, аномалии развития. Иногда расстройства семяизвержения наступают вследствие повреждения нервных волокон после хирургических вмешательств в тазовой области. Нередко при первичной анэякуляции у мужчин сохранена эрекция, что позволяет им вести половую жизнь, а причиной обращения является бесплодие в браке.
Болезненная эякуляция, как правило, указывает на наличие воспалительного процесса в предстательной железе, семенных пузырьках или в мочеиспускательном канале, при этом соответствующее обследование позволяет выявить причину воспаления и ликвидировать ее.
Таким образом, в настоящее время фундаментальные исследования особенностей анатомического строения полового члена, физиологических механизмов эрекции и биохимических реакций в кавернозной ткани, а также совершенствование оперативной техники и развитие медицинской промышленности позволяют применять разнообразные подходы к лечению больных с копулятивными расстройствами и в большинстве случаев восстановить утраченную функцию. Представление о многофакторности и многогранности этой проблемы требует междисциплинарного подхода и динамического наблюдения.
16.8. ПРИАПИЗМ
Под приапизмом понимают немотивированное переполнение кавернозных тел кровью, сопровождающееся резким увеличением полового члена, болезненной и непрерывающейся эрекцией. В генезе этого неотложного патологического состояния - нарушение кровоснабжения кавернозных тел, проявляющееся венозным стазом вследствие сдавливания вен, развитием тромбоза с последующим фибринолизом и пропитыванием кавернозных лакун массами фибрина.
Этиология и патогенез. В большинстве наблюдений отмечается идиопатический приапизм, которому нередко предшествует длительное половое возбуждение, в прочих случаях этот фактор этиологической роли не играет. Приапизм может возникать на фоне системных гематологических заболеваний (лейкозы, серповидно-клеточная анемия), опухолей и хронических инфекционных заболеваний органов малого таза, после травмы полового члена или спинного мозга, а также при применении некоторых лекарственных средств. В последние годы при-апизм в основном наблюдается как осложнение интракавернозных инъекций у больных с импотенцией.
Главную роль в патогенезе приапизма играет дисбаланс кровообращения в кавернозных телах, заключающийся в нарушении венозного
оттока при активном артериальном притоке. В кавернозных телах полового члена развивается застой крови, нарушается газообмен, возникают отек и ишемия кавернозной ткани. Тромбоз кавернозных тел, сопровождающийся образованием фибрина, в течение 3 суток сменяется лизисом фибрина и склерозированием кавернозной ткани с последующей утратой эректильной функции.
Гипоксия кавернозной ткани в сочетании с инфекционными факторами способствует возникновению кавернита, а в тяжелых случаях приводит к гнойному каверниту и гангрене полового члена. Эти осложнения всегда заканчиваются утратой функции органа, иногда потерей самого органа, а в некоторых случаях могут привести к смерти больного.
Диагностика не вызывает трудностей и основывается на факте наличия болезненно эрегированного полового члена. При этом кавернозные тела резко напряжены, а головка полового члена остается ненапряженной.
Дифференциальная диагностика приапизма и кавернита базируется на выявлении общих и местных признаков воспаления. Иногда для уточнения диагноза выполняют пункцию кавернозных тел. При приапизме после пункции сначала отделяется темная, а в последующем, в процессе промывания кавернозных тел изотоническим раствором натрия хлорида с добавлением гепарина, - светлая (артериальная) кровь. При каверните, за исключением гнойных форм, весь кавернозный объем выполнен инфильтрированной кавернозной тканью, поэтому отделяемого не наблюдается. При гнойном каверните после пункции иглой Дюфо отмечается гнойное отделяемое. Гангрена полового члена характеризуется наличием поверхностных и глубоких участков некроза. На начальных стадиях заболевания головка имеет малиновый или фиолетовый цвет, отмечается отторжение некротизи-рованных поверхностных пластов спонгиозной ткани. В последующем головка приобретает черный цвет, жизнеспособными остаются только отдельные участки кожи полового члена.
Лечение приапизма начинают с консервативных мероприятий, включающих эпидуральную анестезию, локальную гипотермию, пункцию кавернозных тел, аспирацию крови и промывание их растворами адреналина и гепарина. Толстоигольная пункция наиболее эффективна при вызванном фармакологическими средствами приапизме давностью до 1 суток. Дополнительно назначают противовоспалительные, обезболивающие препараты, антибиотики, средства, улучшающие реологические свойства крови, - декстран (реополиглюкин) и микроциркуляцию - пентоксифиллин (трентал). При неэффективности консервативных
мероприятий или возникновении рецидива приапизма выполняют экстренную операцию, принцип которой заключается в создании адекватного венозного оттока из кавернозных тел через спонгиозное тело (баланокавернозный, спонгиокавернозный анастомоз либо через большую подкожную вену бедра (сафенокавернозный анастомоз). В последнем случае подкожная вена ноги после ее отсечения в средней трети, разворота и подведения к половому члену анастомозируется конец в бок с кавернозным телом с той же стороны. Отток осуществляется в бедренную вену.
Прогноз в отношении эректильной функции зависит от своевременности и адекватности лечебных мероприятий. При каверните выполняется широкое дренирование кавернозных тел с оставлением в их просвете трубчатых силиконовых дренажей для оттока экссудата или гноя и орошения растворами антибиотиков. Мочу отводят с помощью троакарной цистостомии. При гангрене полового члена производят ампутацию или экстирпацию полового члена. Отведение мочи с помощью цистостомии обязательно. В послеоперационном периоде необходима антибактериальная и дезинтоксикационная терапия. Сексуальная реабилитация в последующем возможна только с помощью эндопротезирования полового члена. После органоуносящих вмешательств выполняют фаллопластику.
16.9. БОЛЕЗНЬ ПЕЙРОНИ
Болезнь Пейрони, или фибропластическая индурация полового члена, была впервые описана в 1561 г. Габриеле Фаллопием и названа в честь приближенного к королю Франсуа Луи XV хирурга Франсуа де ля Пейрони, которому удалось успешно провести лечение нескольких пациентов, жаловавшихся на боль и искривление полового члена при эрекции.
Этиология и патогенез этого заболевания ясны не до конца. По мнению большинства исследователей, его пусковым механизмом является незначительная травма, которая приводит к формированию гематомы в пределах белочной оболочки, окружающих кавернозные тела. В зоне повреждения происходит активация репаративных процессов по типу фиброзирования с участием фибробластов и медиаторов воспаления, нередко сопровождающаяся болезненными ощущениями и приводящая к частичной или полной утрате эластичности фрагмента белочной оболочки и искривлению полового члена при эрекции.
Высокая частота сочетания болезни Пейрони с коллагенозами (контрактурой Дюпюитрена, склеродермией, келоидозом, плечелопаточным
периартритом, дерматомиозитом, фиброзными утолщениями на пальцевых фалангах и др.) позволяет отнести ее к этой группе заболеваний. Более высокое содержание тропоэластина и α-эластина в организме пораженных мужчин предполагает наличие аутоиммунных механизмов развития этой болезни.
Клинические признаки. Поводом для обращения к врачу обычно служат искривление полового члена, которое может препятствовать проведению полового акта, а также уплотнение в половом члене и болезненные ощущения при эрекции. Боль обычно является ранним признаком заболевания. Формирование фиброзной бляшки происходит постепенно в течение 12-18 месяцев, за это время степень кривизны полового члена может изменяться. В большинстве случаев бляшки располагаются под дорсальным пучком, реже - на уретральной или латеральной поверхности или на межкавернозной перегородке. Они никогда не поражают спонгиозное тело и уретру и не мешают мочеиспусканию, а также не изъязвляются и не озло-качествляются, однако со временем могут стать очень плотными - при гистологическом исследовании в них обнаруживают хрящевые участки и зоны кальцификации. На поздних этапах развития болезни может наблюдаться отсутствие тумесценции дистальнее зоны поражения, обусловленное локальной несостоятельностью веноокклю-зивного механизма.
Для постановки диагноза обычно достаточно изучить жалобы, собрать анамнез и произвести объективное обследование больного. Фиброзные бляшки легко определяются при пальпации полового члена в виде отдельно расположенных или сливающихся в виде хорды образований хрящевидной плотности, не связанных с кожей. Исследование полового члена при эрекции позволяет оценить степень искривления и ригидности кавернозных тел. Размеры бляшек более точно можно измерить при УЗИ, при котором они представлены в виде гиперэхоген-ных образований с акустическими тенями, обзорная рентгенография и КТ полового члена дают возможность выявить обызвествленные участки фибропластической индурации белочной оболочки.
Лечение пациентов с болезнью Пейрони - трудная и не до конца решенная задача. Отсутствие четких представлений об этиологии и патогенезе этого заболевания не позволяет разработать эффективную тактику ведения больных. Не нуждаются в лечении мужчины при отсутствии жалоб и признаков прогрессирования заболевания. Консервативное лечение применяют на ранних этапах развития болезни для уменьшения выраженности боли и предотвращения дальнейшего
фиброзного перерождения белочной оболочки. Для этого используют витамин Е, тамоксифен, электрофорез с лидазой и кортикостероидны-ми гормонами и т. д., однако улучшение наблюдают лишь у 30-60 % пациентов. Большинство авторов не рекомендуют введение препаратов непосредственно в бляшки, так как инъекционная микротравма может оказаться фактором, усугубляющим степень индурации. В последние годы появились сообщения об уменьшении искривления полового члена после применении ДУВЛ.
Показания к оперативному лечению - наличие деформации, препятствующей проведению полового акта, а также развитие эректильной дисфункции. При сохранной эрекции деформацию полового члена устраняют с помощью реконструктивных оперативных вмешательств. Иссекают бляшку и замещают ее лоскутом (кожным, фасциальным; участком белочной оболочки, вены и др.) или, не удаляя бляшку, укорачивают белочную оболочку с противоположной стороны за счет иссечения ее фрагмента или наложения гофрирующих швов.
При развитии эректильной дисфункции у пациентов с болезнью Пейрони можно выполнить эндокавернозное протезирование, в ходе которого обычно также производят осторожное рассечение фиброзной бляшки для уменьшения последующего напряжения белочной оболочки полового члена.
Контрольные вопросы
1. Как следует обследовать и лечить больного, страдающего энурезом?
2. Что такое стрессовое недержание мочи? Как диагностировать и как лечить данное патологическое состояние?
3. Как поставить диагноз больному с гиперактивностью мочевого пузыря?
4. С какими болезнями следует дифференцировать водянку оболочек яичка?
5. Как поставить диагноз больному с инородным телом мочевого пузыря, уретры? В чем состоит лечение?
6. Какие формы мужского бесплодия вам известны?
7. Какие нарушения сперматогенеза могут быть выявлены по результатам спермограммы?
8. Какие формы половых расстройств у мужчин вы знаете? В чем заключается их коррекция?
9. Как оказать помощь больному с приапизмом?
10. Что такое болезнь Пейрони? Как поставить диагноз и как лечить больного?