Нейрохирургия: учебник. - 2-е изд., перераб. и доп. -С.В. Можаев, А.А. Скоромец, Т.А. Скоромец. 2009. - 480 с. : ил.
|
|
|
|
ГЛАВА 7. СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ ГОЛОВНОГО И СПИННОГО МОЗГА
СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ ГОЛОВНОГО МОЗГА
Эпидемиология
Сосудистые поражения головного мозга - одна из наиболее актуальных проблем здравоохранения. В большинстве индустриально развитых стран на сосудистые заболевания мозга приходится 12,5-14% общей смертности. Летальность от инсультов в США и России стоит на третьем месте в статистике общей смертности, в Германии - на втором, в Японии - на первом. В этих странах смертность от мозговых инсультов превышает таковую от инфаркта миокарда в 2-3 раза. Чаще умирают в остром периоде инсульта (до 50% больных). Трудоспособными остаются лишь 20% работавших до инсульта. Эта неутешительная статистика обусловлена особенностями кровоснабжения головного мозга и его метаболизма. Мозг потребляет и не способен создавать резервы, депонировать питательные вещества и нуждается в постоянной их доставке. Известно, что у здоровых людей через 100 г мозгового вещества за 1 мин протекает в среднем 54 мл крови, а общий объём церебрального кровообращения в минуту составляет 700-1000 мл крови. Мозг расходует 3,3 мл кислорода и 5,4 мг глюкозы на 100 г своего веса - это в 5 раз больше, чем миокард, и в 20 раз больше, чем скелетная мышца. На мозг приходится 20% всей потребности в кислороде.
Анатомия сосудов головного мозга
Головной мозг получает кровоснабжение из двух внутренних сонных артерий, которые отходят от общих сонных артерий, и двух позвоночных артерий, берущих начало от подключичных артерий.
Внутренние сонные артерии проникают в полость черепа через каналы сонных артерий, проходят через пещеристые пазухи, где они делают крутой изгиб (внутренний сифон), и на основании черепа у наружного угла зрительного перекрёста (хиазмы) делятся на пере-
дние мозговые и средние мозговые артерии (рис. 7-1, 7-2). Передние мозговые артерии анастомозируют между собой с помощью передней соединительной артерии. После входа в полость черепа от каждой
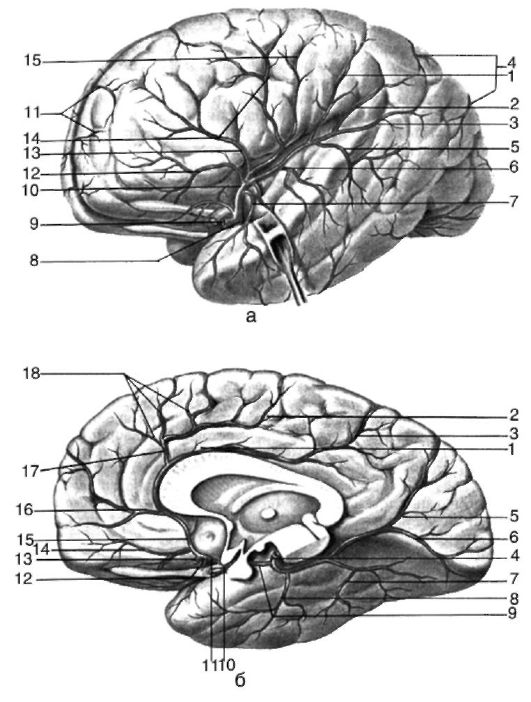 Рис. 7-1. Артерия наружной и внутренней поверхности полушарий большого мозга: а -
наружная поверхность: 1 - левая средняя мозговая артерия; 2 - конечная
ветвь передней мозговой артерии; 3 - латеральная глазничнолобная ветвь
средней мозговой артерии; 4 - левая передняя мозговая артерия; 5 -
лобная ветвь средней мозговой артерии; 6 - артерия прецентральной
извилины; 7 - артерия центральной борозды; 8 - передняя теменная артерия
(ветвь средней мозговой артерии); 9 - задняя теменная артерия (ветвь
средней мозговой артерии); 10 - артерия угловой извилины (ветвь средней
мозговой артерии); 11 - передняя височная артерия (ветвь средней
мозговой артерии); 12 - конечная часть задней мозговой артерии; 13 -
задняя височная артерия (ветвь средней мозговой артерии); 14 -
промежуточная височная артерия (ветвь средней мозговой артерии); 15 -
внутренняя сонная артерия; б - внутренняя поверхность: 1 -
внутренняя сонная артерия; 2 - передняя височная ветвь задней мозговой
артерии; 3 - задняя соединительная артерия; 4 - передняя соединительная
артерия; 5 - левая передняя мозговая артерия; 6 - возвратная артерия
(ветвь передней мозговой артерии); 7 - глазничные ветви передней
мозговой артерии; 8 - правая передняя мозговая артерия; 9 - ветвь
передней мозговой артерии к полюсу лобной доли; 10 - мозолисто-краевая
артерия (ветвь передней мозговой артерии); 11 - медиальные лобные ветви
передней мозговой артерии; 12 - перикаллезная артерия (ветвь средней
мозговой артерии); 13 - парацентральная артерия (ветвь передней мозговой
артерии); 14 - предклинная артерия (ветвь передней мозговой артерии);
15 - правая центральная мозговая артерия; 16 - теменно-затылочная ветвь
задней мозговой артерии; 17 - шпорная ветвь задней мозговой артерии; 18 -
задняя височная ветвь задней мозговой артерии
Рис. 7-1. Артерия наружной и внутренней поверхности полушарий большого мозга: а -
наружная поверхность: 1 - левая средняя мозговая артерия; 2 - конечная
ветвь передней мозговой артерии; 3 - латеральная глазничнолобная ветвь
средней мозговой артерии; 4 - левая передняя мозговая артерия; 5 -
лобная ветвь средней мозговой артерии; 6 - артерия прецентральной
извилины; 7 - артерия центральной борозды; 8 - передняя теменная артерия
(ветвь средней мозговой артерии); 9 - задняя теменная артерия (ветвь
средней мозговой артерии); 10 - артерия угловой извилины (ветвь средней
мозговой артерии); 11 - передняя височная артерия (ветвь средней
мозговой артерии); 12 - конечная часть задней мозговой артерии; 13 -
задняя височная артерия (ветвь средней мозговой артерии); 14 -
промежуточная височная артерия (ветвь средней мозговой артерии); 15 -
внутренняя сонная артерия; б - внутренняя поверхность: 1 -
внутренняя сонная артерия; 2 - передняя височная ветвь задней мозговой
артерии; 3 - задняя соединительная артерия; 4 - передняя соединительная
артерия; 5 - левая передняя мозговая артерия; 6 - возвратная артерия
(ветвь передней мозговой артерии); 7 - глазничные ветви передней
мозговой артерии; 8 - правая передняя мозговая артерия; 9 - ветвь
передней мозговой артерии к полюсу лобной доли; 10 - мозолисто-краевая
артерия (ветвь передней мозговой артерии); 11 - медиальные лобные ветви
передней мозговой артерии; 12 - перикаллезная артерия (ветвь средней
мозговой артерии); 13 - парацентральная артерия (ветвь передней мозговой
артерии); 14 - предклинная артерия (ветвь передней мозговой артерии);
15 - правая центральная мозговая артерия; 16 - теменно-затылочная ветвь
задней мозговой артерии; 17 - шпорная ветвь задней мозговой артерии; 18 -
задняя височная ветвь задней мозговой артерии
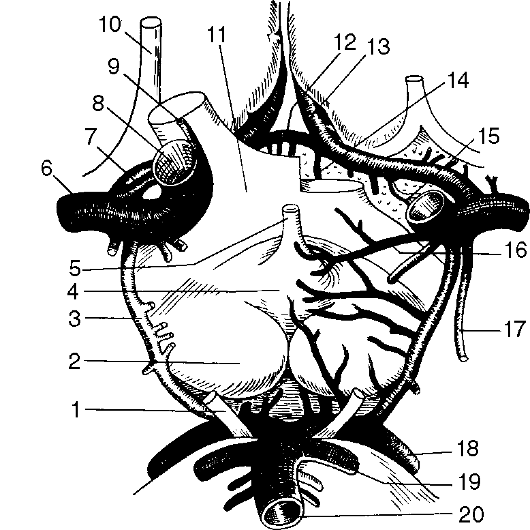 Рис. 7-2. Артерии
головного мозга: 1 - глазодвигательный нерв; 2 - сосковое тело; 3 -
задняя соединительная артерия; 4 - серый бугор; 5 - воронка гипофиза; 6 -
средняя мозговая артерия; 7 - передняя мозговая артерия; 8 - внутренняя
сонная артерия; 9 - глазничная артерия; 10 - обонятельный тракт; 11 -
зрительный перекрест; 12 - передняя соединительная артерия; 13 -
передняя мозговая артерия; 14 - верхняя хиазмальная артерия; 15 -
возвратная артерия Гюбнера; 16 - верхняя гипофизарная артерия; 17 -
передняя ворсинчатая артерия; 18 - задняя мозговая артерия; 19 - верхняя
мозжечковая артерия; 20 - основная артерия
Рис. 7-2. Артерии
головного мозга: 1 - глазодвигательный нерв; 2 - сосковое тело; 3 -
задняя соединительная артерия; 4 - серый бугор; 5 - воронка гипофиза; 6 -
средняя мозговая артерия; 7 - передняя мозговая артерия; 8 - внутренняя
сонная артерия; 9 - глазничная артерия; 10 - обонятельный тракт; 11 -
зрительный перекрест; 12 - передняя соединительная артерия; 13 -
передняя мозговая артерия; 14 - верхняя хиазмальная артерия; 15 -
возвратная артерия Гюбнера; 16 - верхняя гипофизарная артерия; 17 -
передняя ворсинчатая артерия; 18 - задняя мозговая артерия; 19 - верхняя
мозжечковая артерия; 20 - основная артерия
внутренней сонной артерии отходят глазничная, передняя ворсинчатая и задняя соединительная артерии.
Две позвоночные артерии начинаются от подключичных артерий и, пройдя через отверстия в поперечных отростках СV1-С1 позвонков, делают изгиб под углом 90°, ложатся в артериальные борозды атланта и далее проходят через большое затылочное отверстие в полость черепа. Они располагаются на передней поверхности продолговатого мозга и соединяются у заднего края моста мозга, образуя базилярную артерию. Последняя выше спинки турецкого седла, у переднего края моста мозга, разделяется на две задние мозговые артерии, каждая из которых соединяется с внутренней сонной артерией через заднюю соединительную артерию.
Артериальное кольцо, которое образуют на основании мозга анастомозирующие артерии, носит название артериального круга
большого мозга, или виллизиева круга (многоугольника), в честь описавшего его в 1664 г. английского анатома Т. Уиллиса (Виллизия). В физиологических условиях, вследствие одинакового давления в сосудах виллизиева круга, кровь из внутренней сонной артерии одной стороны не поступает в противоположное полушарие. В случаях нарушения кровотока в одной из мозговых артерий происходит его компенсация за счёт коллатерального кровоснабжения из ветвей внутренней сонной артерии противоположной стороны и позвоночных артерий.
Передняя мозговая артерия кровоснабжает медиальную поверхность и верхненаружные отделы лобной (рис. 7-3), частично теменной долей, парацентральную дольку, базальную поверхность лобной доли, большую часть мозолистого тела (за исключением задних отделов), переднее бедро внутренней капсулы, передние отделы головки хвостатого ядра, скорлупы, бледного шара, частично гипоталамическую область, эпендиму переднего рога бокового желудочка.
Средняя мозговая артерия кровоснабжает конвекситальные отделы лобной, теменной и височной долей, медиальную поверхность полюса височной доли.
Передняя ворсинчатая артерия снабжает кровью 2/3 заднего бедра внутренней капсулы, ретролентикулярную часть хвостатого ядра, внутренние сегменты бледного шара, боковую стенку нижнего рога бокового желудочка.
Задняя мозговая артерия кровоснабжает кору и белое вещество затылочной доли, большую часть теменной, задние и медиобазальные отделы височной доли, значительную часть зрительного бугра, задние отделы гипоталамической области, мозолистого тела, зритель-
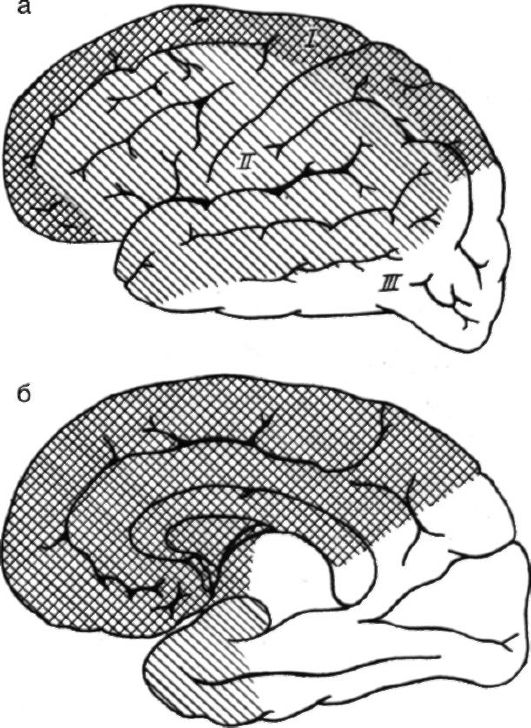 Рис. 7-3. Зоны
кровоснабжения мозговых артерий: а - наружная поверхность коры
полушария мозга; б - медиальная поверхность полушария мозга; I -
передняя мозговая артерия; II - средняя мозговая артерия; III - задняя
мозговая артерия
Рис. 7-3. Зоны
кровоснабжения мозговых артерий: а - наружная поверхность коры
полушария мозга; б - медиальная поверхность полушария мозга; I -
передняя мозговая артерия; II - средняя мозговая артерия; III - задняя
мозговая артерия
ную лучистость, субталамическое ядро (люисово тело) и частично средний мозг.
Основная артерия снабжает кровью мост мозга, мозжечок.
Позвоночная артерия питает кровью продолговатый мозг, верхние шейные сегменты спинного мозга, частично мозжечок.
Представленная морфологическая структура артерий основания мозга встречается относительно редко. По данным литературы, более чем в половине случаев обнаруживают те или иные отклонения от этого типа строения: отсутствие одной или двух соединительных артерий, отхождение задней мозговой артерии не от базилярной, а от внутренней сонной (задняя трифуркация внутренней сонной артерии); отхождение обеих передних мозговых артерий от одной внутренней сонной артерии (передняя трифуркация) и т.д.
Классификация нарушений мозгового кровообращения
Принятая в 1984 г. в Советском Союзе классификация нарушений мозгового кровообращения во многом соответствует Международной классификации болезней (МКБ-10).
■ А. Начальные проявления недостаточности кровообращения:
• головного мозга;
• спинного мозга.
■ Б. Преходящие нарушения мозгового кровообращения:
• транзиторные ишемические атаки;
• гипертонические церебральные кризы:
- с общемозговыми нарушениями;
- с очаговыми нарушениями.
■ В. Инсульт:
• субарахноидальное кровоизлияние (под оболочки головного и спинного мозга);
• геморрагический инсульт (в головной и спинной мозг);
• ишемический инсульт (церебральный и спинальный), который может возникнуть как при поражении (окклюзии) прецеребральных артерий, так и при эмболии церебральных артерий;
• инсульт с восстановленным неврологическим дефицитом - «малый инсульт»;
• последствия ранее перенесенного инсульта.
■ Г. Прогрессирующие нарушения мозгового кровообращения:
• хроническая субдуральная гематома;
• дисциркуляторная энцефалопатия (атеросклеротическая, гипертоническая, токсическая).
Этиология
Нарушения мозгового кровообращения могут возникать в результате многих причин. В 85-90% случаев основной причиной их развития становится атеросклероз, гипертоническая болезнь или их сочетание. Эти расстройства также могут быть вызваны аномалиями сердечно-сосудистой системы: мешотчатые аневризмы и АВМ, аплазии и гипоплазии мозговых сосудов, болезнь Нисимото-Такеути- Кудо (моя-моя), пролапс митрального клапана и т.п. Весьма важное место в их возникновении принадлежит артериальной гипотонии, заболеваниям лёгких, инфекционно-аллергическому васкулиту, системным заболеваниям соединительной ткани, токсическим поражениям сосудов мозга, сахарному диабету. Определённую роль играют заболевания крови, поражения и повреждения сосудов мозга костными образованиями и опухолями.
Патогенез
Патогенетические факторы, вызывающие развитие ишемических инсультов и преходящих нарушений мозгового кровообращения, достаточно разнообразны. Основными среди них являются следующие.
Сосудистая мозговая недостаточность
Её наиболее частыми причинами являются атеросклероз (85- 90%), гипертоническая болезнь и их сочетание. Сосудистая мозговая недостаточность может быть вызвана микроэмболами из сердца и атеромотозно измененных крупных сосудов (дуга аорты, магистральные артерии головы). Эмбологенным материалом могут быть кристаллы холестерина, кусочки пристеночных тромбов, распадающихся атероматозных бляшек, конгломераты тромбоцитов, образующихся в области измененного участка стенки крупного сосуда. Главным патогенетическим фактором в атеросклеротическом процессе является атерогенная дислипопротеинемия. При ней изменяется соотношение между атерогенными (холестерин и триглицериды) и неатерогенными липопротеидами. При нарастании процесса атеросклеротическая бляшка кровоснабжается со стороны адвентиции, в ней накапливаются липопротеиды. Бляшка увеличивается в
размере и может полностью закупорить просвет сосуда. Поверхность бляшки может изъязвляться и стать источником микроэмболии. Увеличение атероматозной бляшки в сочетании с тромбозом составляет морфологическую основу стенозирующих поражений мозговых сосудов. Наиболее часто подвергаются стенозированию и окклюзии внечерепные артерии в местах изгибов и отхождений артерий. Различают три уровня поражения атеросклерозом вне- и внутричерепных артерий.
■ I уровень - устья брахиоцефальных артерий, подключичные и общие сонные артерии (26,2%).
■ II уровень - бифуркация общей сонной артерии, внутренняя сонная и позвоночная артерия (особенно часто при наличии аномалии Киммерле) до вхождения в полость черепа (46,1%).
■ III уровень - все внутричерепные окклюзии и стенозы сонных и позвоночных артерий. Их частота 27,7%.
Опасная для мозга гипоперфузия мозга возникает при сужении артерии на 50% и более. Такое сужение является показанием для хирургического лечения.
Механизм компенсации нарушенного мозгового кровообращения состоит в развитии коллатерального кровотока. Существует 8 возможных путей развития коллатерального кровообращения:
• вертебрально-вертебральный;
• каротидно - базилярно -вертебральный;
• каротидно-субклавикулярный;
• через переднюю соединительную артерию;
• через заднюю соединительную артерию;
• экстраинтракраниальный;
• назоорбитальный;
• через среднюю мозговую и заднюю мозговую артерии. Сосудисто-мозговая недостаточность также возникает вследствие
нарушения микроциркуляции из-за изменения физико-химических свойств крови, приводящих к повышению вязкости крови, агрегации эритроцитов, снижению их деформированности (нарушение реологии крови), может быть следствием гипоксии и гипогликемии. Спондилогенная патология (сдавление позвоночных артерий остеофитами в области унковертебральных сочленений, подвывихи позвонков в шейном отделе позвоночника и другие причины), а также патологическая извитость сонных и позвоночных артерий нередко приводят к сосудисто-мозговой недостаточности.
Весьма важное значение для реализации ишемического инсульта имеет сочетание нескольких факторов. Так, развитие ишемического инсульта при окклюзии сосудов мозга, как правило, должно сопровождаться недостаточностью коллатерального кровообращения, стенозом с понижением артериального давления и замедлением мозгового кровотока. Длительный спазм сосудов, развившийся в результате разрыва аневризмы, особенно у больных с атеросклерозом мозговых артерий, обычно вызывает развитие ишемических поражений головного мозга и нередко приводит к гибели больного.
Гипертонические церебральные кризы возникают вследствие дисфункции гипоталамо-ретикулярного комплекса и нарушения регуляции тонуса мозговых сосудов. Их появление сопровождается регионарной гиперемией мозга (гиперперфузии мозга под повышенным давлением), изменением проницаемости сосудов, выходом белка и воды из сосудистого русла, диапедезными микрогеморрагиями, отёком мозга и вторичным сдавлением сосудов отечной жидкостью. Результатом этих изменений будет уменьшение мозгового кровотока. Гипертонические кризы, при которых значительно выражен отёк мозга, носят название острой гипертонической энцефалопатии.
В патогенезе развития ишемического инсульта важное значение имеет повышение рСО2, снижение образования АТФ, расширение коллатералей, приводящее к реактивной гиперемии, повышению агрегации форменных элементов, стазу крови, нарушению микроциркуляции. Следствием представленного выше будут плазморрагия, отёк-набухание головного мозга и инфаркт. Таким образом, основные патогенические факторы ишемического инсульта следующие.
■ Нарушение энергетического обмена с образованием недоокисленных продуктов.
■ Нарушение микроциркуляции головного мозга вследствие изменения реологических свойств крови.
■ Развитие отёка-набухания головного мозга.
■ Перекисное окисление липидов с образованием цитотоксических продуктов.
По характеру морфологических изменений инсульты делятся на ишемические, геморрагические и смешанные.
В бассейне сонных артерий ишемический инсульт встречается в 5-6 раз чаще, чем в вертебрально-базилярном бассейне. Очаговые симптомы развиваются на противоположной стороне от окклюзированной мозговой артерии.
ПРЕХОДЯЩИЕ НАРУШЕНИЯ МОЗГОВОГО КРОВООБРАЩЕНИЯ
Преходящими нарушениями мозгового кровообращения называют такие нарушения, которые возникают внезапно и вызывают кратковременные неврологические расстройства (от нескольких минут до одних суток).
Этиология и патогенез
Как правило, преходящие нарушения мозгового кровообращения обусловлены микрогеморрагиями, начинающимся тромбозом или сужением крупного магистрального сосуда, микроэмболиями, когда нормально сформированный и ещё сохранённый виллизиев круг способен восстановить кровоток дистальнее места окклюзии. Иногда возникновение преходящих нарушений мозгового кровообращения может быть обусловлено «обкрадыванием» (патогенной компенсацией), когда при окклюзии одного сосуда кровь перетекает в его бассейн из сохраненной соседней магистральной артерии, и в бассейне этой последней артерии возникает дефицит кровотока с клиническими проявлениями.
Клиническая картина
Клиническая картина преходящих нарушений мозгового кровообращения зависит от локализации и продолжительности дисциркуляторных расстройств. Как правило, эпизод длится от нескольких минут до 12 ч с последующим полным восстановлением неврологического статуса.
При поражении сонных артерий развиваются головокружения (часто связанные с изменением положения головы), беспричинная тошнота, изменения характера (раздражительность, забывчивость), а также двигательные и чувствительные нарушения противоположной поражению стороны тела.
При нарушении кровотока во внутренней сонной артерии на уровне отхождения глазничной артерии развивается преходящий оптико-пирамидный синдром, который проявляется снижением остроты зрения или слепотой глаза на стороне патологии и гемипарезом контралатеральных конечностей.
Преходящие нарушения мозгового кровообращения в вертебрально-базилярном бассейне характеризуются внезапным появлением сильного головокружения, шумом в ушах, горизонтальным нистагмом, статической атаксией и другими координаторными нарушениями. Могут возникать зрительные расстройства в виде гемианопсий или фотопсий, а также слабость или парастезии в конечностях. Возможны внезапные падения без утраты сознания (синдром «падающей капли», англ. «drop attack»).
Лечение
При появлении преходящего нарушения мозгового кровообращения необходимо детальное исследование магистральных сосудов шеи и головы для принятия решения о целесообразности микроангиохирургического вмешательства и выбора его варианта (шунтирование, тромбинтимэктомия и т.д.).
В качестве профилактики мозгового или спинно-мозгового инсульта назначают противосклеротические препараты и антиагреганты.
При наличии гиперкоагуляции (по данным коагулограммы) или увеличении числа тромбоцитов более 300 000, а также при предположении об артериальной эмболии показано применение ацетилсалициловой кислоты или дипиридамола. Ацетилсалициловая кислота в малых дозах (0,15 мг 2 раза в сутки или 0,25 мг 1 раз в сутки) ингибирует тромбоксан А2, стимулирующий агрегацию тромбоцитов, и тем самым способствует предотвращению ишемических инсультов. Большие дозы ацетилсалициловой кислоты (0,5 мг в сутки и более) ингибируют как тромбоксан А2, так и простациклин - сильный антиагрегант.
ИШЕМИЧЕСКИЙ ЦЕРЕБРАЛЬНЫЙ ИНСУЛЬТ
Ишемический инсульт (инфаркт головного мозга) - это острое нарушение мозгового кровообращения, при котором, в отличие от преходящего нарушения мозгового кровообращения, симптомы поражения нервной системы сохраняются более суток.
Клиническая картина
Условно выделяют малые инсульты с лёгким течением и обратимым неврологическим дефицитом (неврологические симптомы
исчезают в сроки до трех недель) и большие, протекающие значительно тяжелее, с грубыми и необратимыми неврологическими проявлениями.
Варианты развития инсульта.
■ Острый (30-35% случаев) - неврологические симптомы развиваются в течение нескольких минут, часа.
■ Подострый (40-45% случаев) - симптоматика постепенно нарастает от нескольких часов до недели.
■ Хронический (20-30% случаев) - более 7 дней.
Общемозговые симптомы бывают ярко выражены в основном при остром развитии инсульта. Как правило, такое развитие инсульта наступает после эмоциональных переживаний.
При подостром и хроническом развитии ишемического инсульта часто бывают «предвестники» в виде приступов головной боли; чувства онемения щеки, руки, ноги; затруднения речи; приступов головокружения, потемнения в глазах; снижения остроты зрения; сердцебиения. Эти проявления носят кратковременный характер. При таком развитии заболевания очаговые симптомы преобладают над общемозговыми. Вариант очаговых симптомов зависит от локализации инсульта.
Например, при тромбозе внутренней сонной артерии развиваются гемипарез и парез нижней мимической мускулатуры, интеллектуально-мнестические расстройства, нарушения речи, оптико-пирамидный синдром или гомонимная гемианопсия, а также нарушения чувствительности. В 25% случаев можно выслушать систолический шум над областью стеноза, в 17% - пальпаторно обнаружить снижение пульсации сонной артерии и её болезненность. У 20% больных возникают эпилептические припадки. Нередко больные жалуются на приступы брадиили тахикардии, которые обусловлены вовлечением в атеросклеротический процесс сонного синуса. При исследовании глазного дна на пораженной стороне обнаруживают простую атрофию диска зрительного нерва.
При тромбозе внутренней сонной артерии через некоторое время после развития инсульта может произойти быстрое восстановление неврологических расстройств, связанное с реканализацией тромба. Однако в дальнейшем нередко наступает повторная окклюзия сосуда с увеличением тромба и распространением его на сосуды виллизиева круга. При этом снова ухудшается состояние больного и возможен даже летальный исход.
Инструментальные методы исследования
Основным инструментальным методом диагностики ишемических поражений головного мозга служит ангиография сосудов головного мозга, позволяющая диагностировать состояние вне- и внутричерепных сосудов, уровень их окклюзии, а также развитие коллатерального кровотока (рис. 7-4).
Для визуализации головного мозга в настоящее время применяют КТ и МРТ. Эти методы исследования позволяют выявить зоны ишемии мозговой ткани уже через 6-7 ч после развития инсульта. В последние годы внедрена в клиническую практику МРТ с сосудистой программой (рис. 7-5), которая позволяет устанавливать не только наличие ишемического инсульта, но и выявлять сосуд, подвергшийся закупорке.
ПЭТ может намного раньше, по сравнению с КТ и МРТ, выявлять нарушения перфузии и метаболизма мозговой ткани. Установлено, что не кровоток, а метаболизм является решающим в оценке степени ишемического поражения головного мозга.
Важным неинвазивным методом исследования, позволяющим определить проходимость экстра- и интракраниальных артерий, степень их сужения в до- и послеоперационном периодах в настоящее время считают транскраниальную допплерографию с дуплексным сканированием.
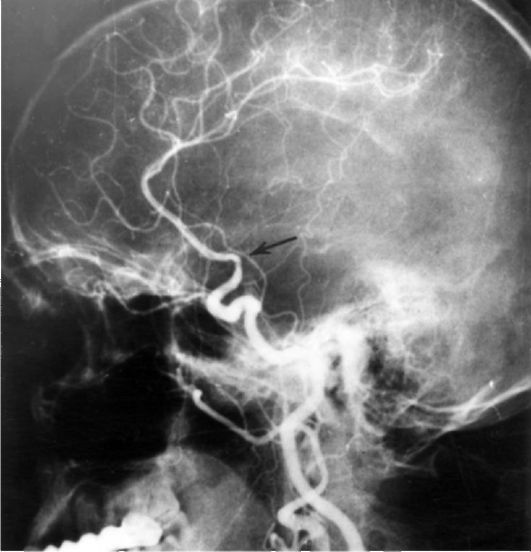 Рис. 7-4. Окклюзия основного ствола a. cerebri media (стрелкой показан тромбоз средней мозговой артерии в области устья)
Рис. 7-4. Окклюзия основного ствола a. cerebri media (стрелкой показан тромбоз средней мозговой артерии в области устья)
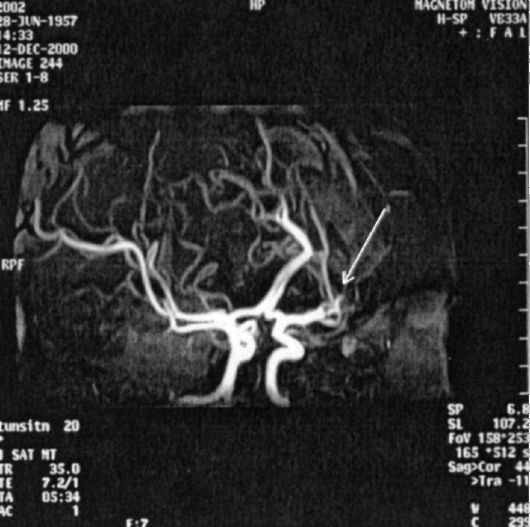 Рис. 7-5. Магнитно-резонансная томография сосудов головного мозга (стрелкой указан тромбированный сосуд бассейна средней мозговой артерии)
Рис. 7-5. Магнитно-резонансная томография сосудов головного мозга (стрелкой указан тромбированный сосуд бассейна средней мозговой артерии)
Лечение
При развитии церебрального инсульта больного следует срочно госпитализировать, лучше в специализированное нейрососудистое или нейрореанимационное отделение.
Важно помнить, что медикаментозное лечение наиболее эффективно в первые 2-4 ч с момента возникновения инсульта. Это так называемое терапевтическое окно, когда можно эффективно воздействовать на микроциркуляторные, молекулярно-генетические и энергетические нарушения в ишемизированной зоне мозга.
Медикаментозное лечение ишемического инсульта включает коррекцию АД и реологических свойств крови, борьбу с гипоксией и перекисным окислением липидов, устранение отёка мозга и антикоагулянтную терапию.
Коррекция АД. Известно, что повышение системного АД вызывает структурные и функциональные изменения в системе мозгового кровообращения. В ответ на повышение АД вначале возникают только адаптивные изменения: гипертрофия гладких мышц резистивных внутричерепных артерий и сдвиг кривой ауторегуляции мозгового кровообращения в область более высоких давлений. Однако постепенно наступают стойкие изменения сосудистой стенки в виде гиалиноза, артериосклероза и микроаневризм, нарушающие нормальную спо-
собность этих сосудов к расширению и сужению в ответ на колебания артериального давления. На любой стадии этого процесса быстрый и чрезмерный (т.е. превышающий верхнюю границу ауторегуляции мозгового кровотока) подъём АД приводит к нарушению мозгового кровообращения, отёку мозга и его оболочек, дилатации мелких внутричерепных артерий и гиперперфузии мозга. Всё это обусловливает нарушение гематоэнцефалического барьера с повышением проницаемости сосудов к белкам плазмы, а также вазогенный отёк мозга и его оболочек. В некоторых сегментах артерий выявляются локальные участки спазма.
Степень безопасного снижения артериального давления зависит от проходимости магистральных артерий. С одной стороны, дистально от сужения или окклюзии сосуда нет столь выраженного подъёма АД, что является своего рода защитой от кровоизлияния. С другой стороны, при наличии грубого стеноза увеличивается опасность очаговой ишемии мозга при снижении АД. Вместе с тем при высоком артериальном давлении не следует применять сосудорасширяющие препараты (нимодипин, папаверин), пока АД не будет снижено до оптимального уровня. Для определения этого уровня следует учитывать самочувствие пациента при разных уровнях АД, стабильность высоких значений АД, особенно диастолического, наличие признаков хронической дисфункции мозга (псевдобульбарный парез, паркинсонизм, гипомнезию, деменцию), эффективность различных гипотензивных препаратов, применённых ранее.
Как правило, лечение начинают с небольших доз гипотензивных препаратов во избежание резкого снижения АД. Считают, что только подъём систолического АД выше 230 мм рт.ст. или диастолического выше 140 мм рт.ст. требует немедленного введения нитропруссида натрия либо азаметония бромида, клонидина, эналаприла. При систолическом АД ниже 180 мм рт.ст. или диастолическом АД ниже 105 мм рт.ст. гипотензивную терапию не проводят. Определяющим считают уровень «рабочего» АД до развития церебрального инсульта. При хорошем оснащении реанимационного отделения гипотензивную терапию контролируют картированной ЭЭГ, регистрацией зрительных и звуковых потенциалов и транскраниальной допплерографией. С их помощью удаётся довольно точно судить об изменениях мозгового кровообращения под влиянием различных вазоактивных лекарственных средств. Важно оценивать при этом и динамику неврологических симптомов.
Коррекция реологических свойств крови
Наиболее эффективно внутривенное капельное введение пентоксифиллина (трентала*) в течение 10-12 дней с последующим переходом на внутримышечное введение (агапурин*) или приём в форме драже на протяжении месяца. Внутривенное капельное введение реополиглюкина* в дозе 10 мл на килограмм массы тела ежедневно в течение 5-7 дней. Назначение этого препарата желательно проводить совместно с эуфиллином 2,4% 5-10 мл. При этом необходимо поддерживать нормальное содержание электролитов в плазме крови и умеренные величины гематокрита (30-40). Выравниванию реологических свойств крови способствует применение дипиридамола, ацетилсалициловой кислоты, пирикарбата, ксантинола никотината и пентоксифиллина.
Борьба с гипоксией
Назначение нейропротекторов, нейростимуляторов и антигипоксантов.
■ Нейропротекторы: нейроплегики, барбитураты (фенобарбитал по 0,05 г 3 раза в день), натрия оксибат. Последний препарат снижает энергетические потребности мозга. Этот препарат вводят внутривенно струйно, медленно (в течение 2-3 мин) в дозе 10 мл 20% раствора. Противопоказанием для его назначения считают гипокалиемию.
■ Нейростимуляторы и антигипоксанты: холина альфосцерат по 4 мл внутривенно или внутримышечно, актовегин* по 5 мл внутримышечно или солкосерил* внутримышечно по 2 мл, пирацетам 20% по 10 мл внутривенно, гамма-аминомасляная кислота 2 г - 3 раза в день). В острой фазе инсульта назначают кортексин* по 10-20 мг внутримышечно или церебролизин* внутривенно по 5-10 мл.
■ Пиридитол также обладает защитными свойствами против гипоксии. Препарат применяют внутрь по 100 мг 3 раза в сутки.
Борьба с перекисным окислением липидов
С этой целью используют антиоксиданты - витамины Е, А, Р, РР.
Устранение отёка мозга
При тяжёлых формах ишемического инсульта, протекающих с общемозговыми симптомами и отёком мозга, необходимо назначать препараты, уменьшающие отёк мозга.
Осмотические диуретики повышают осмотическое давление плазмы и способствуют тем самым переходу жидкости из ткани мозга в
сосудистое русло. Чаще всего назначают маннитол из расчета 1-1,5 г/ кг в сутки, скорость введения препарата 60-80 капель в минуту. Поскольку дегидратирующий эффект препарата сменяется феноменом отдачи, необходимо через 3-4 ч после введения препарата назначить 2 мл фуросемида внутривенно. Для уменьшения отёка мозга можно принимать глицерол внутрь. Препарат вводят в виде 10% раствора из расчёта 1 г/кг. Можно назначать салуретики: фуросемид, который вводят внутривенно или внутримышечно (однократная доза - 20-40 мг). При назначении этих препаратов важно предупреждать развитие гипокалиемии и своевременно восполнять дефицит калия.
Глюкокортикоиды обладают стабилизирующим действием на клеточные мембраны и подавляют продукцию спинно-мозговой жидкости. Наиболее эффективен дексаметазон в дозе от 16 до 24 мг в сутки. Менее активен преднизолон. Гормоны надо назначать в период с 8 ч утра до полудня. Не следует назначать кортикостероиды при высоком артериальном давлении, гиперосмолярности, язвенной болезни, диабете.
Антикоагулянтная терапия
Сразу после установления диагноза ишемического инсульта следует назначать антикоагулянты.
■ Гепарин натрия вводят по 5000-10 000 ЕД под кожу живота. Лечение гепарином продолжают в течение 4-6 дней под контролем коагулограммы.
■ Антикоагулянты непрямого действия (фениндион) назначают за один-два дня до отмены гепарина натрия. Лечение антикоагулянтами непрямого действия проводят под контролем протромбинового времени, которое исследуют не реже 1 раза в 2-3 дня. Коагулограммужелательноделатьодинразв7-10дней.Оптимально
снижение протромбина до уровня 40-50 мгр%. Для купирования геморрагических осложнений, связанных с назначением гепарина натрия, в экстренных случаях применяют протамина сульфат (5 мл 1% раствора внутривенно).
Новокаиновая блокада звёздчатого симпатического узла
Шейным вегетативным ганглиям принадлежит важная роль в регуляции церебральной гемодинамики, особенно в условиях острой ишемии мозга при церебральной вегетососудистой дистонии или после перенесённой нейроинфекции и травм головного мозга. У таких больных для снятия высокого симпатэргического тонуса показана новокаиновая блокада звёздчатого симпатического узла.
Блокаду выполняют в положении больного на спине, с несколько запрокинутой головой. На два пальца выше грудиноключичного сочленения выполняют инфильтрацию кожи 0,5% раствором новокаина. Отведя сосудисто-нервный пучок вместе с кивательной мышцей латерально, а трахею - медиально, указательным пальцем нащупывают поперечный отросток 6 шейного позвонка. Иглу осторожно вводят до поперечного отростка, предпосылая введению иглы струю новокаина. Достигнув поперечного отростка, оттягивают иглу назад на 1-2 мм - игла оказывается в клетчаточном пространстве у звездчатого ганглия. Вводят 20 мл 0,5% раствора новокаина. При появлении крови в игле процедуру следует прекратить, поскольку это свидетельствует о попадании иглы в сонную или позвоночную артерию.
При правильно выполненной блокаде через 5-10 мин у больного развивается синдром Бернара-Горнера (сужение зрачка, опущение верхнего века, западение глазного яблока). Больной часто ощущает тепло в половине лица на стороне блокады. Последующие блокады можно выполнять, используя 1% раствор новокаина в количестве 15-20 мл.
Хирургическое лечение ишемического церебрального инсульта
Хирургическое вмешательство на экстра- и интракраниальных сосудах.
Наиболее распространена операция эндартериоэктомии подключичной, позвоночной, общей и внутренней сонных артерий (рис. 7-6). Во время этой операции удаляют стенозирующую или окклюзирующую сосуд атероматозную бляшку. В последнее время применяют баллонную и ультразвуковую дилатацию как экстра-, так и интракраниальных сосудов. Проводят также шунтирующие операции - это аортоподключичное и подключично-каротидное шунтирование, а также реконструктивные операции на позвоночной и сонной артериях.
В 60-70-е годы XX в. стали широко применять экстраинтракраниальное анастомозирование - переключение кровотока из наружной сонной во внутреннюю сонную артерию. Чаще всего создают анастомоз между поверхностной височной и угловой артерией из бассейна средней мозговой артерии (рис. 7-7).
В 70-80-е годы предложена и внедрена в практику операция аутотрансплантации реваскуляризированного фрагмента большого сальника на ишемизированные участки мозга.
В 80-е годы начата разработка новой методики введения внутренних протезов в поражённые участки сосудистой системы.
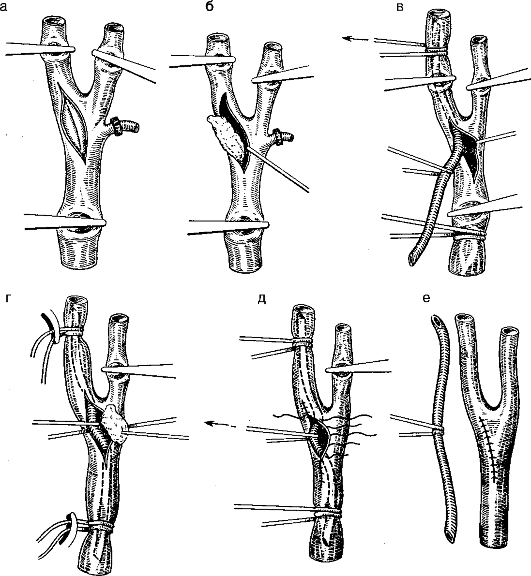 Рис.
7-6. Эндартериоэктомия. Наружное и внутреннее шунтирование сонных
артерий: а - разрезают артерию с рассечением бляшки; б - выполняют
атеромэктомию; в - вводят внутренний шунт; г - удаляют бляшку; д -
извлекают шунт; е - зашивают артерию
Рис.
7-6. Эндартериоэктомия. Наружное и внутреннее шунтирование сонных
артерий: а - разрезают артерию с рассечением бляшки; б - выполняют
атеромэктомию; в - вводят внутренний шунт; г - удаляют бляшку; д -
извлекают шунт; е - зашивают артерию
Применяют также паллиативные вмешательства - операции на симпатической нервной системе: симпатэктомию верхнего шейного или звездчатого узлов, периартериальную десимпатизацию; артериоэктомию сегмента облитерированной внутренней сонной артерии на шее; исправление патологической извитости сонной артерии на шее. Иногда эти операции выполняют комбинированно.
Хирургическое вмешательство при ишемических заболеваниях головного мозга позволяет уменьшить летальность до 11% и улучшить прогноз, поскольку снижает частоту повторных церебральных инсультов и повышает степень социальной и трудовой адаптации больных.
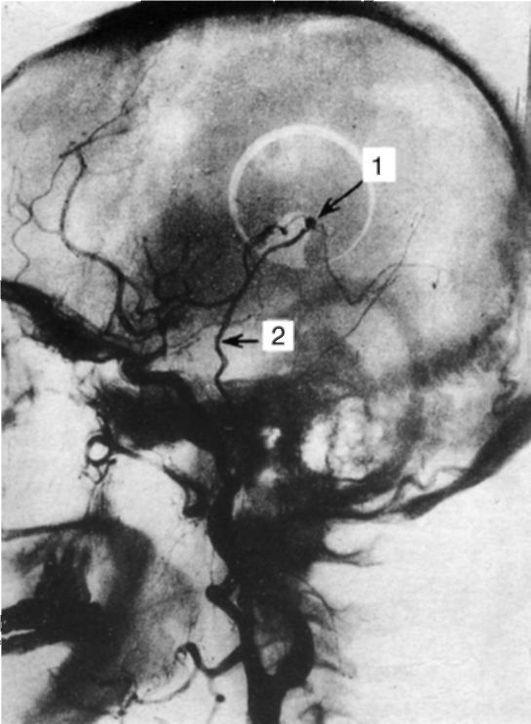 Рис. 7-7. Экстраинтракраниальный анастомоз наружной и внутренней сонной артерии: 1 - анастомоз; 2 - поверхностная височная артерия
Рис. 7-7. Экстраинтракраниальный анастомоз наружной и внутренней сонной артерии: 1 - анастомоз; 2 - поверхностная височная артерия
ГЕМОРРАГИЧЕСКИЙ ЦЕРЕБРАЛЬНЫЙ ИНСУЛЬТ
Геморрагическим инсультом называют кровоизлияние в вещество головного мозга, в желудочки или подоболочечные пространства.
Этиология и патогенез
Причиной кровоизлияния в мозг чаще всего становится гипертоническая болезнь и мелкие аневризмы мозговыхсосудов. Геморрагические инсульты могут развиваться также при атеросклерозе, артериальных и артериовенозных аневризмах, опухолях мозга, васкулитах. Различают кровоизлияния в большие полушария головного мозга, в ствол мозга и в мозжечок. По локализации в больших полушариях кровоизлияния делятся на латеральные - кнаружи от внутренней капсулы, медиальные - кнутри от неё и смешанные, занимающие всю область подкорковых ганглиев.
При гипертонической болезни сосудистая стенка мелких артерий мозга подвергается гиалинизации. При атеросклерозе отложение холестерина приводит к сужению просвета сосудов и истончению сосудистой стенки за счёт дегенерации внутреннего эластического и мышечного слоёв. Постоянное повышение АД, а также его периодические подъёмы могут привести к разрыву изменённой стенки сосуда.
Атеросклеротические изменения особенно ярко проявляются в крупных сосудах в местах их изгибов, поворотов, где происходят гемодинамические удары. В ряде случаев ток крови может отслаивать повреждённый участок интимы с формированием локального выпячивания - аневризмы.
Другим важным фактором развития локального поражения крупной артерии считают закупорку мелких сосудов, питающих её стенку (vasa vasorum). Нарушение кровообращения на этом участке приводит к некрозу интимы и мышечного слоя с последующим формированием аневризмы по вышеописанному механизму. Причиной кровоизлияния может быть также спонтанный разрыв врожденной артериальной или артериовенозной аневризм.
Клиническая картина
Клиническая картина при внутричерепных кровоизлияниях зависит от распространённости кровоизлияния, наличия и локализации внутримозговой гематомы. Для геморрагического инсульта характерно внезапное начало (чаще во время или после физической нагрузки, эмоционального эпизода, при активной деятельности, иногда под влиянием атмосферных условий) и быстрое нарастание угнетения сознания.
При распространении крови в базальные цистерны нарушается отток ликвора по субарахноидальным пространствам, что способствует формированию в них ликворостаза и отёку-набуханию головного мозга. Раздражение интерорецепторов оболочек и стенок сосудов мозга продуктами распада эритроцитов обусловливают выраженную болевую реакцию, спазм сосудов и вторичные ишемические поражения мозга, особенно в гипоталамической области. Возникают также нарушения свертывающей системы крови по типу афибриногенемии.
У больных при геморрагических инсультах часто выявляют изменения свёртывающей системы крови (замедление свёртывания).
Типы геморрагического инсульта
■ Субарахноидальное кровоизлияние встречается чаще всего и клинически характеризуется интенсивной головной болью, чаще в лобно-височных областях, сжимающего характера, светобоязнью, болями за глазными яблоками, которые усиливаются при их движении. Возможны повторные приступы рвоты и тошнота. Иногда эти проявления заболевания ошибочно расценивают как симптомы
гриппа. Общее состояние больных удовлетворительное или средней тяжести. Наблюдается тенденция к подъему АД выше нормальных цифр, тахикардия (до 80-90 в минуту), температура тела повышается до субфебрильной. В самом начале заболевания выявляются умеренно выраженные оболочечные симптомы. При спинно-мозговой пункции в ликворе обнаруживают кровь. Что дает основание поставить диагноз внутричерепного кровоизлияния.
■ Паренхиматозно-субарахноидальное кровоизлияние чаще развивается у людей с гипертонической болезнью и атеросклерозом, протекает более тяжело, чем субарахноидальное, поскольку общемозговые и очаговые симптомы выражены значительно больше. В трети таких случаев образуется внутримозговая гематома. Сознание у больных нарушено до уровня оглушения - сопора, часто возникает двигательное возбуждение, возможны эпилептические припадки. Очаговые неврологические симптомы зависят от локализации кровоизлияния. Характерны высокое АД и тахикардия (до 90-110 в минуту). Температура тела обычно достигает 38-38,5°С. Общее состояние больных средней тяжести или тяжёлое. В общем анализе крови - лейкоцитоз со сдвигом лейкоцитарной формулы влево. Ликвор часто бывает кровянистым, ксантохромным и редко - нормальным. Ликворное давление, как правило, повышено.
■ Вентрикулярно-паренхиматозно-субарахноидальное кровоизлияние. Состояние больного тяжелое или крайне тяжелое - нередко выявляют признаки децеребрационной ригидности, стволовые нарушения, расстройства дыхания центрального типа (Куссмауля, Биота, Гаспингса). Возможно появление синдрома «трёх геми-» (гемианопсия, гемианастезия, гемиплегия), часто с низким мышечным тонусом и двусторонними патологическими стопными знаками. При раздражении кожи туловища и конечностей нередко возникают горметонические судороги с вытягиванием и приведением верхней конечности к туловищу. Гемодинамические показатели характеризуются неустойчивостью, которая проявляется в начале гипертоническим типом, а затем быстро сменяется их снижением. Сознание нарушено до уровня сопора, комы. При спинно-мозговой пункции ликвор интенсивно окрашен кровью. В клиническом анализе крови - лейкоцитоз со сдвигом лейкоцитарной формулы влево. При этом типе кровоизлияния быстро развиваются выраженный дислокационный синдром, расстройства кровообраще-
ния, обусловленные нарушением микроциркуляции во всех отделах головного мозга по типу остановки мозгового кровотока. Дифференциальная дагностика острого периода инсультов Своевременная диагностика геморрагического и ишемического инсультов (табл. 7-1) имеет важное значение для назначения адекватной терапии.
Таблица 7-1. Дифференциальная диагностика характера инсульта
Признаки | Геморрагический инсульт | Ишемический инсульт |
1 | 2 | 3 |
Возраст | Чаще 40-60 лет | Старше 60 лет |
Ревматический порок с мерцательной аритмией | Редко | Часто |
Начало | Внезапное, чаще после физической нагрузки или психотравмы | Медленное, чаще с предвестниками |
Время суток | Днём, вечером | Во сне и утром |
Головная боль | Сильная, интенсивная | Обычно отсутствует |
Рвота | Часто | Не типично |
Сознание | Утрачивается в 50-60% случаев | Утрачивается реже, примерно в 30% случаев |
Поражение черепных нервов | VII, XII пара по центральному типу | Постоянное или временное поражение нервов II , VII, XII пар по центральному типу |
Нарушение речи | Обычно при кровоизлиянии в доминантное полушарие примерно у 25% больных | При патологии в доминантном полушарии |
Двигательные нарушения | Наличие с самого начала заболевания | Часто преобладают над общемозговыми симптомами |
Чувствительные нарушения | Возможны | Редко |
Вегетативные нарушения | Практически всегда | Редко |
Окончание табл. 7-1
1 | 2 | 3 |
Артериальное давление | Как правило, повышено более 180 мм рт.ст. | Иногда повышенное до 180 мм рт.ст. |
Стволовые симптомы | Часто | Редко |
Ликвор | Кровянистый или ксантохромный, ликворное давление повышено | Бесцветный, ликворное давление нормальное или умеренно повышено |
Лейкоцитоз, нейтрофилез, индекс Крепса | Обычно имеется | Отсутствует |
Смещение М-эхо | Имеется | Иногда бывает от 2 до 4 мм |
КТ, МРТ | Характерная картина для каждого заболевания | |
Лечение
Медикаментозное лечение
Медикаментозное лечение геморрагического инсульта должно быть направлено на уменьшение отёка головного мозга, головной боли, вегетативных расстройств, снижение АД, температурной реакции, ликвидацию рефлекторного спазма сосудов, нормализацию микроциркуляции, устранение нарушений свертывающей системы крови.
Резкое снижение АД нежелательно, поскольку оно может значительно ухудшить циркуляцию крови в мозговых сосудах, особенно в условиях отёка и острой внутричерепной гипертензии. В подобных случаях используют бендазол (0,5% раствор 4-8 мл внутривенно или внутримышечно), папаверин (2% раствор 2 мл внутривенно или внутримышечно), мафусол*, магния сульфат, инстенон*. Снижать АД можно не ниже 30% от исходного уровня. Дальнейшее снижение может вызвать нарушение ауторегуляции мозгового кровообращения.
При ослаблении сердечной деятельности вводят 0,06% раствор коргликона* или 0,05% раствор строфантина-К в дозе 0,25-1 мл с глюкозой или раствором натрия хлорида внутривенно, никетамид 1-2 мл подкожно, сульфокамфокаин* 2 мл внутримышечно или внутривенно. Проведение более энергичной гипотензивной терапии в случаях её необходимости следует отложить до тех пор, пока не будет достиг-
нут положительный эффект дегидратационной терапии, проявляющийся в улучшении состояния сознания и уменьшении стволовых симптомов. При улучшении состояния больного можно назначить внутривенное или внутримышечное введение 1 мл 0,01% раствора клонидина. Эту дозу разводят в 20 мл физиологического раствора натрия хлорида. В случаях высокого АД могут быть применены ганглиоблокаторы: азаметония бромид 0,5-1 мл 5% раствора, гексаметония бензосульфонат 1 мл 2,5% раствора или димеколония йодид 1 мл. Эти препараты вводят внутримышечно или внутривенно. Их можно сочетать с 1% раствором дифенгидрамина (2 мл).
В качестве противоотёчных препаратов вводят только салуретики по обычной схеме, представленной в разделе о лечении ишемических инсультов.
С целью повышения свёртываемости крови и уменьшения сосудистой проницаемости назначают кальция хлорид в виде 1% раствора, менадиона натрия бисульфит 6 мл 1% раствора внутримышечно, аскорбиновую кислоту 5-10 мл внутривенно, этамзилат по 2 мл внутримышечно или внутривенно 3-4 раза в сутки.
С целью снижения фибринолитической активности крови применяют вещества, угнетающие фибринолиз - аминокапроновую кислоту внутривенно капельно 100 мл с интервалом в 3-6 ч. Суточная доза препарата может быть 24 г, курс - 5-6 дней. Кровотечение обычно продолжается несколько минут. Поэтому длительно вводить гемокоагулянты нет необходимости. Для предотвращения диссеминированного свертывания крови после введения 300 мл аминокапроновой кислоты можно внутривенно капельно ввести 1,5 мл (5000 ЕД) гепарина натрия. При выраженном атеросклерозе от введения аминокапроновой кислоты следует воздержаться, так как возможны тромботические осложнения. Показано назначение ингибитора фибринолиза апротинина (трасилол*, контрикал*). Суточная доза трасилола* составляет 25 000-75 000 ЕД внутривенно, в течение 4-10 дней. Контрикал* вводят внутривенно капельно по 10 000-40 000 ЕД в течение первой недели заболевания.
С целью снятия спазма назначают вазодилататоры, антагонисты кальция - нифедипин, нимодипин, которые уменьшают периферическое сосудистое сопротивление, а также препараты, блокирующие активность серотонина и других биогенных аминов.
Для снятия раздражения диэнцефальных отделов мозга применяют прометазин 2,5% 2 мл внутримышечно. Введение этого препарата
необходимо комбинировать с 50% метамизолом натрия (2 мл); при высоких значениях АД можно рекомендовать ганглиоблокаторы (азаметония бромид 0,5-1 мл). Комбинация этих препаратов вводится внутримышечно. Частота введения - через каждые 4-6 ч. Головная боль при кровоизлияниях в мозг, как правило, характеризуется большой интенсивностью, иногда приходится рекомендовать 1% раствор тримеперидина (1 мл).
С целью нейропротекции назначают препараты, не влияющие на гемостаз: кортексин - по 20 мг в сутки, холина альфосцерат - по 4 мл в сутки, актовегин* - по 5 мл в сутки, цитофлавин* - по 10 мл в сутки, этилметилгидроксипиридина сукцинат - по 4 мл в сутки и т.д.
Люмбальные пункции повторяют как можно реже в связи с опасностью усиления дислокации, при этом для лабораторного исследования выводят не более 2-4 мл спинно-мозговой жидкости.
Больным в острой фазе церебрального инсульта не делают клизм для освобождения кишечника, так как натуживание при этой процедуре может повлечь повышение внутричерепного давления и спровоцировать повторное кровоизлияние.
При латеральных внутримозговых гематомах, которые не разрушают внутреннюю капсулу, показано их хирургическое удаление.
АНЕВРИЗМЫ АРТЕРИЙ ГОЛОВНОГО МОЗГА
Излюбленное место локализации аневризм - места деления сосудов I и II порядка на ветви. Самая частая локализация аневризм - супраклиновидный отдел внутренней сонной артерии (30-34%), передняя мозговая, передняя соединительная артерии - 28-30%, средняя мозговая артерия - 16-20%, вертебрально-базилярная система - 5- 15%. Множественные аневризмы встречаются в 20% наблюдений.
Этиология и патогенез
Примерно в половине наблюдений причиной внутричерепного кровоизлияния являются артериальные аневризмы сосудов головного мозга. Они бывают врожденными и приобретенными. В переводе с греческого «аневризма» означает «расширяю». Внешне она часто имеет вид мешочка, в котором различают шейку, тело и дно (рис. 7-8). Обычно диаметр сосудистого мешка колеблется от нескольких мил-
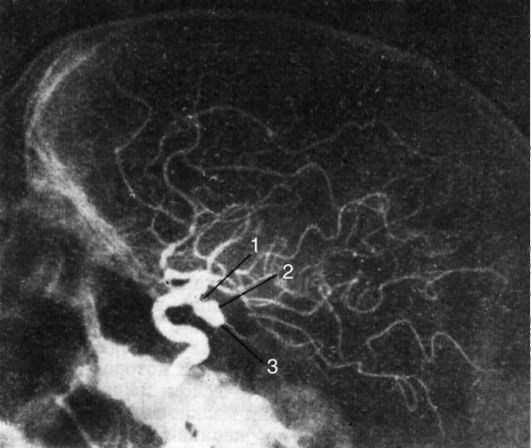 Рис. 7-8. Артериальная мешотчатая аневризма в каротидном бассейне:
Рис. 7-8. Артериальная мешотчатая аневризма в каротидном бассейне:
1 - шейка аневризмы;
2 - тело аневризмы; 3 - дно аневризмы
лиметров до 2 см. Аневризмы более 2 см в диаметре считают гигантскими. Встречаются одинаково часто у мужчин и женщин.
Разрывы аневризм обычно происходят в возрасте от 30 до 50 лет (примерно, в 91% наблюдений). Неразорвавшиеся аневризмы находят у 7-8%, а бессимптомные - у 0,5% больных. При первом разрыве аневризмы летальность составляет более 40%, после второго эпизода разрыва она достигает 42%.
Разрыв аневризмы почти всегда происходит в области её дна, где при микроскопическом исследовании нередко можно увидеть точечные отверстия, прикрытые тромботическими массами.
Клиническая картина
В клиническом течении аневризм головного мозга выделяют три периода: догеморрагический, геморрагический и постгеморрагический. У половины больных с аневризмами головного мозга заболевание в догеморрагическом периоде никак не проявляется. У других больных в этом периоде может возникать локальная головная боль в области лба, глазниц (по типу мигрени). Бывают эпизоды головной боли с менингеальными симптомами (от нескольких часов до 1-2 сут). Эти симптомы чаще появляются у людей старше 40 лет, и таким больным нередко ставят диагноз «офтальмоплегическая мигрень». Другими проявлениями могут быть эпилептические припадки неясного генеза,
а также симптомы, обусловленные поражением II, III и V пар черепных нервов.
Геморрагический период длится 3-5 нед после разрыва аневризмы. Клиническая картина зависит от локализации разорвавшейся аневризмы.
■ При разрыве супраклиноидной аневризмы возникает характерный для поражения глазодвигательного нерва (III пары) синдром верхней глазничной щели: птоз, расширение зрачка, нарушение движений глазного яблока вверх, кнутри и книзу, локальные боли в лобно-орбитальной области, центральная скотома в поле зрения, иногда слепота.
■ При разрыве аневризмы передней мозговой или передней соединительной артерии появляются расстройства сознания, нарушения психики, моторная афазия, парезы дистальных отделов нижней конечности с одной стороны, симптом Бабинского.
■ Разрыв аневризмы средней мозговой артерии сопровождается гемипарезом (гемиплегией), гемианестезией, зрительными и афатическими нарушениями.
■ Разрыв аневризмы вертебрально-базилярной системы характеризуется появлением общемозговых симптомов, поражением каудальной группы черепных нервов, мозжечковыми, стволовыми симптомами с нарушением дыхания, вплоть до его остановки.
Лечение
В 1931 г. английский нейрохирург Дот (Dott) впервые окутал аневризму мышцей, а в 1937 г. Денди (Dendy) клипировал шейку аневризмы с благоприятным результатом. Первые операции по поводу артериальных аневризм в России были выполнены в 1959 г. в Ленинграде профессором Б.А. Самотокиным и в Минске профессором Е.И. Злотником.
Операции на артериальной аневризме производят транскраниальным доступом. Расположение трепанационного окна определяется локализацией аневризмы. Для подхода к аневризме передней мозговой - передней соединительной артерии, супраклиноидному отделу внутренней сонной артерии и к начальным отделам средней мозговой артерии используется лобно-височный доступ. Аневризма выделяется из арахноидальных спаек, после чего на ее шейку накладывается клипс (рис. 7-9). Это транскраниальное оперативное вмешательство
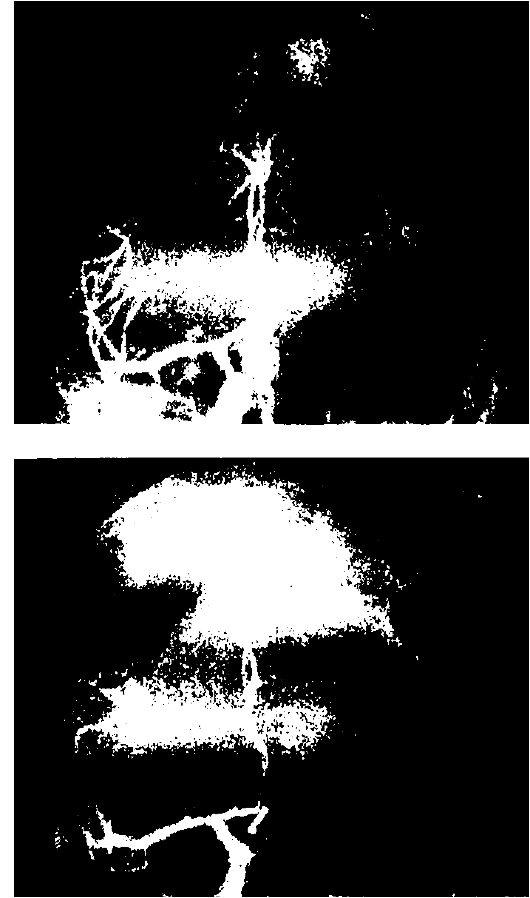 Рис. 7-9. Клипирование
шейки аневризмы: а - до операции; видна большая аневризма передней
соединительной артерии; б - после операции; видна клипса, наложенная на
шейку аневризмы; кровоток в артериях сохранен
Рис. 7-9. Клипирование
шейки аневризмы: а - до операции; видна большая аневризма передней
соединительной артерии; б - после операции; видна клипса, наложенная на
шейку аневризмы; кровоток в артериях сохранен
производится в первые, но не позже вторых суток после разрыва аневризмы. Если в этот период операция не произведена, то следующим сроком для оперативного вмешательства будут пятая и последующие недели после разрыва аневризмы.
В 70-е годы ХХ столетия профессор А.Ф. Сербиненко предложил новый метод лечения артериальных аневризм, получивший название баллонизации. Метод предполагает чрезкожную пункцию иглой внутренней или общей сонной артерий. Через эту иглу в сосуд вводят фторопластовый катетер со сбрасываемым баллоном на конце, который заводят в мешотчатую аневризму под контролем рентгеноскопии. После застывания введенного в баллон силикона, баллон сбрасывают и извлекают катетер. Данная методика позволяет выключить аневризму из кровообращения. Последний метод лечения получил
широкое распространение во всех нейрохирургических клиниках мира (рис. 7-10).
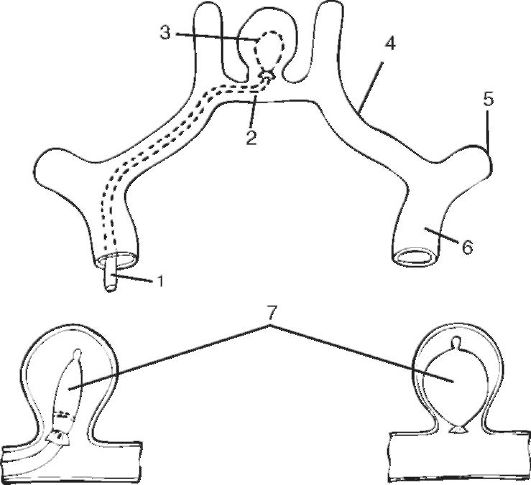 Рис. 7-10. Окклюзия
аневризмы баллоном: 1 - катетер; 2 - передняя соединительная артерия; 3
- аневризма; 4 - передняя мозговая артерия; 5 - средняя мозговая
артерия; 6 - внутренняя сонная артерия; 7 - баллон
Рис. 7-10. Окклюзия
аневризмы баллоном: 1 - катетер; 2 - передняя соединительная артерия; 3
- аневризма; 4 - передняя мозговая артерия; 5 - средняя мозговая
артерия; 6 - внутренняя сонная артерия; 7 - баллон
В 80-е годы XX в. предложена более совершенная методика окклюзии мешотчатых аневризм - с помощью койлов (спиралей).
Прогноз
Статистика результатов лечения аневризм сосудов головного мозга показала, что летальность после хирургического вмешательства с выключением аневризмы находится в пределах от 8 до 28%, а у больных, получавших только медикаментозное лечение, - 42%.
АРТЕРИОВЕНОЗНЫЕ МАЛЬФОРМАЦИИ ГОЛОВНОГО МОЗГА
АВМ (аневризмы) - это сосудистые аномалии в виде клубка патологических сосудов разного диаметра. Капиллярная сеть в них отсутствует. В артериовенозной аневризме различают сосуды притока, изменённые патологические сосуды и сосуды оттока. Как правило, насчитывается 1-4 сосуда оттока (сброса) крови (рис. 7-11).
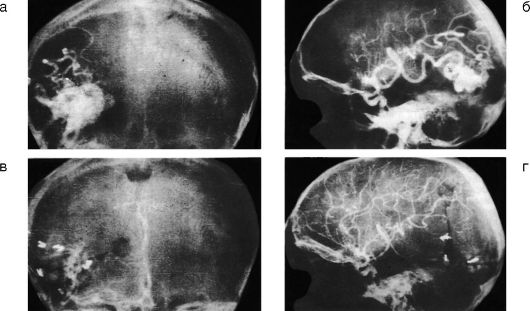 Рис. 7-11. Артериовенозная мальформация правой затылочной доли. Каротидная ангиография: а, б - до операции; в, г - после операции
Рис. 7-11. Артериовенозная мальформация правой затылочной доли. Каротидная ангиография: а, б - до операции; в, г - после операции
Артериовенозные аневризмы чаще всего локализуются в бассейне средней мозговой артерии на стыке лобной, теменной и височной долей. В процессе развития в сосудистую сеть мальформации вовлекается все большее количество сосудов.
Патогенез
Кровоток в аневризме повышен в связи с отсутствием имеющегося в нормальных условиях капиллярного сопротивления. В результате повышенного кровотока через артериовенозное соустье (шунты) происходит обкрадывание участков мозга, которые кровоснабжаются артериями, питающими артериовенозную аневризму. Кровь, поступившая в бассейн аневризмы, быстро сбрасывается в синусы мозга и покидает их. Получающая недостаточное питание мозговая ткань подвергается гипоксии, что приводит к появлению неврологических симптомов выпадения и раздражения.
Клиническая картина
Часто проявлением заболевания становятся эпилептические припадки как результат гипоксии и раздражения мозга самой аневризмой.
Второй вариант течения АВМ - разрыв аневризмы. Клинически этот тип проявляется паренхиматозно-субарахноидальным кровоизлиянием. Поскольку давление крови в сосудах аневризмы относительно невысокое, то вентрикулярно-паренхиматозный тип кровоизлияния встречается довольно редко.
Первые проявления заболевания возникают в детском возрасте - 8- 14 лет. Как правило, это эпилептические припадки. Разрыв мальформации чаще происходит в возрасте 18 лет и старше. Клиническая картина заболевания в этом случае идентична возникающей при разрыве артериальной аневризмы, но протекает несколько мягче и благоприятнее.
Диагностика
Для диагностики данной патологии необходим тщательный сбор анамнеза, динамики клинической картины, проведение ангиографии с исследованием нескольких артериальных бассейнов, КТ, МРТ с сосудистой программой и ПЭТ. Обязательным является проведение люмбальной пункции, при которой выявляется субарахноидальное кровоизлияние.
Дифференциальная диагностика заболевания должна проводиться с разрывом артериальной аневризмы, опухолью головного мозга, менингитом, менингоэнцефалитом и эпилепсией.
Лечение
Хирургическое лечение АВМ заключается в поэтапном, пофрагментном выключении питающих мальформацию артериальных сосудов и сосудов оттока через транскраниальный доступ с последуюшим поэтапным удалением образования (рис. 7-12).
Как отдельный метод лечения, а также как этап комплексного лечения применяют эмболизацию сосудов артериовенозной аневризмы полистироловыми, металлическими и другими эмболами. Неоднократное повторение (2-3 раза) этой процедуры позволяет уменьшить объём мальформации, произвести при необходимости транскраниальную операцию или облучение мальформации протонным пучком. Такая тактика позволяет добиться полного излечения или облегчить состояние больного.
Небольшие околостволовые артериовенозные аневризмы, которые не могут быть эмболизированы или удалены транскраниальным доступом, подвергают облучению протонным пучком.
Медикаментозное лечение соответствует таковому при разрыве артериальной аневризмы, которое было представлено выше.
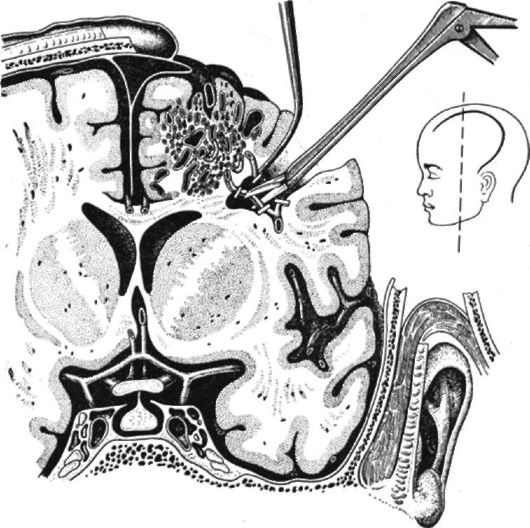 Рис. 7-12. Удаление артериовенозной мальформации. Клипирование приводящих артерий
Рис. 7-12. Удаление артериовенозной мальформации. Клипирование приводящих артерий
Прогноз
Послеоперационная летальность при этой патологии в настоящее время составляет 3-15%, а при консервативной терапии - 40-45%.
КАРОТИДНО-КАВЕРНОЗНОЕ СОУСТЬЕ
Этиология и патогенез
Каротидно-кавернозное соустье - это анастомоз между внутренней сонной артерией и кавернозным синусом. Наиболее частая причина данного заболевания - черепно-мозговая травма. Значительно реже возникновение соустья бывает обусловлено разрывом артериальной аневризмы кавернозной части внутренней сонной артерии, врожденным каротидно-базилярным анастомозом, повреждением внутренней сонной артерии во время операции. Образовавшееся соустье между сонной артерией и кавернозным синусом вызывает расширение синуса, застой крови в венах глазницы и мягких тканей лица.
Клиническая картина
Основные клинические проявления заболевания - пульсирующий экзофтальм, гиперемия склеры, расширение сосудов склеры и
мягких тканей лица со стороны соустья, хемоз, пульсирующий шум на стороне экзофтальма, синхронный с пульсом. Больные отмечают головную боль в лобно-височной области, ухудшение зрения, нарушение движений глазного яблока. Очень важный симптом - систолический шум выше уровня соустья, исчезающий при сдавлении внутренней сонной артерии на шее со стороны патологии и возникающий вновь при прекращении сдавления. Этот шум ощущает сам больной и обнаруживает при аускультации врач. Проявления заболевания со временем нарастают, а из-за наличия анастомозов между кавернозными синусами симптомы могут возникать и на противоположной стороне.
Диагностика
Диагностика заболевания возможна на основании тщательного изучения анамнеза больного, динамики развития симптомов заболевания, краниографического, ангиографического исследований, МРТ с сосудистой программой.
Дифференциальную диагностику следует проводить с опухолью глазницы, аневризмой кавернозной части внутренней сонной артерии, тиреотоксикозом.
Лечение
Для лечения этой патологии до 70-х годов ХХ в. применяли перевязку внутренней сонной артерии на шее и её интракраниальное выключение ниже отхождения глазничной артерии. В настоящее время применяют баллонизацию кавернозного синуса с помощью сбрасываемых баллонов (рис. 7-13) и окклюзию кавернозного синуса койлами. Эти методики намного повысили эффективность хирургического лечения каротидно-кавернозного соустья.
СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ СПИННОГО МОЗГА
Кровоснабжение спинного мозга
От интракраниальной части позвоночных артерий вниз к спинному мозгу идут две передние и две задние спинно-мозговые ветви, которые кровоснабжают 2-3 верхних шейных сегмента спинного мозга. Остальные его сегменты получают кровь из 3-8 передних
и 12-16 задних радикуломедуллярных артерий (рис. 7-14). Каждая такая артерия, подходя с соответствующим корешком к спинному мозгу, делится на восходящую и нисходящую ветви. Эти ветви соединяются с соседними радикуломедуллярными артериями и формируют вдоль спинного мозга три продольные анастомотические цепочки: на передней поверхности спинного мозга формируется передняя спинно-мозговая артерия, а на задней его поверхности - две задние спинно-мозговые артерии. В передней спинно-мозговой артерии, на уровне разделения радикуломедуллярной артерии, кровоток расходится - вниз и вверх. Из основного ствола этой анастомотической цепочки кровь направляется в глубину передней спинно-мозговой щели по бороздчатым артериям, которые отходят от неё, подобно частоколу. Эти бороздчатые (сулькокомиссуральные) артерии снабжают две вентральные трети поперечника спинного мозга: передние рога серого вещества, передние и боковые канатики, переднюю спайку, центральное вещество спинного мозга, основание задних рогов. Задняя спинно-мозговая артерия питает задний канатик, задний рог и частично задние отделы бокового канатика. Между передней и задними спинно-мозговыми артериями на поверхности спинного мозга имеются поперечные анастомозы - окружные артерии. От них в поверхностные слои проводниковых систем мозга также отходят погружные веточки, которые на поперечном срезе спинного мозга выглядят как «сосудистый венец».
Хотя уровни вхождения радикуломедуллярных артерий в позвоночный канал весьма вариабельны, интрамедуллярное ветвление сосудов достаточно постоянно. Именно это позволяет по клиническим проявлениям довольно четко локализовать уровень поражения спинного мозга. Если симптомы возникают остро и соответствуют зоне васкуляризации одной из артерий (интрамедуллярных, экстра-
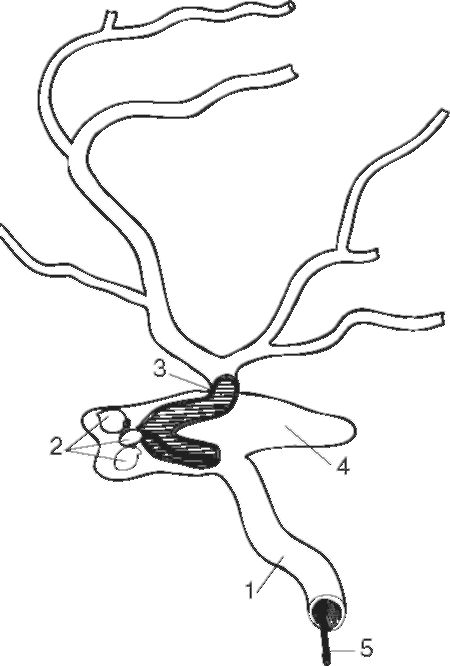 Рис. 7-13. Выключение
каротидно-кавернозного соустья сбрасываемыми баллонами: 1 - внутренняя
сонная артерия; 2 - баллоны; 3 - внутренняя сонная артерия (срез);
Рис. 7-13. Выключение
каротидно-кавернозного соустья сбрасываемыми баллонами: 1 - внутренняя
сонная артерия; 2 - баллоны; 3 - внутренняя сонная артерия (срез);
4 - кавернозный синус;
5 - катетер со сбрасываемыми баллонами
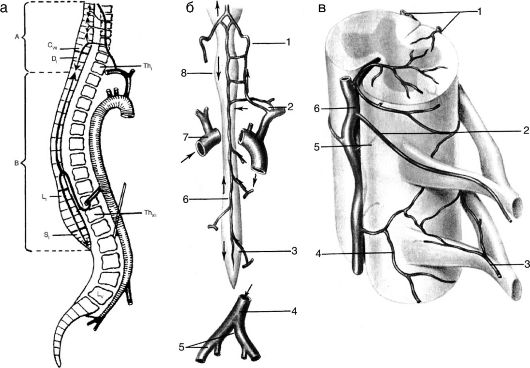 Рис. 7-14. Кровоснабжение
спинного мозга: а - схема кровоснабжения; б - артерии спинного мозга: 1
- позвоночная артерия; 2 - ветвь от реберношейного ствола; 3 - артерия
Адамкевича; 4 - передняя спинномозговая артерия; 5 - дуга аорты; 6 -
передняя спинномозговая артерия; 7 - дуга аорты; 8 - шейное утолщение
спинного мозга; в - кровоснабжение сегмента спинного мозга: 1 -
задние спинномозговые артерии; 2 - радикуломедуллярная артерия; 3 -
корешковая артерия; 4 - пиальная сосудистая сеть; 5 - передние
бороздчатые артерии; 6 - передняя спинномозговая артерия
Рис. 7-14. Кровоснабжение
спинного мозга: а - схема кровоснабжения; б - артерии спинного мозга: 1
- позвоночная артерия; 2 - ветвь от реберношейного ствола; 3 - артерия
Адамкевича; 4 - передняя спинномозговая артерия; 5 - дуга аорты; 6 -
передняя спинномозговая артерия; 7 - дуга аорты; 8 - шейное утолщение
спинного мозга; в - кровоснабжение сегмента спинного мозга: 1 -
задние спинномозговые артерии; 2 - радикуломедуллярная артерия; 3 -
корешковая артерия; 4 - пиальная сосудистая сеть; 5 - передние
бороздчатые артерии; 6 - передняя спинномозговая артерия
медуллярных, перимедуллярных), то по клиническим данным удаёт- ся диагностировать сосудистое поражение тех или иных сегментов спинного мозга.
Этиология и патогенез
Патогенетические факторы, приводящие к нарушению спинномозгового кровообращения, принято разделять на три группы:
• поражения самой сосудистой системы спинного мозга (врож- дённые - сосудистые мальформации, гипоплазии, коарктация аорты и приобретённые - васкулиты, атеросклероз);
• сдавление снабжающих спинной мозг сосудов на любом участке кровотока от аорты до интрамедуллярных разветвлений (сдав-
• ление аорты и её ветвей беременной маткой, парааортальными увеличенными лимфатическими узлами; компрессия радикуломедуллярных артерий грыжей диска, опухолью, фрагментами перелома позвонка, рубцово-спаечным процессом и т.п.) ятрогенные поражения сосудистой системы спинного мозга, т.е. осложнения различных врачебных мероприятий (аортографии, ламинэктомии с пересечением корешков, различных блокад с введением лекарственных средств в эпидуральную клетчатку, перидуральной спинальной анестезии, грубых приёмов мануальной терапии и др.).
Клиническая картина
При закупорке передней спинно-мозговой артерии ишемия развивается в вентральных двух третях поперечника спинного мозга, что проявляется синдромом Преображенского: нижний смешанный парапарез, проводниковая параанестезия диссоциированного типа (выпадает болевая и температурная чувствительность, но сохраняются суставно-мышечное, тактильное и вибрационное чувство, которые проводятся задними канатиками, получающими кровь из системы задних спинальных артерий), нарушение контроля сфинктеров тазовых органов. Классический синдром Преображенского описан при ишемии грудных и верхнепоясничных сегментов.
При закупорке передней радикуломедуллярной артерии поясничного утолщения развивается синдром Станиловского-Танона, при котором, в отличие от синдрома Преображенского, нижний парапарез вялый, периферический.
При ишемии в передней радикуломедуллярной артерии шейного утолщения развивается вялый верхний и спастический нижний парапарез (сочетанный тетрапарез).
Ишемия может локализоваться и в небольшой зоне бассейна передней спинальной артерии: в области передних рогов - в таком случае развивается клиническая картина полиомиелоишемии (периферические парезы миотомов); в области вокруг центрального канала (сирингомиелический синдром); в одной половине поперечника спинного мозга, правой или левой (ишемический синдром Броун-Секара); в боковых канатиках спинного мозга и передних рогах (ишемический синдром бокового амиотрофического склероза).
При закупорке задней спинальной артерии развивается синдром Уиллиамсона: сенситивная атаксия, снижение сегментарного глубокого рефлекса, симптом Бабинского.
В 10-12% случаев спинального инсульта ишемия поражает практически весь поперечник спинного мозга с соответствующей клинической картиной, которая зависит от локализации ишемии по длиннику спинного мозга: шейные сегменты, грудные, поясничные, пояснично-крестцовые.
Лечение
Нейрохирургические вмешательства требуются при нарушениях спинно-мозгового кровообращения вследствие врожденных артериовенозных аневризм и различных компрессионных факторов, таких, как грыжи межпозвонковых дисков, опухоли и опухолевидные заболевания.
Лечение миелоишемий
Лечение больных с острым ишемическим инсультом спинного мозга проводится поэтапно.
Первый этап - специализированная неврологическая скорая помощь. В первые минуты и часы острейшего периода ишемического инсульта пациентам вводят спазмолитические, улучшающие коллатеральное кровообращение, антиагреганты, нейропротекторы, ноотропные, витаминные препараты. При наличии интенсивных болевых ощущений и резких парестезий применяются анальгетики и транквилизаторы.
Второй этап - специализированное лечение в неврологическом либо нейрохирургическом стационаре или в палате интенсивной терапии. Здесь больной находится в остром периоде болезни. Вводят спазмолитические и улучшающие коллатеральное кровообращение и микроциркуляцию средства, антикоагулянты, препараты, улучшающие сердечно-сосудистую деятельность, ноотропы, нейропротекторы, миорелаксанты и др.
Важное значение следует придавать уходу за больным. Из-за постельного режима и выключения функции спинного мозга очень быстро могут присоединиться пролежни и гипостатическая пневмония. Поэтому постель должна быть идеально гладкой и чистой, следует поворачивать
больного на бок через каждые 1-1,5 ч, кожу спины протирать камфорным спиртом* или резорцино-салициловым спиртовым раствором*, проводить сеансы ультрафиолетового облучения субэритемными дозами, под крестец и пятки подкладывать мягкие резиновые круги.
Лечение положением, т. е. особой укладкой паретичных конечностей, проводят с первых дней спинального инсульта. Ноги сгибаются в коленных суставах под углом 15-20°, под колени подкладывают валики из марли и ваты. При помощи специального приспособления стопам придают положение тыльного сгибания под прямым углом. Пассивная гимнастика и лёгкий массаж начинаются одновременно с лечением положением.
Для устранения гипостатических явлений в легких проводится дыхательная гимнастика по 5 мин через каждый час. При появлении клинических признаков гипостатической пневмонии назначаются антимикробные средства.
Много внимания приходится уделять обеспечению функций тазовых органов. При недержании мочи приспосабливаются мочеприемники, а при задержке мочи проводится катетеризация мочевого пузыря с последующим промыванием его антисептическими растворами или устанавливается система Манро. Иногда приходится накладывать надлобковый свищ. Очистительные клизмы необходимо проводить ежедневно.
Для профилактики тромбофлебита (флеботромбоза) в нижних конечностях и в венах малого таза рекомендуются пассивная гимнастика ног, возвышенное их положение и легкий массаж (при отсутствии варикозного расширения поверхностных вен голеней и бедер).
Наряду с активным лечением, направленным на компенсацию ишемических явлений в спинном мозгу, больные подвергаются детальному исследованию. Проводится рентгенография позвоночника (включая томографию), пневмомиелография или изотопомиелометрия, флебоспондилография, сцинтиграфия, селективная спинальная ангиография, КТ поперечника позвоночника и спинного мозга и т.п. При уточнении этиологии ишемического или геморрагического спинального инсульта определяется дальнейшая лечебная тактика, направленная на радикальное устранение причины заболевания. Это может быть комплекс медикаментозных и физиопроцедурных мероприятий или же хирургическое лечение (при компрессионном характере спинального инсульта или сосудистой мальформации).
Третий этап (в неврологическом стационаре) - лечение в раннем восстановительном периоде. Продолжается введение сосудорасширяющих препаратов, преимущественно пероральным путем. Хороший эффект дают сеансы гипербарической оксигенации, сеансы массажа шеи, спины, поясницы, конечностей, а также лечебная физкультура.
Четвертый этап - лечение в специализированном реабилитационном центре. Больной продолжает принимать препараты, улучшающие мозговой метаболизм, антиагреганты, сосудорасширяющие препараты. Главное внимание на этом этапе уделяется немедикаментозным терапевтическим воздействиям: лечебной физкультуре, массажу мышц, физиопроцедурам, бальнеопроцедурам (жемчужные, сероводородные, радоновые ванны, подводный массаж, плавание).
Пятый этап - лечение в реабилитационном кабинете поликлиники. Здесь больной получает комплекс поддерживающих терапевтических мероприятий, закрепляющих эффект, полученный на предыдущих этапах лечения. Продолжают лечебную физкультуру, массаж. При необходимости проводится лечение иглоукалыванием, вводятся препараты, снижающие активность синапсов (понижающие мышечный тонус, снижающие глубокие рефлексы). В последующем больные находятся на диспансерном наблюдении, получают повторные курсы вазоактивных препаратов, улучшающих метаболизм нервной ткани, витамины. При нормализации функций тазовых органов и имеющихся резидуальных явлений нарушения функции спинного мозга проводится лечение в специализированных санаториях (Евпатория, Саки, Пятигорск, Белокуриха и др.).
При компрессионной природе ишемического инсульта лечебные мероприятия уже на втором этапе (и по возможности раньше) направляются на устранение сдавления. Наиболее частой причиной компрессии корешков и радикуломедуллярных артерий оказывается грыжа межпозвонкового диска. В таких случаях применяется весь комплекс лечебных мероприятий, назначаемых при спонлилогенных поражениях нервной системы (постельный режим на твердом ложе, вытяжение позвоночника, массаж, лечебная физкультура, дегидратаппонные и противогистаминные препараты, физиопроцедуры, а также хирургическое лечение - удаление грыжи диска). Хирургическое лечение показано также при сдавлении сосудов опухолью или отломками позвонка.
В целях улучшения микроциркуляции в ишемизированной зоне спинного мозга применяется трансплантация сальника. Проводят оперативные вмешательства по декомпрессии позвоночных и радикуломедуллярных артерий.
Для лечения болезненных спазмов мышц нижних конечностей при инфаркте спинного мозга с положительным эффектом применяли ботулиновый токсин типа А.
При геморрагическом характере спинального инсульта (гематомиелия, гематораксис) в первые часы и сутки вводятся коагулянты (менадиона натрия бисульфит, аминокапроновая кислота, этамзилат и др.).
Вместе с тем в связи с возможностью возникновения гиперкоагуляционного синдрома и ухудшения условий микроциркуляции коагулянты применяются не более 2-3 сут. При отсутствии признаков повторного кровотечения подключают введение противоотечных и вазоспастических препаратов, витаминов, особенно аскорбиновой кислоты. Спустя две недели рекомендуется начинать легкую лечебную физкультуру в постели.
При спинальной субарахноидальной геморрагии постельный режим без физических напряжений назначается на 8-10 нед - время, необходимое для организации тромба (прорастания его соединительнотканными элементами), с целью предупреждения повторного кровотечения в месте первого разрыва сосуда.
Прогноз
Улучшение состояния больного в послеоперационном периоде наступает примерно в 20% случаев. У большинства оперированных больных, подвергшихся декомпрессивной ламинэктомии, определялось быстрое ухудшение в 40% случаев. Главным фактором является время начала лечения. Начинать лечить необходимо как можно быстрее, желательно в той стадии, когда любой неврологический дефицит еще может регрессировать. Летальный исход наступает в 8-9% случаев. Непосредственной причиной смерти являются острая сердечнососудистая недостаточность, паралич дыхания спинального генеза, тромбоз и разрыв аорты, уросепсис, кахексия при злокачественных новообразованиях, присоединение воспаления легких.
Нетравматическая спинальная субарахноидальная геморрагия или гематомиелия развиваются обычно на почве сосудистых мальформаций.
АРТЕРИОВЕНОЗНЫЕ МАЛЬФОРМАЦИИ СОСУДОВ СПИННОГО МОЗГА
Эпидемиология
АВМ составляют 4-5% всех объёмных процессов в позвоночном канале. У мужчин АВМ встречаются в два раза чаще, чем у женщин. Заболевание может возникнуть в любом возрасте, но в 80% случаев оно манифестирует в возрасте от 20 до 60 лет.
Историческая справка
Первое сообщение об АВМ спинного мозга было представлено О. Хебольдом (1885), который дал подробное описание острой гематомиелии и поперечного поражения спинного мозга у девочки с развитием соответствующих синдромов. Заболевание закончилось летальным исходом, автор сумел при аутопсии увидеть причину гематомиелии. Первое подробное описание «артеривенозной фистулы» было сделано Ф. Брашем в 1900 г. Первое хирургическое описание АВМ спинного мозга, несмотря на неудовлетворительные результаты после операции, сделал Ф. Краузев 1910 г., а первую успешную операцию на спинном мозге по поводу АВМ произвел К. Эльсберг в 1916 г.
Этиология и патогенез
АВМ - аномалии сосудистой системы, состоящие в сохранении имеющихся в эмбриональном периоде многочисленных прямых связей между артериями и венами. Артерии и вены образуют артериовенозные мальформации (АВМ). Стенки этих сосудов так атипичны и деформированы, что даже микроскопически их разграничение весьма затруднительно. АВМ спинного мозга встречаются в 10,7% среди всех АВМ. У 79% больных они локализуются на грудном и поясничном уровнях спинного мозга. В среднем мальформация располагается на уровне четырёх-пяти сегментов, иногда в процесс вовлекается и большее их число.
Заболевание может проявиться в любом возрасте, но наиболее часто - между 40 и 50 годами. Первые клинические проявления спинного мозга возникают у 50% больных в возрасте до 30 лет. Средняя продолжительность развертывания клинических симптомов до специфического лечения составляет около 10 лет.
Классификация
Все аневризмы и гемангиомы спинного мозга можно разделить по анатомо-топографическим признакам на пять видов.
■ Интрамедуллярные АВМ частично или тотально расположены в спинном мозге. Кровоснабжение и дренирование осуществляется спинальными сосудами.
■ Экстраперимедуллярные АВМ (фистулы) расположены на поверхности спинного мозга. Кровоснабжение подобных мальформаций может происходить из передней, задних и радикулярных артерий, отток происходит по одноименным венам.
■ Экстра(ретро)медуллярные АВМ - редкая форма. Кровоснабжаются из задней спинальной артерии или задних корешковых ветвей.
■ Интрадуральные артериовенозные фистулы локализуются в твердой мозговой оболочке. Кровоснабжение осуществляется из корешковых артерий. Отток происходит исключительно по спинальным венам.
■ Медуллярные, перимедуллярные, дуральные, эпидуральные, мышечные и позвонковые гемангиобластомы. Кровоснабжение геманглиобластом перечисленных локализаций происходит из спинальных, оболочечных, корешковых и мышечных сосудов. Отток осуществляется по спинальным экстрамедуллярным венам. Общим для всех мальформаций выступает наличие шунта или
фистулы и существование афферентных и эфферентных сосудов. Они отличаются локализацией по длиннику, периметру и поперечнику спинного мозга, размерами и характером гемодинамики.
К первому типу относят АВМ с пучком патологических сосудов и дренажной веной, которые имеют обычно значительную протяженность. При этом типе имеется один или два гипертрофированных афферентных сосуда. Артериовенозный шунт расположен обычно на определенном расстоянии от начала афферентного сосуда. Отток из аневризмы может осуществляться в двух направлениях сразу по нескольким венам или по единственной вене спинного мозга.
При малом диаметре афферентного сосуда лечение таких аневризм должно быть оперативным. Если размеры сосудов позволяют провести через них тромбирующие агенты, то показана эмболизация. Чаще всего аневризмы этого типа кровоснабжаются из передней, задних спинальных артерий или большой радикуломедуллярной артерии.
Ко второму типу относят АВМ с клубком компактных сосудов, имеющие мелкопетлистое строение. В этом сосудистом клубке обыч-
но трудно определить артериовенозные шунты. Кровоснабжение аневризмы может осуществляться из нескольких или одной радикуломедуллярной артерии. Независимо от расположения, аневризмы экстраинтрамедуллярной локализации имеют венозные шунты и разной величины расширения, из которых происходят кровотечения.
Аневризмы второго типа располагаются на задней поверхности спинного мозга и вентрально. В некоторых случаях эти аневризмы имеют длинные дренажные вены. Гломусного типа АВМ могут располагаться интра- и экстрамедуллярно. Афферентный сосуд (артерия Адамкевича) приобретает большие размеры с фузиформными расширениями, напоминающими артериальные аневризмы. Лечение этих форм АВМ эндоваскулярное и хирургическое.
К третьему типу отнесли большие АВМ спинного мозга, имеющие крупные питающие сосуды и дренажные вены. Эти распространенные мальформации встречаются редко и, вследствие крупных размеров, их называют незрелыми или ювенильными мальформациями. Этот тип мальформации отличается от других форм усиленным кровотоком через все отделы, большими размерами и перимедуллярным распространением. При аускультации выслушивается характерный систолический шум. Частые субарахноидальные кровоизлияния и большие размеры АВМ приводят к развитию параличей.
К четвертому типу отнесли АВМ, в которых наблюдалось прямое артериовенозное шунтирование без наличия включенных в сеть мелких сосудов. Артерия и вена соединяются между собой по аналогии с хирургическим анастомозом «конец в конец», «конец в бок».
Клиническая картина
Поражения спинного мозга при АВМ развиваются вследствие субарахноидального кровоизлияния, псевдотуморозного воздействия или тромбирования сосудов аневризмы. При этом возникают и разнообразные клинические синдромы.
До настоящего времени распознавание спинальных сосудистых аномалий остается трудным: вследствие сходства клинической картины их часто принимают за опухоли или рассеянный склероз. Одним из первых клинических проявлений болезни считается корешковая боль. Возникновение этой боли связывают с давлением расширенных сосудов на задние корешки или с тромбозом вен.
Боли в конечностях усиливаются в ночное время, после горячей ванны или курортного лечения. Боли сочетаются с нарушениями чувствительности, которая постепенно и незаметно переходит в анестезию. Углубление расстройств чувствительности наступает нередко после физических нагрузок.
Вместе с корешковой болью появляются очаговые спинальные симптомы, варьирующие в зависимости от уровня поражения. Болезнь протекает с ремиссиями и в основном имеет прогрессирующий характер.
В клинике у больных с АВМ одновременно с нарушениями в мочеполовой системе появляются расстройства походки из-за слабости ног и быстрой утомляемости, фасцикулярные подёргивания и судороги в ногах, нарушается чувствительность. С течением времени походка становится спастической или спастико-атактической. В следующей фазе болезни, продолжающейся около 2 лет с момента появления существенной слабости в конечностях, у больного развивается спастический нижний парапарез с нарушением чувствительности, нарастают расстройства тазовых органов и в конечном итоге развивается синдром поперечного поражения спинного мозга.
В редких случаях при аускультации вдоль аорты можно определить сосудистый шум аневризмы. Считают, что его удаётся выслушать при гигантских юношеских и экстраспинальных мальформациях. Изредка в диагностике сосудистых мальформаций спинного мозга помогают кожные ангиомы. Считается доказанным, что два сосудистых образования, одно - в спинном мозгу, второе - на коже, кровоснабжаются из одного артериального сосуда, т.е. метамера, хотя кровообращение у них раздельное. В дальнейшем были сообщения о сочетании АВМ спинного мозга с АВМ других локализаций - головного мозга.
Диагностика
Диагностика АВМ проводится с последовательным применением миелографии, КТ или МРТ и селективной спинальной ангиографии.
Введение в практику водорастворимых контрастных веществ улучшило диагностику АВМ на всех уровнях спинного мозга.
Контраст при миелографии, распрастраняясь по субарахноидальному пространству, обтекает вокруг и между афферентными и эфферентными сосудами образования, изображая на снимках дефект
извитых и расширенных сосудов. Такие сосуды иногда имеют симметричные изгибы и равномерную извитость, так называемый симптом «серпантинной дорожки». Последний может сочетаться с частичной задержкой контрастного вещества на уровне расположения аневризмы или с полной остановкой по типу блока (рис. 7-15). Признаки «серпантинного» сосудистого дефекта определялись в 87% случаев, в 9% наблюдений имелись признаки частичной или полной остановки контрастного вещества.
Интрамедуллярные АВМ на миелограммах также имеют червеобразной формы сосуды в виде контрастных теней. Они могут быть различной конфигурации.
Воспалительные заболевания оболочек после субарахноидального кровоизлияния диагностируются с помощью миелографии. Контрастное вещество, гомогенно заполняя субарахноидальное пространство, встречает препятствия (спайки) и временно останавливается. Постепенно оно проникает выше или ниже, задерживаясь на уровне временного препятствия, и образует на миелограммах контрастные участки различной плотности. На некоторых снимках определяются мелкие, патологически измененные сосуды на фоне неравномерного распределения контрастного вещества. Вблизи сосудистого конгломерата с частичной остановкой контрастного вещества, наряду с изображением патологических сосудов, выявляются кистозные образования, располагающиеся по ходу расширенного сосуда.
Большинство АВМ локализуется на передней и боковых поверхностях спинного мозга, поэтому следует производить снимки в двух проекциях.
Миелографическая картина при субдуральных и интрамедуллярных гемангиобластомах имеет схожие черты с АВМ. В некоторых случаях, несмотря на экстрамедуллярную и даже экстравертебральную их локализацию, на переднезадних миелограммах определяется мощный дренирующий сосуд, принадлежащий спинному мозгу. Гемангиобластому можно отличить по экскавации тел позвонков, более мелкопетлистому рисунку. Чаще чем при аневризмах наблюдается блок субарахноидального пространства на уровне локализации сосудистого конгломерата. В таких случаях приходится выполнять восходящую и нисходящую миелографию.
Таким образом, восходящая и нисходящая миелография с водорастворимыми веществами способствует установлению диагноза при АВМ спинного мозга. При миелографии устанавливается примерная
локализация процесса, проводится дифференциальная диагностика между АВМ и гемангиобластомой. Важным достоинством миелографии является выявление серьезного сопутствующего заболевания арахноидальной и мягкой мозговых оболочек - спинального арахноидита. Полученная в результате миелографии информация позволяет решить некоторые диагностические вопросы, а также выбирать оптимальные методы лечения.
МРТ имеет важное преимущество перед КТ: она полностью неинвазивна и позволяет получить срезы спинного мозга в любой плоскости.
Для исследования позвоночника выбирается режим Т1-взвешен- ные МРТ, для изображения дисков - Т2-взвешенные МРТ. Метод обладает широким спектром физических параметров, оказывающих различное влияние на яркость изображения тех или иных тканей.
Цереброспинальная жидкость в субарахноидальном пространстве хорошо отличается от спинного мозга, Т1-взвешенные МРТ показывают спинной мозг, имеющий сигнал выше, чем цереброспинальная жидкость в протонной плотности. На Т2-взвешенных МР-томограммах цереброспинальная жидкость имеет более яркий сигнал, чем спинной мозг.
Для исследования шейного, грудного и поясничного отделов спинного мозга выполняется сагиттальное сечение, позволяющее визуализировать на срезах не только медиальные структуры и перимедуллярные образования. Фронтальные срезы малоинформативны.
Сагиттальные срезы позволяют измерить переднезадний размер спинного мозга, обнаружить уровень сосудистого конгломерата и определить размеры сосудов. Сосуды на МРТ имеют линейные структуры с четко различимой стенкой и равномерно-темным сигналом, «пустым» внутри просвета. Однородность сигнала внутри просвета сосуда свидетельствует о нормальном кровотоке (кровь играет роль естественного контрастного вещества).
В режиме Т1 трудно дифференцировать вещество спинного мозга от конгломерата АВМ, потому что обе структуры издают идентичный сигнал.
При МРТ-обследовании в режиме Т2 визуализация сосудов АВМ становится более четкой. Сосуды определяются в виде извитых теней типа «серпантинной дорожки», так называемые участки отсутствия сигнала.
Тромбированные аневризмы приобретали в режиме Т2 повышенный сигнал, идентичный гемангиоме.
АВМ экстраинтрадуральной локализации могут иметь мощные дренажные вены с вовлечением вен спинного мозга и интрапаравертебральных венозных сплетений. На МРТ-снимках при данной патологии визуализируется большой «клубок сосудов» пониженного сигнала, замещая на сагиттальных срезах весь спинной мозг, субарахноидальные пространства и проникая даже несколько шире - в паравертебральное пространство.
В основном на МРТ наблюдаются три зоны изменения интенсивности сигнала внутри просвета аневризмы: зона истинного кровотока; зона турбулентных течений, имеющая более светлое окрашивание; зона тромботических масс, имеющих светлое, почти белое окрашивание.
МРТ данные позволяют в 83% случаев установить правильный диагноз, в остальных 17% случаев имеются косвенные симптомы. Анатомические исследования выявили три региона кровоснабжения спинного мозга - разделение по отделам является условным для удобства выполнения селективной спинальной ангиографии. Первый отдел - шейный и верхнегрудной (от сегмента С до DIII) - кровоснабжается из радикуломедуллярных ветвей позвоночных артерий, реберно-шейного и щитошейного стволов. Второй отдел - среднегрудной (от сегмента ThIV до ThVIII) - васкуляризируется из радикуломедуллярных ветвей межреберных артерий. Кровоснабжение третьего отдела - нижнегрудного и поясничного (с ThXI и ниже, все поясничные и сакральные сегменты) - осуществляется в основном (85%) из большой радикуломедуллярной артерии Адамкевича.
В настоящее время для исследования артериальной системы шейного отдела спинного мозга используется метод чрезбедренной артериографии по методу Сельдингера с избирательным введением контрастного вещества в позвоночную артерию, реберно-шейный и щитошейный стволы.
Для исследования грудного отдела спинного мозга предпочтение отдается селективной артериографии межреберных и поясничных артерий, которая дает надежные диагностические данные и качественное изображение.
Ангиографические признаки АВМ спинного мозга являются весьма разнообразными. Афферентные артерии могут быть множественными и единичными, отходить с одной или двух сторон. Кровоснабжающие мальформацию сосуды обычно гипертрофированы, а в некоторых случаях имеют большую протяженность - 6-7 позвонков.
АВМ спинного мозга на всех уровнях кровоснабжаются из тех же артериальных сосудов, что и спинной мозг. Иногда выявляются аномальные афферентые сосуды.
В АВМ кровоток ускорен вследствие отсутствия в них капиллярной фазы кровообращения. Так же как и в головном мозгу, важным и постоянным патофизиологическим фактором при АВМ является локальное уменьшение притока крови к спинному мозгу, обусловленное существованием артериовенозного шунта, по механизму синдрома «обкрадывания». Особенно быстро возникает клиническое ухудшение, когда прогрессивно увеличивается сброс крови через шунт в венозную систему, минуя клетки спинного мозга. Развивается вторичная ишемия вследствие резкого уменьшения кровоснабжения спинного мозга. Кроме того, спинной мозг сдавливается увеличенными извитыми дренажными венами.
Кровоток через АВМ бывает ускоренным. В этих случаях изображения патологически измененных сосудов на снимках исчезают примерно через 2-3 с ангиографического обследования. Поэтому при АВМ для получения максимальной информации необходимо выполнить наибольшее количество снимков в первые секунды обследования.
АВМ сосудов спинного мозга обычно кровоснабжаются из одной или нескольких (максимум из 6) расширенных афферентных артерий, впадающих в венозную систему в одну или несколько вен, формируя таким образом клубок патологических сосудов - мальформации различных размеров и форм. Кровоснабжающие аневризмы сосуды не имеют капиллярных сетей, как это бывает в нормальных анатомических условиях, а заканчиваются непосредственно в самой мальформации, образуя шунт с венозной системой (см. рис. 7-15).
Дренажные вены обычно многочисленнее, крупнее и состоят из нескольких ветвей. Дренажные вены АВМ бывают одиночными и множественными. Отток из АВМ может осуществляться по передней и задним спинальным венам вверх или вниз, по корешковым венам непосредственно в паравертебральные венозные коллекторы и сплетения.
Лечение
При ювенильной форме мальформации проводится только эмболизация или окклюзия афферентных сосудов баллонами. Хирургическое лечение невозможно, даже декомпрессия дает плохие результаты.
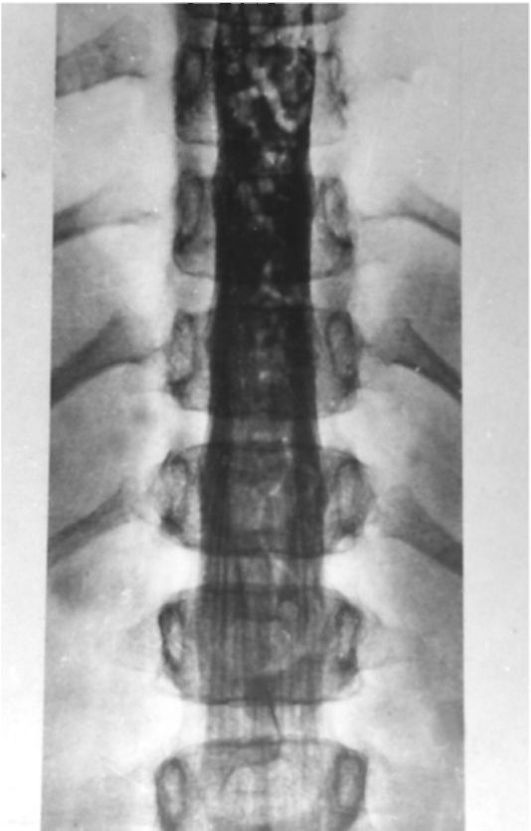 Рис. 7-15. Миелография при артериовенозной мальформации спинного мозга. «Серпантинная дорожка»
Рис. 7-15. Миелография при артериовенозной мальформации спинного мозга. «Серпантинная дорожка»
К настоящему времени самый большой опыт диагностики с помощью селективной спинальной ангиографии и лечения эндоваскулярной эмболизацией имеет профессор Т.П. Тиссен (Москва).
Интрамедуллярные АВМ (ангиомы) раньше считались неоперабельными. Однако в связи с применением микрохирургической техники стало возможным и их лечение.
В нашей стране такими вмешательствами являются ламинэктомия с клипированием или удалением сосудистой мальформации, а в последние годы разработаны эндоваскулярные приемы выключения аневризмы из кровотока: эмболизация аневризмы холестериловыми эмболами и заполнение аневризмы сбрасываемыми баллонами (рис. 7-16).
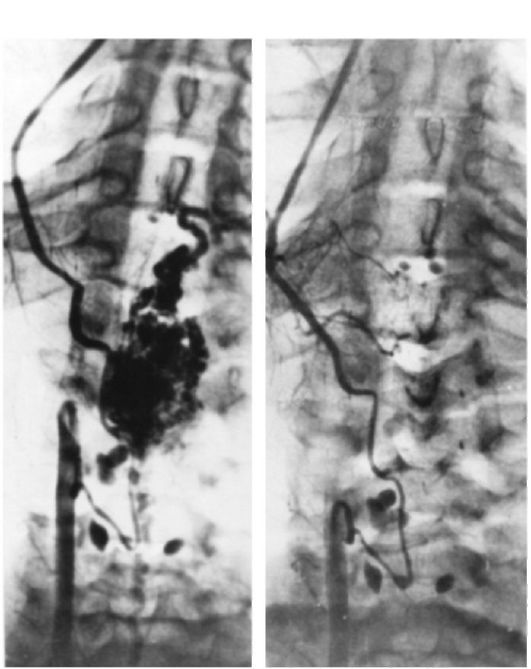 Рис. 7-16. Артериовенозная мальформация спинного мозга. Ангиографическое исследование: а - до операции; б - после операции.
Рис. 7-16. Артериовенозная мальформация спинного мозга. Ангиографическое исследование: а - до операции; б - после операции.
Хирургическое лечение артериовенозных мальформации и сосудистых опухолей спинного мозга
Большинство нейрохирургов прибегают к декомпрессивной ламинэктомии, которая приводит к уменьшению корешковых болей, ликвидации псевдотуморозного влияния мальформаций на структуры спинного мозга.