Нейрохирургия: учебник. - 2-е изд., перераб. и доп. -С.В. Можаев, А.А. Скоромец, Т.А. Скоромец. 2009. - 480 с. : ил.
|
|
|
|
ГЛАВА 4. МЕТОДИКИ ОПЕРАТИВНОГО ВМЕШАТЕЛЬСТВА НА ЧЕРЕПЕ И ПОЗВОНОЧНИКЕ
ПОКАЗАНИЯ И ПРОТИВОПОКАЗАНИЯ К НЕЙРОХИРУРГИЧЕСКОЙ ОПЕРАЦИИ
Все нейрохирургические вмешательства подразделяют на экстренные и плановые.
Под экстренными вмешательствами понимают те операции, которые требуют незамедлительного их выполнения для спасения жизни больного. Для проведения этих операций применяют необходимый минимум диагностических мероприятий.
Плановые нейрохирургические операции предполагают полный комплекс обследований, подготовку больного к операции и использование в ходе неё самых современных технических и тактических приёмов. Как правило, эти операции характеризуются радикальностью выполнения, широким использованием микрохирургических приёмов, меньшим числом осложнений и летальных исходов.
Показания к нейрохирургическому оперативному вмешательству подразделяют на абсолютные и относительные.
Абсолютные показания
К абсолютным показаниям относят все наблюдения, при которых существует угроза жизни больного в ближайший период при поступлении больного в стационар. Этими показаниями могут быть: внутричерепные гематомы, дислокационный синдром при опухолевой, сосудистой патологии, разрывы аневризм в первые 2 сут от момента разрыва, огнестрельные повреждения, выпадения грыжи диска с компрессией спинного мозга и его сосудов и другие.
Относительные показания
К относительным показаниям относят все те наблюдения, при которых заболевание само по себе не опасно для жизни, но по истече-
нии какого-то времени его осложнения могут привести к инвалидизации больного или даже к его гибели. Примером таких заболеваний могут быть аневризмы сосудов головного мозга, опухоли головного мозга, ликворные свищи с рецидивирующим менингоэнцефалитом и другие. Сюда же относят заболевания, не опасные для жизни, даже с учётом осложнений, но проявляющиеся неврологическими симптомами, излечимыми только хирургическим путём. Это могут быть дефекты костей черепа, повреждения периферических нервов, грыжи межпозвонковых дисков с нарушениями спинно-мозгового кровообращения и другие. Относительными показаниями к операции служат заболевания, основное проявление которых - боль. Например, невралгия тройничного нерва, туннельные невропатии и другие.
Принятие решения о назначении операции зависит от многих факторов: сложности операции, взаимоотношения с сосудами, подкорковыми структурами, стволом, функционального состояния головного мозга, обширности поражения, возраста больного, возможностей развития инфекций в послеоперационном периоде, а также ожидаемого результата оперативного вмешательства.
Операции выполняют под общим обезболиванием.
В случае близости патологического процесса к важным вегетативным центрам, участвующим в регуляции кровообращения, дыхания, обмена веществ и ряда других функций, основой профилактики расстройств жизненно важных функций наряду с нейровегетативной блокадой, заместительной терапией глюкокортикоидами служит атравматичное, физиологически дозволенное с использованием микрохирургических приёмов и увеличительной оптики оперативное вмешательство. В последние годы используют адекватное анестезиологическое пособие, которое предполагает применение нейролептоаналгезии или фентанилклофелинового наркоза при постоянном клинико-физиологическом мониторинге. Всё это улучшило контроль состояния больного на всех этапах оперативного вмешательства и позволило значительно повысить результативность лечения.
Абсолютные противопоказания
К абсолютным противопоказаниям для операции в нейрохирургии относят ситуации, при которых риск вмешательства превышает ожидаемые результаты как в плане жизни, так и глубокой инвалидизации. Например, считают нецелесообразным оперировать больного,
у которого выявлены множественные метастазы как при удалённом, так и неудалённом первичном очаге. Не следует планировать проведение операции, которая сохраняла бы жизнь больного на непродолжительный период при развитии у него в послеоперационном периоде гемиплегии, тотальной афазии или слепоты. Сюда же относят наблюдения, когда хирурги не уверены, что продлят жизнь больного на более значительный срок, чем он проживёт без операции.
В нейрохирургии, так же как и в хирургии, вообще все оперативные вмешательства подразделяют на радикальные, при которых объёмное образование удаляют полностью, и оперативные вмешательства с частичным его удалением. В тех случаях, когда основное заболевание неизлечимо, но для продления жизни больного достаточно ликвидировать гипертензионно-гидроцефальный синдром, в нейрохирургии применяют ликворошунтирующие вмешательства - паллиативные операции.
В нейрохирургии широко используют реконструктивные операции на периферических нервах, сосудах, синусах, костях черепа и позвоночнике.
С 1947 г. производят стереотаксические операции, предложенные Spitgel, Wycis, Marks и Lee.
С 70-х годов ХХ в. в нейрохирургии внедрены микроскоп и микрохирургическая техника, позволившие добиться блестящих успехов, значительного снижения летальности и увеличения радикальности хирургических вмешательств.
ВИДЫ КРАНИОТОМИЙ
Вне зависимости от характера поражения мозга первоначально необходимо обеспечить к нему доступ путём вскрытия черепа или позвоночного канала.
В современной нейрохирургии существуют два метода трепанации костей свода черепа - резекционный и костно-пластический.
Резекционная трепанация
Резекционную трепанацию производят при наличии показаний к декомпрессии и в процессе первичной хирургической обработки проникающего черепно-мозгового ранения. Кость при этом удаляют на протяжении, необходимом для достижения поставленной цели.
Удаление кости осуществляют двумя способами. При одном из них кость, лишённую надкостницы, резецируют кусачками из наложенного фрезевого отверстия. Этот метод носит название резекционного. Иногда данный способ применяют для удаления участков черепа с внутрикостным ростом опухоли.
При другой разновидности этого способа выпиливают костный лоскут, который отделяют от мягких тканей (надкостницы, мышц) и затем удаляют (рис. 4-1, см. цв. вклейку). В настоящее время такой вид трепанации называют костно-пластической декомпрессивной трепанацией.
Костно-пластическая трепанация
При костно-пластической трепанации выкраивают кожно-апоневротический лоскут, затем образуют костно-надкостничный или костно-надкостнично-мышечный лоскут, которые откидывают в сторону на время манипуляций в полости черепа, а после окончания операции укладывают на место.
Трепанации черепа производят как в плановом, так и экстренном порядке. Перед операцией бреют голову, после этого кожу головы обрабатывают этиловым спиртом и накладывают повязку, смоченную 70% этиловым спиртом. На операционном столе кожу головы дважды обрабатывают спиртом, затем йодом. В настоящее время в связи с появлением новых антисептических растворов кожу головы обрабатывают этими растворами.
Обезболивание включает общее и местное - 0,5% раствором новокаина, которым инфильтрируют всю зону оперативного вмешательства, выполняя при этом также гидравлическую препаровку тканей.
В зависимости от места операции больной лежит на боку или на спине с приподнятой на 10-15° головой, что несколько уменьшает застойные явления в сосудах головы и кровопотерю. При некоторых локализациях внутричерепной патологии применяют полусидячее положение.
Краниотомия при супратенториальном расположении патологического процесса
При доступе к лобной, височной, теменной и затылочной долям применяют следующую методику. Вначале выкраивают и откидывают в сторону большой кожно-апоневротический лоскут на широком основании. При выкраивании лоскута обращают внимание на
сохранность артериальных сосудов, питающих лоскут. Необходимо, чтобы питание лоскута осуществлялось двумя, а ещё лучше тремя артериальными сосудами. В случае экстренного оперативного вмешательства используют вертикальный или подковообразный разрез кожи в височно-теменной области по Кушингу (1905) (рис. 4-2). При этих доступах края раны разводят в стороны. Кровотечение из сосудов кожи останавливают накладыванием зажимов или скобок Мишеля, которые удаляют в конце операции перед наложением кожных швов. Рассечение надкостницы осуществляют электроножом соответственно предполагаемому костно-надкостничному лоскуту. Разрезы в области височной мышцы должны сопровождаться хорошим гемостазом кровоточащих сосудов с помощью коагуляции. Распатором скелетируют кость по линии рассечения надкостницы на ширину
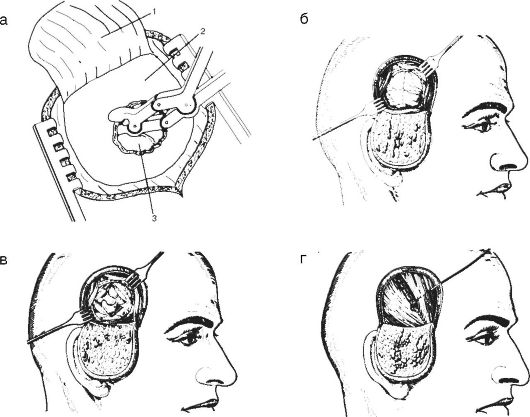 Рис. 4-2. Резекционная
подвисочная трепанация по Кушингу: а - выполняют резекцию кости из
фрезевого отверстия; б - образуют трепанационное отверстие и обнажают
твердую мозговую оболочку; в - вскрывают твёрдую мозговую оболочку; г -
послойно зашивают рану; 1 - лоскут надкостницы; 2 - кость; 3 - твёрдая
оболочка
Рис. 4-2. Резекционная
подвисочная трепанация по Кушингу: а - выполняют резекцию кости из
фрезевого отверстия; б - образуют трепанационное отверстие и обнажают
твердую мозговую оболочку; в - вскрывают твёрдую мозговую оболочку; г -
послойно зашивают рану; 1 - лоскут надкостницы; 2 - кость; 3 - твёрдая
оболочка
наносимых в последующем фрезевых отверстий. Обычно образовывают 4-6-9 фрезевых отверстий, которые соединяют между собой пропилами, оставляя неповреждённой питающую ножку мышечно-надкостничного лоскута. Некоторые нейрохирурги питающую ножку не оставляют. Для пропилов используют проводник Поленова и пилу Джильи. После образования костно-надкостничного лоскута его откидывают с помощью двух элеваторов (лопаточки Буяльского) в сторону и фиксируют к белью с помощью специальных крючков или лигатур. В настоящее время для выпиливания костно-надкостничного лоскута используют электроили пневматические трепаны. Их применение значительно облегчает и ускоряет этот этап оперативного вмешательства. При поднятии костно-надкостничного лоскута в нижних отделах височной кости может произойти повреждение средней оболочечной артерии в месте её выхода из костного канала. Если обрыв артерии не произошёл, то с помощью электрокоагуляции производят выключение этой артерии у места вхождения в костный канал. При случившемся повреждении артерии в костном канале производят её «замазывание» в нём с помощью воска. При необходимости расширения трепанационного отверстия в нижние отделы височной области дополнительно резецируют височную кость к основанию средней черепной ямки. Размеры трепанационного окна обычно достигают 6-7x8-9 см. После обнажения твёрдой мозговой оболочки её лучше рассекать П-образно основанием к верхнему сагиттальному синусу с дополнительными насечками книзу и в стороны. Обращают особое внимание на тщательную остановку кровотечения из сосудов оболочки. Недостаточный гемостаз сосудов может повлечь за собой образование в послеоперационном периоде эпи- и субдуральных гематом в области раны (рис. 4-3).
Рассечение твёрдой мозговой оболочки лучше производить после предварительного введения под её предполагаемый разрез мозгового шпателя. Появляющееся и с трудом останавливаемое кровотечение из эпидурального пространства прекращают подшиванием оболочки к надкостнице. Кровотечение из диплоических вен и эмиссарных выпускников должно быть остановлено промазыванием их воском. Наложение зажимов на сосуды твёрдой мозговой оболочки и их перевязку в нейрохирургии практически не используют. При наличии внутричерепной гипертензии для уменьшения значительного напряжения твёрдой мозговой оболочки и выраженной протрузии мозга, возникшей после её рассечения, показано внутривенное введение
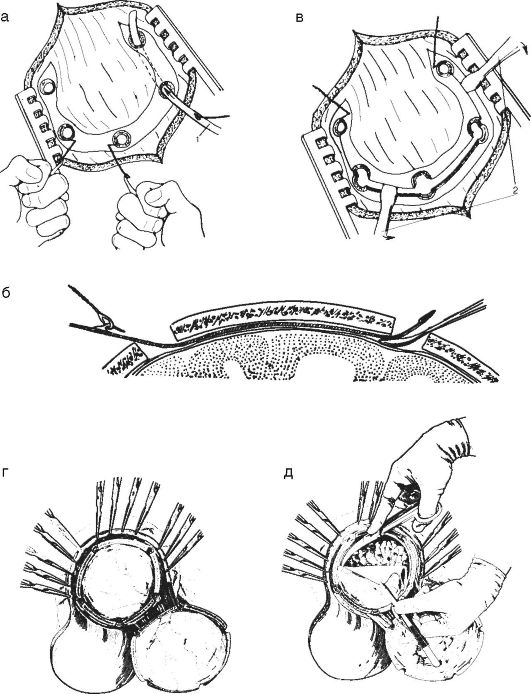 Рис. 4-3. Костно-пластическая
трепанация черепа: а, б - после выкраивания кожно-апоневротического
лоскута накладывают фрезевые отверстия, между костью и твердой оболочкой
проводят проводник с крючком, на котором надета петля проволочной пилы
Джигли; в - после выпиливания откидывают костно-пластический лоскут; г, д
- затем вскрывают твердую оболочку и обнажают кору головного мозга; 1 -
проводник; 2 - элеваторы
Рис. 4-3. Костно-пластическая
трепанация черепа: а, б - после выкраивания кожно-апоневротического
лоскута накладывают фрезевые отверстия, между костью и твердой оболочкой
проводят проводник с крючком, на котором надета петля проволочной пилы
Джигли; в - после выпиливания откидывают костно-пластический лоскут; г, д
- затем вскрывают твердую оболочку и обнажают кору головного мозга; 1 -
проводник; 2 - элеваторы
фуросемида от 40 до 60 мг. В особо тяжёлых случаях, при высокой внутричерепной гипертензии, за 1 ч до операции внутривенно вводят маннитол из расчёта 1-2 г/кг. Можно производить вентрикулярную разгрузочную пункцию переднего или заднего рога бокового желудочка в типичных местах с медленным выведением спинно-мозговой жидкости. При неосложнённом течении хирургического вмешательства твёрдая мозговая оболочка должна быть зашита наглухо. В случаях сохраняющейся внутричерепной гипертензии, при некоторых локализациях опухолей, в остром периоде черепно-мозговых травм, остром периоде разрыва артериальных аневризм, при злокачественных глиомах, выраженном отёке-набухании головного мозга твёрдую мозговую оболочку не зашивают, а дефект в ней прикрывают гемостатической губкой или в него вшивают свободный участок апоневроза, надкостницы или участок лиофилизированной твёрдой мозговой оболочки. Костный лоскут укладывают на место и фиксируют швами за надкостницу. При продолжающемся отёке-набухании головного мозга в конце операции может быть произведено удаление костного лоскута с его сохранением для последующей пластики дефекта, о чём будет сказано ниже. Наружная декомпрессия мозга может быть создана не только за счёт удаления костного лоскута, но также дополнена резекцией нижних отделов костного лоскута. Кожную рану ушивают послойно, последовательно, с предварительной остановкой кровотечения из крупных сосудов с помощью биполярной коагуляции. В мозговую рану при необходимости устанавливают трубку или мягкие резиновые выпускники. Под кожно-апоневротический лоскут также заводят резиновый выпускник. Выпускники и трубки удаляют через 1-3 сут после операции, поэтапно подтягивая их при каждой перевязке.
Краниотомия задней черепной ямки
Положение больного на операционном столе - лёжа на животе лицом вниз. При невозможности придать такую позу больному показано положение на боку. Благоприятные условия для уменьшения венозного кровотечения возникают при положении сидя.
Доступ в заднюю черепную ямку применяют для удаления опухолей, локализующихся в ней, при черепно-мозговой травме и для вмешательства на сосудах вертебрально-базилярного бассейна. Наиболее широко распространён доступ, предложенный в 1926 г. Фразье и Тауном, а затем в 1928 г. Наффцигером (рис. 4-4). В последующем доступ был усовер-
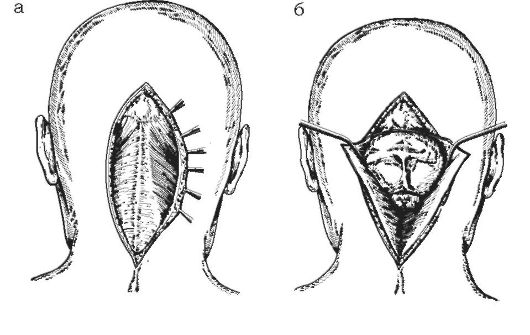
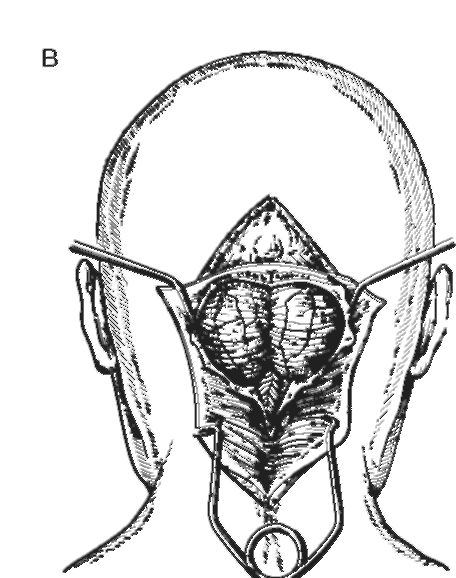 Рис. 4-4. Вскрытие
задней черепной ямки срединным разрезом по Наффцигеру: а - разрезают
кожу; б - рассекают мышечно-апоневротический слой и обнажают чешую
затылочной кости и заднюю дужку атланта; в - выполняют резекцию чешуи
затылочной кости и задней дужки атланта, вскрывают твёрдую мозговую
оболочку и обнажают заднюю поверхность мозжечка
Рис. 4-4. Вскрытие
задней черепной ямки срединным разрезом по Наффцигеру: а - разрезают
кожу; б - рассекают мышечно-апоневротический слой и обнажают чешую
затылочной кости и заднюю дужку атланта; в - выполняют резекцию чешуи
затылочной кости и задней дужки атланта, вскрывают твёрдую мозговую
оболочку и обнажают заднюю поверхность мозжечка
шенствован И.С. Бабчиным. Разрез проводят по линии остистых отростков от V шейного позвонка вверх в затылочную область на 4 см выше наружного затылочного бугра. Поверхностные мягкие ткани отсепаровывают от глубокой фасции широко в стороны. Выкраивают полуромб из мышц шеи, вершина которого обращена к большому затылочному отверстию. Скелетируют затылочную кость и дугу атланта, которые затем частично резецируют. Твёрдую мозговую оболочку рассекают V- образно вершиной к атлантозатылочному сочленению. После удаления патологического образования задней черепной ямки разрез твёрдой мозговой оболочки не зашивают. Дефект в ней прикрывают апоневрозом, лиофилизированной твёрдой мозговой оболочкой или гемостатической губкой. Накладывают швы на мышцы, апоневроз, кожу.
Хороший доступ к структурам задней черепной ямки возникает при арбалетном разрезе по Кушингу (рис. 4-5) или подковообразном разрезе.
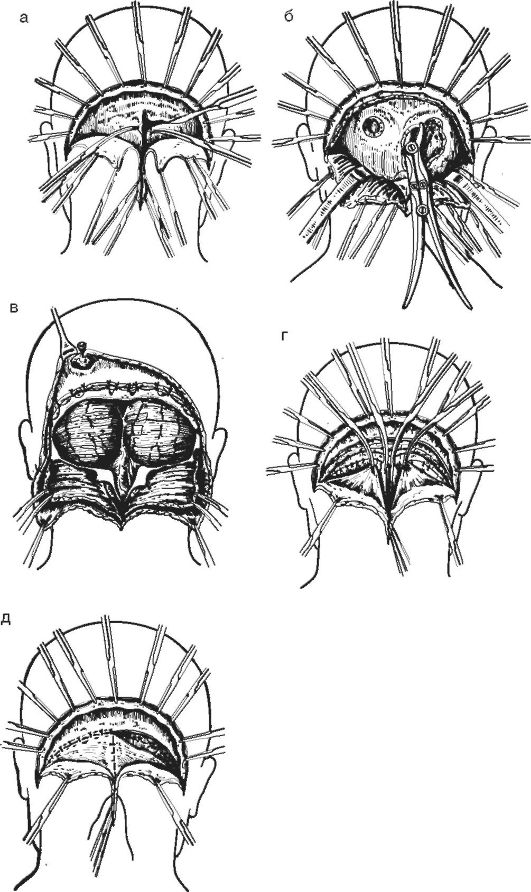 Рис. 4-5. Вскрытие
задней черепной ямки арбалетным разрезом по Кушингу: а - разрезают кожу
и мышечно-апоневротический слой; б - расширяют фрезевые отверстия на
чешуе затылочной кости, удаляют заднюю дужку атланта; в - выполняют
вентрикулярную пункцию, вскрывают твердую мозговую оболочку, обнажают
полушария мозжечка; г, д - зашивают мягкие ткани наглухо
Рис. 4-5. Вскрытие
задней черепной ямки арбалетным разрезом по Кушингу: а - разрезают кожу
и мышечно-апоневротический слой; б - расширяют фрезевые отверстия на
чешуе затылочной кости, удаляют заднюю дужку атланта; в - выполняют
вентрикулярную пункцию, вскрывают твердую мозговую оболочку, обнажают
полушария мозжечка; г, д - зашивают мягкие ткани наглухо
Принципы выполнения мозговой части оперативного вмешательства
Внедрение в клиническую практику в 70-х годах ХХ в. микроскопа и микрохирургической техники, усовершенствование хирургической тактики и техники выполнения оперативных вмешательств, улучшение технического оснащения и совершенствование анестезиологического обеспечения операций позволили значительно улучшить результаты хирургических вмешательств. При некоторой нейрохирургической патологии летальность в ведущих клиниках мира в настоящее время отсутствует. Достижение этих результатов оказалось возможным при учёте следующих весьма важных положений. Во-первых, одно из условий успешного проведения операций - защита важных в функциональном отношении зон мозга и его сосудов от операционных травм. Во-вторых, хирургическая тактика зависит от особенностей локализации патологического процесса, от соотношения с сосудами и важными в функциональном отношении зонами головного мозга, а также от степени компенсации нарушений артериального и венозного церебрального кровотока.
В-третьих, от технической оснащённости при выполнении оперативного вмешательства. Защита функционально важных стволовых структур во время операции предполагает не только современное комплексное анестезиологическое пособие, но также применение системы модифицированных хирургических мероприятий, включающих тактику, широкое применение увеличительной оптики и микрохирургию. Весьма важна физиологичность разрезов мягких тканей, сохранение путей оттока крови от головного мозга. При выполнении мозгового этапа оперативного вмешательства необходимо щадящее отношение не только к артериальным сосудам, но также и к венозным, особенно в случае магистрального типа их строения.
С этой целью необходимо обязательное применение микрохирургического инструментария, увеличительных луп (2,5-6 крат), а также операционного микроскопа, что позволит с большой вероятностью атравматично производить выделение и отделение сосудов от опухолей, их мобилизацию из мозга. Сохранение как крупных, так и мелких сосудов предотвращает появление в послеоперационном периоде ишемических поражений головного мозга, сопровождающихся грубыми очаговыми неврологическими симптомами. Перед выполне-
нием каких-либо манипуляций на мозге хирург не должен спешить, а чётко представить себе область мозга, на которой он будет производить манипуляции. Определить взаимоотношение этой области с другими участками головного мозга. Ни в коем случае нельзя производить рассечение мозга в функционально значимых участках, поскольку в послеоперационном периоде у таких больных будут грубые неврологические выпадения. Доступ к этим областям следует осуществлять через зоны, повреждение которых не будет сопровождаться появлением грубых очаговых неврологических симптомов. Так, например, доступ к опухоли левой височной доли у правшей может происходить через её полюс или базальные отделы (рис. 4-6). Объём оперативного вмешательства зависит от состояния больного во время операции, кровопотери, состояния гемодинамики, а также данных электрофизиологического контроля. При появлении нарушений со стороны этих показателей необходимо хирургическое вмешательство остановить на время и оценить создавшуюся ситуацию. В случае регресса патологических реакций операцию можно продолжить. При отсутствии положительной динамики показателей вмешательство следует закончить и отложить на следующий этап, сроки выполнения которого будут зависеть от степени компенсаторных возможностей организма больного.
Кровотечение во время оперативного вмешательства при разрезе мягких тканей может быть остановлено простым прижатием пальцами краёв раны к костям черепа. Кровотечение из сосудов твёрдой мозговой оболочки останавливают коагуляцией (лучше биполярной), клипированием, которое в настоящее время нейрохирурги применяют довольно редко из-за опасности развития
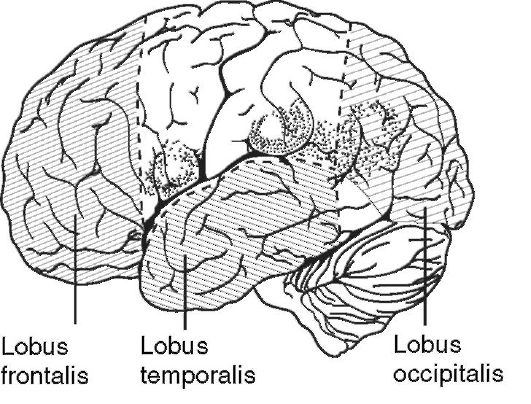 Рис. 4-6. Наружная
поверхность левого полушария. Заштрихованы зоны коры мозга, при
повреждении или удалении которых не будут развиваться паралич
конечностей или моторная афазия
Рис. 4-6. Наружная
поверхность левого полушария. Заштрихованы зоны коры мозга, при
повреждении или удалении которых не будут развиваться паралич
конечностей или моторная афазия
эпилептических припадков, а также невозможности проведения в послеоперационном периоде МРТ. Кровотечение из средней оболочечной артерии, повреждённой в костном канале, следует останавливать медицинским воском. Общепринятая методика по остановке кровотечения из паренхимы головного мозга - использование гемостатической губки, гемостатической плёнки и реже биполярной коагуляции. Кровоточащие небольшого диаметра артериальные и венозные сосуды обычно подвергаются биполярной коагуляции. В настоящее время кровотечение из функционально важных сосудов диаметром более одного миллиметра останавливают наложением швов, восстанавливающих просвет сосуда, что выполняют под микроскопом при увеличении в 7,5-15 крат с помощью нитей 10-11/00.
Оперативное вмешательство обычно заканчивают наложением швов на твёрдую мозговую оболочку, что позволяет восстановить герметичность субдурального пространства. Однако в случае острых внутричерепных гематом, после удаления абсцессов мозга, больших оболочечных опухолей, частичного удаления внутримозговых новообразований, при протрузии мозга в операционную рану или его коллапсе, что бывает после удаления хронических внутричерепных гематом, в остром периоде разрыва артериальных аневризм, огнестрельных ранениях, базально расположенных опухолях мозга зашивание твёрдой мозговой оболочки нецелесообразно из-за развития и нарастания отёка мозга в послеоперационном периоде с последующей дислокацией и ущемлением ствола. Несвоевременная диагностика этого осложнения чревата гибелью больных или при своевременной диагностике повторной операцией с удалением костного лоскута и снятием швов с твёрдой мозговой оболочки для создания декомпрессии. В некоторых случаях при отсутствии угрозы нарастания отёка головного мозга в дефект твёрдой мозговой оболочки вшивают участок апоневроза, надкостницы или лиофинизированной твёрдой мозговой оболочки. Костный дефект обычно закрывают костно-надкостничным лоскутом, образованным в начале операции. В случаях сохраняющегося или возникшего во время операции отёка мозга, обусловленного вышеперечисленными ситуациями, костный лоскут может быть удалён, после чего накладывают швы на надкостнично-апоневротические лоскуты и кожу. Обычно под кожный лоскут вводят 1 или 2 резиновых выпускника для оттока раневого отделяемого.
СТЕРЕОТАКСИЧЕСКАЯ НЕЙРОХИРУРГИЯ
Стереотаксис (стереотаксический метод) обеспечивает малотравматичный прицельный доступ к различным, в том числе и глубоким, образованиям мозга и локальные воздействия на них.
Появление стереотаксического метода обычно связывают с работами российского анатома Д.Н. Зернова, который в 1889 г. предложил прибор энцефалометр.
В 1906 г. английские исследователи Кларк и Хорсли создали стереотаксический метод для лабораторных животных. Для попадания инструментом в заранее предназначенную точку мозга ими разработаны стереотаксический аппарат, содержащий систему координат, и первые стереотаксические карты мозга экспериментальных животных. Ими же предложен термин «стереотаксис» (от греческого «стереос» - пространство, «таксис» - расположение, порядок). Применение стереотаксиса в клинике для вмешательств с целью диагностики и лечения больных людей началось благодаря работам американских неврологов Шпигеля и Вайсиса (1947).
Среди отечественных авторов следует упомянуть пионеров советского стереотаксиса Н.С. Мисюка, Э.И. Канделя (1965, 1981), автора книги «Основы стереотаксической нейрохирургии» Л.В. Абракова (1975).
Приёмы стереотаксиса можно условно разделить на две части: стереотаксическое наведение и стереотаксические воздействия. Основа стереотаксического наведения - геометрия, метод координат. Стереотаксическое наведение включает определение положения стереотаксических мишеней в пространстве и нацеливание на них стереотаксического инструмента.
Метод координат позволяет выразить в числах пространственное положение точек относительно какой-либо системы координат. В стереотаксисе используют несколько типов системы координат. Прямоугольная система координат - три взаимно перпендикулярные плоскости, называемые координатными плоскостями. Точка пересечения координатных плоскостей - начало координат. Линии пересечения координатных плоскостей - оси системы координат - называют латинскими буквами x, y, z. Положение любой точки в прямоугольной системе координат задаётся тремя числами - тремя координатами точки (тремя расстояниями точки до координатных плоскостей). В полярной системе координат положение точки задаёт- ся тремя числами - одним расстоянием (длина радиуса-вектора) и
двумя углами. При постоянной длине радиуса-вектора полярная система координат превращается в экваториальную систему координат.
Любая стереотаксическая методика содержит несколько систем координат.
Система координат мозга
В клиническом стереотаксисе прямоугольная система координат мозга строится по внутримозговым ориентирам, чаще всего используют переднюю и заднюю коммиссуры мозга. Ось х проходит через центры коммиссур от затылка ко лбу, начало координат 0 - середина расстояния между коммиссурами, ось z проходит от базальных отделов мозга к темени, ось y слева направо (рис. 4-7).
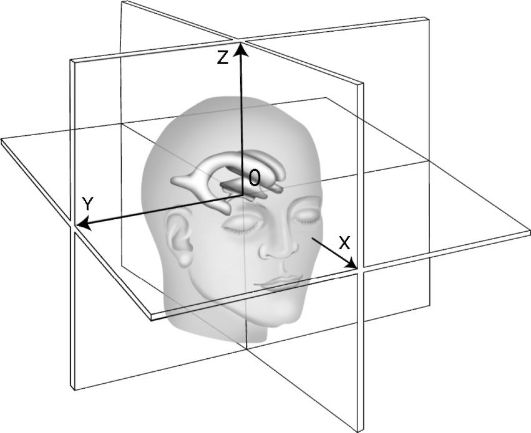 Рис. 4-7. Система координат мозга (объяснение в тексте)
Рис. 4-7. Система координат мозга (объяснение в тексте)
Система координат стереотаксического атласа
Стереотаксический атлас - обычно набор фотографий срезов мозга с изображениями мозговых структур, плоскости срезов строго параллельны координатным плоскостям системы координат. Правила построения системы координат стереотаксического атласа и системы координат мозга аналогичны. Это позволяет измерять в атласе координаты целевых точек и переносить их в системы координат мозга.
Система координат стереотаксического аппарата
Стереотаксические аппараты - устройства для прицельного введения в мозг пациента стереотаксического инструмента - моделируют
в своей конструкции одну или две системы координат. Современные аппараты обычно содержат прямоугольную и экваториальную систему координат.
Система координат локализатора
Систему координат локализатора, так же как систему координат стереотаксического аппарата, относят к инструментальным системам координат. Локализаторы - устройства, которые фиксируются на голове пациента и содержат в своей конструкции модель прямоугольной системы координат. Различают рентгеновские локализаторы, КТ-локализаторы, МРТ-локализаторы, ПЭТ-локализаторы. Они позволяют определять координаты объекта по его рентгеновскому, КТ-, МРТ-, ПЭТ-изображению (рис. 4-8).
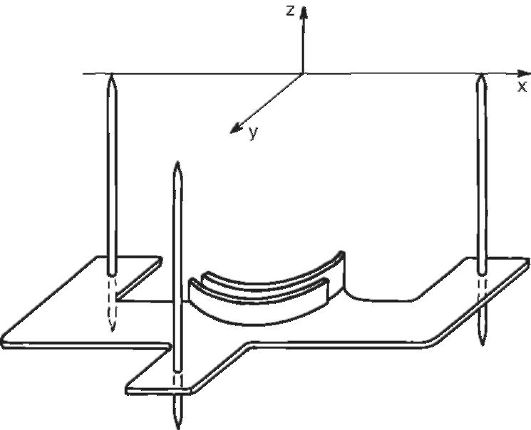 Рис. 4-8. Локализатор
Рис. 4-8. Локализатор
Стереотаксическая интроскопия
Для определения пространственного положения внутримозговых образований в клинике используют стереотаксическую контрастную рентгенографию (пневмоэнцефалографию, вентрикулографию, ангиографию), КТ, МРТ и ПЭТ. Основное и главное отличие стереотаксического исследования (интроскопия) от обычного диагностического заключается в том, что стереотаксис всегда требует количественной оценки изображения, возможности его измерения для последующих расчётов пространственного положения точек, внутримозговых образований или деталей технических устройств. На плёнках или компьютерных томограммах должны присутствовать изображения дета-
лей, моделирующих систему координат стереотаксического аппарата или локализатора. Специальная прикладная научная дисциплина - вычислительная рентгенограмметрия - создана для использования рентгеновского изображения в стереотаксисе. Расчётная стереотаксическая МРТ - самый современный вид стереотаксической интроскопии. Она даёт наиболее детальную картину внутримозгового пространства, атравматична и безвредна, обеспечивает минимальные ошибки в определении пространственного положения стереотаксических мишеней.
Преобразование стереотаксических координат - перевод координат целевой точки (стереотаксической мишени) из одной системы координат в другую. Поскольку каждая стереотаксическая методика включает несколько систем координат, приходится производить последовательно несколько преобразований одной и той же точки в разные системы координат. Например, из системы координат стереотаксического атласа в системы координат мозга и далее в системы координат рентгеновского локализатора, прямоугольную систему координат стереотаксического аппарата и, наконец, в экваториальную систему координат стереотаксического аппарата. После этого возможно прицельное погружение стереотаксического инструмента в мозг.
В клиническом стереотаксисе используют три способа преобразования координат:
• с помощью вычислений (аналитический способ); в современном стереотаксисе вычисления производят с использованием компьютера;
• с помощью геометрических построений; такие построения могут быть произведены на плоскостях рентгеновских плёнок или экране томографа;
• с помощью фантомного моделирования; стереотаксический фантом - устройство, предназначенное для моделирования в пространстве системы координат и целевых точек.
Стереотаксические расчёты - обязательный этап каждой стереотаксической методики. Его проводят после этапа интроскопии или одновременно с ним. Его суть заключается в построении системы координат, определении их взаимного пространственного положения и преобразовании координат целевых точек в системы координат стереотаксического аппарата.
Контактные и дистантные стереотаксические воздействия
Все возможные виды стереотаксических воздействий можно разделить на две группы:
• контактные воздействия, требующие введения стереотаксического инструмента в мозг; их осуществляют с помощью интрацеребральных электродов, криозондов, биопсийных игл и т.д.; их главный недостаток - необходимость хирургического вмешательства, однако именно такие воздействия и такие инструменты составляют подавляющее большинство всех воздействий и инструментов, принятых в клиническом стереотаксисе;
• дистантные воздействия, не требующие погружения в мозг; они могут быть бескровными, и это важнейшее их достоинство, однако ограниченный характер воздействий, очень высокая стоимость и одномоментность применения существенно сужают возможности применения дистантных воздействий.
Наиболее широко известные аппараты дистантного воздействия предназначены только для локальных разрушений ткани. Например, разработанный Лекселлом γ-нож (фирма Электа, Швеция) содержит более двухсот источников γ-излучения, направленных в одну точку пространства. В процессе стереотаксического наведения зону мозга, намеченную к разрушению, совмещают с этой точкой. Другой пример - сфокусированный пучок протонов, исходящий из мощного ускорителя (например, ускоритель Санкт-Петербургского института ядерной физики). Голова больного в специальном устройстве располагается так, чтобы протонный пучок проходил через зону мозга, намеченную к разрушению. При этом голова вращается вокруг указанной зоны. Эта зона разрушения получает максимальную радиационную нагрузку, а покровные ткани головы гораздо меньшую. γ-Нож и протонный пучок в основном используют для разрушения небольших опухолей, лечения АВМ.
Стереотаксические инструменты для контактных воздействий - устройства, прицельно погружаемые в мозг для осуществления локальных дозированных воздействий.
Долгосрочные электроды - тонкие, гибкие, обычно изготавливаемые из благородных металлов или неокисляющихся сплавов, покрытые биологически инертной изоляцией. Обычно электроды имплантируют в виде пучков по 4 или 6 электродов в пучке; диаметр каждого электрода - 0,1 мм; длина контактной, лишённой изоляции поверхности каждого электрода - около 1 мм. Поскольку электродные пучки гибкие, их прицельное введение производят с помощью
тонкой металлической трубки (иглы-направителя). После погружения направитель удаляют, а пучок фиксируют к костным краям фрезевого отверстия. Электроды могут оставаться в мозгу пациента до нескольких месяцев. Долгосрочные электроды позволяют регистрировать электрокортикограмму и электросубкортикограмму, электрические потенциалы нейронных групп, вызванные потенциалы, а также проводить стимуляции электрическими импульсами, электрополяризации (временные выключения структур мозга током малой продолжительности и силы), электролизисы (воздействия большей продолжительности и силы для лечебных локальных деструкций нервной ткани).
Электроды для интраоперационного контроля и воздействий - жёсткие, круглого сечения, диаметр - около 2 мм. Такой электрод может иметь одну или несколько контактных поверхностей и использоваться для регистрации кортикограммы и субкортикограммы, проведения диагностических электрических стимуляций и лечебных деструкций. Деструкцию проводят с использованием переменного тока высокой частоты. В результате этого воздействия нервная ткань нагревается и разрушается. Такой способ называют диатермокоагуляцией.
Криозонд (криохирургический аппарат) - устройство для локальной интраоперационной деструкции нервной ткани путём её замораживания. Криодеструкцию считают наиболее физиологичным методом выключения нервной ткани, она реже других методов даёт такие осложнения, как внутримозговое кровотечение. Криозонд - устройство круглого сечения с закруглённым концом, диаметр - 2-3 мм. В рабочем конце криозонда расположена активная камера, в которую подаётся хладоагент. По всей своей длине, кроме активной камеры, криозонд снабжён тепловой защитой чаще всего в виде вакуумированного пространства. В качестве хладоагента могут быть использованы сжиженные газы (жидкий азот), сжатые газы (азот), легкоиспаряющиеся жидкости (закись азота), твёрдая углекислота (температура -78°С) с ацетоном. В последнем случае ацетон под давлением поступает в активную камеру, охлаждает её и затем удаляется. Такой криохирургический аппарат при наличии термодатчика в активной камере позволяет управлять процессом охлаждения, в частности, проводить диагностическое обратимое охлаждение нервной ткани и в случае необходимости экстренно прекращать процесс замораживания.
Разработаны инструменты для стереотаксической биопсии, с помощью которых можно брать кусочки ткани для гистологического исследования (биоптаты).
Стереотаксические системы - промышленно выпускаемые комплексы приборов, инструментов и компьютерных программ, предназначенные для проведения стереотаксических вмешательств. Наиболее известные зарубежные стереотаксические системы: Лекселла фирмы Электа (Швеция), Рихерта-Мундингера фирмы Фишер (Германия), БРВ фирмы Радионикс (США) и др.
Стереотаксическая система «Поаник». Эта отечественная компьютеризированная стереотаксическая система разработана лабораторией стереотаксических методов Института мозга человека РАН и ГНЦ РФ ЦНИИ «Электроприбор» (рис. 4-9). Важное достоинство ПОАНИК - атравматичная маркировка головы больного с помощью оттиска зубов пациента. При каждом прикусывании пациентом своего оттиска зубы верхней челюсти погружаются в соответствующие углубления оттиска, который занимает относительно черепа и мозга одно и то же пространственное положение. На оттиске могут быть поочерёдно зафиксированы локализаторы для рентгенографии, КТ, МРТ и ПЭТ. Благодаря этому возможно проведение интроскопии заблаговременно до операции без травмирования больного. Эта система позволяет проводить стереотаксические операции в нейрохирургических отделениях, которые не имеют собственного томографа, а интроскопическая подготовка может быть выполнена на томографе, географически удалённом от операционной.
Функциональная и нефункциональная стереотаксия
Функциональная стереотаксия - наведение и воздействие на ядра и проводящие пути головного мозга для диагностики и лечения сложных хронических заболеваний центральной нервной системы, таких, как паркинсонизм, органические гиперкинезы, эпилепсия, неукротимые боли, некоторые психические расстройства.
Стереотаксические воздействия, используемые в функциональной стереотаксии, можно разделить на три
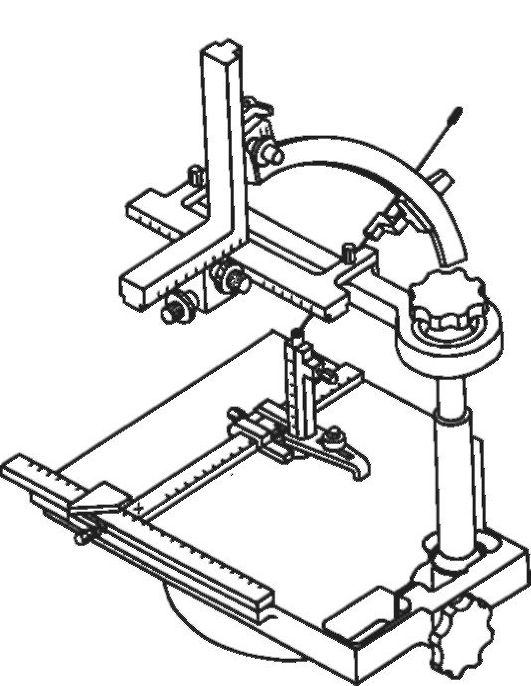 Рис. 4-9. Стереотаксическая система «Поаник».
Рис. 4-9. Стереотаксическая система «Поаник».
группы. Первая, наиболее часто применяемая, - локальные необратимые разрушения структур-мишеней. Разрушению могут быть подвергнуты те структуры, которые служат очагами патологической гиперактивности, вызывающей характерные для данного заболевания клинические проявления, например эпилептический очаг. Однако гораздо чаще локальному разрушению подвергаются морфологически и биохимически интактные структуры, которые в мозгу служат проводниками патологической активности. Вторая группа - временные, обратимые воздействия. Они более щадящие, более «физиологичные». Например, обратимые холодовые выключения структур с помощью локального охлаждения до -10°С или диагностические и лечебные электрические стимуляции. Последние, в зависимости от параметров (частота, сила тока, экспозиция), могут вызывать функциональную активацию структуры или, наоборот, её дисфункцию. Третья группа - трансплантация тканей, например аутотрансплантация тканей надпочечников или трансплантация эмбриональной ткани.
Выделяют четыре основных направления в функциональной стереотаксии:
• стереотаксия двигательных нарушений;
• стереотаксия боли;
• стереотаксия эпилепсии;
• стереотаксическая психохирургия.
СТЕРЕОТАКСИЯ ДВИГАТЕЛЬНЫХ НАРУШЕНИЙ
Стереотаксис можно использовать при ряде заболеваний с двигательными нарушениями:
• болезнь Паркинсона и паркинсонизм;
• посттравматические гиперкинезы (гемигиперкинезы);
• деформирующая мышечная (торсионная) дистония;
• эссенциальный тремор;
• хорея Хантингтона;
• детский церебральный паралич.
У больных с болезнью Паркинсона и паркинсонизмом могут быть использованы три основных вида воздействий:
• стереотаксическая трансплантация эмбриональной ткани, содержащей дофаминергические нейроны, которые трансплантируют в головки хвостатых ядер (однако этот вид трансплантации пока используют редко);
• стереотаксическая имплантация долгосрочных электродов для проведения лечебных электрических стимуляций; при этом могут использоваться миниатюрные вживляемые под кожу стимуляторы;
• локальные стереотаксические деструкции, которые применяют чаще других методов.
Стереотаксическими мишенями у больных с двигательными нарушениями могут быть ядра таламуса: вентролатеральный комплекс, срединный центр таламуса, медиальный членик бледного шара, субталамическая зона.
Вентролатеральный комплекс включает три ядра. Разрушение их приводит к снижению выраженности паркинсонических проявлений в конечностях контралатеральной (по отношению к оперируемой гемисфере) стороны (рис. 4-10). К этим ядрам относят:
• вентрооральное переднее ядро (оно имеет отношение к снижению мышечной ригидности);
• вентрооральное заднее ядро (его разрушение приводит к устранению гиперкинезов);
• вентральное интермедианное ядро (наружное и внутреннее); его разрушают, чтобы избавиться от тремора (причём тремора не только паркинсонического) в конечностях, в первую очередь в руках.
Срединный центр таламуса - его деструкция снижает выраженность паркинсонических проявлений и в большей степени ригидности; эта мишень менее эффективна, чем ядра вентролатерального комплекса, но в отличие от них позволяет повлиять и на ипсилатеральную сторону.
Медиальный членик бледного шара - его деструкция, особенно в области, прилежащей к лентикулярной петле, снижает мышечную ригидность, тремор и брадикинезию, прежде всего в контралатеральной ноге.
Субталамическая зона (поля Фореля) - эффективная стереотаксическая мишень у больных с двигательны-
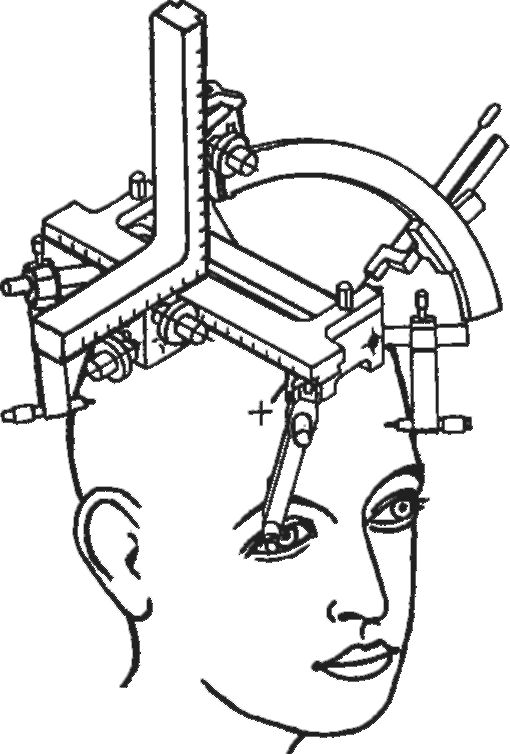 Рис. 4-10. Прицельное погружение стереотаксического инструмента в мозговые мишени
Рис. 4-10. Прицельное погружение стереотаксического инструмента в мозговые мишени
ми нарушениями (ригидность, в меньшей степени тремор), но требующая большей осторожности и точности попадания, чем ядра таламуса.
Перечисленные мишени могут быть использованы не только для лечения паркинсонизма, но и аналогичных двигательных нарушений при других нозологиях. Например, для стереотаксического лечения эссенциального тремора, гиперкинетической формы так называемого детского церебрального паралича и др.
СТЕРЕОТАКСИЧЕСКАЯ ПСИХОХИРУРГИЯ
Стереотаксис успешно применяют для коррекции целого ряда психопатологических расстройств. При этом его используют для трансплантации тканей эмбрионального мозга, электрических диагностических и лечебных стимуляций. Однако, как и в других разделах функциональной стереотаксии, подавляющее большинство воздействий - локальные деструкции.
В психохирургии используют следующие стереотаксические мишени:
• поясные извилины: наиболее частая мишень при лечении обсессивно-компульсивных расстройств, депрессий, алкоголизма, тревожности, неукротимых болей; наркомании;
• передние отделы внутренней капсулы; деструкцию проводят при лечении депрессий, навязчивых расстройств;
• миндалевидный комплекс; основная мишень при лечении агрессивности, эпилепсии, гораздо реже - гиперсексуальности;
• ядра таламуса (медиальные, интраламинарные, срединная пластинка); их деструкцию проводят при депрессии, кататоническом возбуждении, агрессии, обсессивно-компульсивных расстройствах, тревожности, тиках;
• субкаудатная область; деструкция показана у больных с обсессивными расстройствами, тревожностью, при депрессии и аффективных расстройствах;
• безымянная субстанция (ядро Мейнерта); его деструкция применяется прежде всего при депрессивных состояниях.
СТЕРЕОТАКСИЯ БОЛИ
Стереотаксис может быть применён для хирургического лечения неукротимых болей различного генеза, в частности при фантомном
болевом синдроме. В качестве лечебных воздействий используют электрические стимуляции через долгосрочные электроды, но чаще - локальные деструкции. К стереотаксическим мишеням для ликвидации неукротимых болей относят:
• таламические ядра - вентрокаудальное внутреннее ядро, срединный центр, медиальный отдел подушки;
• поясные извилины.
СТЕРЕОТАКСИЧЕСКОЕ
ЛЕЧЕНИЕ ЭПИЛЕПСИИ
При лечении эпилепсии применяют перечисленные выше способы воздействия: трансплантацию тканей эмбрионального мозга и значительно чаще - электрические стимуляции и локальные деструкции. Одним из ведущих диагностических методов при эпилепсии остаётся скальповая ЭЭГ. Данные, получаемые с её помощью, должны быть подкреплены другими электрофизиологическими исследованиями, в частности диагностическими электрическими стимуляциями, производимыми при кортико-субкортикографии. Известно, что в эпилептизированной структуре мозга стимуляция вызывает характерный ответ, так называемый послеразряд. В связи с этим значительную часть стереотаксической операции может занимать прицельная имплантация в мозг электродов. При данной методике электрофизиологические исследования могут производиться как в процессе операции, так и в послеоперационном периоде через электроды, введённые в мозг. При стереотаксическом лечении эпилепсии существуют два подхода. Первый - одномоментный, более предпочтительный, состоит в локализации очага и его разрушении. Если это невозможно из-за расположения очага в околостволовых структурах мозга или при неустановленных очагах, применяют второй подход - двухэтапный, при котором сначала диагностируют очаги, а затем, спустя 2-3 нед, производят второй этап операции - разрушение очагов. Чаще всего стереотаксис применяют для диагностики и лечения височных форм эпилепсии, поскольку гиппокамп и миндалевидный комплекс имеют самые низкие пороги судорожной готовности и именно в этих структурах, чаще чем в других, локализуются эпилептические очаги.
НЕФУНКЦИОНАЛЬНАЯ СТЕРЕОТАКСИЯ
Наведение на опухоли мозга, инородные тела, гематомы, абсцессы. Сюда входят: биопсия опухолей, пункция абсцессов с их дренированием, промыванием полости абсцесса растворами антибиотиков и при необходимости - осмотр стенок полости с помощью стереотаксически введённого эндоскопа, эвакуация гематом, стереотаксическое удаление инородных тел. К нефункциональной стереотаксии можно отнести также нейронавигацию. Эту технологию используют во время открытых нейрохирургических операций. Задача нейронавигации состоит в том, чтобы с помощью луча лазера низкой интенсивности или после стереотаксически введённого тонкого катетера указать нейрохирургу путь к небольшой глубоко расположенной опухоли или другому патологическому очагу.
КРИОХИРУРГИЧЕСКИЙ МЕТОД В НЕЙРОХИРУРГИИ
Криохирургия - метод лечения, при котором для получения лечебного эффекта используют низкие температуры.
При замораживании клеток любой ткани происходит образование кристаллов льда первоначально во внеклеточном пространстве, а затем внутри клетки. Первый процесс начинается при температуре среды около -5-10°С, а для второго необходимо снижение температуры до -20°С и ниже. Внеклеточное образование кристаллов льда приводит к уменьшению содержания воды в межклеточном пространстве, вследствие чего увеличивается концентрация электролитов вне клетки. Из-за появления градиента осмотического давления молекулы воды диффундируют через клеточную мембрану в межклеточное пространство, приводя к дегидратации клетки, увеличению внутриклеточного содержания электролитов, изменению рН. При этом выходят из строя механизмы активного транспорта. Этот феномен назвали «осмотическим шоком». Последующее охлаждение приводит к разрушению клеточных мембран и внутриклеточных структур образующимися кристалликами льда. Состояние, при котором прекращается движение цитоплазмы в охлаждённой клетке и возникает связанное с этим угнетение внутриклеточного метаболизма, получило название «терминальный шок». При криодеструкции выделено три зоны криовоздействия по мере отдаления от зонда: первая - зона крионекроза,
вторая - зона некробиоза с резко выраженными дистрофическими изменениями опухолевых клеток, третья - краевая зона опухоли, характеризуется умеренным периваскулярным и перицеллюлярным отёком ткани, с наличием небольших участков некробиоза.
С помощью криохирургии возможно производить разрушение и удаление опухолевой ткани открытым путём. Данная методика может быть использована для стереотаксического разрушения небольших новообразований, глубинных мозговых мишеней при лечении паркинсонизма, гиперкинезов, болевых синдромов и височной эпилепсии.
МЕТОДИКИ ЗАКРЫТИЯ ДЕФЕКТОВ ЧЕРЕПА
Первое детальное описание пластики трепанационного дефекта золотой пластинкой относят к 1565 г., оно было выполнено Петронием. С тех пор для краниопластики использовали различные материалы, в частности ауто-, гомо- и гетерогенные костные трансплантаты, костную стружку, металлы и акрилаты. Основные требования, предъявляемые к применяемому для краниопластики материалу, следующие: тканевая толерантность, простая техника приготовления, низкая температурная проводимость, прочность, рентгенопозитивность и малая стоимость.
В настоящее время используют две методики краниопластики: остеопластическую реконструкцию (аутоили гомогенным костным трансплантатом) и аллопластическую имплантацию индифферентных для организма протезов-эксплантатов. Применяют методику, предполагающую хранение выпиленного костного лоскута в 0,25-0,5% растворе формалина*, а также метод замораживания с последующей стерилизацией в автоклаве перед закрытием костного дефекта тому же пациенту. В 1923 г. Пфемистер предложил методику стерилизации костного лоскута его кипячением в течение 40 мин - 1 ч с последующей имплантацией лоскута на место трепанации. Экспериментальные и клинические исследования показали, что аутотрансплантаты, независимо от жизнеспособности пластического материала и методов его консервации, оказывают на репаративный процесс остеогенеза более выраженное стимулирующее воздействие, чем аллотрансплантаты. В качестве аллотрансплантатов применяют пластмассы: стиракрил, протакрил или металл - титан.
Техника операции
Разрез мягких тканей выполняют по старому послеоперационному рубцу. При невозможности его использования разрез делают с учётом сохранения кровоснабжения костного лоскута. Разрез надкостницы лучше производить, отступив от края костного дефекта кнаружи на 1-1,5 см. При возможности разделяют надкостнично-оболочечноапоневротический лоскут на две части продольно. Нижний лоскут отделяют от краёв костного дефекта. Моделируют аллотрансплантат по форме костного дефекта, после чего трансплантат фиксируют лигатурами к его краям. Сверху на трансплантат накладывают наружный листок разделённого лоскута, сшивают его края. Выпускники под кожно-апоневротический лоскут лучше не вводить.
ТЕХНИКА ЛАМИНЭКТОМИИ
Для подхода к спинному мозгу используют вскрытие позвоночного канала путём ламинэктомии, которую выполняют под наркозом. Положение больного на операционном столе - на животе или на боку. Необходимый уровень ламинэктомии определяют отсчётом от анатомических ориентиров: основание черепа в области заднего края большого отверстия затылочной кости, VII шейный позвонок (его остистый отросток не смещается при наклонах головы кзади), нижние углы лопаток, XII ребро, линия, соединяющая верхние ости или гребни подвздошных костей (IV и V поясничные позвонки) и I крестцовый позвонок. Уровень предстоящей ламинэктомии может быть уточнён посредством предварительно произведённой рентгенографии с контрастной зафиксированной меткой. Линию кожного разреза намечают с помощью 1% раствора метиленового синего*. Размеры операционного поля устанавливают с таким расчётом, чтобы кожный разрез был проведён на один позвонок выше и ниже позвонков, подлежащих ламинэктомии. Линейный кожный разрез при ламинэктомии производят по линии остистых отростков или слегка отступив в сторону. Рассекают апоневроз, после чего скелетируют мышцы с каждой стороны остистых отростков (рис. 4-11), а пространство между мышцами и каждой стороной остистого отростка тампонируют марлевыми салфетками на 3-5 мин. После извлечения салфеток останавливают кровотечение из мышц. Щипцами Листона резецируют остистые отростки как можно ближе к их основанию (рис. 4-12). Затем при-
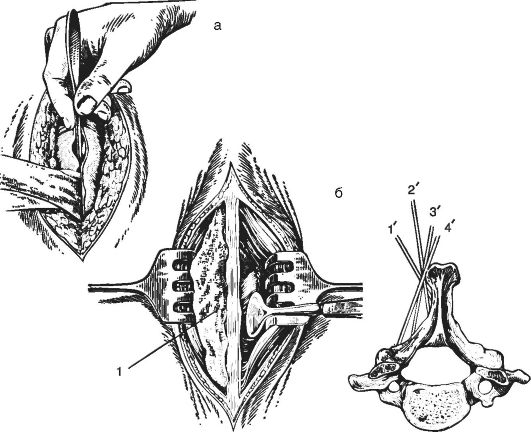 Рис. 4-11. Скелетирование
остистых отростков и дужек позвонков: а - рассекают апоневроз; б -
выполняют скелетирование боковых поверхностей остистых отростков и дужек
позвонков с помощью распатора; 1 - тампонада марлей для гемостаза; Г-4'
- последовательность положения распатора
Рис. 4-11. Скелетирование
остистых отростков и дужек позвонков: а - рассекают апоневроз; б -
выполняют скелетирование боковых поверхностей остистых отростков и дужек
позвонков с помощью распатора; 1 - тампонада марлей для гемостаза; Г-4'
- последовательность положения распатора
ступают к резекции дужек из междужковых пространств щипцами Борхардта или ламинэктомом. Обычно резецируют участок дужки, равный 2-3 см. Резекцию дужек шейных позвонков следует производить до суставных отростков. Дальнейшее их удаление, особенно на уровне шейного отдела, опасно из-за возможного ранения позвоночной артерии (на уровне С2-С5) или спинно-мозгового корешка. Число удаляемых дужек от 2 до 4-5, но не более, что зависит от характера и размеров патологического процесса. В последние годы в связи с наличием микроинструментария для нейрохирургических вмешательств нередко операции на структурах позвоночного канала (например, удаление грыжи диска) проводят при гемиламинэктомии. После удаления дужек в рану предлежит эпидуральная клетчатка с проходящи-
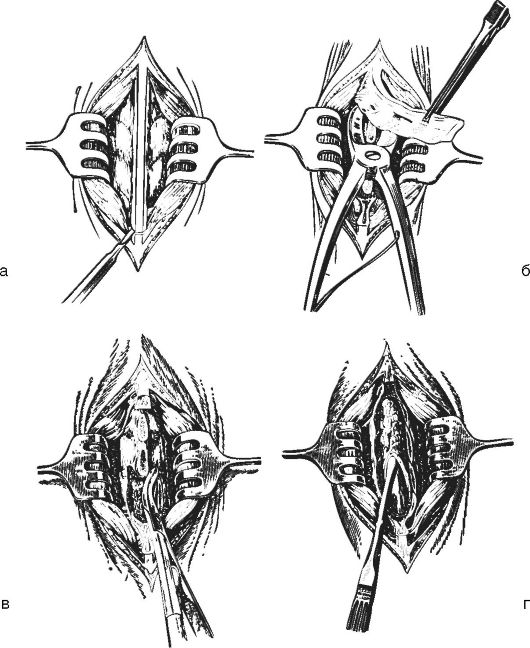 Рис. 4-12. Ламинэктомия:
а - вскрывают мягкие ткани и обнажают боковые поверхности остистых
отростков и дужек позвонков; б - удаляют блок остистых отростков
кусачками Листона; в - удаляют участки дужек позвонков для расширения
доступа в позвоночный канал; г - отделяют эпидуральную клетчатку от
твердой мозговой оболочки и рассекают её
Рис. 4-12. Ламинэктомия:
а - вскрывают мягкие ткани и обнажают боковые поверхности остистых
отростков и дужек позвонков; б - удаляют блок остистых отростков
кусачками Листона; в - удаляют участки дужек позвонков для расширения
доступа в позвоночный канал; г - отделяют эпидуральную клетчатку от
твердой мозговой оболочки и рассекают её
ми венами. При повреждении этих вен может начаться значительное венозное кровотечение. При операции на шейном отделе в этом случае существует опасность воздушной эмболии. В связи с этим в случаях повреждения эпидуральных вен желательна лёгкая тампонада эпиду-
рального пространства марлевыми полосками. Неизменённая твёрдая мозговая оболочка обычно сероватого цвета. При отсутствии в ней патологических изменений и образований под ней она эластичная и хорошо передаёт пульсацию спинного мозга. Разрез твёрдой мозговой оболочки проводят по средней линии почти до верхнего и нижнего углов операционной раны. Оба края рассечённой оболочки лигатурами подшивают к мышцам своей стороны или берут лигатуры на держалки, что позволяет расширить разрез оболочки. Подлежащую паутинную оболочку рассекают микроножницами или разрывают с помощью диссектора. Осматривают заднюю, боковые, а после рассечения зубовидных связок, фиксирующих спинной мозг к твёрдой мозговой оболочке, и переднюю его поверхность. Для мобилизации спинного мозга в грудном отделе иногда приходится пересекать 1-2 спинно-мозговых корешка с одной стороны. Оперативное вмешательство в большинстве случаев заканчивают зашиванием твёрдой мозговой оболочки и наложением послойных швов на рану. В последние годы стали применять костно-пластическую методику ламинэктомии. Эту методику используют в основном при выполнении плановых оперативных вмешательств.