Акушерство. Клинические лекции : учебное пособие / Под ред. проф. О.В. Макарова. - 2007. - 640 с. :
|
|
|
|
ЛЕКЦИЯ 9 НЕДОНАШИВАНИЕ БЕРЕМЕННОСТИ
Недонашивание беременности и преждевременные роды на современном этапе являются актуальным социальным вопросом, так как он непосредственно связан с уровнем здоровья населения.
Невынашивание - самопроизвольное прерывание беременности в различные сроки беременности до 38 нед. Привычное невынашивание - прерывание беременности два раза и более. Недонашивание - прерывание беременности в сроки от 28 до 37 нед (менее 259 дней).
Несмотря на современные достижения в акушерстве и фармакотерапии, частота преждевременных родов составляет, по данным литературы, от 6 до 15% и за последние 5 лет не имеет тенденции к снижению. Частота преждевременных родов в РФ остается значительной, достигая в среднем 14% , и в первую очередь определяет высокие показатели перинатальной заболеваемости и смертности. Согласно статистическим данным Комитета Здравоохранения г. Москвы за 2000-2001 гг., при частоте недонашивания 6,9% более 70% детей, умерших от перинатальных причин, составляют недоношенные дети. Наибольшая летальность отмечается среди глубоконедоношенных детей с гестационным возрастом менее 32 нед и массой тела менее 1500 г, основная причина смерти которых - респираторный дистресс-синдром.
Именно поэтому главной акушерской задачей наряду с пролонгированием беременности является снижение роли респираторного дистресс-синдрома в структуре смертности. Эта задача имеет два направления: максимальное пролонгирование беременности и проведение профилактики респираторного дистресс-синдрома.
Преждевременные роды - прерывание беременности на сроках 22-37 нед. В связи с особенностями акушерской тактики и выхаживания детей целесообразно выделение следующих гестационных интервалов:
• преждевременные роды в 22-27 нед;
• преждевременные роды в 28-33 нед;
• преждевременные роды в 34-37 нед.
Факторы риска преждевременных родов
В структуре причин преждевременных родов около 28% занимают случаи индуцированного родоразрешения вследствие тяжелых форм гестоза, гипоксии плода, отслойки плаценты и антенатальной гибели плода.
72% - это спонтанные преждевременные роды, из которых около 40% индуцируются преждевременным разрывом плодных оболочек.
Предрасполагающие факторы преждевременных родов
Социальные и поведенческие: низкое социально-экономическое положение матери, недостаточное питание, курение, возраст первородящей матери менее 16 или более 30 лет, психосоциальные стрессы.
Патология беременности: отслойка и предлежание плаценты, антифосфолипидный синдром, истмико-цервикальная недостаточность, инфицирование околоплодных вод и хориоамниальная инфекция, преждевременный разрыв плодных оболочек, гестоз, аномалии развития матки, миома матки, многоплодная беременность, многоводие.
Генетические факторы: преждевременные роды у членов семьи и в анамнезе.
Экстрагенитальные заболевания: артериальная гипертензия, бронхиальная астма, гипертиреоидизм, наркомания, сахарный диабет, Rh-изоиммунизация.
Особенности течения и осложнения преждевременных родов.
• Преждевременное излитие околоплодных вод.
• Неправильные положение и предлежание плода.
• Аномалии родовой деятельности.
• Отслойка плаценты.
• Кровотечение в последовом и раннем послеродовом периодах.
• Инфекционные осложнения в родах и в послеродовом периоде.
• Гипоксия плода.
• Респираторный дистресс-синдром новорожденного.
Высокий уровень неэффективности терапии преждевременных родов связан, с одной стороны, с их полигенной природой и частой невозможностью своевременного выявления этиологических факторов и проведения специфического лечения; а с другой стороны - с неэффективностью токолитической терапии, как правило, вследствие неадекватного подбора режима введения.
Клиническая картина угрожающих преждевременных родов.
• Боли в пояснице и в нижней части живота.
• Возбудимость и тонус матки повышены.
• Шейка матки сохранена, наружный зев ее закрыт.
Клиническая картина начавшихся преждевременных родов.
• Регулярная родовая деятельность.
• Динамика раскрытия шейки матки (более 2-4 см).
На сегодняшний день в нашей стране основным официальным руководством, регламентирующим ведение угрожающих преждевременных родов, является Приложение ? 1 к Приказу Минздрава Российской Федерации ? 318 от 4 декабря 1992 г.
Структура заболеваемости недоношенных новорожденных.
• Врожденное инфицирование.
• Пневмопатии.
• Родовая травма.
• Пороки развития.
Респираторный дистресс-синдром
Данный синдром - основная причина смерти недоношенных детей в развитых странах.
Легкие плода заполнены жидкостью, секретируемой эпителием потенциальных воздушных пространств. В первые минуты после рождения происходит абсорбция этой жидкости, вероятно, стимулируемая повышением концентрации катехоламинов в циркулирующей крови плода, и легкие обычно быстро очищаются от жидкости. Легочный сурфактант образует нерастворимую пленку на поверхности раздела воздух-жидкость в альвеолах, замещая молекулы воды в поверхностном слое и снижая поверхностное натяжение. Основным компонентом сурфактанта является фосфолипид-дипалмитоил-фосфатидилхолин.
Синтез фосфатидилхолина усиливают тиреоидные гормоны, эстрогены, пролактин, эпидермальный фактор роста, а секрецию фосфолипидов сурфактанта из альвеолоцитов 2-го типа в значительной степени стимулируют кортикостероиды. Вообще адренергические агонисты увеличивают секрецию сурфактанта в потенциальные воздушные пространства и лечение матери β-адренергическими средствами может уменьшить тяжесть респираторного дистресс-синдрома у новорожден-
ного. Однако возможно также, что назначение высоких доз или длительных курсов адренергических агонистов может привести к истощению внутриклеточных запасов сурфактанта, если скорость его синтеза невелика.
Химический состав сурфактанта
• Фосфолипиды 80%
- Фосфатидилхолин 65%
- Фосфатидилглицерин 5%
- Фосфатидилэтаноламин 5%
- Сфингомиелин 3%
- Прочие компоненты 2%
• Нейтральные липиды 10%
• Белки 10%
Пренатальная диагностика
Оценка зрелости легких плода по анализу околоплодных вод
• Этаноловый «пенный» тест Клементса.
• Определение отптической плотности плодных вод спектрофотометром или фотоэлектрокалориметром (длина волны 650 нм).
• Отношение концентраций лецитин/сфингомиелин (Л/С >2,0).
• Наличие фосфатидилглицерина (>2 мкг/мл).
• Определение количества ламеллярных телец: отношение фосфолипидов ламеллярных телец к общим фосфолипидам >0,35.
Известно, что зрелость плода целесообразно определять по сумме следующих параметров: календарные сроки беременности, данные УЗИ, биохимические параметры околоплодных вод. Наиболее простые тесты оценки степени зрелости легких плода перечислены ниже.
1. Этаноловый «пенный» тест Клементса.
К 3-5 мл плодных вод, полученных путем амниоцентеза, добавляют 1 мл 95% раствора этилового спирта. Пробирку встряхивают в течение 15 с два раза с интервалом в 5 мин. Тест считается положительным при наличии пузырьков, покрывающих поверхность жидкости, сомнительным - при наличии пузырьков по окружности пробирки, отрицательным - при отсутствии пузырьков.
2. Определение оптической плотности вод спектрофотометром или фотоэлектрокалориметром (на длине волны 650 нм после центрифугирования в течение 10 мин со скоростью 2000 об/мин).
3. Наиболее распространенные и диагностически ценные критерии синтеза и секреции системы сурфактанта получают путем определения липидной составляющей околоплодных вод.
Уровень общих липидов околоплодных вод довольно значительный и составляет в среднем 0,5 г/л. Особую роль играют фосфолипиды, выявление содержания которых и имеет основное диагностическое значение для оценки зрелости легких плода.
К концу III триместра беременности фосфолипиды в наибольшем количестве представлены фосфатидилхолином (синоним: лецитин) и сфингомиелином; минорными фракциями являются фосфатидилсерин, фосфатидилинозит.
Увеличение количества фосфолипидов в процессе беременности происходит главным образом за счет повышения концентрации лецитина. За период от 24 до 40 нед беременности наблюдается 6-кратное увеличение его уровня (с 0,62±0,05 до 3,84±0,17 мг%), а доля в общей фракции фосфолипидов возрастает с 43,9 до 71,2%.
В то же время содержание сфингомиелина, превышающее таковое лецитина в срок 22-24 нед, напротив, уменьшается в процессе беременности и после 35 нед становится значительно ниже, чем уровень лецитина.
Эти изменения в составе фосфолипидов отражает отношение концентраций лецитин/сфингомиелин (Л/С), которое широко используется для определения степени зрелости легких плода, поскольку отражает наличие в околоплодных водах именно легочного сурфактанта1.
Во II триместре беременности этот показатель равен примерно1,5; в 35-36 нед - 1,8-2,0; в 37-38 нед - 2,5-2,7. Как правило, при Л/С, равном 2 и более, отмечается зрелость легких плода, и риск возникновения СДР у новорожденных сводится у минимуму.
Второй критерий зрелости легких плода - концентрация фосфатидилглицерина.
В начальном периоде развития плода основным фосфолипидом сурфактанта является фосфатидилинозитол (сфингомиелин), а уровень фосфатидилглицерина остается низким. Высокий уровень сфингомиели-
1 Изучение зависимости между содержанием указанных фосфолипидов в околоплодных водах и моче плода позволило сделать вывод о том, что моча не может являться существенным источником фосфолипидов в амниотической жидкости и, следовательно, значение легочного сурфактанта в формировании амниотического фосфатидилхолина и сфингомиелина является превалирующим.
на в крови плода снижается в сроки, близкие к окончанию беременности, и по мере уменьшения его концентрации увеличивается продукция фосфатидилглицерина, что лежит в основе клинического использования его уровня в околоплодных водах в качестве показателя зрелости легких плода. Присутствие фосфатидилглицерина в амниотической жидкости - достоверный признак зрелости сурфактантной системы.
Фосфатидилглицерин в околоплодных водах выявляется в 35-36 нед беременности. Критерием зрелости легких считают его уровень, равный 2 мкг/мл и выше.
4. Следующий диагностический критерий зрелости легких плода определяется путем оценки ламеллярных телец.
Как уже было сказано, сурфактант синтезируется альвеолярным эпителием 2-го типа. Ламеллярные тельца этого эпителия служат местом накопления легочного сурфактанта и основные компоненты ламеллярных телец являются частью системы сурфактанта.
Следует подчеркнуть, что содержание фосфолипидов ламеллярных телец коррелирует с уровнем общих фосфолипидов, причем отношение между первыми и вторыми, равное 0,35, эквивалентно соотношению Л/С, равному 2.
Лечение угрозы преждевременных родов.
• Постельный режим.
• Немедикаментозные средства:
- психотерапия;
- электрорелаксация матки;
- иглоукалывание;
- электроаналгезия;
- электрофорез магния.
• Медикаментозная терапия:
- седативная (настойки пустырника, валерианы);
- токолитическая терапия;
- профилактика СДР плода;
- этиологическая: гормонотерапия, антибиотикотерапия.
Профилактика респираторного дистресс-синдрома
Глюкокортикоиды увеличивают секрецию сурфактанта альвеолоцитами 2-го порядка.
Противопоказания: бактериальная, вирусная инфекция, туберкулез, опоясывающий лишай.
Побочные эффекты: гипергликемия, лейкоцитоз, иммуносупрессия, задержка жидкости - отек легких, ВЖК, энтероколит.
Схемы профилактики респираторного дистресс-синдрома плода
• Дексаметазон - курсовая доля 20 мг по 4 мг внутримышечно через 6 ч (? 5).
• Бетаметазон - курсовая доля 24 мг по 12 мг внутримышечно через 12 ч (? 2).
Гидрокортизон по 500 мг внутримышечно ? 4 через 6 ч. Общая доза = 2 г.
Обычно эффект наступает через 24-48 ч.
Лекарственная терапия
Анализ частоты преждевременного прерывания беременности за последние 10 лет показывает отсутствие значительного ее снижения. Большое количество лекарственных веществ и других вмешательств используется для подавления преждевременных родов, но, к сожалению, стопроцентного эффекта не дает ни один метод (ACOG, 1995). В настоящее время с целью лечения угрожающих родов и остановки родовой деятельности используются токолитические препараты с различным механизмом действия - β2-адреномиметики, сульфат магния, нестероидные противовоспалительные средства, блокаторы кальциевых каналов, две новые группы токолитических агентов - доноры оксида азота, такие как нитроглицерин и глицерилтринитрат, и конкурентные агонисты окситоцина - препарат атозибан.
1. β2-адреномиметики
Механизм действия данной группы заключается в стимуляции рецепторов гладкой мускулатуры матки и увеличении синтеза цАМФ, который играет важную роль в подавлении маточных сокращений.
Адренергические рецепторы при связывании катехоламинами могут стимулировать или ингибировать аденилатциклазу, а последняя в свою очередь влияет на уровень цАМФ в клетке. При нормальном течении беременности с 28-й нед отмечается постепенное увеличение уровня цАМФ. Перед родами его концентрация снижается. Уровень цАМФ при нормальной беременности составляет: 28-30 нед - 15,79 нмоль/л; в 31-36 нед - 18,59 нмоль/л; в 37-38 нед - 17,16 нмоль/л; в 40-41 нед - 13,28 нмоль/л. Повышению сократительной активности матки способ-
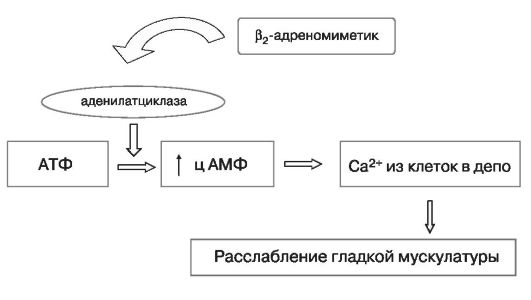 ствует снижение цАМФ в плазме крови в 1,5-2 раза по сравнению с нормой.
ствует снижение цАМФ в плазме крови в 1,5-2 раза по сравнению с нормой.
В нашей стране наибольшее распространение получили фенотерол (партусистен), тербуталин (бриканил), гинипрал (гексопреналин) и новый отечественный β2-адреномиметик - сальгим. Препарат является производным сальбутамола гемисукцината и янтарной кислоты, принимающей участие в цикле Кребса и дающей антигипоксический эффект.
Партусистен. Массивный токолиз: внутривенно капельно1 мг/сут (2 ампулы по 500 мкг) на 400 мл физиологического раствора со скоростью 3-4 мкг/мин (25-30 капель в 1 мин) Поддерживающая доза: энтерально 2-3 мг (4-6 таблеток) в сутки.
Гинипрал (гексопреналин) - высокоселективный β2-адреномиметик, избирательно действующий на миометрий (индекс селективности 5:1). Массивный токолиз: внутривенно капельно 100-150 мкг (4-5 ампул по 25 мкг) на 400 мл физиологического раствора со скоростью 0,3 мкг/мин (15-20 капель в 1 мин). Поддерживающий токолиз: внутривенно капельно со скоростью 0,075 мкг/мин (8-10 капель в 1 мин), энтерально 2-3 мг (4-6 таблеток) в сутки.
Сальгим. Массивный токолиз: внутривенно капельно 10 мг (2 ампулы по 5 мг) на 400 мл физиологического раствора со скоростью 20-25 мкг/мин (15-20 капель в 1 мин). Поддерживающий токолиз: энтерально 16-24 мг (4-6 таблеток) в сутки. Противопоказания к применению β2-адреномиметиков: лихорадка, инфекционные заболевания у матери и плода, гипокалиемия, сердечно-сосудистые заболевания: кар-
диомиопатия, нарушения проводимости и ритма сердца; тиреотоксикоз, глаукома, кровотечение при беременности, сахарный диабет.
Потенциальные осложнения, вызываемые β2-адреномиметиками: гипергликемия; гипотензия; гипокалиемия; отек легких; аритмия; ишемия миокарда.
2. Сульфат магния
Эффект сульфата магния связан с конкурентным взаимодействием ионов магния и блокировкой кальциевых каналов клетки, что в свою очередь снижает внутриклеточное поступление кальция и активность киназ легких цепей миозина.
Ионы магния в больших концентрациях могут угнетать сократительную способность миометрия как in vitro, так и in vivo за счет конкурирования со свободными ионами кальция. Магнезиальный токолиз может быть эффективен в терапевтичекой концентрации препарата в сыворотке не менее 6 мэкв/л (5,5-7,5 мг%). Большой зарубежный и собственный опыт свидетельствует: эффективный магнезиальный токолиз обеспечивается следующим режимом введения - 6 г сухого вещества в течение 1 ч и 3 г в час в суточной дозе 24 г.
Данные литературы в отношении токолитической эффективности сульфата магния противоречивы. Semchyshyn (1983) сообщил, что непреднамеренное (случайное) введение 17,3 г сульфата магния в течение 45 мин не купировало сократительную активность матки. И все-таки большинство авторов отмечают меньшую эффективность сульфата магния по сравнению с таковой β2-адреномиметиков. По нашим данным, эффективность токолиза при угрожающих преждевременных родах была сопоставима при использовании гинипрала и сульфата магния и составила 94,7 и 90% соответственно. В латентной фазе I периода родов эффективность гинипрала составила 83,3%, а сульфата магния - 30%.
Эффекты сульфата магния
Концентрация Mg2+ в сыворотке крови | Эффект |
6-8 мэквл/л (72-96 г/л) | Эффективное подавление сокращений миометрии |
10 мэквл/л (120 г/л) | Угнетение коленных рефлексов |
> 12 мэквл/л (144 г/л) | Остановка дыхания |
Конечно, гипермагниемия имеет свои негативные последствия. Побочные эффекты в виде гипотензии, чувства жара, гиперемии лица возникают при массивном магнезиальном токолизе практически в половине случаев. Вследствие курареподобного действия высоких доз сульфата магния при уровне его в сыворотке, превышающем 10 мэкв/л (120 г/л), наблюдается угнетение рефлекторной активности, в том числе коленных рефлексов. В концентрации более 10 мэквл/л магний дает токсический эффект, а более 12 мэкв/л - вызывает паралич дыхательной мускулатуры. Сульфат магния в токсических концентрациях дает осложнения: отек легких, респираторную депрессию, остановку сердца, глубокий мышечный паралич, гипотензию.
Поэтому магнезиальный токолиз следует проводить с учетом потенциальных осложнений под строгим контролем диуреза (не менее 30 мл/ч), активности коленных рефлексов или концентрации магния в сыворотке крови.
Влияние токолитиков на сердечный ритм плода по данным КТГ
Сульфат магния
• Снижение вариабельности.
• Уменьшение количества акцелераций.
• Отсутствие влияния на частоту базального ритма.
Гинипрал
• Тахикардия.
• Уменьшение количества акцелераций.
• Снижение вариабельности.
Однако было показано, что введение сульфата магния в режиме 4,5 г в час дает эффект, эквивалентный таковому партусистена, тербуталина, изадрина. Более того, сульфат магния при сочетании преждевременных родов и отслойки плаценты является единственным препаратом выбора для проведения токолиза, что выгодно отличает его от препаратов группы β2-адреномиметиков.
3. Нестероидные противовоспалительные средства Наиболее распространенный препарат этой группы - индометацин, ингибитор простагландинсинтетазы. Однако настороженность вызывают данные, подтверждающие связь применения препарата (особенно до 32 нед беременности) с преждевременным закрытием артериального протока, ВЖК и некротическим энтероколитом. Потенциальными осложнениями при длительном использовании индометацина являются
лекарственный гепатит, почечная недостаточность, кровотечения желудочно-кишечного тракта. Инфузия индометацина вызывает гемодинамические нарушения церебральной циркуляции, а именно: значительное снижение средней скорости кровотока, пика систолической и конечной диастолической скорости кровотока в передней и в средней мозговой артерии.
Индометацин назначается по 50-100 мг каждые 8 ч в течение 2-3 сут. Оправдано его назначение при многоводии, так как он снижает продукцию мочи у плода.
Антагонисты кальция уменьшают сократительную активность миометрия за счет нарушения проникновения ионов кальция в гладкомышечную клетку. Большинством проведенных исследований показана невысокая токолитическая эффективность этой группы препаратов. Побочные действия не выражены. Возможные осложнения, связанные с применением нифедипина, следующие: транзиторная гипотензия, тахикардия, аритмия.
Антагонисты рецепторов окситоцина (атозибан)
Показана эффективность антагонистов рецепторов окситоцина при внутривенном или длительном подкожном введении в срок более 28 нед беременности при интактных плодных оболочках.
Препарат атозибан - небелковый аналог окситоцина, способный подавлять окситоцин-индуцированные сокращения миометрия. Использование препарата для прекращения родовой деятельности одобрено в США. Однако данных о клиническом применении атозибана недостаточно для точной оценки его эффективности и безопасности.
Однако несмотря на большой арсенал современных токолитических средств частота преждевременных родов не имеет значительной тенденции к снижению. Это связано прежде всего с поздним началом лечения, неадекватным выбором препарата, его дозы и режима введения.
Следующим аспектом проведения токолитической терапии, заслуживающим особого внимания, является ее использование при ведении беременных с дородовым излитием вод. Акушерская тактика при дородовом излитии вод (причина не менее 40% всех преждевременных родов) - наиболее сложная и до конца не решенная акушерская задача.
В настоящее время при излитии вод до 34 нед беременности официально принята выжидательная тактика, а длительность проведения токолиза ограничена временем профилактики респираторного дистресс-синдрома плода - т. е. 2 сут. Этот подход регламентирован в Приказе ? 318 МЗ РФ.
Однако значительные успехи неонатологов в выхаживании глубоконедоношенных новорожденных диктуют необходимость пересмотра акушерской тактики при дородовом излитии вод в сторону максимального пролонгирования беременности.
После 28 нед беременности прогрессивно повышается выживаемость новорожденных и снижается процент инвалидизации. Значит, максимальное пролонгирование беременности в эти сроки должно быть стратегической задачей перинатологии.
К сожалению, высокий риск гнойно-септических осложнений матери заставляет крайне осмотрительно относиться к пролонгированию беременности при дородовом излитии вод. Однако четкое выполнение профилактических мероприятий и наличие широкого спектра современных противомикробных препаратов позволяют значительно снизить процент гнойно-септических осложнений и обеспечивают возможность проведения длительного токолиза при дородовом излитии вод.
Схемы профилактической антибиотикотерапии при дородовом излитии вод
1. Эмпирическое назначение антибактериальной терапии сразу после взятия материала для посева.
2. Проведение антибактериальной терапии после получения результатов лабораторных исследований (микроскопия/посев околоплодных вод, посев из цервикального канала).
3. Проведение антибактериальной терапии при появлении клинических признаков хориоамнионита.
Наиболее распространена схема эмпирического назначения антибиотикотерапии и так как первостепенное значение среди бактериальных возбудителей в генезе инфекционного поражения плода имеет стрептококк группы В, то антибиотиками выбора являются полусинтетические пенициллины (ампициллин).
В связи с этим перспективным является проведение длительной токолитической терапии до 32-34 нед беременности в соответствии с уровнем оснащения и квалификации неонатальной службы и на фоне профилактики респираторного дистресс-синдрома плода с учетом четко ограниченных противопоказаний.
Тактика ведения недоношенной беременности (до 34 нед) при дородовом излитии околоплодных вод.
• 1. Профилактика инфицирования: соблюдение гигиенических принципов и норм;
• исключение влагалищных исследований;
• динамический лабораторный анализ микрофлоры.
2. Мониторинг состояния матери:
• термометрия;
• клинико-лабораторный анализ крови;
• визуальная оценка выделений (вод) из половых путей.
3. Мониторинг состояния плода:
• КТГ;
• динамическая оценка объема околоплодных вод (индекс амниотической жидкости).
4. Профилактика респираторного дистресс-синдрома плода.
5. Токолитическая терапия.
6. Антибиотикотерапия.
Противопоказания к токолитической терапии при преждевременном разрыве плодных оболочек
1. Гестационный срок более 34 нед.
2. Появление признаков системного воспаления (лихорадка, лейкоцитоз со сдвигом лейкоцитарной формулы).
3. Появление клинических признаков хориоамнионита и/или эндометрита.
4. Внутриутробное страдание и гибель плода.
5. Осложнения беременности и другие патологии, при которых показано прерывание беременности независимо от наличия плодного пузыря.