Медицинская микробиология, вирусология и иммунология: том 1 : учебник / Под ред. В.В. Зверева, М.Н. Бойченко, 2010.
|
|
|
|
ГЛАВА 8 УЧЕНИЕ ОБ ИНФЕКЦИИ
8.1. Инфекция. Формы инфекционного процесса
Понятия «инфекция» и «инфекционная болезнь» не являются синонимами.
Понимая под инфекцией взаимодействие патогенного (болезнетворного) микроорганизма и восприимчивого (чувствительного) хозяина в определенных условиях внешней среды, следует заметить, что инфекционная болезнь - это крайняя степень проявления инфекционного процесса, когда образуется патологический очаг и появляется специфическая клиническая симптоматика.
В основе инфекции лежит феномен паразитизма, определяющий антагонистические взаимоотношения симбионтов.
Классифицируют различные формы инфекционного процесса (инфекции) в зависимости от природы патогена, происхождения, условий возникновения инфекции, характера и длительности ее течения и т.д.
В зависимости от природы патогена, принадлежности к определенному таксону существует классификация инфекций по этиологическому принципу: бактериальные (дизентерия, сальмонеллез, дифтерия, туберкулез, гонорея и т.д.), вирусные (грипп, ВИЧинфекция, оспа, энцефалит, бешенство и т.д.), грибковые (кандидоз, аспергиллез, трихофития и др.), протозойные (малярия, токсоплазмоз, лямблиоз), прионные (куру, болезнь Крейтцфельда-Якоба, скрепи).
Если геном возбудителя интегрируется (встраивается) в геном хромосомы хозяина, то возникший инфекционный процесс может передаваться по наследству через генетический материал из поколения в поколения хозяина. Это интегративная форма инфекции. Примером интегративной формы инфекции являются инфекции
вирусной этиологии (лизогения в микробном мире, концерогенез - раковые линии мышей). Большинство инфекций, которыми болеет человек, по наследству не передаются (туберкулез, холера, грипп и т.д.) и называются неинтегративными. Нельзя путать интегративную форму инфекции с врожденной, когда возбудитель передается от матери плоду через плаценту (сифилис, ВИЧинфекция и т.д.), или новорожденный во время родов инфицируется при прохождении через родовые пути матери (бленнорея).
По происхождению инфекции делят на экзогенные и эндогенные.
Экзогенная инфекция возникает при попадании возбудителя в организм извне. Для экзогенной инфекции обязательно наличие трех элементов эпидемического процесса: источник инфекции, механизм передачи патогена, восприимчивый организм. Например, для сифилиса: источник инфекции - больной человек, механизм передачи патогена половой, восприимчивый организм - человек. Эндогенная (оппортунистическая) инфекция вызывается представителями нормальной микрофлоры при снижении защитных сил организма (иммунодефицитные состояния). Возбудители эндогенной инфекции относятся к условно-патогенным видам микроорганизмов. Пример эндогенной инфекции - фурункул носа стафилококковой этиологии (Staphylococcus epidermidis). Инфекция возникла при переохлаждении организма и развитии местного иммунодефицита слизистой оболочки носа. Эндогенная инфекция может развиться и при перемещении микроорганизмов из одного биотопа человека в другой за счет искусственного переноса руками, инструментами либо естественного перехода микроорганизма - его транслокации (миграции). Пример такой формы - эшерихиозный цистит, возбудитель Escherichia coli, которая попала на слизистую оболочку мочеполовой системы из кишечника.
По локализации патогена в организме различают местную и генерализованную формы инфекции. Местная или очаговая инфекция имеет место, когда возбудитель локализуется в определенном органе либо ткани и не распространяется по организму. Например, при ангине возбудитель (чаще всего Streptococcus pyogenes) находится на слизистой оболочке миндалин; при фурункулезе возбудитель Staphylococcus aureus - в волосяном фолликуле.
При генерализованной инфекции патоген распространяется по организму, преодолевая различные защитные барьеры: лимфоид-
ную ткань, гематоэнцефалический барьер, фасции мышечной ткани, соединительную ткань и т.д. Кровь является одним из частых путей распространения патогена - гематогенный путь. Если возбудитель, распространяясь по крови, не размножается в ней, то такое явление называют бактериемией или вирусемией (в зависимости от принадлежности патогена к той или другой таксономической группе). В случае, когда бактерии размножаются в крови, развивается одна из тяжелых форм генерализованной инфекции - сепсис. Сепсис может перейти в септикопиемию, когда патоген размножается во внутренних органах, вызывая в них образование гнойных очагов воспаления. При высокой концентрации бактерий и их токсинов в крови может развиться токсико-септический шок за счет массивного поступления токсинов. Вследствие генерализации инфекции поражаются различные органы и ткани организма (менингококковый менингит, туберкулез позвоночника).
Инфекционный процесс классифицируется в зависимости от числа проникших в организм видов патогена и динамики их действия. Моноинфекция вызывается патогеном одного вида (туберкулез, дифтерия). Смешанная (микст) инфекция - одновременное заражение двумя видами возбудителей и более и развитие сразу нескольких заболеваний (ВИЧ-инфекция и гепатит В при заражении через шприц у наркоманов; сифилис, гонорея и хламидиоз при половом заражении). Реинфекция - повторное заражение тем же видом возбудителя после выздоровления. Реинфекция возможна при заболеваниях, после которых не остается стойкий иммунитет: после гонореи, сифилиса, дизентерии. Если повторное заражение происходит тем же возбудителем до выздоровления, то возникает суперинфекция (сифилис). Вторичная инфекция возникает на фоне развившегося первичного заболевания и вызывается другим видом возбудителя. Вторичная инфекция может быть экзогенной или эндогенной. Чаще вторичная инфекция развивается как эндогенная, когда вследствие ослабления организма первичным заболеванием представители нормальной микрофлоры тела человека вызывают вторичное заболевание как осложнение первичного, например, при гриппе развивается стафилококковая пневмония, при СПИДе - пневмоцистная пневмония.
По длительности течения различают острые и хронические инфекции. Острые инфекции протекают непродолжительное время, их срок исчисляется днями, неделями (грипп, корь, холера, чума).
Хронические инфекции протекают в течение нескольких месяцев, лет (бруцеллез, туберкулез, сифилис). При определенных условиях (неэффективное лечение) острые инфекции могут переходить в хронические (гонорея, дизентерия). Хронические инфекции протекают в виде ремиссии и рецидива, которые сменяют друг друга. При ремиссии больной может чувствовать себя удовлетворительно, клинические симптомы болезни могут не проявляться либо проявляются в незначительной степени. При рецидиве имеют место обострение патологического процесса, выраженность клинической картины. При хроническом инфекционном процессе возбудитель персистирует в организме хозяина, т.е. длительно паразитирует в его тканях и клетках.
Особенности эпидемиологии инфекционного процесса позволяют классифицировать несколько форм инфекции. Эпидемической называется инфекция, когда ею охвачено население больших территорий (одной или нескольких стран), например грипп, холера.
Эндемическая инфекция локализуется в определенной географической местности, где возбудитель циркулирует между определенными видами животных в данной географической местности (чума, бруцеллез, туляремия).
В зависимости от источников заражения человека различают антропонозные, зоонозные и сапронозные инфекции. При антропонозных инфекциях единственным источником заражения является человек (ВИЧ-инфекция, сифилис). При зоонозных инфекциях основным источником заражения являются животные (бешенство, сибирская язва, бруцеллез). Возбудителями сапронозных инфекций являются сапрофиты, обитающие во внешней среде (легеонеллезы, листериоз). Следовательно, источниками заражения сапронозами являются объекты внешней среды: почва (столбняк, газовая гангрена), вода (лептоспирозы).
В настоящее время большое распространение получила госпитальная (внутрибольничная) инфекция, которая возникает в лечебно-профилактических учреждениях (стационарах, родильных домах и т.д.). Источником возникновения госпитальной инфекции часто является медицинский персонал: бактерионосители стафилококков, энтеробактерий и других условно-патогенных или патогенных микроорганизмов.
Типичное инфекционное заболевание чаще всего протекает в манифестной форме и характеризуется определенными клиническими
проявлениями (симптомокомплексом) и циклическим течением. Например, при типичном течении брюшного тифа наблюдается тифозный статус, развивается розеолезная сыпь на 8-10-й день болезни и т.д. Болезнь протекает стадийно и продолжается 3-4 нед.
Возможно атипичное (стертое) течение болезни без характерного симптомокомплекса. При стертом течении брюшного тифа сыпь появляется рано (на 4-6-й день), скудная; тифозный статус не выражен. В ряде случаев болезнь может протекать вообще без проявления каких-либо симптомов, и результат развившегося патологического процесса может проявиться лишь в виде смертельно опасных осложнений (легочное кровотечение при бессимптомно протекающем туберкулезе легких, перитонит как следствие перфорации кишечника брюшнотифозными язвами, порок сердца как следствие ревматического эндокардита).
Инфекционный процесс может протекать в форме бессимптомной инфекции: латентной (скрытой) или бактерионосительства (вирусоносительства). При латентной форме инфекции возбудитель длительное время находится в организме (персистирует), но не проявляет своего патогенного действия. Например, туберкулезная палочка может персистировать многие годы в ткани легкого здорового человека, вирус герпеса пожизненно персистирует в чувствительных ганглиях тройничного нерва, возбудитель бруцеллеза персистирует в мезентериальных лимфатических узлах. При латентной инфекции возбудитель не выделяется во внешнюю среду, латентная инфекция может переходить в манифестную форму (болезнь) при снижении иммунитета.
Бактерионосительство - длительное или кратковременное пребывание возбудителя в организме здорового человека. В отличие от латентной инфекции, бактерионосители выделяют возбудителя в окружающую среду и являются источниками распространения инфекции (брюшной тиф, дифтерия, стафилококковая инфекция). Медленная инфекция характеризуется персистенцией патогена, при которой имеет место многомесячный или многолетний инкубационный период, после которого медленно, но неуклонно развиваются симптомы заболевания, всегда заканчивающегося летально (ВИЧ-инфекция, бешенство, проказа).
В развитии инфекционной болезни выделяют 4 основных периода: инкубационный, продромальный, разгар болезни и реконвалесцентный (выздоровление).
Инкубационный период - период адгезии возбудителя на чувствительные клетки организма в месте входных ворот. Это могут быть миндалины, верхние дыхательные пути, слизистая оболочка желудочно-кишечного, репродуктивного тракта и др. В окружающую среду возбудитель не выделяется. Длительность периода от нескольких часов (грипп), дней (чума, туляремия, дифтерия) до нескольких месяцев (бешенство) и даже лет (СПИД, проказа, губчатая энцефалопатия).
В продромальный период имеет место колонизация чувствительных клеток, участков организма возбудителем. Осуществляется расселение микроорганизмов в биотопе хозяина и начинают появляться неспецифические (общие) симптомы болезни (повышается температура, возникают головная боль, потоотделение, слабость и др.). В этот период возбудитель также, как правило, не выделяется в окружающую среду.
Последующее интенсивное размножение возбудителя в организме хозяина знаменует разгар болезни с появлением специфической симптоматики (высыпания на коже при тифах, параличи нижних конечностей при полиомиелите, пленчатые налеты на слизистых оболочках носа, зева, гортани при дифтерии и др.). В этот период больной заразен, так как возбудитель выделяется во внешнюю среду. Наконец, после прекращения размножения возбудителя и по мере выведения его из организма наступает период реконвалесценции (выздоровления). К этому моменту начинается восстановление нарушенных функций. Как правило, прекращается выделение микроорганизмов, но в некоторых случаях возможно формирование реконвалесцентного бактерионосительства с длительным пребыванием возбудителя в организме хозяина, перенесшего инфекцию.
Особое место при характеристике инфекции имеют пути ее передачи, что важно для эпидемиологических целей. Существуют три основных варианта передачи возбудителя человеку: горизонтальный, вертикальный и артифициальный (искусственный).
Горизонтальный вариант включает воздушно-капельную передачу возбудителя от больного здоровому (грипп, дифтерия); фекально-оральный (холера, брюшной тиф), контактный (сифилис, гонорея) и трансмиссивный (чума, энцефалиты) пути.
Для вертикального варианта типичен трансплацентарный путь передачи возбудителя от матери плоду (сифилис, краснуха) или в родах от матери новорожденному (бленнорея).
Артафициальный (рукотворный, искусственный) вариант предусматривает передачу возбудителя при инструментальном обследовании больного, введении инъекций, при оперативных вмешательствах (гепатиты, СПИД).
Различают 4 уровня инфекционного процесса: популяционный, организменный, клеточный и молекулярный.
Популяционный уровень определяет взаимодействие возбудителя с восприимчивыми особями популяции. Для организменного уровня важен комплекс (система) реакций восприимчивого хозяина на инфекцию. Клеточный или тканево-органный уровень - это выбор возбудителем соответствующих клеток-мишеней макроорганизма. На молекулярном уровне рассматривается конкурентное взаимодействие биомолекул патогена и хозяина в условиях инфекции.
8.2. Движущие силы инфекционного процесса
Исходя из определения инфекционного процесса, выявляют, по крайней мере, 3 основных участника инфекции: возбудитель, хозяин и факторы внешней среды.
Возбудитель болезни - микробная клетка - характеризуется количественными и качественными характеристиками: патогенностью (видовой признак) и вирулентностью (индивидуальная характеристика штамма).
Платформа, на которой развертывается инфекция, - это организм человека-хозяина, который должен быть восприимчив к инфекту (видовой признак) и быть чувствительным к нему (индивидуальная характеристика), т.е. иметь инфекционную чувствительность. При этом физиологические характеристики хозяина, состояние его естественной резистентности играют при этом далеко не последнюю роль.
И наконец, третий участник инфекции - условия внешней среды, в которой происходит инфицирование организма возбудителем. Различные физические, химические, биологические и социальные факторы среды имеют существенное значение для формирования и развития инфекционного процесса. При гибели патогена либо хозяина инфекционный процесс прерывается. В условиях же взаимной адаптации патогена и хозяина (персистенции патогена) имеет место продолжение инфекционного процесса в форме рези-
дентного бактерионосительства, латентной инфекции или хронического заболевания. Факторы внешней среды, хотя и в различной степени, участвуют в формировании инфекционного процесса, определяя его развитие и исход.
Таким образом, возникновение, течение и исход инфекционного процесса зависят от качественных и количественных характеристик партнеров в каждой конкретной ситуации взаимодействия паразит-хозяин. Скажем, при чуме и ВИЧ-инфекции ведущая роль в развитии инфекционного процесса принадлежит возбудителю, ибо он почти в 100% случаев вызывает болезнь и высокую летальность (исключается факт вакцинации). Развитие эндогенных, вторичных инфекций, вызываемых условно-патогенными микробами (Klebsiella pneumoniae, Escherichia coli и др.), во многом определяют защитные силы хозяина. Для возникновения госпитальных инфекций (стафилококковые и др.) важное значение имеет как иммунный статус хозяина, так и состояние противоэпидемических мероприятий в лечебно-профилактическом учреждении, т.е. условия внешней среды. По какому сценарию будет развиваться инфекция, это и определяют движущие силы инфекционного процесса.
8.3. Роль возбудителя в инфекционном процессе и его основные биологические характеристики
Возбудитель как участник инфекционного процесса характеризуется двумя основными качествами: патогенностью и вирулентностью.
Патогенность - видовой признак: способность определенного вида микроорганизмов вызывать соответствующий инфекционный процесс у одного или нескольких видов организма хозяина. Например, патогенные виды Vibrio cholerae, S. Typhi, N. gonorrhoeae способны вызывать соответствующую инфекцию у человека, но не у других видов.
Но этот диапазон (спектр) патогенности у разных микробов различный. Если названные микроорганизмы (печальная «привилегия» рода человеческого) патогенны только для человека, то число восприимчивых хозяев для других микроорганизмов значительно больше и не ограничивается только человеком. Для Mycobacterium tuberculosis составляет 9 видов, Y. рestis - 11 видов, Br. аbortus -
21 вид, а для F. tularensis - 141 вид, включая не только животных, но и птиц. Диапазон патогенности микробов сформировался в результате длительной эволюции системы паразит-хозяин. Отсюда и разные корни происхождения патогенных видов микроорганизмов.
От возбудителей болезней предков человека - человекообразных обезьян произошли вирусы герпеса и иммунодефицита человека, малярийный плазмодий. Микробы - паразиты членистоногих - способствовали отбору возбудителей сыпных тифов (риккетсиозов). Нормальная микрофлора тела человека - родоначальник возбудителей дизентерии, дифтерии, полиомиелита. Дикие животные до появления человека страдали от бешенства, чумы, туляремии. От домашних животных к человеку перешли такие болезни, как корь, брюшной тиф, натуральная оспа. Микробы-сапрофиты дали начало возбудителям холеры, сифилиса, лептоспирозов.
Патогенные виды микробов реализуют свою способность вызывать инфекционный процесс у большинства особей популяции восприимчивого вида макроорганизма.
Если же способность микроба вызывать инфекцию у восприимчивого вида макроорганизма в значительной степени определяется состоянием иммунитета особей популяции и, как правило, инфекция развивается в условиях иммунодефицита, то такие виды микробов называются условно-патогенными, например Escherichia coli, Staphylococcus epidermidis, Klebsiella pneumoniae.
Вирулентность - индивидуальный, штаммовый признак: степень (количественная мера) реализации патогенности вида каждым конкретным штаммом по отношению к конкретному индивидууму - хозяину. Если штамм Vibrio cholerae выделен от больного А, погибшего от холеры, значит, он оказался по отношению к этому индивидууму высоковирулентным. Степень вирулентности конкретного штамма внутри популяции патогенного вида микроорганизмов можно оценивать по клиническому течению инфекционного процесса у человека, от которого выделен данный штамм; на модели in vivo путем воспроизведения экспериментальной инфекции на животных; на модели in vitro путем качественного и количественного изучения факторов вирулентности конкретного штамма (клинико-лабораторные исследования).
На модели экспериментальной инфекции проводят количественную оценку вирулентности штамма, используя условно при-
нятые единицы измерения вирулентности: DLM и LD50. DLM (от лат. Dosis letalis minima) - наименьшее количество микробных клеток, способное вызвать гибель 95% животных восприимчивого вида определенной массы, пола и возраста при определенном способе заражения и в течение заданного времени. LD50 - количество бактерий, вызывающее гибель 50% животных в эксперименте. В ряде случаев с экспериментальной целью определяют DCL (от лат. Dosis certa letalis) - смертельную дозу, вызывающую 100% гибель инфицированных животных.
Вирулентность возбудителя можно регулировать в сторону как ее снижения, так и повышения. В свое время французские исследователи Кальмет и Жерен культивировали возбудитель туберкулеза (бычьего типа) на картофельно-глицериновых средах с добавлением желчи (неблагоприятный фактор для возбудителя) в течение 13 лет. В результате им удалось осуществить около 230 посевов возбудителя, потерявшего вирулентность, и на основе авирулентного штамма создать вакцину БЦЖ (бациллы Кальмета-Жерена) для профилактики туберкулеза. В ряде случаев вирулентность микробов снижается под воздействием различных физико-химических факторов, лекарств и т.д. Снижение вирулентности штаммов называют аттенуацией (ослаблением).
С другой стороны, известно, что путем пассажа (проведения) через организм восприимчивых животных удается повысить вирулентность возбудителя, что нередко бывает необходимо при проведении экспериментальных работ.
К условиям, регулирующим вирулентность возбудителя, относят химический состав бактерийной клетки, особенности ее метаболизма, структуру генома и среду обитания (экологию).
8.3.1. Факторы вирулентности
Классификация факторов вирулентности зависит от их структуры, происхождения, механизма действия и назначения.
По структуре и происхождению факторы вирулентности можно классифицировать на две основные группы: структурные компоненты бактериальной клетки и секретируемые факторы.
8.3.1.1. Структурные компоненты бактериальной клетки
К ним относятся капсула, пили, пептидогликан клеточной стенки, белки наружной мембраны и липополисахарид грамотри-
цательных бактерий, которые подробно изложены в материалах диска.
8.3.1.2. Секретируемые факторы
Помимо структур бактериальной клетки, способствующими проявлению ее вирулентных качеств, известна группа микробных секретируемых факторов, участвующих в инфекционном процессе: бактериоцины, экзотоксины, ферменты «защиты и агрессии», секретируемые факторы персистенции.
Бактериоцины - белки, медиаторы межмикробного взаимодействия, секретируются бактериальной клеткой в качестве антагонистически активных веществ. Бактериоцины выделяются в условиях близкородственного антагонизма внутри вида, рода бактерий. Бактериоцины обеспечивают колонизацию вирулентным штаммом определенного биотопа, подавляя нормальную микрофлору: колицины Shigella flexneri подавляют Escherichia coli, стафилококкцины S. аureus подавляют S. еpidermidis и т.д. Колициногенные штаммы шигелл чаще вызывают затяжные и более тяжелые формы заболевания, чем неколициногенные. Бактериоциногенные штаммы стафилококков значительно чаще выделяются от больных из патологических очагов, чем с кожи и слизистых оболочек здоровых людей. При хронических формах стрептококковой инфекции (ревматизм, хронический тонзиллит) бактериоциногенные штаммы обнаруживаются в 2 раза чаще, чем у здоровых людей.
Экзотоксины - вещества белковой природы, секретируемые вирулентными штаммами микроорганизмов и оказывающие токсическое действие на клетки и ткани организма хозяина.
К факторам вирулентности относятся и ферменты, продуцируемые бактериальной клеткой. Ферменты вирулентности образно называют ферментами «защиты и агрессии». Ферменты защиты обеспечивают устойчивость патогена к иммунитету хозяина: фермент коагулаза свертывает плазму крови, вследствие чего вокруг бактериальной клетки образуется защитная капсула; протеазы иммуноглобулинов разрушают антитела. Ферменты агрессии обеспечивают распространение патогена по организму, они разрушают структуры клеток и тканей организма: гиалуронидаза разрушает соединительную ткань (S. аureus, S. рyogenes), нейраминидаза расщепляет сиаловые кислоты оболочек клеток (вирус гриппа), фибринолизин растворяет сгустки фибрина (S. рyogenes), ДНКаза
разрушает нуклеиновые кислоты (S. aureus), эластаза расщепляет лизоцим клеток организма (Pseudomonas).
Ферменты метаболизма бактерий, вызывающие образование токсичных веществ при расщеплении субстратов организма, также рассматривают в качестве ферментов вирулентности: микробная уреаза при гидролизе мочевины образует токсичные вещества (Helicobacter pylori), декарбоксилаза при разрушении белка способствует накоплению биогенных аминов (Salmonella Enteritidis). Вирулентность бактерий обеспечивается ферментами супероксиддисмутазой и каталазой, которые инактивируют высокоактивные кислородные радикалы при фагоцитозе (Leg. pneumophila, M. tuberculosis).
Секретируемые факторы персистенции бактерий подавляют специфические и неспецифические механизмы защиты хозяина, обеспечивая бактериям выживание при инфекции. По химической природе это в основном бактерийные протеазы, расщепляющие специфический субстрат хозяина, создающий ему защиту от патогена. Они обеспечивают антилизоцимную, антиинтерфероновую, антикомплементарную, антигистоновую, антилактоферриновую и антигемоглобиновую активность. Подробно изложено в материалах диска.
В реализации вирулентности возбудителя важна доставка вирулентных протеинов на поверхность бактериальной клетки в место контакта ее с поверхностью эукариотической клетки и/или введения протеинов в цитозоль клетки хозяина. В процессе эволюции у бактерий выработано несколько типов секреторных систем, которые подробно описаны в разделе 3.1.5. Термин «секреция» используется для описания активного транспорта протеинов из цитоплазмы через внутреннюю и наружную мембраны в супернатант (окружающую среду) бактериальной культуры или на поверхность бактериальной клетки. Секреция отличается от экспорта, который заключается в транспортировке протеинов из цитоплазмы в периплазматическое пространство. Напомним, что I тип секреторной системы является sec-независимым путем (не находится под контролем sec-гена, отвечающего за секрецию). Этим путем транспортируются α-гемолизин E. coli, внеклеточная аденилатциклаза B. pertussis, протеазы P. aeruginosa. Молекулы, транспортируемые I типом секреторной системы, требуют для транспортировки 3-4 вспомогательные молекулы, участвующие в образовании трансмембранного канала, через который и происходит выход протеинов.
II тип секреции - основной для экстраклеточных расщепляющих энзимов грамотрицательных бактерий. Эта система использует традиционные sec-зависимые пути для выведения экспортируемых молекул через внутреннюю мембрану в периплазматическое пространство. II тип секреторной системы участвует в экспорте огромного количества разнообразных молекул, включая вирулентные факторы: пили у P. aeruginosa (4 типа) и родственные им, энзим-pullulanase y Klebsiella, пектические энзимы и целлюлазы y Erwinia, эластазы, экзотоксин А, фосфолипазы С и другие протеины y Pseudomonas aeruginosa, амилазы и протеазы у Aeromonas hydrophila и т.д.
III тип секреторной системы - большая экспортная система, независимая от sec-системы, которая играет существенную роль в секреции вирулентных факторов у возбудителей болезней человека и растений. III тип секреторной системы отвечает за секрецию наружных протеинов Yersinia spp., факторов инвазии и вирулентности сальмонелл и шигелл, молекул сигнальной трансдукции энтеропатогенной кишечной палочки и вирулентных факторов некоторых возбудителей заболеваний растений, а также вовлечен в биосинтез поверхностных органелл - флагеллярных белков.
В отличие от I типа секреторного пути, являющегося истинной секреторной системой, в котором секреторные энзимы приобретают активность в экстраклеточном пространстве, тип III - это механизм для транслокации протеинов в цитозоль эукариотической клетки, ибо он обеспечивает сборку на поверхности бактериальной клетки супермолекулярных структур, участвующих в транспорте протеинов в эукариотическую клетку. Аппарат III типа секреторной системы включает около 20 протеинов, большинство которых располагается во внутренней мембране, и цитоплазматическую мембранно-связанную АТРазу (АТФазу).
V тип секреторной системы включает группу так называемых аутотранспортеров - семейство секреторных протеинов, осуществляющих свой собственный транспорт из бактерий: гонококковую IgA-протеазу и IgA-протеазу H. influenzaece.
8.3.2. Патогенетические факторы возбудителя при инфекции
Классификация факторов патогенности по назначению и механизму действия включает патогенетически значимые продукты
бактерийной клетки, определяющие этапность развития инфекционного процесса и его исход. Эти факторы объединяют в 4 группы: колонизации, инвазии, токсигенности и персистенции.
8.3.2.1. Факторы колонизации патогена
Колонизация - расселение микроорганизмов в определенном биотопе хозяина. Этот этап инфицирования организма начинается с адгезии - прикрепления возбудителя к клеткам организма у входных ворот инфекции. За прикрепление микроба отвечают специальные структуры - адгезины. У грамотрицательных бактерий в этот процесс включаются пили (ворсинки), белки наружной мембраны, а у грамположительных микроорганизмов - тейхоевые кислоты, поверхностные белки. Адгезия специфична у каждого возбудителя с учетом его тропности к тканям, клеткам хозяина, где и осуществляется рецепторлигандное прикрепление возбудителя. Последующее закрепление возбудителя на эукариотических клетках организма вызывает расселение микроорганизмов в инфицированном биотопе хозяина. Этому способствуют участие бактериальных протеаз, блокирующих секреторную защиту организма IgA, продукция бактериоцинов, антиоксидантов, продукция сидерофоров, конкурирующих с лактоферрином за ионы Fe. Таким образом, адгезия и последующая колонизация - начальные (ранние) стадии патогенеза инфекционного процесса.
8.3.2.2. Факторы инвазии микроорганизмов
Инвазия - проникновение возбудителя внутрь клеток организма (пенетрация), преодоление естественных барьеров организма (кожа, слизистые оболочки, лимфатическая система и др.). Этим процессом управляют инвазины - молекулы бактерий, способствующие проникновению патогена в клетку. В этот период усиливается действие токсичных продуктов - уреаза осуществляет гидролиз мочевины с образованием в организме аммиака, токсичных биогенных аминов. Микроорганизмы продуцируют гемолизин, разрушающий эритроциты, лейкоцидин, разрушающий лейкоциты, спридинг-факторы - ферменты агрессии, способствующие генерализации инфекции за счет распространения возбудителя в организме. Включаются в работу такие ферменты агрессии, как лецитовителлаза, расщепляющая липопротеид мембран клеток хозяина, фибринолизин, устраняющий сгусток фибрина для дальнейшего распространения микроба по организму; гиалуронидаза,
расщепляющая гиалуроновую кислоту - вещество соединительной ткани; нейраминидаза - фермент распространения патогена, IgA-протеаза, обеспечивающая устойчивость возбудителя к перевариванию фагоцитами и действию антител и др. Процесс инвазии у некоторых грамотрицательных бактерий обеспечивается III типом секреторной системы, которая отвечает за секрецию факторов инвазии, в частности, у сальмонелл и шигелл, молекул сигнальной трансдукции энтеропатогенной кишечной палочки. В процессе инвазии в эпителиальные клетки возбудитель (S. Typhimurium) вступает в интимные отношения с клетками и использует физиологические механизмы обеспечения их жизнедеятельности для обслуживания собственных нужд, вызывая массивную реаранжировку цитоскелета клетки хозяина и активацию вторичных мессенжеров - транзитное повышение уровня инозитолтрифосфата и выброс Ca2+.
В защите от фагоцитоза принимают участие как поверхностные структуры бактериальной клетки, так и продуцирумые ею вещества. Антифагоцитарной активностью обладают капсулы (S. pneumoniae, N. meningitidis), поверхностные белки: А белок у S. aureus, M-протеин у S. pyogenes. Некоторые бактерии, например возбудитель коклюша, продуцируют внеклеточную аденилатциклазу, ингибирующую хемотаксис, таким образом позволяя бактерии избежать захвата фагоцитами. Ферменты супероксиддисмутаза и каталаза инактивируют высокореактивные кислородные радикалы при фагоцитозе (Y. pestis, L. pneumophila, S. Typhi). Отмечено участие секреторной системы III типа у некоторых бактерий в реорганизации цитоскелета фагоцита, предотвращающее образование фаголизосомы.
8.3.2.3. Факторы токсигенности бактерий
Токсигенность - продукция бактериями токсичных веществ, повреждающих клетки и ткани организма хозяина.
Наличие токсина у бактерий является патогенетически значимым в ходе развития инфекционного процесса. Токсичный компонент присутствует практически при любой инфекции и проявляет свое действие, хотя и в разной степени.
Токсины, секретируемые возбудителем в среду, обнаруживаются в фазе роста и накапливаются в цитоплазме. Это белки - экзотоксины. Эндотоксины входят в состав клеточной стенки и высвобождаются лишь при гибели микробной клетки.
К эндотоксинам относят ЛПС клеточной стенки грамотрицательных бактерий, пептидогликан, тейхоевые и липотейхоевые кислоты, гликолипиды микобактерий. Хорошо изучены эндотоксины энтеробактерий (эшерихии, шигеллы, сальмонеллы, бруцеллы). Некоторые бактерии одновременно образуют как экзо-, так и эндотоксины (холерный вибрион, некоторые патогенные кишечные палочки и др.).
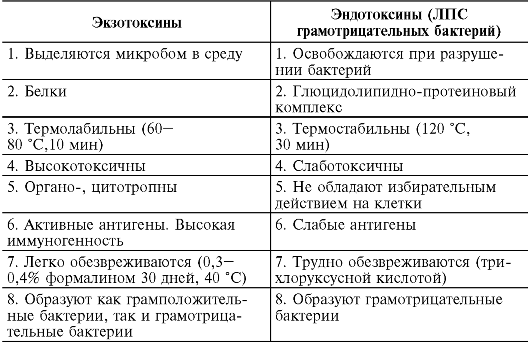
Сравнительная характеристика бактериальных экзотоксинов и эндотоксина ЛПС клеточной стенки грамотрицательных бактерий представлена в табл. 8.1.
Таблица 8.1. Сравнительная характеристика токсинов бактерий
 Экзотоксины
секретируются живой бактериальной клеткой, являются белками, полностью
инактивируются под действием высокой температуры (90-100 °С). Они
обезвреживаются формалином в концентрации 0,3-0,4% при 37 °С в течение
3-4 нед, при этом сохраняют свою антигенную специфичность и
иммуногенность, т.е. переходят в вакцину-анатоксин (столбнячный, дифтерийный, ботулиновый, стафилококковый и др.).
Экзотоксины
секретируются живой бактериальной клеткой, являются белками, полностью
инактивируются под действием высокой температуры (90-100 °С). Они
обезвреживаются формалином в концентрации 0,3-0,4% при 37 °С в течение
3-4 нед, при этом сохраняют свою антигенную специфичность и
иммуногенность, т.е. переходят в вакцину-анатоксин (столбнячный, дифтерийный, ботулиновый, стафилококковый и др.).
Экзотоксины обладают специфичностью действия на клетки и ткани организма, определяя клиническую картину заболевания.
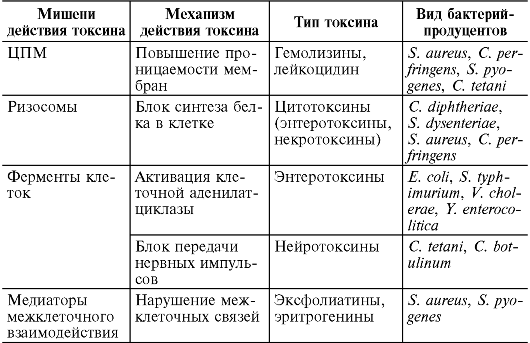
Специфичность экзотоксина определяется механизмом его действия на определенные мишени (табл. 8.2). Способность микробов к продукции экзотоксинов обусловлена в основном конвертирующими бактериофагами.
Таблица 8.2. Механизмы действия экзотоксинов
 Информация об эндотоксинах заложена в хромосомных генах бактерий, как и в любом другом клеточном компоненте.
Информация об эндотоксинах заложена в хромосомных генах бактерий, как и в любом другом клеточном компоненте.
Эндотоксины, в отличие от экзотоксинов, обладают меньшей специфичностью действия. Эндотоксины всех грамотрицательных бактерий (E. coli, S. Typhi, N. meningitidis, Brucella abortus и др.) угнетают фагоцитоз, вызывают падение сердечной деятельности, гипотонию, повышение температуры, гипогликемию. Большое количество поступившего в кровь эндотоксина приводит к токсикосептическому шоку.
Как и вирулентность, сила действия токсинов измеряется величиной летальных доз DLM, LD50, DCL, определяемая на животных.
Токсины, повреждающие ЦПМ клеток организма, способствуют лизису клеток: эритроцитов (гемолизины стафилококков, стрептококков и др.), лейкоцитов (лейкоцидин стафилококков).
Разнообразна группа токсинов, нарушающих функцию ферментов клетки. Экзотоксин C. diphtheriae, являясь цитотоксином, блокирует синтез белка на рибосоме клеток миокарда, надпочечников, нервных ганглиев, эпителиоцитов слизистой оболочки зева. Развивается некроз клеток и тканей, воспаление: дифтеритическая пленка, миокардит, полиневрит. Энтеротоксины холерного вибриона, энтеротоксигенных штаммов E. coli, S. aureus и др. активируют аденилатциклазу в эпителиоцитах слизистой оболочки тонкой кишки, что приводит к повышению проницаемости стенки кишечника и развитию диарейного синдрома. Нейротоксины палочек столбняка и ботулизма блокируют передачу нервных импульсов в клетках спинного и головного мозга.
Особая группа токсинов стафилококков и стрептококков (эксфолиатины, эритрогенины) нарушает межклеточные взаимодействия, что приводит к поражению кожи (пузырчатка новорожденных, скарлатинозная сыпь) и других органов.
Эритрогенный токсин является суперантигеном, вызывает прлиферацию Т-клеток, активируя тем самым каскад компонентов эффекторного звена иммунной системы, выброс медиаторов с цитотоксическими свойствами - интерлейкинов, факторов некроза опухоли, γ-интерферона. Инфильтрация лимфоцитов и локальное действие цитокинов играют важную роль в патогенезе инвазивной стрептококковой инфекции при целлюлитах, некротических фасцитах, септических поражениях кожи, поражениях внутренних органов.
8.3.2.4. Факторы персистенции патогенов
Персистенция возбудителя - форма симбиоза, способствующая длительному переживанию микроорганизмов в инфицированном организме хозяина (от лат. рersistere - оставаться, упорствовать).
Переход бактерий из одной среды существования в другую (внешняя среда - клетка хозяина) - вынужденный ход микроорганизмов, позволяющий в конечном счете обеспечить им выживание как вида, поэтому персистенция бактерий в организме рассматривается как стратегия выживания вида. Смена экологической ниши бактериальной клеткой и ее переход в организм хозяина сопровождаются неизменным появлением новых биологических характеристик у бактерий, облегчающих адаптацию патогена к новым условиям среды обитания.
Выживание бактерий в тканях хозяина определяется динамическим процессом равновесия между разрушением бактерий защитными факторами организма и накоплением (размножением) бактерий, которые угнетают или избегают защитные механизмы макроорганизма.
При блокировании бактериями защитных механизмов хозяина, т.е. освоении ими экологической ниши, определенную роль играют структурные особенности патогена.
В отличие от вирусов или риккетсий, бактерии имеют свои особенности при персистировании, связанные со своеобразием строения бактериальной клетки. Наличие пептидогликана, который присутствует только у прокариот и отсутствует в эукариотических клетках, делает его отличной иммунологической мишенью в организме хозяина, быстро определяющем чужеродную субстанцию. Пептидогликан - маркер чужеродности бактерий в условиях инфицированного хозяина. Поэтому любые адаптационные процессы бактериальной клетки, направленные на защиту (или изоляцию) пептидогликановой структуры клеточной стенки, можно рассматривать в качестве механизмов персистенции бактерий.
В процессе взаимодействия обоих участников инфекции у возбудителя эволюционно закрепилось 4 способа защиты пептидогликана от факторов иммунитета: экранирование клеточной стенки бактерий; продукция секретируемых факторов, инактивирующих защиту хозяина; антигенная мимикрия; образование форм с отсутствием (дефектом) клеточной стенки бактерий (L-формы, микоплазмы).
Персистенция микроорганизмов - базовая основа формирования бактерионосительства.
В патогенетическом плане бактерионосительство - одна из форм инфекционного процесса, при которой наступает динамическое равновесие между микро- и макроорганизмом на фоне отсутствия патологических изменений, но с развитием иммуноморфологических реакций и антительного ответа.
Для бактерионосительства характерна взаимная адаптация паразита и хозяина в целях симбиоза и возможной персистенции патогена. При этом, с одной стороны, происходит селекция биоваров носительских штаммов с комплексом факторов колонизации, персистенции и патогенности, а с другой - имеет место перестройка механизмов защиты хозяина с формированием его иммуноком-
прометированного статуса (иммунный дисбаланс, толерантность, дефицит местного иммунитета). В итоге создаются условия для персистенции (выживания) возбудителя, что и приводит к бактерионосительству. (Подробно механизм развития персистенции и формирования бактерионосительства изложены в материалах диска.)
8.3.3. Генетика вирулентности бактерий
Рассматривать жизнь возбудителя в инфицированном организме, вероятно, следует как серию шагов генной активации в ответ на дискретный комплекс окружающих условий. Эта генная регуляция вирулентности бактерий является экологически зависимой, обеспечивающей пластичность микроорганизмов, их адаптивные потенции.
Известно, что бактерии обладают одним большим эволюционным механизмом, благодаря которому идет формирование патогенных представителей. Гены вирулентности чаще всего обнаруживаются в больших сложных блоках, обозначенных как хромосомные вставки или патогенные острова (см. подробнее раздел 5.1.5). Эти острова и островки связаны между собой общими последовательностями, что указывает на приобретение ДНК-сегмента с помощью таких событий, как «незаконные» рекомбинации, имеющие сходство с транспозицией или вставкой фага. Эти ДНК-блоки наиболее часто встраиваются в горячие точки хромосомы - наиболее восприимчивые участки к вторжению чужеродных ДНК или места встраивания фага. Например, большие сегменты ДНК, кодирующие различные вирулентные факторы, встроены в одно и то же место хромосомы как у уропатогенной, так и у энтеропатогенной E. coli - возбудителей двух различных заболеваний, причем последовательности, расположенные внутри патогенного островка, не обнаруживают гомологии с теми, что имеют место у непатогенных клонов, подобных E. coli K-12, но последовательности, непосредственно прилегающие к патогенному островку, демонстрируют общность у патогенных и непатогенных штаммов.
Регионы хромосомных ДНК, кодирующих несколько кластрированных генов вирулентности, общие среди микроорганизмов от возбудителей растений до Helicobacter pylori и Yersinia pestis. В то же время, несмотря на определенную консервативность (в частности,
хромосом E. coli, S. Typhimurium), бактериальные хромосомы не являются константными, а постоянно изменяются. Фенотипические изменения способны модифицировать патогенность внутри различных клональных вариантов одного вида. Например, хромосома S. Typhi, которая вызывает заболевание только у человека, подлежит большой геномной реаранжировке в ходе своей эволюции по сравнению с нетифоидными сальмонеллами, а именно инверсиям, транспозициям и вставкам через события гомологических рекомбинаций. Естественно, некоторые из этих событий могут изменять вирулентность S. Typhi и повышать ее специфические адаптационные способности к организму человека. Регуляцию и экспрессию хромосомных вирулентных факторов могут изменять и такие эпизоды, как перетасовка хромосомных генов.
Считают, что патогенные микроорганизмы эволюционируют не за счет медленной адаптивной эволюции предсуществующих генов, а через сумму скачков, как правило, овладевая генетическими сегментами (которые кодируют множественные вирулентные факторы) не только родственных, но и неродственных организмов, и включают даже эукариотические последовательности (приобретение тирозиновой фосфатазы Yersinia). В последующем приобретенная генетическая информация интегрируется в хромосому или стабильную плазмиду. Соответствующая селекция вирулентных факторов обеспечивает сохранность таких последовательностей у возбудителей, а распространение этой генетической информации через мобильные генетические элементы (многие вирулентные гены кодируются на мобильных генетических элементах ДНК) дает гарантию возможности получения любыми микроорганизмами селективных преимуществ. Информация, которая не является необходимой, в основном теряется, так как отсутствует селективное условие для ее сохранения.
Экспрессия факторов вирулентности тесно связана с различными сигналами окружающей среды, в том числе с температурой, концентрацией ионов, осмомолярностью, уровнем железа, рН, наличием источника углерода, уровнем кислорода и рядом других, пока не установленных. Возбудитель способен использовать как один сигнал, так и их комплекс, чтобы «почувствовать», какое микроокружение он оккупирует внутри хозяина или даже внутри специализированного компартмента единственной клетки хозяина. Поэтому на каждом шаге инфекционного цикла (в ходе
достижения бактериями своих биологических задач) в ответ на калейдоскоп защитных ответов хозяина происходят динамическое включение и выключение различных генов - согласованный и взаимообусловленный процесс.
Например, экспрессия одного из антифагоцитарных факторов возбудителя чумы, фракции F1, экспрессируется максимально при 35-37 °С, когда возбудитель находится в организме человека, и падает при 28 °С при нахождении его в организме блохи. Инвазивные гены обычно включаются на ранней стадии инфекции, но репрессируются, когда бактерия оказывается внутри клетки хозяина. Дезорганизация экспрессии патогенных факторов во времени может разрушить процесс инвазии бактерий.
Таким образом, регуляция патогенности - это комплексное событие. Все вирулентные факторы могут контролироваться одновременно несколькими регуляторными системами, которые измеряют различные параметры окружающей среды, и в то же время несколько регуляторных систем могут регулировать один вирулентный фактор. Кроме того, регуляторные факторы обычно регулируют сами себя, что создает иерархию в регуляции и тонком контроле за экспрессией вирулентных факторов. В результате уровень вирулентности определяется средней величиной всех сигналов (окружения и регуляции).
8.4. Роль макроорганизма в инфекционном процессе
Организм хозяина - это платформа, на которой развертывается инфекционный процесс со всеми его проявлениями, и если микроб определяет специфичность инфекции, то особенности ее течения и формы проявления определяются состоянием макроорганизма.
Как и у микроба, здесь следует различать два основных признака: видовой и индивидуальный. Видовой признак - это восприимчивость хозяина к инфекту.
Восприимчивость - видовой признак, характеризующий способность определенного вида организмов (хозяев) участвовать в инфекционном процессе при взаимодействии с патогеном.
Организм человека восприимчив к холерному вибриону, но летучие мыши имеют врожденную устойчивость к этому возбудите-
лю. Для возбудителя туляремии организм зайцев, мышей, хомячков - подходящая ниша, где бактерии размножаются и вызывают инфекцию, но кошки, лисицы, хорьки генетически устойчивы к этому патогену. Ряд заболеваний характерен только для организма человека - сифилис, гонорея, дифтерия, так как подобрать других кандидатов для воспроизведения экспериментальной инфекции практически не удается за счет природной устойчивости животных к этим патогенам.
Что касается индивидуального признака, характеризующего меру восприимчивости организма к инфекции, то его определяют как инфекционную чувствительность.
Инфекционная чувствительность - это индивидуальная восприимчивость организма хозяина к патогену, вызывающему болезнь. Часто вместо термина «инфекционная чувствительность» используют термин с противоположным значением - «естественная резистентность», что делает эти понятия синонимами. Но и в том и в другом случае речь идет о врожденном (естественном) иммунитете, который, кроме своей неспецифичности в отношении к инфекту, всегда стойкий и передается по наследству, так как генетически запрограммирован.
Этот естественный иммунитет или естественная резистентность к патогену направлены на поддержание гомеостаза организма. Это неспецифическое распознавание чужеродной для хозяина информации (патогенов) осуществляется по единой программе, активность системы постоянная и не зависит от специфичности чужеродного агента. Он имеет как клеточную (клетки покровов и внутренних барьеров, фагоцитирующие клетки, естественные киллеры), так и гуморальную (лизоцим, комплемент, β-лизины, белки острой фазы и др.) основу. Среди факторов, определяющих естественную резистентность организма к инфекции выделяют: возраст хозяина, эндокринологический и иммунный статус, состояние физической активности, центральной нервной системы, эндогенные биологические ритмы, входные ворота инфекции и др.
Возраст существенно определяет уровень неспецифической защиты организма. У новорожденных в течение первого месяца жизни значительно снижена бактерицидная активность сыворотки крови. У детей чаще развиваются генерализованные формы инфекции, сепсис, тяжелее протекают многие инфекционные заболевания: сальмонеллезы, дизентерия, туберкулез и др. Только
у новорожденных имеет место колиэнтерит, так как их организм еще не вырабатывает секреторные IgA - основной фактор защиты слизистой оболочки тонкой кишки. Снижен уровень естественной резистентности у лиц пожилого возраста. В связи с нарушением функции лизосом у пожилых снижена активность внутриклеточного уничтожения патогена, поэтому они чаще болеют рецидивным сыпным тифом (болезнь Брилла) и чаще страдают от брюшнотифозного бактерионосительства.
Известен ряд болезней - коклюш, корь, дифтерия, которые типичны для детей. Лица пожилого возраста чаще погибают от пневмонии. Туберкулезная инфекция охватывает людей зрелого возраста.
Есть незначительные различия в уровне показателей естественной резистентности у лиц женского и мужского пола. У женщин выше, чем у мужчин, уровень бактерицидной активности сыворотки. Известно, что они более устойчивы к менингококковой и пневмококковой инфекции. Однако отдать предпочтение какомулибо полу в плане резистентности организма к инфекции затруднительно.
Эндокринологический статус человека имеет важное значение в регуляции уровня естественной резистентности. Гормон задней доли гипофиза окситоцин стимулирует активность фагоцитов, Т- и В-лимфоцитов. Глюкокортикоиды снижают уровень естественной резистентности, а минералкортикоиды повышают его. Больные сахарным диабетом чувствительны ко многим инфекциям, особенно к туберкулезу, фурункулезу стафилококковой этиологии. Снижение функции паращитовидных желез часто приводит к развитию кандидоза. Гормоны щитовидной железы стимулируют большинство факторов естественной резистентности. Их успешно используют для лечения сепсиса, вирусных гепатитов, менингококковой инфекции.
Иммунный статус человека определяет его индивидуальную чувствительность к отдельным инфекциям. Лица со II группой крови чаще болеют пневмонией и сепсисом стафилококковой этиологии, натуральной оспой, гриппом. У них ниже уровень интерферона в клетках и крови по сравнению с лицами с другой группой крови. Лица с I группой крови чаще подвержены чуме и проказе. Наличие в HLA-системе (комплекс гистосовместимости) антигена А9 способствует устойчивости этих лиц к острым респираторным
заболеваниям. Лица, у которых в HLA-системе есть антигены А10, В18, DR, болеют ими чаще.
Состояние физической активности человека регулирует уровень его естественной резистентности. Спортсмены-профессионалы, члены сборных команд высокочувствительны к инфекциям, так как интенсивные тренировки и участие в ответственных спортивных соревнованиях истощают резервы организма, снижают его естественную резистентность: уровень бактерицидной активности сыворотки, фагоцитарный потенциал нейтрофилов у классных спортсменов на фоне их высокой спортивной формы оказывается сниженным более чем в 2 раза по сравнению с лицами, занимающимися обычной физкультурой. В то же время занятия физкультурой и повышение двигательного режима являются средством усиления естественной резистентности организма к инфекции, что находит объяснение в нормализации уровня комплемента и лизоцима, в повышении способности крови к самоочищению.
Центральная нервная система принимает активное участие в регуляции уровня естественной резистентности организма к инфекции. Грызуны во время зимней спячки устойчивы к возбудителю чумы, но по мере просыпания весной погибают от чумной инфекции. Кролики во время медикаментозного сна резистентны к вирусу осповакцины, от которого они погибают во время бодрствования. В условиях стресса резко снижается естественная резистентность организма. У мышей после иммобилизационного стресса развивалась смертельная форма гриппозного энцефалита, тогда как в нормальных условиях мыши были резистентны к вирусу гриппа. Интересно, что на поверхности лимфоцитов и макрофагов имеются рецепторы к медиаторам нервной системы: β-адренорецепторы, холинорецепторы и др.
Эндогенные биологические ритмы. У человека с момента его рождения все процессы в организме протекают с определенной цикличностью. Выявлена определенная цикличность в динамике показателей естественной резистентности к инфекции (установлены месячные и суточные биоритмы).
Определены хронобиограммы иммунологических показателей здорового человека, что отражает различные временные интервалы максимальных значений факторов гуморальной и клеточной природы естественной резистентности. Это оказалось важным для
выбора времени оптимального введения лекарств больным при инфекционной патологии.
Значение для развития инфекции имеют и ее входные ворота. Входные ворота инфекции - место проникновения возбудителя в организм человека - во многом определяет возможность развития инфекционного процесса. Вирус гриппа, попав в кожу или на слизистую оболочку желудочно-кишечного тракта, не в состоянии вызвать заболевание. Грипп возникнет только при условии колонизации возбудителем слизистой оболочки верхних дыхательных путей. Существует понятие «колонизационная резистентность», которая определяет защитные возможности организма у входных ворот инфекции. В связи с этим инфекции разделяют на воздушно-капельные (грипп, менингококковая инфекция, дифтерия), кишечные (холера, дизентерия, гепатит А), инфекции наружных покровов (столбняк, газовая гангрена, бешенство), трансмиссивные (чума, малярия, туляремия).
8.4.1. Анатомо-физиологические барьеры организма при инфекции
Естественная резистентность организма включает ряд анатомофизиологических барьеров, препятствующих как проникновению патогена в организм, так и его распространению по организму. Среди основных анатомо-физиологических барьеров естественной защиты организма при инфекции выделяют: кожу и слизистые оболочки (наружный барьер), нормальную микрофлору; лимфатические узлы, клетки ретикулоэндотелиальной системы, воспаление; кровь - клеточные и гуморальные факторы; гематоэнцефалический барьер. (Подробно этот раздел изложен в материалах диска.)
Кожа не только является механическим барьером для патогена, но и обладает бактерицидным свойством за счет секретов сальных и потовых желез. Чистота кожи повышает ее бактерицидность. Известен показатель бактерицидной активности кожи, который определяется по отношению к индикаторным тест-штаммам E. coli. Этот показатель входит в число стандартных тестов оценки резистентности организма космонавтов перед полетом в космос. Повреждение кожи является условием для развития раневых инфекций: газовой гангрены, столбняка, бешенства.
Слизистые оболочки обеспечивают защиту не только как механический барьер за счет слизи, целостности эпителиального покрова, функции ворсинок. Эпителиоциты слизистых оболочек и железы разных биотопов выделяют на поверхность бактерицидные секреты: слюну, слезную жидкость, желудочный сок, сок тонкой кишки, вагинальный секрет, лизоцим и т.д. При нарушении барьерной функции слизистые оболочки становятся входными воротами инфекции для многих патогенов: возбудителей кишечных инфекций и инфекций дыхательных путей, возбудителей заболеваний, передающихся половым путем и др.
Важная роль в защите биотопов организма от патогена отводится нормальной (резидентной или индигенной) микрофлоре. Основными представителями нормальной микрофлоры толстой кишки являются кишечная палочка и бифидобактерии, в носоглотке - коринеформные бактерии и непатогенные нейссерии, на коже - эпидермальные стафилококки.
Микрофлора слизистой оболочки желудочно-кишечного тракта у детей существенно отличается от таковой у взрослых и меняется в зависимости от возраста ребенка, условий его существования, характера питания и т.д. Так, у детей до прорезывания зубов в микрофлоре рта преобладают аэробные бактерии. После прорезывания зубов микрофлора рта ребенка аналогична микрофлоре взрослых, что связано и с изменением характера питания.
Огромное количество микроорганизмов содержится в полости кишечника. Исследование кишечной флоры у детей показало, что микробы в мекониуме появляются со второй половины первых суток жизни. Вначале появляются кокки, затем в кишечнике определяются грамположительные палочки со спорами. В небольшом количестве в мекониуме обнаруживаются также кишечные палочки, вульгарный протей. С 3-го дня, когда появляются бифидобактерии, споровые палочки исчезают.
Основой кишечной микрофлоры у детей, находящихся на грудном вскармливании, являются бифидобактерии, которые составляют около 90% всех микробов кишечника. Встречаются кишечные палочки, энтерококки, ацидофильная палочка и аэрогенные бактерии. У детей, находящихся на искусственном вскармливании, превалируют кишечные палочки, а количество бифидобактерий снижается. Защитная роль нормальной микрофлоры состоит в выделении антагонистически активных веществ (антибиотиков,
бактериоцинов, микроцинов), подавляющих патоген, его способности колонизировать кожу, слизистые оболочки. Нормальная микрофлора образует пленку в биотопе. Кроме защитного антагонизма, известны детоксицирующая, иммуностимулирующая и витаминообразующая функции нормальной микрофлоры, ее участие в пищеварении. Подавление нормальной микрофлоры вследствие заболевания или широкого применения антибиотиков приводит к формированию дисбактериоза, который может стать причиной развития различных форм патологии, в том числе и микробного генеза. Для профилактики и лечения дисбактериоза используются эубиотики - препараты, содержащие живые антагонистически активные штаммы, - представители нормальной микрофлоры организма (колибактерин, бифидумбактерин, лактобактерин).
Второй защитный барьер организма включает функцию лимфатических узлов, клеток ретикулоэндотелиальной системы, развитие воспаления. Лимфатические узлы выполняют барьерфиксирующую функцию, могут длительно задерживать патоген, не допуская его проникновение в кровь, например фиксация гемолитического стрептококка в лимфоидной ткани миндалин, задержка бруцелл, возбудителя чумы, стафилококка, туберкулезных палочек в регионарных лимфатических узлах. За счет лимфатических узлов предотвращается развитие генерализованной формы инфекции. При подавлении барьерной функции лимфатических узлов могут развиться бактериемия (брюшной тиф, бруцеллез) и сепсис (чума, стафилококковая и стрептококковая инфекции).
Печень, селезенка, эндотелий кровеносных сосудов за счет клеток ретикулоэндотелиальной системы являются своеобразными фильтрами, в которых застревают патогены и таким образом не допускается генерализация инфекции (брюшной тиф). Воспаление в своей основе является защитной реакцией организма, так как в результате воспалительной реакции вокруг патогена концентрируются специализированные клетки, которые должны либо уничтожить возбудителя, либо ограничить его распространение, например при гнойном мастите стафилококковой этиологии в ткани молочной железы образуется локальный гнойный очаг (абсцесс), предотвращающий генерализацию стафилококковой инфекции.
Одним из методов лечения хронических инфекций является назначение препаратов, усиливающих воспалительную реакцию организма как защитную (хроническая гонорея, хроническая дизен-
терия). Но иногда воспаление может выполнять противоположную патогенетическую функцию, т.е. способствовать развитию патологического процесса, нарушению структуры и функции органа (ткани): воспаление легких (пневмония), воспаление почек (нефрит). В таком случае назначают противовоспалительную терапию.
Третья достаточно мощная преграда на пути распространения патогена по организму - это кровь. Бактерицидная активность крови, т.е. ее способность к самоочищению, обеспечивается комплексом гуморальных и клеточных факторов естественной резистентности организма. Если кровь перестает выполнять свою бактерицидную функцию, то возбудитель беспрепятственно пребывает и размножается в крови, а через кровь проникает и локализуется в разных органах и тканях. В таких случаях развиваются тяжелые, генерализованные формы инфекции, сепсис и септикопиемия, которые создают реальную угрозу жизни организма-хозяина (чумной сепсис, сибиреязвенный сепсис, стафилококковая септикопиемия).
Четвертый барьер организма - гематоэнцефалический, который защищает ткань мозга (головного, спинного) от поражения патогеном. В защитные структуры гематоэнцефалического барьера входят оболочки мозга, стенки кровеносных сосудов, питающих мозговую ткань. Проникновение возбудителя в мозговую ткань приводит к развитию менингоэнцефалитов (менингококк, риккетсии Провачека, вирусы бешенства и энцефалитов). Ткани головного мозга защищены нейросекретируемыми гормонами задней доли гипофиза - окситоцином и вазопрессином, которые наряду с антимикробной активностью подавляют и персистентный потенциал многих патогенов, что используется в клинической практике для борьбы с инфекцией.
8.4.2. Факторы естественной резистентности организма
Раздел изложен в материалах диска.
8.5. Роль внешней среды в инфекционном процессе
Внешняя среда является обязательным участником в инфекционном процессе, его третьей движущей силой. Факторы внешней среды (физические, химические, биологические и социальные)
могут существенно влиять на развитие, течение и исход инфекционного процесса.
Важным физическим фактором является температура. Классические опыты Уолкера и Боринга на модели экспериментальной вирусной инфекции показали, что повышение температуры тела организма приводит к активации факторов естественной резистентности, в частности усилению продукции интерферона. При высокой температуре усиливаются механизмы противовирусной защиты. Поэтому при лечении больных вирусными инфекциями не оправдано снижение высокой температуры, если нет для этого жизненно важных показаний. С другой стороны, снижение в холодное время года температуры тела человека (простудный фактор) приводит к ослаблению естественной резистентности. В связи с действием разных температур существует сезонность ряда инфекционных заболеваний. Повышение заболеваемости воздушнокапельными инфекциями (острой респираторной вирусной инфекции - ОРВИ, грипп) имеет место в холодное время года (зимой) под действием простудного фактора, кишечными инфекциями - в летне-осенний период, когда в условиях высокой температуры возбудители кишечных инфекций (дизентерия, холера, гепатит А, брюшной тиф) интенсивно размножаются во внешней среде, а также распространяются с пищевыми продуктами и водой.
Особенности питания, наличие витаминов в пище могут существенно влиять на естественную резистентность. В весенний период в связи с авитаминозом обостряются хронические инфекционные заболевания (туберкулез, ревматизм и др.). Витамин В12 и другие производные бензимидазола (дибазол), являясь стимуляторами синтеза белка в организме, повышают его естественную резистентность. Поэтому эти препараты используют для профилактики инфекционных болезней.
Солнце управляет жизненными процессами на нашей планете. Выявлена зависимость между активностью Солнца, его геомагнитной активностью, инфекционной заболеваемостью и смертностью среди людей. Выявлена цикличность патологических процессов и показателей естественной резистентности. Установлена связь между активностью Солнца и экспрессией факторов вирулентности микроорганизмов.
Социальный фактор является мощным фактором внешней среды, влияющим на устойчивость организма к инфекции. Антибиотико-
терапия, вакцинопрофилактика позволяют достаточно эффективно управлять инфекционным процессом. Благодаря глобальным противоэпидемическим мероприятиям человечество избавилось от натуральной оспы, успешно ведет борьбу с полиомиелитом. Но есть болезни, созданные человеком (men made diseases): туберкулез, вирусные гепатиты, ВИЧ-инфекция, болезни, передающиеся половым путем.
Социальные болезни - следствие пороков человеческого общества: наркомании, проституции и т.п. Техногенное загрязнение внешней среды способствует развитию инфекционных заболеваний. Высокое содержание в воздухе, воде солей тяжелых металлов, сероводородсодержащих соединений, радиоактивных элементов приводит к формированию иммунодефицитов в организме, а с другой стороны, в ряде случаев стимулируют экспрессию факторов вирулентности патогена. Так, природный сероводородсодержащий газ Оренбургского, Астраханского, Карачаганакского природных месторождений резко усиливал персистентный потенциал стафилококков, делая население этих газоносных провинций заложниками формирования резидентного стафилококкового бактерионосительства.
Таким образом, формы, течение и исход инфекционного процесса зависят как от вирулентности штамма патогенного микроорганизма, так и от состояния естественной резистентности и иммунитета организма хозяина, где регулирующую функцию выполняют факторы внешней среды.
Задания для самоподготовки (самоконтроля)
А. Назовите форму инфекционного процесса, при которой возбудитель длительное время находится в организме, не проявляя патогенных свойств и не выделяясь в окружающую среду:
1. Бактерионосительство.
2. Латентная инфекция.
3. Медленная инфекция.
4. Острая инфекция.
Б. Назовите факторы, способствующие колонизации бактерий в макроорганизме:
1. Бактериоцины.
2. Адгезины.
3. Эндотоксин.
4. IgA-протеаза.
В. Назовите факторы, способствующие инвазии бактерий:
1. Гиалуронидаза.
2. Эффекторные белки секреторной системы III типа.
3. Эндотоксин.
4. Пили.
Г. В защите от фагоцитоза, помимо поверхностных структур бактериальной клетки, участвуют секретируемые этой клеткой вещества. Отметьте ферменты, принимающие участие в подавлении фагоцитоза бактерий:
1. Внеклеточная аденилатциклаза.
2. IgA-протеаза.
3. Каталаза.
4. Супероксиддисмутаза.
Д. Отметьте положения, характерные для экзотоксина:
1. Является слабым антигеном.
2. Обладает специфичностью действия.
3. Термостабилен.
4. Стимулирует образование в организме нейтрализующих ан-
тител.
Е. У пациента, болеющего гриппом, развилась пневмония, вызванная S. pneumoniae. Назовите форму инфекционного процесса, к которой относится вызванная S. pneumoniae пневмония.
Ж. Одним из методов лабораторной диагностики инфекционных болезней является метод гемокультуры, при котором возбудителя выделяют из крови больного. Назовите состояния инфекционного процесса, при которых возбудитель можно выделить из крови.