Биохимия : руководство к практическим занятиям : учебное пособие / Под ред. проф. Н.Н. Чернова. - 2009. - 240 с. : ил.
|
|
|
|
РАЗДЕЛ 4. МЕТАБОЛИЗМ. ХИМИЯ И ОБМЕН УГЛЕВОДОВ
ВВЕДЕНИЕ
Метаболизм - это совокупность процессов превращения веществ и энергии в живом организме и обмен организма веществами и энергией с внешней средой, вследствие чего происходит постоянное обновление самого организма. С точки зрения физики живой организм существует за счет увеличения энтропии внешней среды в соответствии со вторым законом термодинамики: ∆G = AH - TAS, т. е. если (∆Sорганизма + ∆Sсреды) > 0, тогда ∆G < 0 и в организме могут происходить упорядоченные процессы.
Организм получает энергию в виде пищевых веществ, которые расщепляются в окислительных процессах катаболизма («мета- болическая воронка»). Часть этой энергии трансформируется в высокоэнергетические (макроэргические) соединения (большей частью в АТФ*). Последние, в свою очередь, используются организмом в восстановительных процессах анаболизма в качестве источника энергии для синтеза собственных высокомолекулярных соединений.
Внутриклеточный метаболизм основных классов питательных веществ - углеводов, белков и жиров - представляет собой раз- ветвленную метаболическую сеть, объединяемую в митохондриях общим амфиболическим путем - циклом трикарбоновых кислот (ЦТК). Метаболиты ЦТК участвуют в анаплеротических (восполняющих) реакциях, связывающих обмен разных классов соединений между собой.
* При гидролизе одной фосфоангидридной связи АТФ (АТФ →АДФ + Н3РО4) высвобождается примерно в два раза больше энергии (-∆G? = 7,3 ккал/моль), чем при гидролизе, например, глюкозо-6-фосфата (-∆G? = 3,3 ккал/моль).
Образование АТФ из АДФ и остатка фосфорной кислоты - ферментативный энергозависимый процесс, получивший название фос- форилирование АДФ. В зависимости от источника энергии и механизма образования макроэргической связи различают два основных способа синтеза АТФ:
1) меньший по объему, эволюционно более ранний, который может осуществляться в анаэробных условиях - субстратное фосфорилирование за счет энергии других макроэргических соединений (1,3-бисфосфоглицерат, фосфоенолпируват, сукцинил-КоА, креатинфосфат);
2) сопряженное с дыханием окислительное фосфорилирование, осуществляемое на внутренней мембране митохондрий ферментом АТФ-синтазой за счет энергии разности электрохимических потенциалов ∆μН+, возникающей при раздельном переносе электронов и протонов в дыхательной цепи митохондрий от восстановительных эквивалентов НАДН(Н+) или ФАДН2 на молекулярный кислород в процессе биологического окисления (хемиосмотическая теория П. Митчелла).
Поскольку в организме человека и животных основное количество восстановительных эквивалентов образуется в результате окислительного распада углеводов, целесообразно начать знакомство с обменом веществ и энергии с изучения химии углеводов и их метаболизма. Метаболизм углеводов составляют катаболические энергообразующие пути (гликолиз, гликогенолиз, петозофосфатный путь окисления глюкозы) и анаболические энергозатратные пути (синтез гликогена и глюконеогенез - образование глюкозы из неуглеводных источников: лактата, аминокислот или глицерина).
Направленность, интенсивность и согласованность протекания метаболических процессов регулируется ферментами под контролем гормональной и нервной системы при участии клеточных рецепторов и вторичных переносчиков сигнала. Нарушение регуляции, как и онтогенетические изменения ферментных систем, приводит к патологии обменных процессов и развитию заболеваний.
В данном разделе приводятся лабораторные работы, демонстрирующие специфичность ферментов, расщепляющих углеводы, мето- ды количественного определения глюкозы и построения «сахарных кривых», кроме того, представлены методики определения активности фермента ЦТК - сукцинатдегидрогеназы и метаболита гликолиза - пирувата.
4.1. СПЕЦИФИЧНОСТЬ ДЕЙСТВИЯ ФЕРМЕНТОВ РАСПАДА УГЛЕВОДОВ - АМИЛАЗЫ И САХАРАЗЫ
Крахмал и сахароза - обычные углеводы пищи. Амилаза и сахараза - ферменты, участвующие в расщеплении этих углеводов. Амилаза слюны расщепляет крахмал до мальтозы, и затем мальтаза расщепляет последнюю до свободной глюкозы. Сахараза кишечного сока расщепляет сахарозу до глюкозы и фруктозы. Источником ферментов могут быть слюна (для амилазы) и пекарские дрожжи (для сахаразы).
Цель работы
Убедиться в специфичности действия амилазы слюны и сахаразы дрожжей на соответствующие субстраты.
Принцип метода
О расщеплении крахмала и сахарозы судят по образованию глюкозы, которую определяют пробой Троммера (модификация пробы «медного зеркала» на альдегидную группу). Крахмал и сахароза не содержат способной окисляться альдегидной группы и не дают положительной пробы Троммера при нагревании.
Выполнение работы
Слюну разводят в соотношении 1:5 и полученный раствор используют как источник амилазы. Получение сахаразы осуществляют следующими образом:
В четыре пробирки по каплям добавляют следующие реактивы.
Номер пробы | Крахмал | Сахароза | Амилаза | Сахараза | Окраска в реакции Троммера на наличие глюкозы |
1 | 10 капель | - | 5 капель | - | |
2 | 10 капель | - | - | 5 капель | |
3 | - | 10 капель | 5 капель | - | |
4 | - | 10 капель | - | 5 капель |
Пробы перемешивают и инкубируют при 40 ?С в течение 10 мин, а затем проводят пробу Троммера с содержимым каждой пробирки. Результаты записывают в таблицу.
Проба Троммера на наличие глюкозы
К содержимому исследуемого раствора добавляют равный объем 30%-ного раствора NaOH и 1 каплю 7%-ного раствора CuSO4 (так, чтобы капли не растекались по стенкам пробирки) до появления в верхнем слое неисчезающей голубой мути вследствие образования гидроксида меди(11) Cu(OH)2. Затем осторожно, не встряхивая пробирку, ее нагревают на горелке. При кипячении выпадает желтый осадок гидроксида меди(1) CuOH или красный осадок Cu2O. В случае избытка CuSO4 образуется черный осадок CuO.
Самостоятельное формулирование выводов
Тестовые задания по теме
«Химия углеводов. Энергетический обмен»
I. Определите, верно ли утверждение.
1. Рибоза является альдопентозой.
2. Мальтоза состоит из остатков глюкозы и фруктозы.
3. Запасной формой углеводов у животных является гликоген.
4. Природные моносахариды относятся к L-ряду.
5. Структура гликогена отличается от структуры крахмала большей разветвленностью полисахаридной цепи.
6. Образование АТФ и НАДФН(Н+) характеризует анаболические процессы.
7. При окислении НАДН(Н+) и ФАДН2 в цепи биологического окисления образуется одинаковое количество молекул АТФ.
8. Механизмы синтеза молекулы АТФ при субстратном и окислительном фосфорилировании различаются.
9. KoQ (убихинон) способен присоединять атомы водорода.
10. Биологическое окисление возможно без окислительного фосфорилирования.
II. Цитохром с относят к гемопротеинам.
12. При микросомальном окислении субстратов образуется АТФ.
2. Выберите правильный ответ.
Углеводом не является Макроэргическое соединение -
1) седогептулаза это
2) диоксиацетонфосфат 1) глюкозо-1-фосфат
3) глицериновый альдегид 2) глюкозо-6-фосфат
4) 3-фосфоглицериновая кислота 3) фосфоенолпируват
5) ксилулозо-5-фосфат 4) 2-фосфоглицериновая
кислота 5) глицеральдегидфосфат
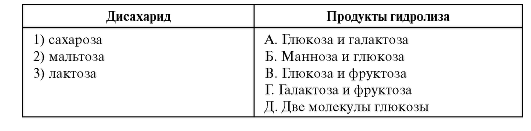
3. Установите соответствие между дисахаридом и продуктами его гидролиза.
4.2. КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ГЛЮКОЗЫ. ПОСТРОЕНИЕ «САХАРНЫХ КРИВЫХ»
А. Ферментативный метод количественного определения глюкозы в сыворотке или плазме крови
Количественное определение глюкозы в крови является одним из основных методов диагностики нарушений углеводного обмена.
Клинико-диагностическое значение
Повышение концентрации глюкозы в сыворотке крови (гипергликемия) наблюдается чаще всего при недостаточной секреции инсулина, а также при гиперфункции щитовидной железы и гиперсекреции гормонов, в частности при опухолях коркового слоя надпочечников и опухолях гипофиза.
Гипогликемия может наблюдаться при гипофункции щитовидной железы, гипофизарной кахексии, Аддисоновой болезни, аденоме поджелудочной железы, а также может быть вызвана голоданием, продол- жительной физической работой или передозировкой инсулина.
Цель работы
Определить содержание глюкозы в исследуемой сыворотке крови ферментативным методом и сравнить полученные результаты с нор- мальными величинами.
Принцип метода
Глюкоза окисляется кислородом воздуха в присутствии высокоспецифичного фермента глюкозооксидазы с образованием перок- сида водорода. Затем пероксид водорода в присутствии фермента пероксидазы реагирует с 4-аминоантипирином и фенолом. В результате образуется окрашенное соединение, оптическая плотность которого при 510 нм пропорциональна концентрации глюкозы в анализируемом образце.
Выполнение работы (см. Приложение 9.2)
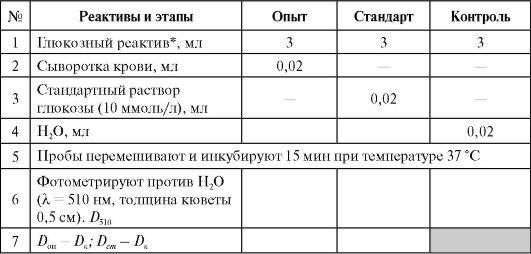
* 4-аминоантипирин, п-гидроксибензолсульфонат, пероксидаза и глюкозооксидаза, фосфатный буфер (pH = 8,0).
Расчеты
Содержание глюкозы в сыворотке крови (моль/л) рассчитывают по формуле:
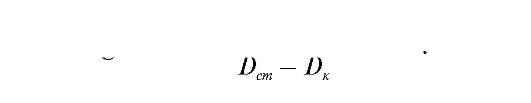
Норма: для сыворотки и плазмы крови 3,9-6,1 ммоль/л, для цельной крови 3,3-5,5 ммоль/л.
Самостоятельное формулирование выводов
Б. Определение глюкозы в крови
с помощью глюкометра (демонстрация)
Принцип ферментативного определения глюкозы положен в основу многочисленных автоматических глюкометров, которые выпуска- ются в комплекте с электрохимическими тест-полосками однократного использования.
Определение концентрации глюкозы в крови осуществляют после нанесения пробы крови на полоску, подключенную к прибору. Прибор обнаруживает пробу крови, определяет концентрацию глюкозы и выводит показания на экран. Прибор может применяться в клинической практике при недоступности лабораторных методов измерения, при скрининговых исследованиях, в полевых условиях и чрезвычайных ситуациях, а также для индивидуального использования с целью постояного контроля за уровнем глюкозы в крови у больных сахарным диабетом.
В. Оральный глюкозотолерантный тест
(синонимы: тест толерантности к глюкозе, реакция организма на сахарную нагрузку)
У здорового человека однократный прием 50-100 г глюкозы вызывает временное повышение ее содержания в крови - пищевую, или алиментарную, гипергликемию. Эта гипергликемия обусловлена тем, что при поступлении сразу большого количества глюкозы печень не успевает утилизировать ее полностью и часть глюкозы поступает в кровь. Повышение содержания глюкозы в крови приводит к выделению инсулина, который нормализует ее содержание в крови уже через 1,5-2 ч. Обычно выделяется избыточное количество инсулина, и уровень глюкозы опускается даже несколько ниже нормы. При инсулиновой недостаточности содержание глюкозы в крови после нагрузки достигает значительно больших величин и сохраняется значительно дольше.
Цель работы
Познакомиться с методикой проведения теста, построить «сахарные кривые» по предложенным данным и самостоятельно их проанализировать.
Выполнение работы
Предварительно у взрослого пациента определяют содержание глюкозы в крови натощак. Затем он принимает внутрь
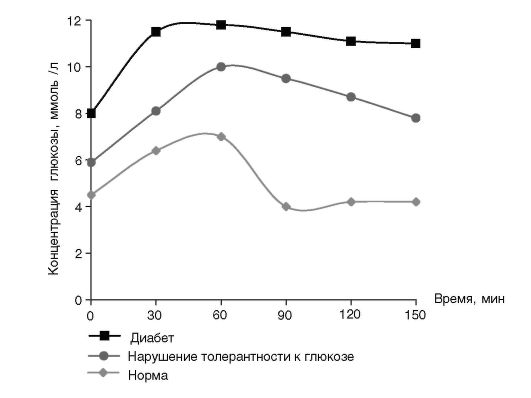
На основании приведенных ниже данных (см. таблицу) предлагается построить «сахарные кривые», сравнить их между собой и сделать вывод об инсулиновом статусе пациентов А, Б и В.
Согласно критериям Всемирной организации здравоохранения (ВОЗ) концентрация глюкозы 7,8-10,0 ммольл-1 в капиллярной цельной крови через 2 ч после нагрузки глюкозой свидетельствует о нарушении толерантности к глюкозе, а выше 11,1 ммольл1 - о сахарном диабете.
Время взятия крови после приема глюкозы, мин | Концентрация глюкозы, ммольл-1 | ||
Пациент А | Пациент Б | Пациент В | |
0 | 5,9 | 4,5 | 8,0 |
30 | 7,0 | 7,0 | 11,5 |
60 | 9,2 | 7,5 | 11,8 |
90 | 9,0 | 5,5 | 11,5 |
120 | 8,0 | 5,5 | 11,0 |
150 | 7,0 | 5,0 | 11,0 |
Самостоятельное формулирование выводов
Тестовые задания по теме
«Распад и синтез гликогена. Гликолиз и гликогенолиз»
I. Определите, верно ли утверждение.
1. Скорость гликолиза и гликогенолиза контролируется фосфофруктокиназой.
2. Синтез и распад гликогена в тканях происходят различными путями.
3. Инсулин активирует фосфорилазу b.
4. Гликоген в мышцах рападается с образованием глюкозо-6-фосфата.
5. Положительный баланс гликогенолиза составляют две молекулы АТФ.
6. Процесс гликолиза обратим.
7. Для включения глюкозы в обменные процессы необходимо ее фосфорилирование.
8. Все ферментативные реакции гликолиза обратимы.
9. Процесс анаэробного гликолиза сопровождается накоплением НАДН(Н).
10. Пируваткиназа относится к классу гидролаз.
II. Альдолаза расщепляет фруктозо-1,6-бисфосфат. 12. Лактатдегидрогеназная реакция обратима.
2. Выберите правильный ответ.
В опыте с мышечной тканью Метаболит гликолиза в эритроцитах,
изучали гликолиз в анаэробных изменяющий сродство гемоглобина
условиях. Скорость гликолиза к кислороду, - это уменьшается при добавлении 1) 1,3-бисфосфоглицерат
1) АДФ 2) 2,3-бисфосфоглицерат
2) АМФ
3) цитрата
4) ацетил-КоА
5) сукцината
3. Установите последовательность лиза.

4.3. ОПРЕДЕЛЕНИЕ АКТИВНОСТИ СУКЦИНАТДЕГИДРОГЕНАЗЫ В МЫШЦАХ. КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ПИРУВАТА В МОЧЕ
А. Определение активности
сукцинатдегидрогеназы в мышцах
Сукцинатдегидрогеназа (СДГ, КФ: 1.3.99.1) - единственный фермент цикла трикарбоновых кислот (цикла Кребса), прочно связанный с внутренней мембраной митохондрий (комплекс II). Коферментом СДГ служит ФАД, акцептирующий два атома водорода от молекулы сукцината и переносящий их непосредственно на коэнзим Q (убихинон) в дыхательной цепи митохондрий. ФАД прочно связан с молекулой СДГ.
Цель работы
Убедиться в способности сукцинатдегидрогеназы мышечной ткани проявлять активность в анаэробных условиях.
Принцип метода
Доказательством проявления активности СДГ может служить изменение окраски искусственного акцептора водорода метиленово- го синего:
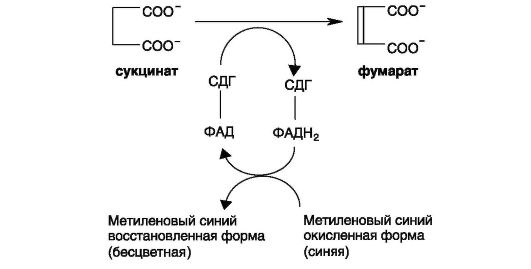
Выполнение работы
Так как восстановленная форма метиленового синего вновь окисляется на воздухе, опыт проводят в анаэробных условиях, предотвращая доступ кислорода наслаиванием на поверхность пробы вазели- нового масла. Контролем служит гомогенат мышц, в котором СДГ инактивирована кипячением. Критерием активности СДГ служит время обесцвечивания опытной пробы в присутствии сукцината в анаэробных условиях.
? | Реактивы и этапы | Опыт | Контроль |
1 | Гомогенат мышц (мясной фарш), мл | 2 | 2 |
2 | Нагревают при 100 ?С в течение 5 мин на водяной бане, а затем охлаждают до комнатной температуры | - | + |
3 | 1 | 1 | |
4 | 2 | 2 | |
5 | Метиленовый синий, 0,05%-ный раствор, капли | 2 | 2 |
6 | Пробы тщательно перемешивают стеклянной палочкой, заливают вазелиновым маслом и инкубируют при комнатной температуре | ||
7 | Окраска | ||
8 | Время обесцвечивания | ||
Самостоятельное формулирование выводов
Б. Количественное определение пировиноградной кислоты в моче
ПВК является промежуточным продуктом распада углеводов в организме. Она содержится во всех органах и тканях.
Клинико-диагностическое значение
Содержание ПВК в крови и моче возрастает при сахарном диабете, сердечной недостаточности, гиперфункции гипофизарно-адрена- ловой системы, токсикозах, при введении некоторых лекарственных средств, а также при недостаточности тиамина.
Цель работы
Определить количество пировиноградной кислоты и сравнить полученные результаты с нормой.
Принцип метода
Пировиноградная кислота, взаимодействуя с 2,4-динитрофенил- гидразином (2,4-ДНФГ), в щелочной среде образует 2,4-динитрофе- нилгидразоны пировиноградной кислоты желто-оранжевого цвета, интенсивность окраски которых пропорциональна концентрации пировиноградной кислоты.
Реакция протекает по уравнению:
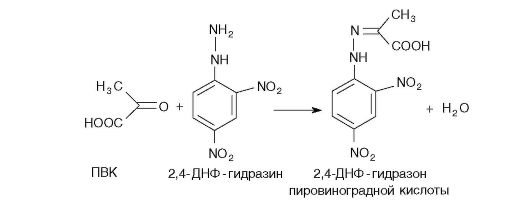
Выполнение работы
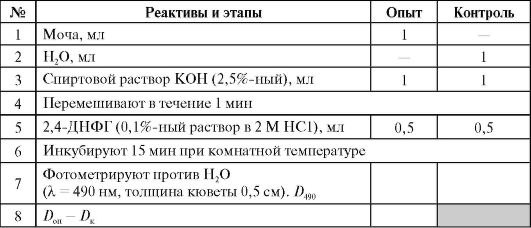
Строят калибровочный график зависимости D490 от содержания ПВК по следующим данным:

Расчеты
Содержание ПВК в суточной моче (на диурез 1500 мл) рассчитывают по формуле:
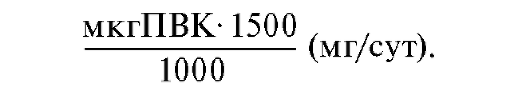
Для пересчета содержания ПВК (мг) в единицы количества вещества (мкмоль) надо умножить соответствующие величины на 11,4 (коэффициент пересчета).
Норма: 10 -25 мг/сут, или 114 -284 мкмоль/сут. Самостоятельное формулирование выводов
Тестовые задания по теме «Аэробный обмен углеводов»
1. Определите, верно ли утверждение.
1. Скорость ЦТК регулируется аллостерическими ферментами цитратсинтазой и изоцитрадегидрогеназой.
2. Положительный баланс ЦТК составляют 15 молекул АТФ.
3. Сукцинил-КоА является макроэргическим соединением.
4. В окислительном декарбоксилировании пировиноградной и α-кетоглутаровой кислот участвует КоА.
5. Доля окисления пирувата в общем энергообмене организма незначительна.
6. Все ферменты ЦТК находятся в митохондриях.
7. Скорость цикла трикарбоновых кислот зависит от концентрации АТФ в клетке.
8. Сукцинатдегидрогеназа катализирует окисление янтарной кислоты.
9. В ЦТК происходит субстратное фосфорилирование.
10. Все атомы глюкозы окисляются в ЦТК до СО2.
11. НАДФН(Н+) образуется в цикле трикарбоновых кислот.
12. Цитрат из митохондрий может попадать в цитоплазму.
2. Выберите правильный ответ.
В цикле трикарбоновых В отсутствие окислительного фосфо-
кислот не участвует фермент рилирования выход АТФ в ЦТК состав-
1) аконитаза ляет (число молекул на 1 оборот цикла)
2) транскетолаза 1) 0
3) сукцинатдегидрогеназа 2) 1
4) фумараза 3) 2
5) малатдегидрогеназа 4) 3
5) 12
3. Установите соответствие между процессом и регуляторным ферментом, участвующим в нем.

Тестовые задания по теме «Пентозофосфатный путь окисления глюкозы. Нарушения обмена углеводов»
1. Определите, верно ли утверждение.
1. Пентозофосфатный путь превращения глюкозы является поставщиком НАДФН(Н+) для восстановительных синтезов.
2. Передозировка инсулина вызывает у больного сахарным диабетом гипогликемию.
3. Фруктозо-6-фосфат - аллостерический регулятор гликолиза.
4. Рибоза должна поступать в организм с пищей.
5. Все ферменты гликолиза и пентозофосфатного пути находятся в цитоплазме.
6. При полном окислении одной молекулы глюкозы максимально может образоваться 38 молекул АТФ.
7. Содержание глюкозы в цельной крови 3,3-5,5 мкмоль/л является нормой.
8. Болезнь Гирке (гликогеноз I типа) связана с наследственным дефектом синтеза глюкозо-6-фосфатазы в печени. 9. Сахароза содержится в крови.
10. Галактоземия является наследственным заболеванием.
11. Пентозофосфатный путь окисления глюкозы может приводить к выделению энергии.
12. НАД+ является коферментом транскетолазы.
2. Выберите правильный ответ.
Основная функция пентозофос- Метаболитом пентозофосфат-
фатного пути в эритроцитах - это ного пути превращения глюкозы
1) образование НАДФН(Н) не является
2) образование рибозо-5-фос- 1) рибозо-5-фосфат фата 2) ксилулозо-5-фосфат
3) расщепление пентозофосфа- 3) фруктозо-6-фосфат тов 4) глицеральдегидфосфат
4) синтез АТФ 5) глюкозо-1-фосфат
5) восстановление Н2О2 до двух молекул воды
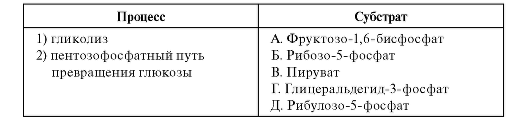
3. Установите соответствие между процессом и участвующим в нем субстратом.
Итоговые тестовые задания
по теме «Химия и обмен углеводов»
1. Определите, верно ли утверждение.
1. Пируваткарбоксилаза - один из ферментов глюконеогенеза.
2. Адреналин индуцирует синтез гликогенсинтазы.
3. Гликоген мышц может поставлять глюкозу в кровь.
4. Глюкокортикоиды индуцируют синтез ферментов глюконеогенеза.
5. Адреналин и глюкагон усиливают синтез гликогена в мышцах.
6. Глицерин может быть субстратом глюконеогенеза.
7. Гипергликемия может наблюдаться при опухолях коры надпочечников.
8. Молочная кислота образуется в тканях мозга.
9. Глюкокиназа содержится в мышечных клетках.
10. Фосфофруктокиназа является аллостерическим ферментом.
11. В эритроцитах происходит гликолиз.
12. Галактоземия новорожденных связана с недостатком гексозо-1- фосфатуридилтрансферазы.
2. Выберите правильный ответ.
Лактат, поступающий в кровоток, Непереносимость молока связана
может снова превращаться с недостатком фермента в глюкозу 1) амилазы
1) в печени 2) альдолазы
2) в сердечной мышце 3) лактазы
3) в эритроцитах 4) енолазы
4) в жировой ткани 5) глюкокиназы
5) в мозге
3. Установите соответствие между процессом и участвующим в нем субстратом.

4.4. КОЛЛОКВИУМ ПО ТЕМЕ «МЕТАБОЛИЗМ. ХИМИЯ И ОБМЕН УГЛЕВОДОВ»
Вопросы для самостоятельной подготовки
1. Общие принципы обмена веществ и энергии. Катаболизм и анаболизм -основные процессы метаболизма. Роль НАДФН(Н+) и АТФ. «Метаболическая воронка».
2. Моносахариды, олигосахариды. Важнейшие представители моносахаридов и олигосахаридов животного организма. Химическое строение, биологическая роль.
3. Полисахариды. Гликоген, его строение, свойства, локализация и роль в организме. Синтез гликогена и его регуляция.
4. Анаэробное расщепление углеводов в организме, его биологическое значение и энергетический эффект. Понятие о субстратном фосфорилировании.
5. Гликолиз. Регуляция.
6. Глюконеогенез. Энергетический эффект процесса. Регуляция.
7. Окислительное декарбоксилирование пировиноградной кислоты. Ферменты и коферменты, участвующие в этом процессе.
8. Цикл трикарбоновых кислот, его биологическое значение и регуляция.
9. Связь ЦТК с процессами биологического окисления.
10. Окислительное фосфорилирование. Хемиосмотическая теория П. Митчелла. Синтез АТФ.
11. Энергетический эффект анаэробного и аэробного путей распада углеводов.
12. Пентозофосфатный путь окисления глюкозы в тканях и его биологическая роль.
13. Механизмы регуляции содержания глюкозы в крови. Явления гипо- и гипергликемии. Сахарный диабет. Диагностическое значение «сахарных кривых».
14. Синтез и распад гликогена в печени. Гликогенолиз в мышцах. Регуляция этих процессов.
15. Регуляция и нарушения углеводного обмена.
16. Возможные пути превращения глюкозо-6-фосфата в печени.
Варианты письменной части коллоквиума
1. Напишите формулу
1) лактозы
2) седогептулозы
3) А-глюкуроновой кислоты
4) 5-фосфорибозил-1-пирофосфата (ФРПФ)
2. Охарактеризуйте фермент
1) ФФК-1
2) изоцитратдегидрогеназу
3) транскетолазу
4) АТФ-синтазу
3. Укажите пути регуляции
1) цикла трикарбоновых кислот
2) гликолиза
3) глюконеогенеза
4) распада и синтеза гликогена
4. Объясните, в какой позиции и почему в молекуле ацетил-КоА будет находиться радиоактивный 14С
1) из 14С1-глюкозы
2) из 14С3-глюкозы
3) из 14С4-глюкозы
4) из 14С5-глюкозы
5. Укажите принципиальное различие
1) субстратного и окислительного фосфорилирования
2) гликолитического и пентозофосфатного путей окисления глюкозы
3) гликолиза и гликогенолиза
4) аэробного и анаэробного путей распада глюкозы
6. Укажите, сколько молекул АТФ и каким путем можно получить при полном окислении одной молекулы
1) фруктозо-6-фосфата
2) ДАФ
3) ФЕП
4) фруктозо-1,6-бисфосфата
Варианты заданий компьютерного тестирования
Инструкция к тесту. Выберите все правильные ответы. 1. Содержание глюкозы в цельной крови в норме составляет
1) 3-5 г/л
2) 0,6-1,0 г/л
3) 3,3-5,5 ммоль/л
4) 60-100 мг/дл
5) ни одно из перечисленных значений
2. Конечный продукт анаэробного гликолиза - это
1) пируват
2) лактат
3) оксалоацетат
4) этанол
5) ацетил-КоА
3. Врожденная непереносимость молока связана с отсутствием в кишечнике фермента из класса
1) оксидоредуктаз
2) трансфераз
3) гидролаз
4) лиаз
5) изомераз
4. Фермент, лимитирующий скорость гликолиза, - это
1) глицеральдегидфосфатдегидрогеназа
2) енолаза
3) фосфофруктокиназа
4) фосфоглицераткиназа
5) триозофосфатизомераза
5. При полном окислении одной молекулы пирувата до CO2 и H2O может максимально образоваться
1) 24 молекулы АТФ
2) 12 молекул АТФ
3) 38 молекул АТФ
4) 15 молекул АТФ
5) 72 молекулы АТФ
6. Количество пировиноградной кислоты в крови увеличивается при недостатке витамина
1) А
2) С
3) D
4) B-1
5) B6
7. Основная функция пентозофосфатного пути в эритроцитах - это
1) образование НАДФН(Н+)
2) образование рибозо-5-фосфата
3) расщепление пентозофосфатов
4) синтез АТФ
5) восстановление H2O2 до двух молекул воды
8. Инсулиннезависимый сахарный диабет наступает
1) при нарушении регуляции гликолиза
2) при повышенной секреции инсулина
3) при повышенной секреции глюкагона
4) при пониженной секреции инсулина
5) при нарушении инсулинзависимого поглощения глюкозы
9. Общая стадия глюконеогенеза и гликолиза, катализируемая одним и тем же ферментом, - это
1) фруктозо-6-фосфат →? глюкозо-6-фосфат
2) глюкозо-6-фосфат -→ глюкоза
3) оксалоацетат → фосфоенолпируват
4) фруктозо-1,6-бисфосфат → фруктозо-6-фосфат
10. Непосредственно из глюкозо-6-фосфата могут образоваться
1) фруктозо-6-фосфат
2) глюкоза
3) 6-фосфоглюконо-δ-лактон
4) глюкозо-1-фосфат
5) фруктозо-1-фосфат
11. В присутствии O2 (эффект Пастера) в дрожжевой клетке не обра- зуется
1) пировиноградная кислота
2) рибулозо-5-фосфат
3) сукцинил-КоА
4) этиловый спирт
5) УДФ-глюкоза
12. Гипергликемию наблюдают
1) при стероидпродуцирующих опухолях коркового вещества надпочечников
2) при гиперфункции щитовидной железы
3) при поражении почек
4) при сахарном диабете
13. При гидролизе лактозы образуются
1) галактоза
2) фруктоза
3) манноза
4) сахароза
5) глюкоза
14. Ферменты практически необратимых реакций гликолиза - это
1) триозофосфатизомераза
2) альдолаза
3) фосфофруктокиназа
4) лактатдегидрогеназа
5) гексокиназа
15. Сахароза в организме может расщепляться только
1) в мозге
2) в печени
3) в мышцах
4) в кишечнике
5) в селезенке
16. Наибольшее содержание гликогена в организме человека (по массе)
1) в печени
2) в мышцах
3) в мозге
4) в почках
5) в жировой ткани
17. Аллостерические регуляторы гликолиза - это
1) АМФ
2) АТФ
3) фруктозо-6-фосфат
4) цитрат
5) пируват
18. Субстратное фосфорилирование происходит
1) в процессе гликолиза
2) в процессе гликогенолиза
3) в процессе глюконеогенеза
4) в пентозофосфатном пути
5) в ЦТК
19. Реакция гидратации в ЦТК - это превращение
1) α-кетоглутарата в сукцинил-КоА
2) Х-малата в оксалоацетат
3) сукцината в фумарат
4) фумарата в L-малат
5) изоцитрата в α-кетоглутарат
20. Количество глюкозы увеличивается в крови
1) при сахарном диабете
2) при потреблении большого количества сахара
3) при гиперфункции щитовидной железы
4) при введении инсулина
21. Передозировка инсулина вызывает у больного сахарным диабетом
1) глюкозурию и гипергликемию
2) галактоземию
3) гипергликемию
4) гипогликемию
5) креатинурию
22. В образовании глюкозо-1-фосфата из гликогена принимает участие фермент
1) амилаза
2) фосфорилаза
3) фосфоглюкоизомераза
4) фосфоглюкомутаза
5) глюкокиназа
23. В отсутствие окислительного фосфорилирования выход АТФ в ЦТК составляет (число молекул на один оборот цикла)
1) 0
2) 1
3) 2
4) 38
5) 12
24. Активность ферментов пентозофосфатного пути наименьшая
1) в молочной железе
2) в эмбриональной ткани
3) в жировой ткани
4) в скелетной мышце
5) в печени
25. При гидролизе сахарозы образуются
1) галактоза
2) манноза
3) фруктоза
4) глюкоза
5) сорбоза
26. Глюкоза может образоваться в организме
1) из ацетил-КоА
2) из пирувата
3) из лактата
4) из глицерина
5) из лейцина
27. Ферменты биосинтеза гликогена из глюкозы - это
1) амилаза
2) фосфорилаза
3) гликогенсинтаза
4) фосфоглюкомутаза
5) гексокиназа
28. Скорость гликолиза в мышечной ткани уменьшается при добавлении
1) АДФ
2) АТФ
3) цитрата
4) АМФ
29. Из пирувата в одну стадию могут образоваться
1) цитрат
2) оксалоацетат
3) лактат
4) ацетил-КоА
5) глицерин
30. Фруктозо-6-фосфат образуется
1) в процессе гликолиза
2) в процессе гликогенолиза
3) в пентозофосфатном пути
4) в ЦТК
5) в процессе глюконеогенеза
31. Фермент, присутствующий и в печени, и в мышцах, - это
1) глюкозо-6-фосфатаза
2) гексокиназа
3) фруктозо-1,6-бисфосфатаза
4) глюкокиназа
32. При окислительном декарбоксилировании трех молекул пирувата при условии сопряжения этой реакции с окислительным фосфорилированием может синтезироваться
1) 3 молекулы АТФ
2) 6 молекул АТФ
3) 9 молекул АТФ
4) 12 молекул АТФ
5) 38 молекул АТФ
33. Гликогеноз I типа (болезнь Гирке) связан с отсутствием в печени фермента
1) глюкокиназы
2) гексокиназы
3) глюкозо-6-фосфатазы
4) фосфофруктокиназы
5) фосфорилазы
34. Недостаточность инсулина сопровождается
1) гипергликемией
2) глюкозурией
3) кетонемией
4) кетонурией
5) гипогликемией
35. Лактат из кровотока превращается в глюкозу
1) в печени
2) в сердечной мышце
3) в эритроцитах
4) в жировой ткани
5) в мозге
36. Макроэргические соединения - это
1) 3-фосфоглицерат
2) ГАФ
3) 1,3-бисфосфоглицерат
4) ацетил-КоА
5) сукцинил-КоА
37. Дисахариды - это
1) лактоза
2) мальтоза
3) фруктоза
4) крахмал
5) сахароза
38. Остатки глюкозы в молекуле гликогена связаны через атомы углерода
1) 1- 1
2) 1 - 2
3) 1 - 4
4) 1 - 5
5) 1 - 6
39. Дефицит глюкозо-6-фосфатазы в печени приводит
1) к накоплению гликогена в печени
2) к гипергликемии
3) к увеличению количества лактата в крови
4) к глюкозурии
40. Первым продуктом расщепления гликогена в мышцах является
1) УДФ-глюкоза
2) глюкозо-1-фосфат
3) глюкозо-6-фосфат
4) фруктозо-6-фосфат
5) глюкоза
41. Коферменты окислительного декарбоксилирования пировиноградной кислоты - это
1) НАД+
2) ТПФ
3) КоА
4) ФАД
5) НАДФ+
42. ТПФ участвует
1) в гликолизе
2) в пентозофосфатном пути
3) в окислительном декарбоксилировании пирувата
4) в ЦТК
5) в глюконеогенезе
43. Фосфофруктокиназа 1
1) активируется АМФ
2) активируется фруктозо-1,6-бисфосфатом
3) активируется НАДН(Н)
4) инактивируется АМФ
44. Первый фермент пентозофосфатного пути превращения глюкозы - это
1) альдолаза
2) транскетолаза
3) фосфорилаза
4) трансальдолаза
5) глюкозо-6-фосфатдегидрогеназа
45. Реакции окисления в цикле Кребса - это превращения
1) α-кетоглутарата в сукцинил-КоА
2) Х-малата в оксалоацетат
3) сукцината в фумарат
4) фумарата в Х-малат
5) изоцитрата в α-кетоглутарат
46. В синтезе гликогена из глюкозы в печени участвуют
1) глюкокиназа
2) гликогенсинтаза
3) фосфорилаза
4) фосфоглюкомутаза
5) глюкозо-1-фосфат-уридилтрансфераза
47. Рибулозо-5-фосфат представляет собой
1) фосфокетогексозу
2) фосфокетопентозу
3) альдопентозу
4) фосфотетрозу
5) фосфокетокислоту
48. Фермент, присутствующий в печени и отсутствующий в мышцах, - это
1) глюкозо-6-фосфатаза
2) гексокиназа
3) пируваткиназа
4) фосфорилаза
49. Кофермент сукцинатдегидрогеназы - это
1) ФАД
2) ФМН
3) НАД+
4) НАДФ+
5) ТПФ
50. Аллостерический фермент в цикле трикарбоновых кислот Кребса - это
1) аконитаза
2) фумараза
3) сукцинатдегидрогеназа
4) фосфофруктокиназа
5) изоцитратдегидрогеназа
51. Ферменты, отсутствующие в мышцах, - это
1) глюкозо-6-фосфатаза
2) гексокиназа
3) пируваткиназа
4) фосфорилаза
5) глюкокиназа
52. Аминокислота, являющаяся основным субстратом глюконеогенеза в печени, - это
1) аланин
2) метионин
3) цистеин
4) аргинин
5) серин
Правильные ответы
1. 2, 3, 4
2. 2
3. 3
4. 3
5. 4
6. 4
7. 1
8. 5
9. 1
10. 1, 2, 3, 4
11. 4
12. 1, 2, 4
13. 1, 5
14. 3, 5
15. 4
16. 2
17. 1, 2, 4
18. 1, 2, 5
19. 4
20. 1, 2, 3
21. 4
22. 2
23. 2
24. 4
25. 3, 4
26. 2, 3, 4
27. 3, 4, 5
28. 2, 3
29. 2, 3, 4
30. 1, 2, 3, 5
31. 2
32. 4
33. 3
34. 1, 2, 3, 4
35. 1
36. 3, 4, 5
37. 1, 2, 5
38. 3, 5
39. 1
40. 2
41. 1, 2, 3, 4
42. 2, 3, 4
43. 1
44. 5
45. 1, 2, 3, 5
46. 1, 2, 4, 5
47. 2
48. 1
49. 1
50. 5
51. 1, 5
52. 1
Раздел 5. Обмен липидов и его регуляция
ВВЕДЕНИЕ
Роль липидов в организме человека и млекопитающих определяется их энергоемкостью (запас легко высвобождаемой химической энергии) и участием в образовании клеточных мембран. Источником липидов являются в основном пищевые жиры животного и растительного происхождения. Кроме того, вместе с жирами в пищеварительный тракт поступают жирорастворимые витамины и незаменимые жирные кислоты: линолевая, линоленовая и арахидоновая.
Расщепление жиров до глицерина и свободных высших жирных кислот (ВЖК) происходит под действием липазы и конъюги- рованных (парных) желчных кислот в двенадцатиперстной кишке. В клетках кишечника всосавшиеся мицеллы, содержащие продукты гидролиза жиров, вступают в процесс ресинтеза, образуя жиры, свойственные данному организму. Транспорт липидов кровью к органам и тканям (вследствие их нерастворимости в воде) осуществляется сывороточными липопротеинами (ЛП). В данном разделе пред- лагается определить кинетику действия липазы и влияние на этот процесс желчных кислот.
Жирные кислоты во многих тканях (особенно в печени и миокарде) вовлекаются в катаболический процесс (β-окисление), протекающий в митохондриях. Все превращения жирных кислот начинаются с их активации, т.е. с образования ацил-КоА. Биосинтез жирных кислот происходит в цитозоле и включает ряд последовательных стадий, завершающихся синтезом пальмитиновой кислоты. Центральную роль в обмене липидов занимает ацетил-КоА.
В синтезе сложных липидов в качестве строительных блоков используются жирные кислоты, глицерин, церамиды, аминоспирты и другие компоненты. В данном разделе предлагается лабораторная работа по определению сложных липидов - фосфатидилхолинов - по фосфору.
Биосинтез холестерина осуществляется преимущественно в печени из ацетил-КоА; важнейшими промежуточными соединениями при этом являются β-гидрокси-β-метилглутарил-КоА (ГМГ-КоА), сквален и ланостерин. Холестерин в составе липопротеинов сыворотки крови переносится к другим органам и тканям, где включается в состав клеточных мембран либо служит предшественником для синтеза стероидных гормонов. В разделе представлена практическая работа по количественному определению холестерина в сыворотке крови.
Под действием активных форм кислорода и свободных радикалов липиды, входящие в состав клеточных мембран, подвергаются пероксидному окислению, конечным продуктом которого является токсичный продукт - малоновый диальдегид (МДА), количественное определение которого предлагается провести.
5.1. КИНЕТИКА ДЕЙСТВИЯ ЛИПАЗЫ
Липаза - фермент поджелудочной железы, катализирующий гидролиз сложноэфирных связей в молекуле триацилглицеролов (ТАГ) в тонком кишечнике. Наиболее активно панкреатическая липаза катализирует гидролиз первой и третьей сложноэфирных связей ТАГ с образованием ди- и моноацилглицеролов (ДАГ и МАГ), затем осуществляется гидролиз 2-моноацилглицеролов. В кишечнике могут всасываться только продукты гидролиза ТАГ: глицерин, высшие жирные кислоты, ДАГ и МАГ.
Существенно облегчают процесс переваривания и всасывания липидов желчные кислоты, холевая и хенодезоксихолевая, а также их конъюгаты с глицином и таурином. Сочетание в химической структуре гидрофобной (стероидная часть) и гидрофильной частей придает парным желчным кислотам свойства поверхностно-активных веществ (детергентов), которые, образуя микроэмульсию, активируют субстрат липазы и диффузию продуктов липолиза в эпителиальные клетки ворсинок кишечника. При этом фермент и субстрат находят- ся в разных фазах (несмешивающиеся жидкости) и взаимодействуют только на границе раздела фаз.
Величина поверхности контакта фермента и субстрата определяет скорость гетерогенного катализа: чем больше поверхность, тем выше скорость ферментативной реакции. Детергентное действие желчных кислот приводит к уменьшению силы поверхностного натяжения на
границе раздела фаз, и крупная капля жира распадается на множество мелких капель, доступных действию фермента.
Дефицит липазы чаще всего связан с заболеваниями поджелудочной железы и сопровождается панкреатической стеатореей (высокое содержание ТАГ в кале без изменения его окраски).
Нарушение экскреторной функции поджелудочной железы при перекрытии ее протока (закупорка камнем, воспалительный процесс) при панкреатитах или непосредственном повреждении ткани железы (опухоль, атеросклероз сосудов, кровоизлияние и др.) существенно сказывается на жировом обмене. При стеаторее организм теряет воду и электролиты, затрудняется всасывание жирорастворимых витаминов.
Цель работы
Оценить кинетику действия липазы, определить характер влияния желчи на активность панкреатической липазы.
Принцип метода
В качестве источника нейтрального жира (ТАГ) используют молоко. Действие фермента оценивают по скорости образования кислых продуктов расщепления (свободных ВЖК). Для этого от общего объема смеси жира с липазой через определенные промежутки времени отбирают для титрования равные части. Титрование кислых продуктов гидролиза осуществляют раствором гидроксида натрия (индикатор фенолфталеин):
R-COOH + NaOH → R-COONa + H2O.
Результаты выражают в миллилитрах пошедшего на титрование раствора щелочи и представляют в виде графика зависимости содер- жания ВЖК в пробе от времени инкубации пробы.
Выполнение работы
В два стаканчика наливают по 10 мл разбавленного водой (1:1) молока. В один из стаканчиков вносят 1 мл желчи (проба 1), в другой - 1 мл Н2О (проба 2). Из каждой пробы отбирают в колбу для титрования по 2 мл образовавшейся смеси и титруют
Значение титрования без липазы (время реакции «0») вычитают из величины последующих титрований. В этом случае полученные гра- фики пройдут через начало координат, так как вычитается исходное количество органических кислот, присутствующих в молоке (исходная кислотность молока). Полученные результаты оформляют в виде графика, показывающего динамику отщепления свободных ВЖК во времени под действием липазы в присутствии и в отсутствие желчи.
Пример графика динамики отщепления свободных ВЖК во времени под действием липазы в присутствии желчи (кривая 1) и в ее отсутствие (кривая 2)
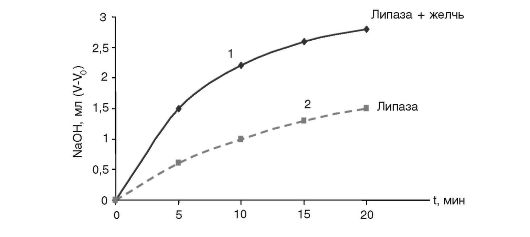
Схема определения
I. Приготовление исходной смеси (в стаканчиках) | ||
Реактивы и этапы Проба 1 Проба 2 | ||
1. Молоко, разбавленное водой (1:1), мл 2. Вода, мл 3. Желчь, мл | 10 1 | 10 1 |
II. Определение исходной кислотности молока | ||
Колба для титрования 1 | Колба для титрования 2 | |
1. Исходная смесь (отбирают аликвоту из стаканчика в колбу для титрования), мл 2. Фенолфталеин (добавляют в каждую колбу), капли | 2 1-2 | 2 1-2 |
Окончание табл.
Титруют пробы раствором NaOH (до розового цвета). Значения записывают в таблицу результатов (V0 и V0 ') | ||
III. Отбор смеси и титрование в присутствии липазы | ||
К оставшейся исходной смеси в оба стаканчика быстро добавляют по 1 мл липазы и отмечают время. Через каждые 5 мин отбирают аликвоты в колбы для титрования | ||
Колба для титрования 1 | Колба для титрования 2 | |
1. Аликвота, мл 2. Фенолфталеин, капли Быстро титруют раствором NaOH (до розового цвета). Значения записывают в таблицу результатов (V и V '). Повторные титрования проводят через каждые 5 мин и результаты заносят в следующую таблицу | 2 1-2 | 2 1-2 |
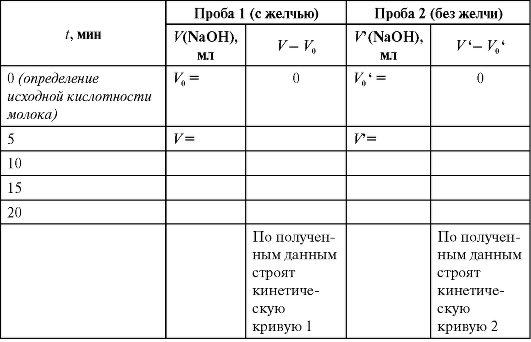
Оформление результатов
Самостоятельное формулирование выводов
Тестовые задания для проверки знаний материала предыдущего семестра
1. Определите, верно ли утверждение.
1. Смесь свободных аминокислот дает положительную нингидриновую реакцию.
2. Гидрофобность серина выше, чем валина.
3. Специфичность действия ферментов определяется коферментом.
4. Витамины А, В и С относят к группе водорастворимых витаминов.
5. Все гормоны имеют белковую природу.
6. Глюкокортикоиды стимулируют глюконеогенез.
7. ТПФ является коферментом реакций карбоксилирования.
8. Активность фосфорилазы контролируется путем фосфорилирования и дефосфорилирования.
9. При тепловой денатурации белка происходит разрыв пептидных связей.
10. Тимин относят к пуриновым основаниям.
11. Все белки имеют четвертичную структуру.
12. Глицерин в печени может превращаться в глюкозу.
2. Выберите правильный ответ.
Белки не могут выполнять При гидролизе лактозы
функцию образуются
1) каталитическую 1) глюкоза и галактоза
2) транспортную 2) манноза и глюкоза
3) структурную 3) галактоза и фруктоза
4) коферментную 4) глюкоза и фруктоза
5) защитную 5) две молекулы галактозы
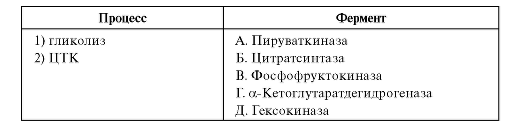
3. Установите соответствие между процессом и участвующим в нем ферментом.
5.2. КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ФОСФАТИДИЛХОЛИНОВ (ЛЕЦИТИНОВ) ПО ФОСФОРУ
Фосфатидилхолины (лецитины) - это холиновые производные фосфатидной кислоты. Сочетание гидрофобных и гидрофильных участков в молекуле придает им амфифильные свойства.
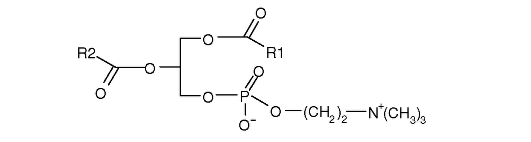
Благодаря амфифильным свойствам фосфатидилхолины образуют гидрофильную оболочку жировых мицелл и обеспечивают всасывание высших жирных кислот и МАГ в кишечнике путем диффузии. Фосфатидилхолины входят в состав липопротеинов - транспортных форм липидов. При этом липопротеины низкой плотности (ЛПНП) и высокой плотности (ЛПВП) содержат соответственно 11-21% и 24-30% фосфолипидов, основную часть которых составляют фосфатидилхолины. Фосфатидилхолины служат основными компонентами биомембран, наиболее богаты ими клетки мозга, нервной ткани, сердца и печени.
Повышение уровня ЛПНП наблюдается при гиперлипопротеи- немии II типа (семейная гиперхолестеринемия), гиперкортицизме, сахарном диабете, гипотиреозе. Понижение уровня ЛПНП происходит при синдроме мальабсорбции, муковисцидозе, тяжелом голодании. Количество ЛПВП повышается при хроническом алкоголизме и снижается при обтурационной желтухе, лимфогрануломатозе. Снижение интенсивности обмена фосфоглицеридов в мозге имеет место при инсулиновой коме. Недостаток холина или метионина нарушает синтез фосфатидилхолинов в печени, что приводит к жировой инфильтрации печени.
Цель работы
Определить содержание фосфатидилхолинов в сыворотке крови и сравнить полученный результат с нормой.
Принцип метода
Количество фосфатидилхолинов рассчитывают по содержанию фосфора. Сначала из пробы удаляют белки и экстрагируют фосфолипиды спиртом, затем оставшиеся органические вещества разрушают путем минерализации в присутствии концентрированной серной кислоты. При этом углерод превращается в СО2, водород в Н2О, азот в сульфат аммония, фосфор в анион фосфорной кислоты. После добавления пероксида водорода азот удаляется в виде летучих оксидов, и в пробе остается только нелетучий фосфор и его оксиды, количество которых определяют фотометрически в реакции с молибдатом аммония в присутствии аскорбиновой кислоты по калибровочному графику.
Выполнение работы
Приготовление рабочего раствора сыворотки
1. Депротеинизация сыворотки крови. В пробирку наливают 2 мл сыворотки крови и 5 мл спирта, перемешивают стеклянной палочкой, нагревают на водяной бане (80 ?С) в течение 10 мин. Пробирку охлаж- дают и содержимое фильтруют через сухой фильтр в сухую пробирку.
2. Минерализация. Фильтрат (1 мл) переносят в тугоплавкую колбу Кьельдаля для сжигания и по стенкам колбы осторожно добавляют 10 капель концентрированной H2SO4. Через 15 мин после начала сжигания в колбу добавляют несколько капель пероксида водорода и продолжают нагревать до просветления жидкости. Колбу охлаждают и содержимое количественно переносят в мерную пробирку.
Стадии 1 и 2 заранее выполняются лаборантом; студенты начинают работу с нейтрализации полученного раствора (стадия 3).
3. Нейтрализация. Содержимое мерной пробирки доводят по универсальной индикаторной бумаге до рН = 7,0 (светло-зеленый цвет) 10%-ным раствором щелочи. В случае добавления избытка щелочи проводят нейтрализацию 10%-ным раствором серной кислоты.
Определение концентрации фосфатидолхолинов по содержанию фосфора
К содержимому мерной пробирки после нейтрализации добавляют 2,5 мл молибдата аммония и 0,5 мл 1%-ного раствора аскорбиновой кислоты, доводят водой до 10 мл. Пробу оставляют на 20 мин при комнатной температуре для развития окраски, а затем проводят измерение оптической плотности на ФЭК в кювете (

Параллельно строят калибровочную кривую. Расчет содержания фосфора в пробе СХ (мкг/мл) проводят по калибровочному графику (данные для его построения приведены в таблице).


Тестовые задания по теме «Расщепление жиров, глицерина и высших жирных кислот»
1. Определите, верно ли утверждение.
1. Жиры расщепляются с образованием свободных жирных кислот.
2. Пальмитиновая и олеиновая жирные кислоты являются ненасыщенными соединениями.
3. Транспортной формой триацилглицеролов являются хиломикроны.
4. Глицерин нельзя отнести к жирам.
5. Наличие желчи ускоряет действие липазы.
6. Активирование жирных кислот требует затраты энергии.
7. Карнитин принимает участие в транспорте ВЖК внутрь митохондрии.
8. Глицерин в живой клетке может превращаться в 3-фосфоглицери- новый альдегид.
9. Предварительное активирование жирной кислоты необходимо для синтеза нейтральных жиров.
10. Белки расщепляются под действием липазы.
11. Желчные кислоты - это производные циклопентанпергидрофенантрена.
12. В молекуле фосфатидной кислоты содержится атом азота.
2. Выберите правильный ответ.
Гормон, активирующий липазу Биологической активностью в адипоцитах, - это обладают
1) инсулин 1) моноациглицеролы
2) адреналин 2) диацилглицеролы
3) кальцитонин 3) триацилглицеролы
4) окситоцин 4) глицерин
5) альдостерон 5) все вышеперечисленные
соединения
3. Установите соответствие между структурой и названием желчных кислот.
5.3. КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ХОЛЕСТЕРИНА В СЫВОРОТКЕ КРОВИ
Холестерин (холестерол) - это высший, полициклический, ненасыщенный, одноатомный, вторичный спирт.
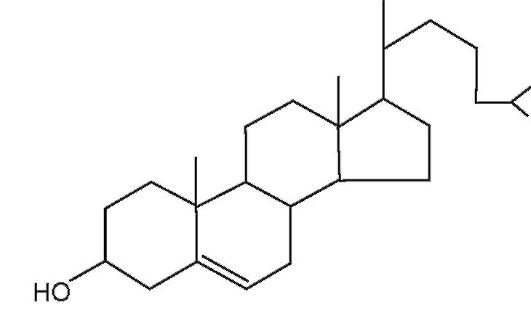
Большая часть холестерина в крови находится в виде холестеридов - сложных эфиров с высшими жирными кислотами: пальмитино- вой, стеариновой или олеиновой. Холестерин и его эфиры нерастворимы в воде и образуют комплексные соединения со специфическими белками, которые являются обязательными компонентами ЛП сыворотки крови и клеточных мембран, влияют на физико-химические свойства плазматической мембраны, регулируют ее проницаемость и влияют на активность интегрированных в нее ферментов. Из холестерина образу- ются физиологически активные вещества: желчные кислоты, стероидные гормоны и провитамины группы D. Холестерин поступает в организм с пищей, но в основном синтезируется из ацетил-КоА в печени и частично в кишечнике. Из печени в ткани он попадает в составе ЛПНП. Избыток холестерина из тканей удаляется ЛПВП в печень. Холестерин - это основной компонент ЛПНП и минорный ЛПОНП и ЛПВП.
На содержание холестерина в сыворотке крови влияют различные факторы: наследственность, питание, состояние эндокринных желез и внутренних органов (печень, почки). Так, например, повышение уровня холестерина в сыворотке крови наблюдается при атеросклерозе, семейной гиперхолестеринемии, декомпенсированном сахарном диабете, нефротическом синдроме, хроническом гепатите, гипопротеинемии. Понижение концентрации холестерина происходит при остром гепатите, болезни Гоше, острых инфекциях, кахексии, анемии, остром панкреатите. Исследуется роль холестерина в про- цессах нейродегенерации и развитии болезни Альцгеймера.
Цель работы
Определить содержание холестерина в сыворотке крови и сравнить полученный результат с нормой.
Принцип метода
Холестеринэстераза гидролитическим путем расщепляет сложноэфирную связь в эфирах холестерина (холестеридах). Образовавшийся свободный холестерин как спирт окисляется холестеринокси- дазой до кето-формы холестерина (холестенона) и пероксида водорода. Последний под действием пероксидазы способен окислять фенол при участии 4-аминоантипирина до окрашенного соединения - хинонимина. Оптическую плотность окрашенного раствора хинонимина определяют фотометрически. Расчет концентрации холестерина проводят по сравнению со стандартным раствором.
Выполнение работы (см. Приложение 9.2)
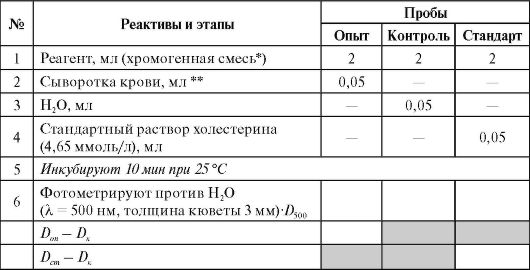
* В состав реагента входят: холестеринэстераза, холестериноксидаза, пероксидаза, 4-аминоантипирин, фенол, фосфатный буфер (рН = 6,5). ** При проведении анализа лошадиной сыворотки крови следует помнить, что содержание холестерина в ней значительно ниже, чем в сыворотке крови человека. Расчеты
Расчет концентрации холестерина проводят по формуле:
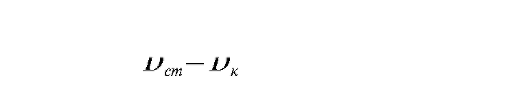
где 4,65 ммоль/л - концентрация холестерина в стандартном растворе. Норма: 4,4-5,5 ммоль/л.
Самостоятельное формулирование выводов Тестовые задания по теме
«β-Окисление высших жирных кислот и их биосинтез»
1. Определите, верно ли утверждение.
1. В β-окислении жирных кислот участвуют ФАД- и НАД-зависимые дегидрогеназы.
2. Полное окисление одной молекулы пальмитиновой кислоты до СО2 и Н2О сопровождается образованием 130 молекул АТФ.
3. Линоленовая кислота является незаменимой для человека.
4. Для образования мевалоновой кислоты необходим НАДФН(Н+).
5. Простагландины образуются из полиненасыщенных жирных кислот.
6. Холестерин в сыворотке крови находится только в свободном состоянии.
7. В биосинтезе высших жирных кислот НАДФН(Н+) можно заменить на НАДН(Н+).
8. Биотин участвует в биосинтезе жирных кислот.
9. В животном организме возможно полное превращение нейтральных жиров в углеводы.
10. Все стадии β-окисления жирных кислот в митохондриях обратимы.
11. Витамины В2 и РР необходимы для нормального протекания β- окисления жирных кислот.
12. С возрастом концентрация холестерина в сыворотке крови человека повышается.
2. Выберите правильный ответ.
Кофермент, участвующий НАДФН (Н+) для биосинтеза
в биосинтезе жирных кислот, но не жирных кислот и холестерина
участвующий в их окислении, - это поставляется за счет
1) ФАД 1) гликолиза
2) НАД+ 2) ЦТК
3) НАДФН (Н+) 3) β-окисления жирных
4) КоА кислот
5) ТПФ 4) биологического окисления
5) пентозофосфатного пути
3. Установите последовательность образования метаболитов β-окисления жирных кислот.

5.4. КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ МАЛОНОВОГО ДИАЛЬДЕГИДА
Свободными радикалами (R*) называют атомы, молекулы или структурные фрагменты молекул, имеющие на внешних орбиталях неспаренные электроны. В силу исключительно высокойреакционной способности радикалы могут взаимодействовать сразличными молекулами, вызывая их повреждение. Малоновый диальдегид (МДА) - конечный продукт свободно-радикального окисления полиненасыщенных высших жирных кислот, входящих всостав фосфолипидов биологических мембран. МДА - химически очень активное вещество: его альдегидные группы взаимодействуют с NH2-группами белков, вызывая необратимую денатурацию последних.
Активация в клетке пероксидных и свободно-радикальных процессов - это один из факторов патогенеза атеросклероза, ишемической болезни сердца, инфаркта, инсульта, язвенной и ожоговой болезни, онкологических, воспалительных и инфекционных заболеваний, синдрома адаптационного перенапряжения и хронической усталости, диабета. Синдром пероксидации проявляется также при низком уровне антиоксидантов, стрессе любого происхождения, действии синтетических лекарств и ксенобиотиков, гиподинамии, старении организма, избыточном потреблении в пищу жиров и углеводов, гипоксических состояниях, воздействии вибрации, электромагнитных полей, радиоактивного и ультрафиолетового излучений.
Цель работы
Определить содержание МДА в сыворотке крови.
Принцип метода
МДА реагирует с тиобарбитуровой кислотой, при этом образуется окрашенное соединение - триметиловый комплекс. Оптическую плотность окрашенного раствора определяют на ФЭК при 532 нм и рассчитывают концентрацию МДА, исходя из молярного коэффициента экстинции триметилового комплекса.
Выполнение работы
Студентам выдается готовый лизат, приготовленный следующим образом: к 2 мл крови добавляют 0,2 мл 0,1%-ного раствора Тритон Х-100 и оставляют на 30 мин при 0 ?С. МДА определяют в образовавшемся лизате по нижеприведенной схеме:
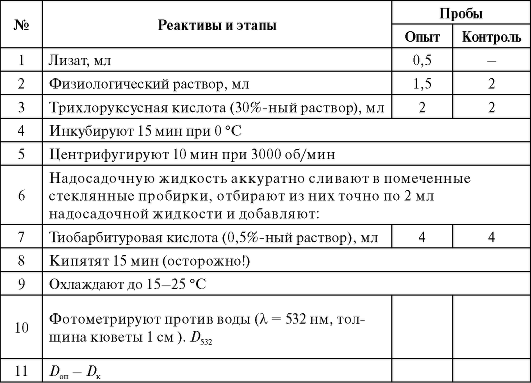
Расчеты
Концентрацию МДА (СХ) вычисляют по формуле: СХ = 76,92 ? (Do? - DK) (мкмоль/л).
Примечание. Величина 76,92 рассчитывается исходя из молярного коэффициента экстинкции триметилового комплекса (1,56 . 105 М-1см-1) и разведения.
Самостоятельное формулирование выводов
Тестовые задания по теме «Обмен липидов и его регуляция»
I. Определите, верно ли утверждение.
1. В организме животных встречаются в основном жирные кислоты с четным числом углеродных атомов.
2. В состав молекулы фосфатидилхолина входит остаток серина.
3. Карнитин осуществляет транспорт активированных жирных кис - лот в митохондрии.
4. Желчные кислоты синтезируются в печени.
5. В биосинтезе фосфатидилхолина участвует ЦТФ.
6. В состав парных желчных кислот может входить глицин.
7. В организме синтезируются гормоны липидной природы.
8. В хиломикронах велико содержание холестерина.
9. Глицерин может превращаться в диоксиацетонфосфат. 10. Для биосинтеза холестерина нужен НАДФН (Н+).
II. Сквален является циклическим соединением.
12. Ацетон может образоваться из ацетоуксусной кислоты.
13. Ацетил-КоА - единственный источник образования ацетоновых тел в организме.
14. Ацетоацетат является дополнительным источником энергии в клетках печени.
15. Донором метильных групп для синтеза фосфатидилхолина является метионин.
16. Ненасыщенные жирные кислоты синтезируются значительно быстрее, чем насыщенные.
17. НАДФН (Н+) является коферментом β-гидрокси-β-метилглутарил-КоА- редуктазы.
18. Энергетический выход полного окисления глюкозы меньше по сравнению с окислением капроновой кислоты.
19. Фосфатидная кислота является общим метаболитом в синтезе триацилглицеролов и фосфатидилхолина.
20. Липаза жировой ткани активируется цАМФ.
21. Пальмитоил-КоА и серин являются источником синтеза сфинголипидов.
22. Адреналин активирует липолиз в жировой ткани.
23. В организме человека ацетил-КоА может превращаться в глюкозу.
24. Малонил-КоА ингибирует карнитиновый транспорт высших жирных кислот в митохондрии.
2. Выберите правильный ответ.
2.1.
Факторы, тормозящие липолиз В синтезе фосфатидилхолина
в жировой ткани, - это принимает участие
1) катехоламины и соматотропин 1) цистеин
2) глюкокортикоиды 2) метионин
3) стресс, физическая нагрузка, 3) треонин голодание 4) глицин
4) глюкагон и кортикотропин 5) аланин
5) инсулин и простагландины
2.2.
В биосинтезе жирных кислот Конечный продукт действия
участвует синтазы жирных кислот - это
1) карнитин 1) бутирил-КоА
2) биотин 2) бутирил-АПБ
3) сфингозин 3) пальмитиновая кислота
4) церулоплазмин 4) стеариновая кислота
5) ФАДН2 5) пальмитоил-КоА

5.5. КОЛЛОКВИУМ ПО ТЕМЕ «ОБМЕН ЛИПИДОВ И ЕГО РЕГУЛЯЦИЯ»
Вопросы для самостоятельной подготовки
1. Механизм β-окисления высших жирных кислот. Роль КоА, карнитина и АТФ в этом процессе.
2. Особенности окисления высших жирных кислот с нечетным числом углеродных атомов.
3. Превращения глицерина. Энергетический эффект полного аэробного окисления молекулы глицерина.
4. Биосинтез высших жирных кислот.
5. Синтез фосфатидилхолинов.
6. Ацетоновые (кетоновые) тела, синтез, биологическая роль. Значение определения ацетоновых тел в моче для диагностики сахарного диабета.
7. Холестерин, его биологическая роль. Основные этапы синтеза. Количественное определение холестерина в сыворотке крови.
8. Транспорт липидов в организме. Липопротеины сыворотки крови.
9. Связь обмена липидов и углеводов.
10. Пероксидное окисление липидов. Роль цитохрома Р-450 в микросомальном окислении гидрофобных соединений.
Варианты письменной части коллоквиума
1. Укажите примерный белково-липидный состав (%)
1) ЛПВН
2) ЛПНП
3) ЛПОНП
4) хиломикронов
2. Напишите реакции
1) биосинтеза ацетоновых тел
2) β-окисления олеиновой кислоты
3) восстановления в биосинтезе ВЖК (укажите источники кофермента)
4) биосинтеза сфингомиелина
3. Укажите, какой основной метаболический процесс является источником энергии
1) в печени
2) в сердечной мышце
3) в эритроцитах
4) в мозге
4. Объясните, каким путем и сколько молекул АТФ максимально можно получить при полном окислении одной молекулы
1) триолеата
2) олеопальмостеарата
3) олеодистеарата
4) стеаропальмофосфатидной кислоты
5. Укажите, какую позицию в молекуле холестерина будет занимать 14С
1) из 14С3-глюкозы
2) из 14С4-глюкозы
3) из 14С1-ГАФ
4) из 14С1-пирувата
6. Укажите, какие атомы углерода могут включаться в глюкозу и глицерин
1) из малонил-АПБ?
2) из пальмитиновой кислоты?
3) из олеиновой кислоты?
4) из стеариновой кислоты?
Варианты заданий компьютерного тестирования
Инструкция к тесту. Выберите все правильные ответы.
1. Аллостерический фермент, регулирующий синтез ВЖК, - это
1) ацетил-КоА-карбоксилаза
2) гексокиназа
3) фосфофруктокиназа
4) липаза
5) ГМГ-синтаза
2. Содержание триацилглицеролов в ХМ составляет примерно
1) 10%
2) 20%
3) 30%
4) 50%
5) 80%
3. В переносе ацетил-КоА из митохондрии в цитоплазму участвует
1) цитрат
2) малат
3) карнитин
4) оксалоацетат
5) альбумин
4. Участники биосинтеза ВЖК - это
1) малонил-КоА
2) биотин
3) сфингозин
4) НАДФН(Н+)
5) ФАДН2
5. В образовании фосфатидилсерина могут участвовать
1) лецитин
2) ЦДФ-диацилглицерол
3) цистеин
4) S-аденозилметионин
5) серин
6. В состав биологических мембран входят
1) диацилглицеролы
2) жирные кислоты
3) холестерин
4) фосфолипиды
5) гликолипиды
7. Рециркуляция между печенью и кишечником характерна
1) для фосфолипидов
2) для моноацилглицеринов
3) для глицерина
4) для лизофосфолипидов
5) для желчных кислот
8. Антиатерогенными свойствами обладают
1) ХМ
2) ЛПВП
3) ЛПНП
4) ЛПОНП
5) холестериды
9. В митохондриях происходят
1) β-окисление жирных кислот
2) синтез цитрата
3) липолиз триацилглицеролов
4) синтез фосфолипидов
5) образование ацетоновых тел
10. Эйкозаноиды образуются из арахидоновой кислоты путем
1) липоксигенизации
2) метилирования
3) декарбоксилазным
4) карбоксилазным
5) циклооксигенации
11. Ингибируют липолиз триациглицеролов в адипоцитах
1) инсулин
2) катехоламины
3) простагландины
4) глюкокортикоиды
5) глюкагон
12. Из холестерина в организме человека могут синтезироваться
1) жирные кислоты
2) диацилглицеролы
3) желчные кислоты
4) половые гормоны
5) глюкокортикоиды
13. Общим метаболитом в синтезе ТАГ и фосфатидилхолина является
1) фосфатидная кислота
2) фосфатидилинозитол
3) этаноламин
4) холин
5) серин
14. В лимфатическую систему кишечника диффундируют
1) ЛПНП
2) ЛПВП
3) ЛПОНП и ЛПВП
4) ЛПНП и ЛПОНП
5) ХМ
15. Коферменты, участвующие в β-окислении жирных кислот, - это
1) НАД+
2) НАДФ+
3) ФАД
4) КоА
5) ТГФК
16. К группе эйкозаноидов относят
1) простагландины
2) простациклины
3) тромбоксаны
4) лейкотриены
5) изопреноиды
17. В биосинтезе фосфатидилхолинов могут участвовать
1) холестерин
2) ЦДФ-холин
3) S-аденозилметионин
4) фосфатидилэтаноламин
5) ЦДФ-диацилглицерол
18. Фосфолипиды - это
1) лецитины
2) кардиолипины
3) ацилглицеролы
4) церамиды
19. Липолиз в жировой ткани угнетается
1) адреналином
2) глюкагоном
3) тироксином
4) инсулином
5) кортикотропином
20. Ацетил-КоА-карбоксилазу тормозят
1) цитрат
2) АТФ
3) пальмитат
4) авидин
5) биотин
21. Уровень холестерина в крови возрастает при введении
1) инсулина
2) адреналина
3) норадреналина
4) глюкагона
5) глюкокортикоидов
22. Ацетил-КоА участвует в синтезе
1) глицерина
2) холестерина
3) пирувата
4) ацетоацетата
5) ВЖК
23. Коферментом в реакциях биосинтеза холестерина и ВЖК служит
1) НАДН(Н)
2) ФАДН2
3) НАДФН(Н)
4) ТПФ
5) ПФ
24. Сукцинил-КоА образуется
1) в процессе биосинтеза холестерина
2) в процессе окисления арахидоновой кислоты
3) в ЦТК
4) в процессе биосинтеза жирных кислот
5) в процессе биосинтеза сфинголипидов
25. Предшественник эйкозаноидов - это
1) пальмитат
2) арахинат
3) арахидонат
4) стеарат
5) олеат
26. Гормоны, активирующие гормончувствительную липазу в адипоцитах, - это
1) адреналин и норадреналин
2) простагландины и инсулин
3) окситоцин и вазопрессин
4) тироксин и глюкокортикоиды
5) гормоны гипоталамуса
27. Липиды, содержащие остаток глицерина, - это
1) церебрози ды
2) ганглиозиды
3) лецитины
4) сфинголипиды
5) кардиолипины
28. Внемитохондриальный синтез ВЖК аллостерически активирует
1) НАДФН(Н)
2) АТФ
3) СО2
4) цитрат
5) авидин
29. Факторы, тормозящие липолиз в жировой ткани, - это
1) катехоламины и соматотропины
2) стресс, физическая нагрузка, голодание, охлаждение
3) глюкагон и кортикотропин
4) инсулин и простагландины
30. В синтезе жирных кислот участвуют
1) НАД+ и ФАД
2) ЦТФ и УТФ
3) АПБ и НАДФН(Н)
4) карнитин и фосфат
5) ПФ и ТПФ
31. В биосинтезе кетоновых тел и холестерина участвуют
1) малонил-КоА
2) сукцинил-КоА
3) β-гидрокси-β-метилглутарил-КоА
4) мевалонат
5) ацетил-КоА
32. Азотсодержащие липиды - это
1) каротины
2) витамины А, Е, K
3) лецитины
4) церамиды
5) триацилглицеролы
33. Атерогенными считают
1) ХМ
2) ЛПОВП
3) ЛПНП
4) ЛПВП
5) ЛПОНП
34. Витамин F представляют жирные кислоты
1) линолевая
2) линоленовая
3) арахидоновая
4) арахиновая
5) олеиновая
35. Ацетоновые тела - это
1) ацетил-КоА и сукцинил-КоА
2) ацетоацетат и β-оксибутират
3) ацетоацетил-КоА и пропионил-КоА
4) пируват и малат
36. Конечный продукт действия синтетазы жирных кислот - это
1) бутирил-КоА
2) бутирил-АПБ
3) пальмитиновая кислота
4) стеариновая кислота
5) олеиновая кислота
37. Коферменты, не участвующие в биосинтезе ВЖК, - это
1) ФАД
2) НАД+
3) биотин
4) НАДФН(Н)
38. Ацетоновые тела синтезируются
1) в цитозоле
2) в митохондриях
3) в ядре
4) в ЭПС
5) в микросомах
39. В энтероцитах кишечника ресинтезируются
1) триацилглицеролы
2) жирные кислоты
3) желчные кислоты
4) кетоновые тела
5) фосфолипиды
40. Концентрация (ммоль/л) общего холестерина в сыворотке крови в норме составляет
1) 0,1
2) 1,0
3) 5,0
4) 7,0
5) 10,0
41. В состав желчи для обеспечения мицеллярной диффузии жирных кислот и моноациглицеролов должны входить
1) соли желчных кислот и холестерин
2) жирорастворимые витамины
3) желчные пигменты
4) липаза и колипаза
5) незаменимые жирные кислоты
42. В синтезе фосфолипидов специфически участвует нуклеозидтрифосфат
1) АТФ
2) ЦТФ
3) ГТФ
4) УТФ
5) ТТФ
43. Первый циклический продукт в биосинтезе холестерина - это
1) меванолат
2) изопентилпирофосфат
3) фарнезилпирофосфат
4) сквален
5) ланостерин
44. Вторичные посредники в передаче гормонального сигнала - это
1) ДАГ
2) инозитол-1,4,5-трифосфат
3) цАМФ
4) адреналин
5) биотин
45. Остаточные хиломикроны (ХМ) - это
1) ХМ, лишившиеся белка
2) ХМ, лишившиеся холестерина
3) ХМ, лишившиеся ТАГ
4) ХМ, разрушающиеся в печени
46. Синтез высших жирных кислот протекает
1) в ядре
2) в рибосомах
3) в лизосомах
4) в цитоплазме
5) в комплексе Гольджи
47. Удлинение цепи высших жирных кислот (С18, C20 ...) может про- исходить
1) в ядре
2) в митохондриях
3) в лизосомах
4) в плазматической мембране
5) в рибосомах
48. В синтезе фосфоглицеролипидов принимают участие
1) 1,2-диацилглицеролы
2) фосфатидная кислота
3) сфингозин
4) цитидинтрифосфат
5) желчные кислоты
49. Транспорт холестерина из периферических тканей в печень осуществляют
1) ЛПВП
2) ЛПНП
3) ЛПОНП
4) желчные кислоты
50. Простагландины синтезируются у человека из кислоты
1) олеиновой
2) пальмитиновой
3) стеариновой
4) арахидоновой
5) арахиновой
51. Восстановленный НАДФ(Н+) для биосинтеза ВЖК и холестерина поставляется в основном за счет
1) гликолиза
2) цикла Кребса
3) β-окисления ВЖК
4) дезаминирования аминокислот
5) пентозофосфатного пути окисления глюкозы
52. Превращение ацетил-КоА в глицерин в организме животных
1) не выяснено
2) возможно
3) невозможно
53. Из холестерина в организме человека не могут образоваться
1) андрогены
2) желчные кислоты
3) желчные пигменты
4) кортикостероиды
5) прогестерон
6) катехоламины
54. Энтерокиназа обнаружена
1) в слюне
2) в желудке
3) в кишечнике
4) в мышцах
5) в печени
55. Укажите, может ли печень использовать ацетоновые тела для получения ацетил-КоА?
1) может
2) не может
3) наукой не установлено
56. Укажите, может ли свободный глицерин использоваться в жировой ткани для синтеза ТАГ?
1) может
2) не может
3) наукой не установлено
Правильные ответы
1. 1
2. 5
3. 1
4. 1, 2, 4
5. 2, 5
6. 3, 4, 5
7. 5
8. 2
9. 1, 2, 5
10. 1, 5
11. 1, 3
12. 3, 4, 5
13. 1
14. 5
15. 1, 3, 4
16. 1, 2, 3, 4
17. 2, 3, 4, 5
18. 1, 2
19. 4
20. 3, 4
21. 1
22. 2, 4, 5
23. 3
24. 3
25. 3
26. 1
27. 3, 5
28. 4
29. 4
30. 3
31. 3, 5
32. 3, 4
33. 3, 5
34. 1, 2, 3
35. 2
36. 3
37. 1, 2
38. 2
39. 1, 5
40. 3
41. 1
42. 2
43. 5
44. 1, 2, 3
45. 3
46. 4
47. 2
48. 1, 2, 4
49. 1
50. 4
51. 5
52. 3
53. 3, 6
54. 3
55. 2
56. 2