Клиническая фармакология: избранные лекции / С.В. Оковитый, В.В. Гайворонская, А.Н. Куликов, С.Н. Шуленин. - 2009. - 608 с.
|
|
|
|
ЛЕКЦИЯ 3 КЛИНИЧЕСКАЯ ФАРМАКОЛОГИЯ СРЕДСТВ ЛЕЧЕНИЯ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Сердечная недостаточность является одним из самых распространенных, тяжелых и прогностически неблагоприятных осложнений заболеваний сердечно-сосудистой системы. В основе данной патологии лежит нарушение сократительной функции миокарда в связи с дистрофическими, биохимическими изменениями его рабочих мышц.
Сердечная недостаточность может развиться в результате:
- уменьшения массы нормально функционирующей сердечной мышцы;
- перегрузки объемом;
- перегрузки давлением.
Уменьшение массы нормально функционирующей сердечной мышцы возникает при поражении миокарда некротического, воспа- лительного характера (миокардиты, миокардиодистрофии, ИБС, кардиомиопатии). Перегрузка объемом развивается вследствие обратного тока крови при пороках сердца (недостаточность митрального или аортального клапанов), усиления притока крови при артериовенозных шунтах. Перегрузка давлением возникает в случае препятствия току крови у больных со стенозом аорты или легочной артерии, при артериальной гипертензии. Основные патогенетические звенья хронической сердечной недостаточности (ХСН) представлены на схеме 3.1.
Таким образом, исходя из патогенеза сердечной недостаточности, основные направления терапии ХСН должны быть следующие.
• Снижение избыточной активации симпатоадреналовой и ренинангиотензин-альдостероновой систем (ингибиторы АПФ, β-адреноблокаторы, антагонисты альдостерона).
• Воздействие на почечное звено сердечной недостаточности (ограничение поступления Na+ и воды в организм, применение диуретиков).
• Снижение периферического сосудистого тонуса (ингибиторы АПФ, блокаторы рецепторов ангиотензина II, вазодилататоры).
• Нормализация сердечного выброса (кардиотонические средства, ингибиторы АПФ, β-адреноблокаторы).
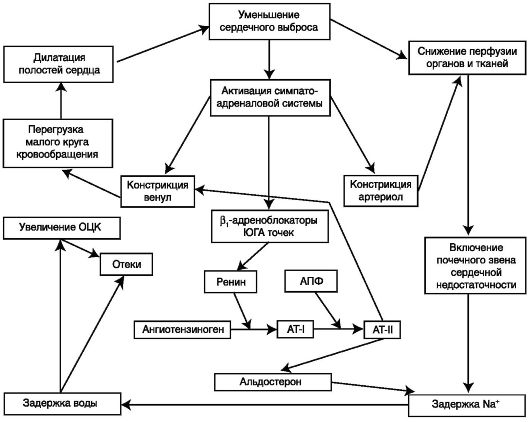
Схема 3.1. Основные патогенетические звенья хронической сердечной недостаточности:
ОЦК - объем циркулирующей крови; АПФ - ангиотензинпревращающий фермент; AT - ангиотензин; ЮГА - юкстагломерулярный аппарат
Выбор медикаментозной терапии основывается на стадии недостаточности кровообращения и функциональном классе сердечной недо- статочности в соответствии с Национальными рекомендациями ВНОК и ОССН по диагностике и лечению ХСН (второй пересмотр, 2006).
Основные цели лечения хронической сердечной недостаточности
• Устранение симптомов ХСН.
• Замедление прогрессирования ХСН и защита органов-мишеней (сердце, мозг, почки, сосуды).
• Повышение качества жизни.
• Снижение количества и продолжительности госпитализаций и, соответственно, расходов на лечение.
• Улучшение прогноза.
Классификация средств для лечения хронической сердечной недостаточности
• Основные:
1. И нгибиторы АПФ.
2. β-адреноблокаторы и смешанные адреноблокаторы.
3. Диуретики.
4. Антагонисты альдостерона.
5. Сердечные гликозиды.
6. Блокаторы рецепторов ангиотензина II.
• Дополнительные:
1. Статины.
2. Антикоагулянты.
• Вспомогательные:
1. Периферические вазодилататоры (нитраты).
2. Блокаторы кальциевых каналов (дигидропиридиновые).
3. Антиаритмические средства.
4. Антиагреганты.
5. Негликозидные кардиотоники.
3.1. ОСНОВНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
К группе основных лекарственных средств, используемых для лечения ХСН, относятся препараты, влияние которых на клиническую картину, качество жизни и прогноз доказаны и не вызывают сомнений.
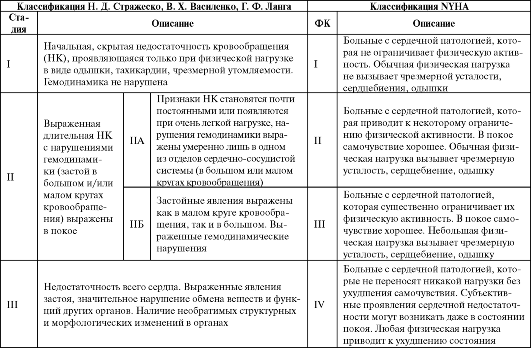
Классификации сердечной недостаточности по стадиям заболевания и функциональному классу (NYHA)
Ингибиторы ангиотензинпревращающего фермента
• Каптоприл (Капотен).
• Эналаприл (Энап).
• Периндоприл (Престариум).
• Лизиноприл (Диротон).
• Фозиноприл (Моноприл).
• Спираприл (Квадроприл).
• Квинаприл (Аккупро).
• Рамиприл (Тритаце).
В настоящее время иАПФ рассматриваются как основные препараты в терапии ХСН. Вопросы, связанные с классификацией, механизмом действия иАПФ на клеточном уровне подробно рассматриваются в предыдущей лекции. Результатом снижения содержания ангиотензина II и накопления брадикинина является артерио- и венодилатация. Расширение артериол приводит к снижению общего периферического сопротивления сосудов и постнагрузки. Следствием расширения вен является снижение венозного возврата и преднагрузки. Увеличение в тканях сосудорасширяющих кининов (брадикинина), в частности, в почках, приводит к дилатации почечных сосудов и, следовательно, улучшению почечного кровотока. Вследствие этого увеличивается фильтрация, повышается выведение избыточного количества Na+ и воды, снижается ОЦК и, как следствие, уменьшается венозный возврат. Уменьшение содержания альдостерона также приводит к увеличению выведения Na+ и воды.
Таким образом, при лечении иАПФ у больных с сердечной недостаточностью снижается давление в венах, правом предсердии, легочной артерии, легочных капиллярах, общее периферическое сопротивление. Вторично возрастает фракция выброса, ударный объем. Частота сердечных сокращений не меняется или урежается, снижается содержание катехоламинов.
Кроме того, через 3-4 недели постоянного применения иАПФ в целевых дозах начинает происходить регрессия ремоделирования сосудов и миокарда, обусловленная уменьшением влияния ангиотензина II на специфические рецепторы в этих тканях. В результате развивается дополнительное снижение ОПСС и редуцируются явления гипертрофии миокарда.
Ингибиторы АПФ показаны всем больным с ХСН при любой этиологии и стадии процесса. Препараты эффективны от начальных признаков заболевания (включая бессимптомную дисфункцию левого желудочка) до самых поздних стадий декомпенсации. Они улучшают клиническую
Таблица 3.1. Особенности применения ингибиторов АПФ с максимальной степенью доказанности при ХСН (по данным рандомизированных клинических исследований)
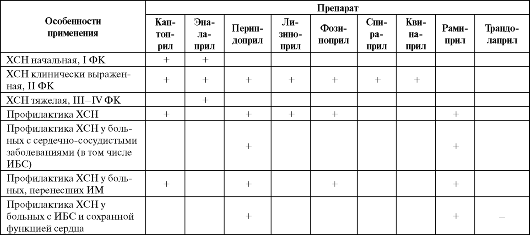
картину заболевания, качество жизни, замедляют прогрессирование болезни, снижают заболеваемость и улучшают прогноз больных с ХСН, т. е. позволяют достичь всех пяти целей лечения ХСН. Использование иАПФ снижает летальность больных, страдающих ХСН III ст. Особенности применения различных иАПФ при ХСН представлены в табл. 3.1.
При назначении иАПФ больным с ХСН следует учитывать, что данное заболевание оказывает значимое влияние на фармакокинетику этих препаратов, что обусловлено снижением их абсорбции из ЖКТ и объема распределения, нарушением биотрансформации и выведения из организма. Влияние ХСН на фармакокинетику иАПФ представлено в табл. 3.2.
Таблица 3.2. Особенности фармакокинетики некоторых ингибиторов АПФ при ХСН (Белоусов Ю. Б., Гуревич К. Г., 2005)
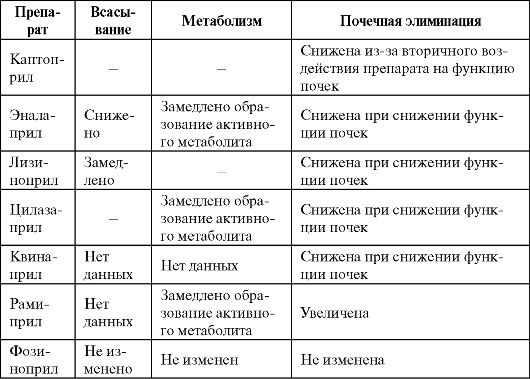
Терапию
ингибиторами АПФ следует начинать с назначения малых доз в связи со
снижением функции почек у многих больных с ХСН. После приема первой
дозы в течение нескольких часов необходимо контролировать АД. Если
снижение АД будет больше
3 дня (а при системной гипотензии не чаще одного раза в неделю) до достижения оптимальной (средней терапевтической) дозы. В случае гипотензии начальные дозы препаратов необходимо уменьшить в 2 раза. Рекомендуемые дозы препаратов представлены в табл. 3.3.
Таблица 3.3. Начальные, средние терапевтические и максимальные дозы ингибиторов АПФ, используемые для лечения ХСН (Национальные рекомендации по диагностике и лечению сердечной недостаточности, второй пересмотр, 2006)
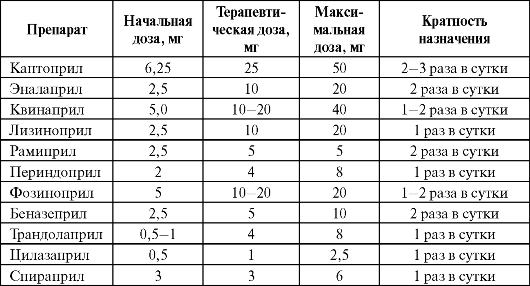
Критериями положительного терапевтического действия препаратов при ХСН являются: улучшение клинического состояния боль- ных (уменьшение одышки, увеличение переносимости физической нагрузки и т. д.), стойкое снижение давления наполнения желудочков в покое и при физической нагрузке, уменьшение риска развития внезапной смерти, ИМ, острых сосудистых катастроф, увеличение продолжительности и качества жизни. При этом раз начатая терапия при адекватно подобранной дозе и отсутствии побочных эффектов должна продолжаться неопределенно долго.
Эффективность использования иАПФ может несколько снижаться при ишемической этиологии ХСН, у женщин, а также ослабляться одновременным приемом нестероидных противовоспалительных препаратов (в меньшей степени малыми дозами ацетилсалициловой кислоты).
Побочные эффекты и особенности взаимодействия иАПФ описаны в лекции «Клиническая фармакология средств лечения артериаль- ной гипертензии». При снижении почечной фильтрации ниже 60 мл в мин доза иАПФ должна быть уменьшена в 2 раза, а при снижении
ниже 30 мл в мин - на 3/4. Это же относится и к лечению пожилых больных с ХСН, у которых почечная функция, как правило, нарушена. Исключение могут составлять фозиноприл и спираприл, имеющие двойной путь выведения из организма.
Противопоказания к назначению иАПФ
• Непереносимость препарата (чаще в виде ангионевротического отека).
• Стеноз аорты, почечных артерий.
• Трансплантация почек.
• Коллагенозы, особенно на фоне лечения иммунодепрессантами.
• Беременность, лактация.
β-адреноблокаторы и смешанные адреноблокаторы
Селективные β1-адреноблокаторы
• Метопролола сукцинат (Беталок ЗОК).
• Бисопролол (Конкор).
• Небиволол (Небилет).
Первая публикация о применении β-адреноблокаторов для лечения хронической сердечной недостаточности была сделана в
- снижение избыточной симпатической стимуляции миокарда;
- снижение активности РААС;
- повышение секреции натрийуретических пептидов;
- влияние на миокардиальную генную экспрессию;
- уменьшение гипертрофии миокарда;
- противоаритмический эффект.
Таким образом, применение β-адреноблокаторов, оказывающих умеренное отрицательное инотропное действие, не противоречит концепции лечения ХСН. Более того, в настоящее время доказано, что при применении БАБ происходит направленное изменение экспрессии генов, кодирующих белки-регуляторы процессов сократимости и патологической гипертрофии левого желудочка (повышается уровень Са2+-зависимой АТФ-азы саркоплазматического ретикулума и α-цепи миозина, снижается уровень β-цепи миозина). Кроме того, β-адре-
ноблокаторы оказывают блокирующее влияние и на некоторые другие нейрогормональные системы, ответственные за прогрессирование ХСН (эндотелиновая, система цитокинов).
У больных с ХСН β-адреноблокаторы оказывают двухфазное влияние на центральную гемодинамику:
- в первые две недели применения препаратов у больных сердечный выброс может снижаться (как за счет уменьшения собственно сократимости, так и в результате снижения ЧСС), а клинические проявления ХСН могут даже несколько нарастать;
- в последующем в результате уменьшения тахикардии и потребности миокарда в кислороде гибернированные кардиомиоциты восстанавливают свою сократимость и сердечный выброс начинает увеличиваться.
Использование β-адреноблокаторов в лечении ХСН позволяет, наряду с улучшением прогноза для больных с ХСН, уменьшить степень ремоделирования сердца, что позволяет замедлить прогрессирование декомпенсации и частоту госпитализаций. По способности снижать риск заболеваемости и смертности декомпенсированных больных β- адреноблокаторы даже превосходят иАПФ. При этом препараты данной группы оказывают одинаково выраженный эффект по снижению смертности как у мужчин, так и у женщин.
В национальных рекомендациях по диагностике и лечению сердечной недостаточности рекомендуется использовать селективные БАБ - бисопролол (Конкор) и метопролола сукцинат (или формы метопролола тартрата с замедленным высвобождением препарата). У больных старше 70 лет возможно применение небиволола, который хотя и не снижает смертность, но уменьшает заболеваемость пациентов и частоту повторных госпитализаций.
Смешанные (а-β)-адреноблокаторы
Доказана эффективность смешанного α-β-адреноблокатора карведилола, обладающего дополнительным антиоксидантным и антипролиферативным эффектом. Более того, анализ вторичных конечных точек испытания COMET у больных с ХСН и систолической дисфункцией левого желудочка продемонстрировал бóльшую профилактическую эффективность карведилола в сравнении с метопрололом в отношении большинства основных сердечно-сосудистых событий, включая инфаркт миокарда (ИМ), нестабильную стенокардию, инсульт и смерть от сердечно-сосудистых причин. Предполагается, что вазопротективная эффективность карведилола обусловлена его специфическим фар-
макологическим профилем в целом и бóльшими антиишемическими возможностями в частности, в сравнении с селективной β1-адреноблокадой. Рекомендуемые дозы препаратов представлены в табл. 3.4.
Таблица 3.4. Начальные, средние терапевтические и максимальные дозы β-адреноблокаторов и смешанных адреноблокаторов, используемые для лечения хронической сердечной недостаточности (Национальные рекомендации по диагностике и лечению сердечной недостаточности, второй пересмотр, 2006)
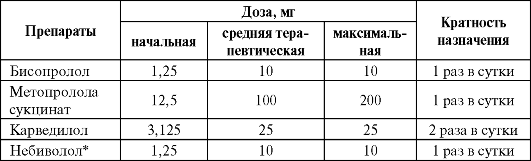
Примечание: * - только у больных старше 70 лет.
Лечение β-адреноблокаторами при ХСН нужно проводить осторожно, начиная с 1/8 терапевтической дозы. Дальнейшее увеличение дозы осуществляется медленно (раз в 2 недели, а при сомнительной переносимости или чрезмерном снижении давления - раз в месяц) до достижения средней терапевтической дозы.
В том случае, если пациент с ХСН уже получает β-адреноблокаторы, не рекомендованные для применения при данной патологии, необходимо постепенно перевести его на применение рекомендованных препаратов (табл. 3.5).
Таблица 3.5. Схема перевода больных с хронической сердечной недостаточностью с атенолола или метопролола тартрата (быстродействующие формы) на рекомендованные β-адреноблокаторы (Национальные рекомендации по диагностике и лечению сердечной недостаточности, второй пересмотр, 2006)
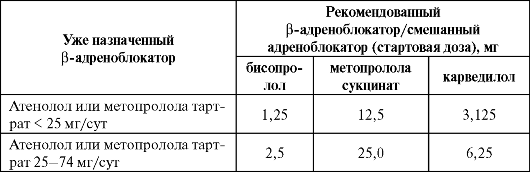
Окончание табл. 3.5
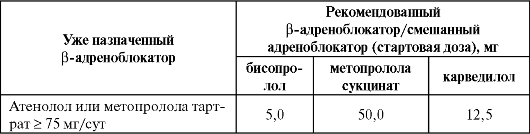
В обычных клинических ситуациях β-адреноблокаторы должны применяться в дополнение к иАПФ и у больных, у которых достигнута стабилизация состояния. В тех случаях, когда имеется преобладание выраженной тахикардии при невысоком АД и сочетание β-адреноблокатора и иАПФ затруднено, можно начать терапию с бисопролола с последующим присоединением иАПФ. Конечная цель в любом случае - максимально быстрый перевод больных с ХСН на комбинацию иАПФ + β-адреноблокатор.
Если в первые две недели лечения β-адреноблокатором наблюдается снижение сердечного выброса и обострение симптомов ХСН, воз- можно некоторое увеличение дозы диуретиков или повышение (если возможно) дозы иАПФ или применение кардиотоников (малые дозы сердечных гликозидов, сенситизаторов кальция).
Противопоказания к назначению β-адреноблокаторов при ХСН
• Бронхиальная астма и тяжелая патология бронхов.
• Симптомная брадикардия менее 50 уд./мин.
• Симптомная гипотензия менее
• Атриовентрикулярные блокады II и более степени.
• Тяжелый облитерирующий эндартериит.
Диуретики
1. Тиазидные и тиазидоподобные диуретики:
1.1. Тиазидные диуретики:
• Дихлотиазид (Гипотиазид).
• Метолазон (Зароксолин).
• Циклометиазид (Циклопентиазид).
1.2. Тиазидоподобные диуретики:
• Клопамид (Бринальдикс).
• Оксодолин (Хлорталидон).
2. Петлевые диуретики:
• Фуросемид (Лазикс).
• Буметанид (Буфенокс).
• Этакриновая кислота (Урегит).
• Торасемид (Диувер).
3. Калийсберегающие диуретики:
• Спиронолактон (Верошпирон).
• Триамтерен (Дайтек).
• Амилорид (Модамид).
• 4. Ингибиторы карбоангидразы: Ацетазоламид (Диакарб).
Задержка жидкости в организме (преимущественно во внеклеточном пространстве) с формированием отечного синдрома является типичным проявлением ХСН. Для выделения этой жидкости из организма необходимо осуществление следующих мероприятий.
1. Перевод избыточной жидкости из внеклеточного пространства в сосудистое русло. Для этого применяют достаточно мощные диуретики, которые за счет снижения объема циркулирующей крови и гидростатического давления обеспечивают переход жидкости из внеклеточного пространства в сосудистое русло. Также эффективно применение на этом этапе иАПФ, БАР, возможно использование кардиотоников. Дополнительный эффект оказывает добавление к терапии средств, повышающих онкотическое давление плазмы крови (альбумин или препараты плазмы) и антагонистов альдостерона (спиронолактона).
2. Доставка
избыточной жидкости к почкам и обеспечение ее фильтрации. Это может
быть осуществлено с помощью кардиостимулирующих средств (в первую
очередь дофамина в «почечной» дозе). При уровне АДс более
3. Блокада реабсорбции натрия (и воды) из первичной мочи в почечных канальцах. Именно на этом этапе диуретики играют решающую роль. Они устраняют отечный синдром и улучшают клиническую симптоматику у больных с ХСН. При правильном применении эти средства позволяют уменьшить число госпитализаций, однако не замедляют прогрессирования заболевания и не улучшают прогноза больных. При неправильном назначении (ударные дозы раз в 3- 7 дней) их влияние на качество жизни может быть даже негативным.
Диуретики (в первую очередь петлевые и тиазидные) следует назначать всем больным с симптомами ХСН, у которых имеется предрасположенность к задержке жидкости. Однако препараты данной группы следует применять не в качестве монотерапии, а, как правило, в комбинации с иАПФ и/или антагонистами альдостерона.
Для лечения сердечной недостаточности I и II ФК без застоя назначение диуретических препаратов нецелесообразно, так как на данном этапе нет видимых нарушений функции почек.
Безусловным показанием к назначению диуретических препаратов является ХСН IIА стадии (II ФК с явлениями застоя). Как правило, ле- чение ХСН II ФК с явлениями застоя начинается с использования малых доз тиазидных диуретиков (ТД), чтобы избежать больших и чрезмерно быстрых потерь воды и электролитов, чреватых развитием толерантности к препаратам. По мере необходимости доза ТД может увеличиваться.
В случае недостаточной эффективности ТД возможно их комбинированное применение с калийсберегающими диуретиками (КСД) 1-
2 раза в неделю или через день в меньших дозах. В тех случаях, когда такая комбинация оказывается неэффективной, применяются петлевые диуретики (ПетД). Следует также отметить, что тиазидные диуретики эффективны только при почечной фильтрации не менее 30- 50 мл/мин, в то время как петлевые реализуют свой эффект даже при фильтрации 5 мл/мин.
Терапия ХСН III ФК осуществляется ПетД (или ТД) совместно с КСД. ТД и КСД лучше назначать однократно утром, натощак. Суточную дозу ПетД можно назначить в 2 приема (утром и в обед) за 1 ч до приема пищи. ТД и КСД рекомендуется назначать за 2 ч до приема петлевых диуретиков. Суточная доза спиронолактона не должна превышать 250-300 мг, триамтерена - 200-250 мг. Иногда может возникнуть необходимость в одновременном назначении ПетД, ТД и КСД. Длительность диуретической терапии зависит от состояния больного и эффективности проводимого лечения.
Возможно
дополнительное назначение ингибитора карбоангидразы ацетазоламида
(диакарба) для сохранения чувствительности к традиционным диуретикам. С
этой целью препарат назначают по
3 раза в сутки курсами по 3-4 дня с двухнедельным перерывом. Доза применяемых мочегонных препаратов подбирается индивидуально. Подробнее диуретики рассмотрены в лекции «Клиническая фармако- логия средств лечения артериальной гипертензии».
ХСН IV ФК предусматривает сочетанное применение ТД и ПетД (иногда требуется назначение сразу двух ПетД) с одновременным использованием антагонистов альдостерона и ацетазоламида (по вышеописанной схеме).
Диуретическая терапия ХСН включает две фазы: быстрой дегидратации и поддерживающую. В фазу быстрой дегидратации превышение диуреза над принятой жидкостью должно составлять 1-2 л/сут при ежедневном снижении массы тела на 0,5-1 кг. В поддерживающей фазе диурез должен быть сбалансированным, а масса тела - стабильной при регулярном назначении мочегонных средств. Дозы некоторых мочегонных препаратов, используемых для лечения ХСН, приведены в табл. 3.6.
Таблица 3.6. Дозы мочегонных препаратов, используемых в лечении хронической сердечной недостаточности
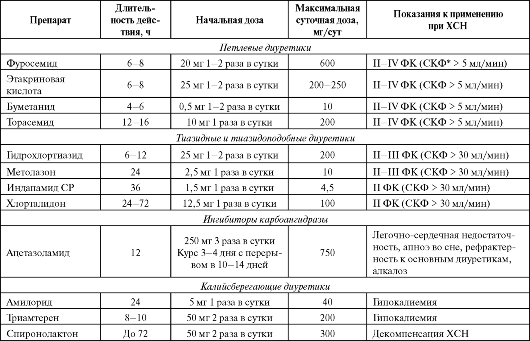
Окончание таблицы 3.6

Примечание: * - скорость клубочковой фильтрации.
Следует учитывать, что активная мочегонная терапия может осложняться обезвоживанием, гипокалиемией (проявляющейся мы- шечной слабостью, анорексией, депрессией сегмента ST, снижением амплитуды зубца Т на ЭКГ), гипонатриемией.
В ряде случаев к диуретическому действию мочегонных препаратов может развиваться толерантность (рефрактерность), которая может быть ранней (так называемое торможение эффекта) и поздней. Ранняя рефрактерность развивается в первые часы или дни после начала активного назначения диуретиков и зависит от гиперактивации нейрогормонов. Она тем сильнее, чем активнее происходит дегидратация. Преодолевается адекватным, но не чрезмерным диурезом, при обязательном одновременном назначении иАПФ и/или спиронолактона.
Поздняя рефрактерность возникает спустя недели и месяцы постоянной диуретической терапии и обусловлена гипертрофией апикальных клеток почечных канальцев. Для борьбы с ней требуется периодическая (раз в 3-4 неделю) смена активных диуретиков и их комбинация с иАПФ.
Нередко рефрактерные отеки возникают на фоне тяжело протекающего основного заболевания, такого как злокачественный миокар- дит Абрамова-Фидлера, дилатационная кардиомиопатия, постинфарктная аневризма левого желудочка.
Основные принципы лечения и профилактики рефрактерных отеков
• Назначать диуретики можно только на фоне приема иАПФ и спиронолактона.
• Ограничение потребления соли (но не жидкости!).
• Базисными препаратами являются петлевые диуретики, которые вводятся в больших дозах, иногда два раза в день (или даже постоянно внутривенно капельно), для обеспечения достаточного диуретического эффекта.
• После введения дозы диуретика, оказавшейся неэффективной, последующая доза должна быть в два раза выше и вводиться только внутривенно.
• Для повышения натрийуретического эффекта петлевых диуретиков одновременно возможно добавление тиазидных диуретиков, а для профилактики потери калия рекомендуется назначение калийсберегающих диуретиков.
• Для улучшения почечного кровотока и увеличения фильтрации (при АДс >
пельницы. Возможно также использование сердечных гликозидов. При более низком АД предпочтительнее назначение дофами- на (2-5 мкг/мин). При выраженной гипотензии в крайнем случае (на период критической гипотензии) допускается дополнительное применение глюкокортикоидов.
• Одновременное использование диуретиков и препаратов альбумина или плазмы крови (как при гипопротеинемии, так и при нормальном уровне белка).
• Эффективным способом преодоления резистентного к медикаментозному лечению отечного синдрома является изолированная ультрафильтрация. Однако она противопоказана при стенозах клапанных отверстий, низком сердечном выбросе и гипотензии. По жизненным показаниям могут применяться механические способы удаления жидкости (плевральная, перикардиальная пункции, парацентез).
Антагонисты альдостерона
• Спиронолактон (Верошпирон).
• Эплеренон (Инспра).
Выделение антагонистов альдостерона в отдельную группу является несколько условным, так как эти препараты обладают свойствами калийсберегающих диуретиков. Однако благодаря выраженному мо- дулирующему действию на нейрогормональную регуляцию они заняли особое место в лечении ХСН.
Так, спиронолактон в дозах 100-300 мг/сут однократно утром или в два приема (утро - обед), на период 1-3 недели успешно применяется как калийсберегающий диуретик в комплексной диуретической терапии при декомпенсированной ХСН, гипергидратации и необходимости лечения активными диуретиками. Он может быть использован в высоких дозах даже при одновременном назначении иАПФ или БАР, если одновременно правильно назначаются мощные диуретики и достигается адекватный диурез.
Критерии эффективности спиронолактона при лечении упорного отечного синдрома
• Увеличение диуреза в пределах 20-25%.
• Уменьшение жажды, сухости во рту, исчезновение специфического «печеночного» запаха изо рта.
• Стабильная концентрация калия и магния в плазме крови, несмотря на достижение положительного диуреза.
В период достижения компенсации (особенно у пациентов с ХСН III-IV ФК) применение спиронолактона считается абсолютно необходимым. По достижении компенсации у больных с ХСН III-IV ФК дозу спиронолактона снижают и переходят на длительный прием невысоких доз препарата (25-50 мг) в качестве дополнительного (к иАПФ и БАБ) нейрогормонального модулятора, позволяющего улучшать течение и прогноз больных с ХСН.
Вопрос о применении малых доз спиронолактона в дополнение к другим нейрогормональным медиаторам у больных с ХСН I-II ФК остается открытым.
Основными побочными реакциями при назначении спиронолактона являются гиперкалиемия, повышение уровня креатинина, гинекомастия (до 10%). Поэтому при наличии повышенного уровня креатинина в сыворотке крови (более 130 мкмоль/л), почечной недостаточности в анамнезе, даже умеренной гиперкалиемии (более 5,2 мкмоль/л) сочетание антагонистов альдостерона с иАПФ требует тщательного клинического и лабораторного контроля.
Более селективным по сравнению со спиронолактоном блокатором альдостероновых рецепторов является новый препарат эплеренон. Его назначение в комплексной терапии ХСН в дозе 25 мг/сут с последующим увеличением через 4 недели до 50 мг/сут приводит к снижению частоты внезапной смерти от сердечно-сосудистых причин (на 21%) и уменьшения частоты госпитализации по поводу ХСН (на 23%). Кроме того, его высокая селективность позволяет избежать таких побочных эффектов, как гинекомастия и импотенция. Однако убедительных данных о том, что назначение эплеренона предпочтительнее, чем спиронолактона, пока не получено.
Сердечные гликозиды
Средней длительности действия:
• Дигоксин (Цедоксин). Длительного действия:
• Дигитоксин (Дигофтон).
Сердечные гликозиды (СГ) остаются в числе средств лечения ХСН, хотя и утратили свои лидирующие позиции. В настоящее время доказано, что СГ, не влияя на общую продолжительность жизни и прогноз заболевания, существенно улучшают качество жизни и симптомы у больных с ХСН (III-IV ФК), снижают потребность в госпитализациях из-за декомпенсаций заболевания (не только у больных с мерцатель-
ной аритмией, но и при синусовом ритме). Высоко эффективны СГ у пациентов с ХСН II-IV ФК в сочетании с мерцательной аритмией.
Сердечные гликозиды - это вещества, избирательно действующие на сердце. Они состоят из сахаристой части (рамноза) - гликона и несахаристой части - агликона или генина. Носителем биологической активности является агликон. От гликона зависит растворимость сердечных гликозидов и их фиксация в тканях.
Основные виды действия сердечных гликозидов
• Положительное инотропное действие (увеличение силы сердечных сокращений).
• Положительное тонотропное действие (снижение размеров дилатированного сердца).
• Отрицательное хронотропное действие (снижение частоты сердечных сокращений).
• Отрицательное дромотропное действие (снижение проводимости в проводящей системе сердца).
• Положительное батмотропное действие (повышение возбудимости волокон Пуркинье и кардиомиоцитов).
Механизм положительного инотропного действия СГ связан с блокадой фермента Na+/К+-АТФ-азы. Сердечные гликозиды связывают SH-группировки Na+/К+-АТФ-азы, что приводит к повышению концентрации Na+ в кардиомиоцитах. Увеличение концентрации внутриклеточного Na+ приводит к снижению выхода Са2+ из кардиомиоцитов. Кроме того, повышение содержания Са2+ в цитоплазме является результатом активации выхода Са2+ из саркоплазматического ретикулума и входа через потенциалзависимые кальциевые каналы цитоплазматической мембраны. Увеличение концентрации внутриклеточного Са2+ приводит к увеличению сопряжения актина и миозина и повышению силы сердечных сокращений. Сердечное сокращение становится более сильным и более коротким, что, однако, ограничивает использование СГ при митральном стенозе.
При этом следует отметить, что мощное положительное инотропное действие СГ развивается при использовании достаточно высоких доз (для дигоксина > 0,375 мг/сут), что потенциально опасно из-за риска развития интоксикации и является предиктором отрицательного влияния на прогноз больных с ХСН.
Механизм отрицательного хроно- и дромотропного действия СГ связан, в основном, с активацией парасимпатической нервной системы. В результате увеличения силы сердечных сокращений кровь во
время систолы с большей силой выбрасывается в аорту, что приводит к активации барорецепторов дуги аорты и рефлекторной активации центров блуждающего нерва. Следствием этого является снижение ЧСС и проводимости атипичных волокон сердца. Кроме того, не исключается и прямое ваготоническое действие СГ. Отрицательный хронотропный эффект сдерживает применение СГ при выраженной брадикардии и при недостаточности клапанов аорты (увеличение перегрузки сердца объемом).
Механизм положительного батмотропного действия также связан с блокадой Na+/К+-АТФ-азы. В результате в волокнах Пуркинье и кардиомиоцитах увеличивается содержание Na+ и Ca2+, что приводит к снижению трансмембранного потенциала и критического уровня деполяризации. Поэтому медленная диастолическая деполяризация быстрее достигает критического уровня и возникает внеочередное сокращение - экстрасистола. Этот эффект проявляется преимущественно в субтоксических дозах СГ или при гипокалиемии или гиперкальциемии.
СГ усиливают и укорачивают систолу, удлиняют диастолу. Результатом положительного инотропного действия будет увеличение сердечного выброса, ударного и минутного объемов, уменьшение конечного диа- столического давления. Снижается выраженность застойных явлений, за счет улучшения гемодинамики почек увеличивается диурез.
При ХСН положительное влияние СГ обусловлено не только и не столько положительным инотропным действием, а прежде всего экстракардиальными эффектами (понижение активности САС и РААС, нормализация барорефлекторных механизмов регуляции сердечной деятельности). Чаще всего препаратом выбора при ХСН является дигоксин, обладающий оптимальными фармакодинамическими свойствами и достаточно полно оцененный в клинических исследованиях.
Согласно современным представлениям, дигоксин должен применяться в малых дозах - до 0,25 мг/сут, а при массе тела более
При наличии почечной недостаточности суточная доза дигоксина должна быть уменьшена пропорционально снижению клиренса кре- атинина (в этом случае возможно применение дигитоксина). У пожилых больных суточные дозы дигоксина должны быть снижены до 0,0625-0,125 мг (1/4-1/2 таблетки в сутки).
При мерцательной аритмии дигоксин является средством первой очереди благодаря его способности снижать атриовентрикулярную проводимость и ЧСС.
Для контроля эффективности и безопасности применения препарата необходимо перед каждым последующим изменением дозы про- водить ЭКГ-исследование. В случае появления признаков передозировки в качестве поддерживающей дозы выбирается предыдущая.
Основные сведения по фармакокинетике СГ представлены в табл. 3.7.
Показателями оптимально проводимой терапии СГ является субъективное улучшение состояние пациента, уменьшение размеров за- стойной печени и отеков, увеличение диуреза, повышение толерантности к физической нагрузке.
Наибольший клинический эффект сердечные гликозиды оказывают у больных с ХСН при низкой фракции выброса (менее 25%), больших размерах сердца (кардиоторакальный индекс более 55%), неишемической этиологии ХСН. Хороший результат достигается при комбинировании сердечных гликозидов с β-адреноблокаторами, при котором лучше контролируется ЧСС, снижается риск развития опасных для жизни желудочковых аритмий и уменьшается опасность обострения коронарной недостаточности.
Длительное применение сердечных гликозидов может привести к их передозировке вследствие кумуляции, особенно у женщин. Этому может способствовать ряд факторов:
1. Гипокалигистия, наблюдающаяся при миокардитах, ИБС и
ХСН.
2. Гипокалиемия, развивающаяся при ХСН, применении диуретиков и глюкокортикоидов.
3. Почечная и печеночная недостаточность, приводящие к нарушению биотрансформации и элиминации СГ.
4. Одновременное применение адреномиметиков (дофамин, адреналин, эфедрин), ингибиторов фосфодиэстеразы (теофиллин), антикоагулянтов (гепарин), противоаритмических средств (хинидин, дифенин), β-адреноблокаторов.
5. Уменьшение размеров функционирующего миокарда (острый период ИМ, миокардит, кардиомегалия).
Интоксикация сердечными гликозидами проявляется целым рядом симптомов. Со стороны ЖКТ могут наблюдаться тошнота, рвота, боли в области эпигастрия. Эти проявления связаны с прямым раздражающим действием препаратов на слизистую оболочку ЖКТ и активацией дофаминовых DA2-рецепторов триггерной зоны. Со стороны сердца может быть брадикардия, атриовентрикулярная блокада, желудочковая экстра-
Таблица 3.7. Фармакокинетика сердечных гликозидов, применяемых при хронической сердечной недостаточности
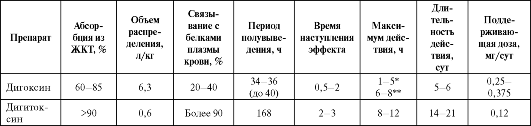
Примечание: * - при внутривенном введении; ** - при пероральном применении.
систолия. В токсической фазе возможно появление политопных желудочковых экстрасистол на фоне тахикардии, изменение вольтажа ST.
Лечение интоксикации сердечными гликозидами
• Отмена препарата.
• Для коррекции гипокалигистии вводится поляризующая смесь: 5% раствор глюкозы (200 мл), инсулин - 4 ЕД, калия-магния аспарагинат (панангин) - 10 мл внутривенно капельно.
• Для связывания ионов Са2+ используются комплексоны: этилендиаминтетрауксусная кислота (ЭДТА) вводится внутривенно капельно 2-4 г в 500 мл 5% раствора глюкозы.
• Для восстановления активности Na+/К+-АТФ-азы применяется донатор SH-групп - унитиол (по 5 мл 5% раствора внутривенно).
• В случае отсутствия эффекта от применения вышеперечисленных препаратов назначают дигинбид, представляющий собой Fab-фраг- менты антител для связывания СГ. Содержимое флакона (40 мг), способное нейтрализовать 0,6 мг дигоксина, растворяют в 4 мл воды для инъекций и вводят внутривенно капельно в течение 30 мин.
Противопоказания к назначению сердечных гликозидов
• Брадикардия менее 55 уд./мин.
• Атриовентрикулярная блокада.
• Нестабильная стенокардия, острый период инфаркта миокарда.
• Синдром Вольффа-Паркинсона-Уайта (WPW-синдром).
• Легочно-сердечная недостаточность III ст.
• Почечная недостаточность (возможно применение дигитоксина).
• Мерцательная аритмия с редким ритмом желудочков.
Блокаторы рецепторов ангиотензина II
• Лосартан (Козаар).
• Валсартан (Диован).
• Кандесартан (Атаканд).
В последние годы были получены убедительные данные, что при ХСН некоторые блокаторы рецепторов ангиотензина II (БАР): лосартан, валсартан и кандесартан - практически сравнимы по эффективности с иАПФ. Тем не менее блокаторы рецепторов к ангиотензину II не следует использовать при лечении ХСН у больных, которые ранее не получали иАПФ. Подробнее эти препараты рассматриваются в лекции «Клиническая фармакология антигипертензивных средств».
Блокаторы рецепторов ангиотензина II можно назначать как в качестве альтернативы иАПФ, так и в комбинации с иАПФ, хотя предпочтение всегда должно отдаваться комбинации иАПФ с β-ад-
реноблокатором. Только при непереносимости β-адреноблокатора стоит переходить на сочетание иАПФ с БАР II. Тройная комбинация иАПФ + БАР II + β-адреноблокатор хотя и может в большей степени блокировать нейрогормоны и процессы ремоделирования миокарда и сосудов, но может приводить к чрезмерному снижению АД и вторичной реактивации нейрогормональных систем, ответственных за прогрессирование ХСН. Поэтому в качестве третьего компонента, дополняющего иАПФ и БАБ, лучше использовать антагонисты альдостерона. Рекомендуемые дозы препаратов представлены в табл. 3.8.
Таблица 3.8. Начальные, средние терапевтические и максимальные дозы БАР II, используемые для лечения хронической сердечной недостаточности (Нацио- нальные рекомендации по диагностике и лечению сердечной недостаточности, второй пересмотр, 2006)
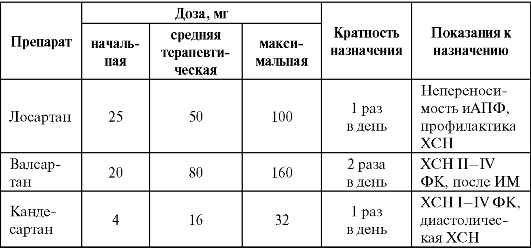
Титрование
доз препаратов осуществляется так же, как и для иАПФ. Стартовая доза
может удваиваться каждые 3-5 дней (при стабильном АД и отсутствии
осложнений) до достижения средних терапевтических или максимальных доз.
При исходной гипотензии (АДс менее
3.2. ДОПОЛНИТЕЛЬНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
К группе дополнительных лекарственных средств, используемых для лечения ХСН, относятся препараты, эффективность и безопасность которых установлены, но требуют уточнения.
Статины
Несмотря на то что имеются данные, позволяющие предполагать способность дополнительного улучшения статинами прогноза больных с ХСН ишемической этиологии, до настоящего времени не полу- чено убедительных результатов по снижению данными препаратами смертности среди пациентов с ХСН. Тем не менее статины, вероятно, могут несколько снижать риск развития ХСН ишемической этиологии и улучшать прогноз пациентов с уже развившейся декомпенсацией.
Таблица 3.9. Рекомендуемые дозы статинов в терапии ХСН (Национальные рекомендации по диагностике и лечению сердечной недостаточности, второй пересмотр, 2006)
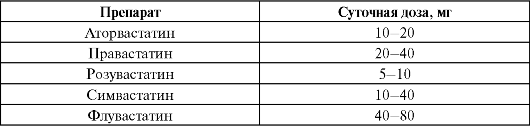
При этом нет необходимости стремиться к достижению максимально переносимых доз статинов. В том случае, если уровень общего холестерина менее 3,2 ммоль/л, от применения препаратов следует воздержаться. Контроль безопасности применения статинов не отличается от такового при гиперлипидемии.
Антикоагулянты
Для предупреждения тромбозов и эмболий у пациентов с декомпенсацией ХСН, находящихся на постельном режиме, могут быть использованы низкомолекулярные гепарины. В частности, одобрено применение эноксапарина (40 мг/сут в течение 2-3 недель) и дальтепарина.
Непрямые антикоагулянты (Варфарин, Синкумар) абсолютно необходимы для больных с мерцательной аритмией и повышенным рис- ком тромбоэмболий:
- в пожилом возрасте;
- при наличии тромбоэмболий в анамнезе;
- при инсультах и транзиторных нарушениях мозгового кровообращения;
- в случае обнаружения внутрисердечных тромбов;
- при резком снижении фракции выброса (менее 35%) и расширении камер сердца (конечный диастолический размер более
Международное нормализованное отношение (МНО) при этом должно поддерживаться в пределах 2-3. Доказательств эффективности непрямых антикоагулянтов у больных с синусовым ритмом (даже при дилатации сердца и наличии тромбов) в настоящее время нет.
К сожалению, непрямые антикоагулянты не могут быть заменены антиагрегантами (ацетилсалициловая кислота, клопидогрел или их комбинация), так как эффективность лечения в таком случае снижается, а при комбинированной терапии риск кровотечений сопоставим с таковым у варфарина.
Несмотря на то что в официальных рекомендациях в качестве дополнительных лекарственных средств лечения ХСН фигурируют лишь статины и антикоагулянты, существует еще целый ряд препара- тов, которые изучаются и рассматриваются в качестве перспективных в терапии хронической сердечной недостаточности.
Ингибиторы ренина
Еще один подход к блокаде РААС - ее угнетение на наиболее раннем этапе активации (образование ренина) с помощью специфических ингибиторов ренина (эналкирена, занкирена, ципрокирена, ремики- рена), проходящих испытания в пилотных исследованиях. Препараты данной группы обладают способностью селективно блокировать превращение ангиотензиногена в АТ-I, что определяет их специфичность. Первые испытания ингибиторов ренина при ХСН показали, что эти препараты повышают ударный выброс, снижают среднее АД и ОПС, улучшают почечный кровоток. Более значимый эффект достигается у пациентов, находящихся на терапии диуретиками, которые, как известно, способны активировать РААС. Пока ингибиторы ренина не нашли широкого применения при ХСН, однако используются в терапии артериальной гипертензии (например, алискирен).
Рекомбинантный натрийуретический пептид типа В
• Несиритид (Натрекор).
Натрийуретические пептиды (А- и В-типы) синтезируются в мозге и миокарде желудочков. Они влияют на высвобождение ряда регуляторных факторов: тормозят секрецию вазопрессина и АКТГ, снижают ак- тивность РААС, уменьшают высвобождение катехоламинов из надпочечников. Синтезирующийся в клетках мозга, натрийуретический пептид (В-тип) играет роль в регуляции уровня Na+ и диуреза, уровня АД.
Установлено, что повышение уровня натрийуретических пептидов ассоциируется с тяжестью сердечной недостаточности. Система-
тическое применение несиритида, рекомбинантного человеческого натрийуретического пептида типа В, вызывает улучшение гемодинамики, включая вазодилатацию, увеличение натрийуреза и снижение активности РААС. Клинические исследования продемонстрировали как гемодинамическое, так и клиническое улучшение состояния пациентов. Дополнительным достоинством препарата является наличие у него положительного инотропного эффекта при достаточно низкой аритмогенности.
Ингибиторы вазопептидаз
• Кандоксатрил.
• Омапатрилат (Ванлев).
Кандоксатрил - ингибитор нейтральной эндопептидазы, разрушающей натрийуретические пептиды, брадикинин и другие биологически активные пептиды. Препараты данной группы назначаются для уменьшения инактивации натрийуретических пептидов и тем самым для потенцирования натрийуретического и сосудорасширяющего действия этого эндогенного фактора у больных с ХСН и артериальной гипертензией. Благоприятное влияние кандоксатрила (400 мг/сут) на функциональный статус больных с ХСН (I - III ФК) сравнимо с эф-
фектом капторила (50-100 мг/сут). Выраженность натрийуретического эффекта кандоксатрила зависит от величины сердечного выброса.
Омопатрилат является «двойным ингибитором металлопротеаз», блокирующим ангиотензинпревращающий фермент и нейтральную эндопептидазу. Этот препарат не уступает иАПФ по клинической эффективности и влиянию на прогноз больных с ХСН. У таких пациентов после 24 недель лечения омапатрилатом (40 мг 1 раз в сутки) увеличивает толерантность к нагрузкам, как и лизиноприлом (20 мг 1 раз в сутки), однако омопатрилат достоверно превосходит лизиноприл по влиянию на заболеваемость и смертность. Вопрос о применении ингибиторов вазопептидаз в широкой клинической практике будет решен окончательно после завершения крупных РКИ.
Блокаторы эндотелиновых рецепторов
• Босентан (Траклир).
• Ситаксентан.
• Тезосентан.
• Амбрисентан.
Концентрация эндотелина (ЭТ), являющегося мощным вазопрессорным агентом, в крови пациентов с ХСН обычно повышена и на- ходится в прямой зависимости от функционального класса, фракции
выброса левого желудочка и толерантности к физической нагрузке. Особенно тесные взаимосвязи существуют со степенью легочной гипертензии. Это объясняется тем, что основной синтез эндотелина при ХСН происходит именно в системе легочного кровообращения.
В настоящее время применяют неселективный блокатор ЭТ-рецепторов босентан, который при ХСН назначают по 500 мг 2 раза в сутки, и тезосентан. Созданы и проходят клиническую апробацию как селективные блокаторы ЭТ-А рецепторов (ситаксентан), так и ингибиторы образования ЭТ-1 (фосфорамидон). Перспективы данной группы препаратов связывают с их кардиопротекторными возможностями, заключающимися в блокировании процессов эндотелин-опосредованного ремоделирования сердца и сосудов. В то же время попытка использования тезосентана у больных с острой декомпенсацией ХСН оказалась неудачной, так как препарат не влиял на клиническое течение и смертность при данной патологии.
Новый препарат из этой группы - амбрисентан - пока изучается как средство лечения легочной гипертензии, способное улучшать показатели выживаемости и отсрочить наступление клинического ухудшения заболевания.
Блокаторы вазопрессиновых V2-рецепторов
• Толваптан.
• Кониваптан.
Учитывая, что перегрузка объемом является частой причиной острой декомпенсации больных с ХСН, а диуретики и некоторые другие лекарственные средства, используемые для борьбы с задержкой жидкости, могут вызывать нарушение функции почек, активно продолжается поиск вмешательств, направленных на уменьшение симптомов и признаков ХСН и улучшение прогноза.
Эффективность блокатора вазопрессиновых V2-рецепторов
(толваптана в дозе 30-90 мг/сут в течение 25-60 дней) была доказана у
больных с застойной ХСН, резистентной к стандартной терапии, в том
числе диуретиками. В этом случае дополнительное введение препарата в
лечебную схему позволило уменьшить дозу диуретика, снизить массу тела
(за первые сутки на
Хотя длительное лечение толваптаном больных, госпитализированных с декомпенсацией ХСН, не оказывает значимого клиническо- го эффекта ни в лучшую, ни в худшую сторону в сравнении с плацебо (препарат не продемонстрировал в РКИ EVEREST долгосрочного влияния на общую и сердечно-сосудистую смертность, а также на заболеваемость пациентов, связанную с ХСН), тем не менее, блокада рецепторов вазопрессина является эффективной и безопасной для ускорения выведения жидкости из организма и улучшения клинической картины ХСН при краткосрочном применении. Поэтому результаты проведенных испытаний поддерживают использование толваптана у пациентов, госпитализированных по поводу ХСН с признаками выраженного застоя жидкости.
3.3. ВСПОМОГАТЕЛЬНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА, ПРИМЕНЯЕМЫЕ ДЛЯ ЛЕЧЕНИЯ
ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
К группе вспомогательных лекарственных средств, используемых для лечения ХСН, относятся препараты, влияние которых на прогноз заболевания неизвестно (или не доказано), а их применение диктуется клинической картиной.
Вазодилататоры
1. Преимущественно венозные вазодилататоры.
• Нитраты (см. классификацию антиангинальных средств).
2. Преимущественно артериальные вазодилататоры.
2.1. Миотропные спазмолитики.
• Гидралазин (Апрессин).
2.2. Блокаторы кальциевых каналов (производные дигидропиридина).
• Амлодипин (Норваск).
• Фелодипин (Плендил).
3. Смешанные вазодилататоры.
• Натрия нитропруссид (Нанипрус).
В настоящее время не существует специфических показаний для применения вазодилататоров при ХСН, однако они могут использо- ваться в качестве дополнительных средств при лечении сопутствующей стенокардии и/или артериальной гипертензии. Следует учитывать, что эти препараты не влияют на прогноз, частоту госпитализации и прогрессирование болезни.
Для лечения ХСН могут применяться препараты первых двух групп. Из нитратов чаще всего в настоящее время используются изосорбида динитрат и изосорбида мононитрат. Вазодилататоры этой группы, оказывая основное действие на вены, снижают преднагрузку, ограничивая венозный возврат крови к сердцу. Уменьшается диастолическое заполнение правых отделов сердца, затем легочной артерии, что сопровождается разгрузкой малого круга кровообращения и снижением диастолического заполнения левого желудочка. Фармакокинетические особенности нитратов, механизм действия на клеточном уровне, особенности фармакокинетики и побочные эффекты рассматриваются в лекции «Клиническая фармакология средств лечения ишемической болезни сердца».
Нитраты назначаются в первую очередь при сочетании ХСН с ИБС в том случае, если имеется стенокардия, которая проходит только от нитратов. При этом следует придерживаться следующих гемодинами- ческих показателей (Мухарлянов Н. М., Мареева В. Ю., 1994):
• Центральное венозное давление более
• АД более 100/60 мм рт. ст.
• АД пульсовое более
• Диастолическое давление в легочной артерии (ДДЛА) более
• Сердечный индекс ≥3 л/мин на м2.
Общим свойством артериальных вазодилататоров является расширение артериол, что приводит к снижению ОПСС, постнагрузки, внутриартериального давления, способствует опорожнению левого желудочка и увеличению сердечного выброса. В настоящее время самостоятельного значения в терапии ХСН препараты данной группы не имеют.
Ограниченное применение (преимущественно у лиц негроидной расы) находит комбинация гидралазина и изосорбида динитрата при непереносимости иАПФ и БАР. При этом следует помнить, что у лиц белой расы всегда предпочтительнее использовать иАПФ.
Блокаторы кальциевых каналов
Амлодипин и фелодипин - единственные блокаторы медленных кальциевых каналов (производные дигидропиридина), которые используются в комплексной терапии ХСН (у больных I-II ФК без застойных явлений, преимущественно диастолической) при упорной стенокардии или гипертензии, высокой легочной гипертензии и выраженной клапанной регургитации. При этом они не ухудшают про-
гноз больных с ХСН. Однако они должны обязательно применяться в комплексе с иАПФ, БАБ и антагонистами альдостерона.
Антиаритмические препараты
Лечение при ХСН требуют лишь опасные для жизни и симптомные желудочковые нарушения ритма. Препаратами выбора при этом являются β-адреноблокаторы, а антиаритмические лекарственные средства I и IV классов противопоказаны. В случае неэффективности β-адреноблокаторов следует использовать препараты III класса (амиодарон, соталол, дофетилид). Амиодарон способен снижать риск внезапной смерти у больных с декомпенсированной ХСН при наличии желудочковых аритмий, в то время как общая смертность достоверно не меняется. Доза препарата при этом должна быть достаточно низкая (около 100-200 мг/сут). У больных с ХСН III-IV ФК применение амиодарона опасно.
Альтернативой амиодарону является соталол. По влиянию на желудочковые аритмии он лишь немного уступает амиодарону. Дозу препарата титруют от 20 мг 2 раза в сутки до 160 мг 2 раза в сутки, увели- чивая ее в два раза каждые 2 недели.
При мерцательной аритмии единственным независимым предиктором лучшей выживаемости больных с ХСН является постоянный прием антикоагулянтов.
Антиагреганты
Вопрос о применении антиагрегантов при ХСН остается до настоящего времени открытым. Считается, что наиболее обоснованным является максимально редкое (только при наличии прямых показаний) назначение минимально эффективных доз препаратов этого класса. Данная позиция обусловлена возможной блокадой синтеза простациклина под влиянием некоторых антиагрегантов (АЦСК) с ослаблением клинического эффекта иАПФ, диуретиков, спиронолактона и даже смешанного адреноблокатора карведилола. Также нет клини- ческих подтверждений большей безопасности применения антиагрегантов с другим механизмом действия (например, клопидогрела) у больных с ХСН.
Негликозидные кардиотоники
Долгосрочное изучение применения негликозидных кардиотоников (блокаторов ФДЭ III типа) показало, что, несмотря на кратковре-
менное улучшение гемодинамики и клинического состояния больных с декомпенсацией ХСН, эти препараты не уменьшают смертности или частоты сердечно-сосудистой госпитализации, не повышают толерантности к физической нагрузке и не редуцируют выраженность клинических симптомов сердечной недостаточности. Более того, некоторые из препаратов данной группы способны повышать риск смерти больных с ХСН. Поэтому в настоящее время они не могут быть рекомендованы для длительного лечения декомпенсации заболевания. Более подробно данные средства рассматриваются в подразделе, посвященном лечению острой сердечной недостаточности.
Основные рекомендации по выбору препаратов для лечения хронической сердечной недостаточности
Обобщение результатов клинических наблюдений, в том числе многоцентровых, несмотря на наличие некоторых разногласий, поз- воляет дать следующие рекомендации по лекарственной терапии ХСН
(табл. 3.10).
3.4. ФАРМАКОТЕРАПИЯ ОСТРОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ
Острая сердечная недостаточность (ОСН) наиболее часто является следствием декомпенсации ХСН, хотя может развиться и у больных без предшествующего заболевания сердца. ОСН характеризуется быстрым возникновением симптомов, характерных для нарушенной функции сердца (сниженный сердечный выброс, недостаточная перфузия и застой в тканях, повышенное давление в капиллярах легких. В этом случае, как правило, диагностируют сердечную астму, отек легких или кардиогенный шок. Выделяют впервые возникшую ОСН у пациентов без предшествующего нарушения функции сердца в анамнезе, а также острую декомпенсацию ХСН. Клинические и гемодинамические признаки различных вариантов ОСН представлены в табл. 3.11.
При любом клиническом варианте ОСН целью неотложного лечения является быстрая стабилизация и улучшение гемодинамики (прежде всего сердечного выброса и ударного объема, давления заклинивания легочной артерии (ДЗЛА), давления в правом предсердии), снижение выраженности симптомов ОСН (в первую очередь выраженности одышки), устранение гипоксемии, восстановление перфузии почек. Общие терапевтические подходы к лечению ОСН (при использовании инвазивного мониторирования) представлены в табл. 3.12.
Таблица 3.10. Основные рекомендации по выбору препаратов для лечения хронической сердечной недостаточности
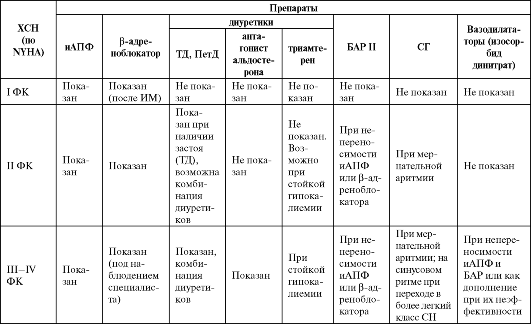
Окончание табл. 3.10
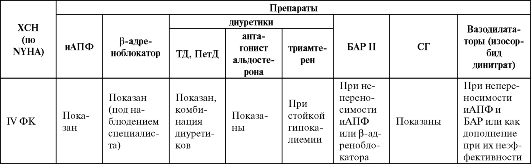
Таблица 3.11. Клинические и гемодинамические признаки при различных вариантах острой сердечной недостаточности (The task force on acute heart failure of the European Society of cardiology, 2006; Российские рекомендации по диагностике и лечению ОСН, 2006)

Окончание таблицы 3.11
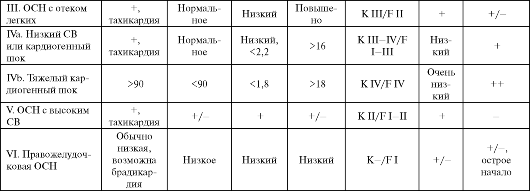
Таблица 3.12. Общие терапевтические подходы к лечению острой сердечной недостаточности (при использовании инвазивного мониторирования) (The task force on acute heart failure of the European Society of cardiology, 2006; Российские рекомендации по диагностике и лечению ОСН, 2006)
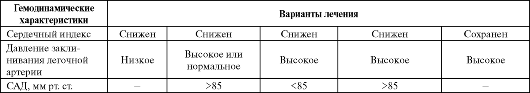
Окончание табл. 3.12

Примечание: при ОСН снижение сердечного индекса - менее 2,2 л/мин на м2, низкое ДЗЛА - менее
Лечение ОСН следует начинать с ликвидации гипоксемии с помощью оксигенотерапии (через маску, носовой катетер или под постоянным положительным давлением) до достижения целевого насыщения артериальной крови кислородом 95-98%. Целесообразность применения оксигенотерапии у пациентов без гипоксемии сомнительна, а иногда и опасна.
Фармакотерапию при ОСН следует проводить с учетом фармакодинамики и фармакокинетики каждого применяющегося препарата и при тщательной оценке возможных терапевтических и токсических взаимодействий применяемых лекарственных средств.
Опиоидные анальгетики
Начальным этапом медикаментозного лечения тяжелой ОСН является введение опиоидных анальгетиков, в частности, морфина, для подавления боли, возбуждения, одышки (вследствие избыточной активации дыхательного центра). При введении препарата уменьшается одышка, снимаются боль, тревога и беспокойство. Кроме того, возникает дилатация вен, что приводит к снижению венозного возврата. Несколько снижается ЧСС. Препарат обычно вводится внутривенно медленно (0,3-0,5 мл 1% раствора - 3-5 мг), хотя возможно внутримышечное и подкожное введение. При отсутствии выраженного угнетения дыхания введение морфина можно повторить через 15-30 мин.
Следует избегать чрезмерно высоких доз препарата, способных вызвать гипотензию, выраженное угнетение дыхания, рвоту.
Риск развития побочных эффектов выше у пожилых и ослабленных больных. Противопоказан морфин при бронхиальной астме, хроническом легочном сердце и отеке легких, сочетающемся с геморрагическим инсультом.
Вазодилататоры
Для уменьшения пред- и постнагрузки используются вазодилататоры (табл. 3.13), которые являются средствами выбора при отсутствии артериальной гипотензии и наличии признаков гипоперфузии, веноз- ного застоя в легких и снижения диуреза. Препараты данной группы способны быстро уменьшить пред- и постнагрузку за счет расширения вен и артериол, что приводит к снижению давления в капиллярах легких, снижению ДЗЛА, периферического сосудистого сопротивления и АД, увеличению сердечного индекса.
Таблица 3.13. Показания к назначению вазодилататоров при острой сердечной недостаточности
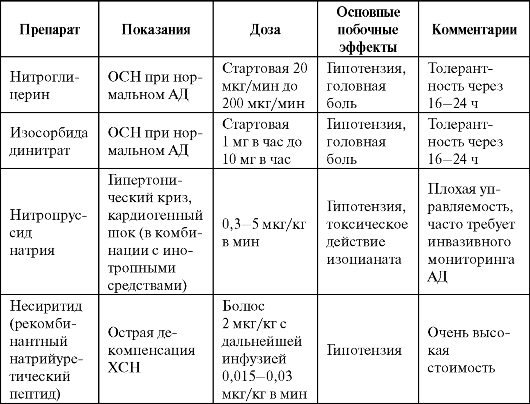
Перед назначением вазодилататоров необходимо обеспечить достаточное давление заполнения желудочков, устранив гиповолемию. Их нельзя использовать при артериальной гипотензии.
Дозы препаратов подбираются с таким расчетом, чтобы обеспечить оптимальную вазодилатацию. Использование неадекватно низких или чрезмерно высоких доз вазодилататоров приводит к снижению их эффективности, развитию толерантности, а чрезмерное расширение сосудов сопровождается снижением АД и нестабильностью гемодинамики.
Применение нитратов можно начать с перорального назначения (особенно на догоспитальном этапе), в виде аэрозоля (нитроглицерин по 400 мкг (2 впрыска) каждые 5-10 мин) или суббуккально (изосорбида динитрат по 1-3 мг) под контролем АД.
Внутривенное введение нитроглицерина (10-20 мг в 100-200 мл 5% раствора глюкозы (20 мкг/мин с увеличением дозы до 200 мкг/мин или изосорбида динитрат 1-10 мг/ч) необходимо проводить, осторож-
но титруя дозу, под тщательным контролем АД. Оптимальным является снижение АД на
При их использовании следует избегать артериальной гипотензии (ее вероятность повышена при гиповолемии, нижней локализации инфаркта миокарда, правожелудочковой недостаточности). Если АДс снизится до 90-100 мм рт. ст., дозу вводимого нитроглицерина следует уменьшить, а в случае дальнейшего снижения АД полностью прекратить введение препарата.
Гипотензия,
возникшая при использовании нитратов, обычно устраняется внутривенным
введением жидкости, сочетание брадикардии и гипотензии - атропином.
Нитраты могут также способствовать возникновению или усугублению
тахикардии, брадикардии, нарушению вентиляционно-перфузионных отношений
в легких и головной боли. Они считаются противопоказанными при
выраженной сократительной дисфункции правого желудочка, когда его
выброс зависит от преднагрузки, при систолическом АД ниже
Смешанный вазодилататор нитропруссид натрия готовят непосредственно перед применением. Сначала разводят содержимое одной ампулы (25 или 50 мг) в 5 мл 5% раствора глюкозы, а затем разводят дополнительно в 250 мл 5% раствора глюкозы.
Введение необходимо начинать медленно со скоростью 5 капель в 1 мин (вводится 0,3 мкг/кг в мин), затем скорость увеличивают, но не более, чем на 10 капель каждые 15 минут (титруют до 1-5 мкг/кг в мин). Дозу препарата титруют очень осторожно, под тщательным контролем, для чего нередко требуется инвазивное мониторирование АД. Эффект препарата развивается очень быстро, начиная с 5 - 7 мин после введения; действие его стабильно на протяжении всей инфузии и прекращается через 20-25 мин после окончания введения. Во избежание развития синдрома отдачи при окончании введения нитропруссида натрия, скорость инфузии уменьшают посте- пенно.
Препарат рекомендуется использовать у больных тяжелой сердечной недостаточностью, а также при преимущественном увеличении постнагрузки (гипертензивная ОСН) или митральной регургитации. Но при развитии ОСН на фоне ОКС предпочтение следует отдавать
нитратам, так как нитропруссид натрия способен вызывать феномен коронарного «обкрадывания».
При гиповолемии нитропруссид натрия, так же как и нитраты, способен вызвать значительное снижение АД с рефлекторной тахикардией, поэтому давление заполнения левого желудочка должно составлять не менее 16-18 мм рт. ст. Другие побочные эффекты включают усугубление гипоксемии при заболеваниях легких (за счет устранения гипоксической констрикции легочных артериол), головную боль, тошноту, рвоту и спазмы в животе.
В случае отсутствия нитропруссида натрия или нитроглицерина при высоких цифрах артериального давления (особенно при нали- чии отека легкого) осторожно может использоваться ганглиоблокатор средней длительности действия пентамин (внутривенно медленно 0,5-1 мл 5% раствора в 20-40 мл изотонического раствора натрия хлорида или 5% раствора глюкозы). Однако следует помнить, что он способен вызвать неуправляемую гипотензию.
Новым подходом к лечению ОСН является использование препарата рекомбинантного мозгового натрийуретического пептида - несиритида (натрекора). Предварительные результаты применения у больных с декомпенсацией ХСН показали более выраженное улучшение показателей гемодинамики и меньшее число побочных эффектов по сравнению с нитроглицерином.
Блокаторы кальциевых каналов
Блокаторы кальциевых каналов не рекомендуется применять при острой сердечной недостаточности.
Диуретики
Диуретики (в первую очередь петлевые) показаны при ОСН с признаками задержки жидкости. Внутривенное введение этих препаратов позволяет добиться вазодилатирующего эффекта, проявляющегося быстрым (через 5-30 мин) снижением давления в правом предсердии и ДЗЛА, а также уменьшением легочного сосудистого сопротивления. При тяжелой декомпенсации СН диуретики способствуют нормализации давления заполнения камер сердца и могут достаточно быстро уменьшить нейрогормональную активность.
Средствами выбора являются мощные петлевые диуретики, лечение которыми можно начинать на догоспитальном этапе. Доза препарата титруется в зависимости от клинического эффекта и уменьшения симптомов задержки жидкости (табл. 3.14).
Таблица 3.14. Особенности применения диуретиков при острой сердечной недостаточности
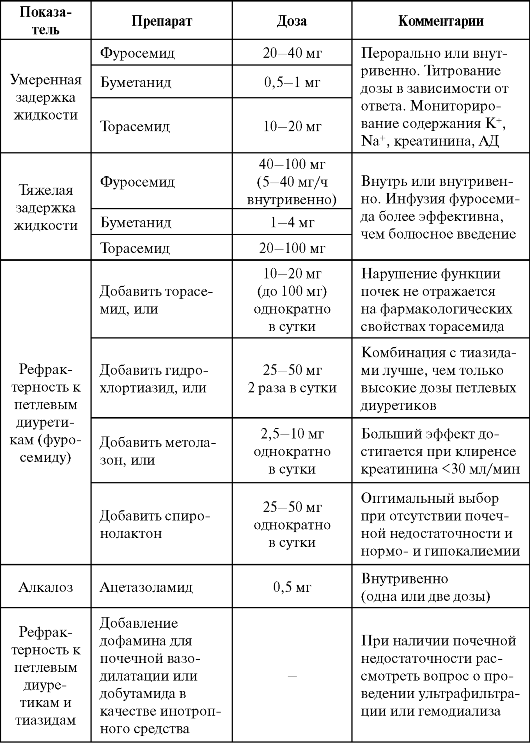
Однократная доза фуросемида при внутривенном введении варьирует в очень широких пределах (от 20 до 140 мг), диуретический эффект наступает через 5 мин, достигает максимума через 30 мин и продолжается в течение 2 ч. Улучшение состояния наблюдается еще до развития диуретического эффекта, что объясняется вазодилатирующим действием препарата. Однако при болюсном введении высоких доз препарата (более 1 мг/кг) существует риск развития рефлекторной вазоконстрикции. Последнее обстоятельство необходимо учитывать особенно у больных с ОКС, когда диуретики желательно использовать в малых дозах, отдавая предпочтение вазодилататорам. В эквивалентных фуросемиду дозах могут использоваться и другие мощные диуретики (буметанид, торасемид). Введение «ударной» дозы фуросемида или торасемида с последующей инфузией более эффективно, чем повторное болюсное введение.
Тиазидные диуретики и спиронолактон могут быть использованы к комбинации с петлевыми диуретиками для потенцирования дейс- твия последних. При этом сочетание низких доз препаратов является более эффективным и сопряжено с меньшим риском возникновения побочных эффектов по сравнению с введением высоких доз одного диуретика. Комбинация петлевых диуретиков с добутамином, дофамином или нитратами также более эффективна и безопасна, чем монотерапия диуретиком в более высоких дозах.
Сочетанное применение низкой дозы фуросемида с постепенным увеличением дозы нитроглицерина до максимально переносимой эф- фективнее устраняет симптомы отека легких, чем введение высоких доз диуретика.
Наиболее тяжелыми побочными эффектами при терапии ОСН диуретиками являются нейрогормональная активация, гипокалиемия, гипомагниемия и гипохлоремический алкалоз, приводящие к аритмиям и нарастанию почечной недостаточности. Кроме того, избыточный диурез может чрезмерно снижать венозное давление, ДЗЛА, диастолическое наполнение желудочков сердца с последующим уменьшением сердечного выброса, особенно у больных тяжелой СН, преимущественно диастолической недостаточностью или дисфункцией правого желудочка.
β-адреноблокаторы
На сегодняшний день нет полностью сформированной стратегии по применению β-адреноблокаторов при ОСН с целью достижения быстрого клинического улучшения. Наличие ОСН считается проти- вопоказанием к назначению препаратов этой группы.
Показаниями могут служить сохраняющаяся артериальная гипертензия, а также ишемия миокарда, тахикардия или аритмия у больных без артериальной гипотензии, признаков периферической гипоперфузии и стандартных противопоказаний к применению β-адреноблокаторов. Тем не менее внутривенное введение β-адреноблокаторов больным с явной ОСН и застойными хрипами в легких следует применять крайне осторожно, избегая быстрого увеличения доз. Предпочтение следует отдавать короткодействующим препаратам (эсмолол, метопролола тартрат).
В отдельных случаях, когда отек легких возникает у больного с субаортальным или изолированным митральным стенозом и связан с возникновением тахисистолии, часто в сочетании с повышенным АД введение β-адреноблокатора способствует купированию симптомов заболевания.
Плазмозаменители
Плазмозаменители
показаны больным в состоянии кардиогенного шока при снижении ЦВД менее
100-120 мм вод. ст. Предпочтительнее использовать низкомолекулярный
декстран (например, реополиглюкин) по 150-200 мл в течение 10 мин под
контролем диастолического давления в легочной артерии (необходимо
поддерживать на уровне
Препараты с положительным инотропным действием
Препараты с положительным инотропным действием показаны при периферической гипоперфузии (артериальная гипотензия, ухуд- шение функции почек), устойчивой к введению жидкости, диуретиков и вазодилататоров в оптимальных дозах, вне зависимости от наличия застоя крови в легких.
Классификация препаратов с положительным инотропным действием (Varro A., Papp J., 1995, с изменениями)
I класс - препараты, положительный инотропный эффект которых связан с увеличением кальциевого тока и повышением содержа- ния цАМФ в кардиомиоцитах:
IA - смешанные (дофамин, допексамин) и β1-адреномиметики (добутамин);
IB - ингибиторы фосфодиэстеразы (ФДЭ) (амринон, милринон, эноксимон);
IC - прямые активаторы аденилатциклазы (форсколин); ID - активаторы кальциевых каналов L-типа (BAY-K 8644).
II класс - препараты, положительный инотропный эффект которых опосредуется через повышение уровня натрия в кардиомиоцитах:
IIА - блокаторы натрий-калиевой АТФ-азы (сердечные гликозиды);
IIВ - активаторы потенциалзависимых натриевых каналов (препараты этой группы клинически не используются в связи с высокой общей токсичностью).
III класс - препараты, усиливающие чувствительность миофиламентов к кальцию (сенситизаторы кальция) (левосимендан, пимобендан, сульфамазол, адибендан).
IV класс - препараты с поливалентным механизмом действия. Они удлиняют реполяризацию и ингибируют ФДЭ (алмокалант, веснаринон, дофетилид).
Препараты данных классов оказывают выраженное положительное инотропное действие и у больных с критической декомпенсацией гемодинамики являются жизнеспасающими средствами (табл. 3.15).
В то же время ряд инотропных препаратов вызывает большое количество опасных побочных эффектов (выраженная тахикардия, наджелудочковые и желудочковые аритмии, ишемия миокарда), что ограничивает их применение. Чтобы уменьшить вероятность аритмогенного эффекта, необходимо поддерживать нормальное содержание в крови К+ (более 4 ммоль/л) и Mg2+ (более 1 ммоль/л).
Дофамин - смешанный адреномиметик с дозозависимым эффектом. В низких дозах (0,5-2 мкг/кг в мин) он активирует дофаминовые DA1-рецепторы, вызывая расширение почечных, мезентериальных, коронарных и мозговых сосудов. В результате расширения почечных сосудов улучшается почечный кровоток и, следовательно, фильтрация и диурез. В дозе 2-3 мкг/кг в мин происходит дополнительная активация β1-адренорецепторов в сердце, что приводит к увеличению силы сердечных сокращений, сердечного выброса и к уменьшению явлений сердечной недостаточности. В дозе 7-10 мкг/кг в мин активируются постсинаптические α1- и пресинаптические β2-адренорецепторы, что приводит к повышению АД и увеличению ЧСС.
Начинают инфузию препарата с дозы 0,5-1 мкг/кг в мин, затем добавляют по 2 мкг/кг в мин каждые 10-30 мин до достижения необходимого клинического и гемодинамического эффектов. Обычно для инотропной поддержки при ОСН, сопровождающейся гипотензией, требуются дозы более 2 мкг/кг в мин. Введение низких доз
Таблица 3.15. Применение при острой сердечной недостаточности препаратов с положительным инотропным действием
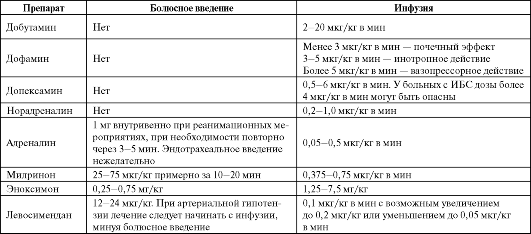
(менее 2-3 мкг/кг в мин) способно улучшить почечный кровоток и усилить диурез при острой декомпенсации ХСН с артериальной гипотензией и олигурией.
Добутамин - синтетический адреномиметик, оказывающий преимущественное действие на β1-адренорецепторы, а также стимулирующий β2- и α1-адренорецепторы. При ОСН добутамин улучшает сократимость миокарда, увеличивает ударный объем и сердечный выброс, системное давление и перфузионный кровоток. Одной из особен- ностей действия препарата является преобладание положительного инотропного эффекта над положительным хронотропным эффектом.
Обычно препарат назначают по 2-3 мкг/кг в мин, увеличивая дозу на 2-3 мкг/кг в мин каждые 10-30 мин до достижения клинического эффекта или до появления нежелательных реакций. Оптимальная поддерживающая доза препарата в первые 72 часа инфузии - 7,5- 15 мкг/кг в мин (иногда до 20 мкг/кг в мин).
Гемодинамические эффекты развиваются уже через 1-2 мин после начала инфузии, хорошо коррелируют с дозой препарата и его концентрацией в плазме. Препарат быстро метаболизируется и выводится из организма через 10-12 мин после окончания инфузии. Длительная инфузия добутамина (более 24-48 ч) приводит к развитию толерантности и частичной потере гемодинамического эффекта.
В случае введения добутамина на фоне β-адреноблокатора для сохранения положительного инотропного эффекта дозу добутамина можно увеличить до 15-20 мкг/кг в мин. Использование препарата (в достаточно высоких дозах - 5-20 мкг/кг в мин) вместе с карведилолом дает возможность повысить сопротивление легочных сосудов. Совместное применение добутамина и ингибитора ФДЭ дает взаимное потенцирование положительного инотропного эффекта.
Снижать дозу препарата следует медленно (например, на 2 мкг/кг в мин каждые сутки) при одновременном острожном назначении вазодилататоров (гидралазин и/или иАПФ).
Допексамин - новый синтетический смешанный адреномиметик, имеющий структурное сходство как с дофамином, так и с добутами- ном. Он оказывает действие на дофаминовые DA1-рецепторы и β-ад- ренорецепторы (главным образом на β2). Аффинитет допексамина по отношению к β2-адренорецепторам в 9,8 раза превосходит этот показатель по отношению к β1-адренорецепторам.
В норме в левом желудочке β1-адренорецепторы преобладают над β2-адренорецепторами в соотношении примерно 4:1. Однако при ХСН это соотношение меняется и количество β1- и β2-адренорецепторов
становится одинаковым. В этом случае селективная стимуляция β2- адренорецепторов может сопровождаться положительным инотропным эффектом. Помимо этого, допексамин оказывает угнетающее действие на механизмы реаптейка катехоламинов, чем также отчасти обусловлено положительное инотропное действие этого препарата.
Стимуляция β2-адренорецепторов в периферических сосудах приводит к расширению сосудов, снижению ОПСС и постнагрузки.
Активация DA1-рецепторов почечных сосудов приводит к увеличению почечного кровотока и соответствующему повышению фильтрации и диуреза. Сравнительная характеристика допексамина и дофамина представлена в табл. 3.16.
Таблица 3.16. Сравнительная характеристика допексамина и дофамина

Примечание: «-» - не действует; «?» - почти не действует; «+» - слабо действует; «++» - действует умеренно; «+++» - выраженное действие.
Максимально выраженное действие допексамина проявляется при его назначении методом постоянной инфузии (от 3 до 24 ч) со скоростью 0,5-6 мкг/кг в мин. Однако повышение ЧСС и повышение потребления кислорода в миокарде (при дозах больше 4 мкг/кг в мин) ограничивают использование этого препарата при ИБС.
Побочные эффекты наблюдаются в 2-5% случаев, в основном при длительной (более 72 ч) инфузии в больших дозах: тошнота, дрожь в теле, тахикардия, боли в грудной клетке (в 2,1% случаев), аритмии (1,5-2,3% случаев). Они быстро проходят при уменьшении дозы препарата или прекращении инфузии.
Смешанные адреномиметики (адреналин, норадреналин) могут быть использованы в том случае, если, несмотря на увеличение сердечного выброса в результате инотропной поддержки и введения жидкости, не удается добиться достаточной перфузии органов. Кроме того, эти препараты могут использоваться во время реанимационных мероприятий, а также для поддержания перфузии при угрожающей жизни гипотензии.
Выбор между адреналином и норадреналином определяется клинической ситуацией. Для более выраженного влияния на гемодинамику адреналин часто комбинируют с добутамином. Сравнительная характеристика адреналина и норадреналина приведена в табл. 3.17.
Таблица 3.17. Реакции на внутривенную инфузию адреналина и норадреналина (Hoffman B. В., 2003)
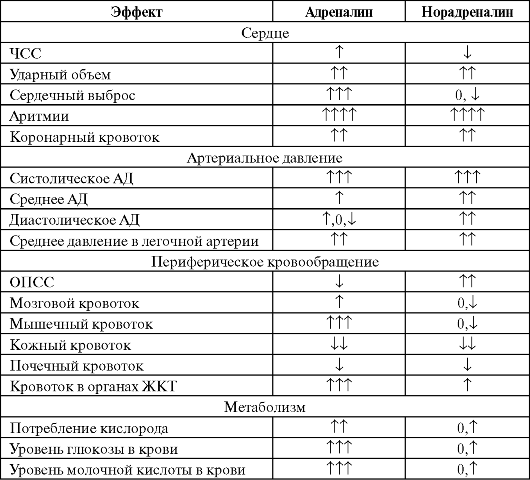
Данные
препараты могут быть использованы во время реанимационных мероприятий,
а также для поддержания перфузии при угро- жающей жизни гипотензии (АД
менее
руется до достижения эффекта и при рефрактерном шоке может составить 8-30 мкг/кг в мин. Допускается комбинированное назначение норадреналина и добутамина с целью достижения более выраженного влияния на гемодинамику.
Применение адреналина и норадреналина необходимо проводить с осторожностью, в течение короткого времени (поскольку дополнительное увеличение ОПСС приводит к еще большему снижению сердечного выброса и нарушению перфузии тканей), желательно в условиях инвазивного мониторирования с определением сердечного выброса и ДЗЛА.
Ингибиторы фосфодиэстеразы III (ФДЭ-III) в настоящее время используются достаточно редко и только при отсутствии артериальной гипотензии. Применение амринона в связи с его способностью повышать летальность у больных с ОСН прекращено. Препараты этой группы, по-видимому, могут быть предпочтительнее добутамина у пациентов, получающих β-адреноблокаторы, и/или при неадекватном ответе на добутамин или другие прессорные амины (см. табл. 3.16).
Вследствие выраженной периферической вазодилатации на фоне применения ингибиторов ФДЭ-III может развиться артериальная гипотензия (особенно у больных с низким давлением наполнения желудочков). Ее можно избежать, отказавшись от первоначального болюсного введения препарата и устранив гиповолемию.
Большие надежды возлагаются на препарат из группы негликозидных кардиотоников - сенситизаторов кальция - левосимендан (пиридазинол динитрил). Он связывается с тропонином С и повышает реакцию миофибрилл на кальций, меняя физиологическую реакцию взаимодействия тропонин С - тропонин J, стабилизирует вызванные кальцием изменения конформации тропонина С, необходимые для активации сократительных белков. Левосимендан усиливает силу сердечных сокращений, одновременно нормализуя диастолическую функцию без изменений концентрации внутриклеточного кальция.
Дополнительно препарат может ингибировать ФДЭ, увеличивая содержание цАМФ, способствовать открытию АТФ-зависимых кали- евых каналов в гладких мышцах сосудов.
При введении левосимендана развивается не только положительный инотропный эффект, но и вазодилатация, связанная с расширением как артериол, так и венул. В отличие от традиционных инотропных препаратов, гемодинамический эффект левосимендана проявляется при одновременном назначении на фоне β-адреноблокаторов.
Левосимендан показан
при ОСН с низким сердечным выбросом у пациентов с систолической
дисфункцией левого желудочка (низкой фракцией выброса) при отсутствии
тяжелой артериальной гипотензии (АДс менее
Побочные эффекты проявляются снижением содержания гемоглобина, показателя гематокрита и К+ в крови.
Сердечные гликозиды
В том случае, если при ОСН снижение артериального давления сопровождается тахисистолической формой мерцательной аритмии, могут применяться сердечные гликозиды. Они незначительно повышают сердечный выброс и снижают давление наполнения камер сердца. Строфантин в дозе 0,5-0,75 мл 0,05% раствора вводят внутривенно струйно (но не менее чем за 3 мин) или капельно (в течение 10- 15 мин). Коргликон применяется внутривенно медленно в дозе 0,75- 1,0 мл 0,06% раствора. Не рекомендуется применение сердечных гликозидов у больных с ОСН на фоне ИМ вследствие возможного ухуд- шения прогноза.
В заключение следует отметить, что, хотя выраженность симптомов ОСН под влиянием интенсивной терапии может быстро уменьшаться, в целом прогноз неблагоприятен, и впоследствии пациентам требуется продолжительное лечение.
ЛИТЕРАТУРА
Арутюнов Г. П. АРА в лечении ХСН до 2003 года. Их преимущества и недостатки по сравнению с традиционными методами терапии / Г. П. Арутюнов // Сердечная недостаточность. - 2004. - Т. 5, ? 2. - С. 72-73.
Белоусов Ю. Б. Клиническая фармакокинетика. Практика дозирования ле- карств / Ю. Б. Белоусов, К. Г. Гуревич. - М.: Литтера, 2005. - 288 с.
Белоусов Ю. Б. Клиническая фармакология и фармакотерапия. - 2-е изд., стереотип. / Ю. Б. Белоусов, В. С. Моисеев, В. К. Лепахин. - М.: Универсум паблишинг, 2000. - 539 с.
Гендлин Г. Е. Лечение хронической сердечной недостаточности диуретиками / Г. Е. Гендлин // Сердечная недостаточность. - 2005. - Т. 6, ? 3. - С. 142.
Диагностика и лечение острой сердечной недостаточности. Российские рекомендации. - М., 2006. - 26 с.
Мареев В. Ю. Аспирин при хронической сердечной недостаточности. Взаимодействие с основными средствами лечения декомпенсации / В. Ю. Мареев // Сердечная недостаточность. - 2003. - Т. 4, ? 3. - С. 153-157.
Мареев В. Ю. Дилатренд в лечении сердечной недостаточности: только β- блокатор или новый класс нейрогормональных модуляторов? / В. Ю. Мареев // Сердечная недостаточность. - 2004. - Т. 5, ? 2. - С. 60-62.
Национальные рекомендации ВНОК и ОССН по диагностике и лечению ХСН (второй пересмотр). - М., 2006. - 35 с.
Обрезан А. Г. Хроническая сердечная недостаточность / А. Г. Обрезан, И. В. Вологдина. - СПб.: Вита Нова, 2002. - 320 с.
Преображенский Д. В. Ингибиторы АПФ и АТ1-блокаторы в клинической практике / Д. В. Преображенский, Б. А. Сидоренко, Т. А. Батыралиев. - М.:
Альянс-ПРЕСИД, 2002. - 224 с.
Преображенский Д. В. Диагностика и лечение хронической сердечной недо- статочности / Д. В. Преображенский, Б. А. Сидоренко. - М.: Миклош, 2004. -
352 с.
Сидоренко Б. А. Лекарственные средства, применяемые при лечении хрони- ческой сердечной недостаточности (часть первая) / Б. А. Сидоренко, Д. В. Пре- ображенский // Кардиология. - 1995. - ? 1. - С. 79-92.
Сидоренко Б. А. Лекарственные средства, применяемые при лечении хрони- ческой сердечной недостаточности (часть вторая) / Б. А. Сидоренко, Д. В. Пре- ображенский // Кардиология. - 1995. - ? 2. - С. 81-93.
Сидоренко Б. А. Карведилол и другие бета-адреноблокаторы в лечении хронической сердечной недостаточности / Б. А. Сидоренко, Д. В. Преображенский И. В. Ревунова // Кардиология. - 1998. - ? 1. - С. 66-71.
Сидоренко Б. А. Блокаторы АТ^ангиотензиновых рецепторов / Б. А. Сидоренко, Д. В. Преображенский.- М.: Информатик, 2001. - 200 с.
Терапевтический справочник Вашингтонского университета / под ред. М. Вудли, А. Уэлан. - М.: Практика, 1995. - 831 с.
CIBIS-II Investigators and Committees. Cardiac Insufficiency Bisoprolol Study (CIBIS-II): a randomised trial // Lancet. - 1999. - Vol. 353. - P. 9-13.
Doughty R. N. Effects ofbeta-blocker therapy on mortality in patients with heart failure / R. N. Doughty, A. Rodgers, N. Sharpe, S. MacMahon // Europ. Heart J. - 1997. - Vol. 18, ? 4. - P. 560-565.
Garg R. For the collaborative Group on ACE Inhibitor Trials. Overview of randomized trials of angiotensin-converting enzyme inhibitors on mortality and morbidity in patients with heart failure / R. Garg, S. Yusuf // JAMA. - 1995. - Vol. 273. - P. 1450-1456.
Gheorghiade M. Review of randomized trials of digoxin therapy in patients with chronic heart failure / M. Gheorghiade, B. Zarowitz // Amer. J. Cardiol. - 1992. - Vol. 69. - P. 48G-63G.
Goodman, Gilman's. The pharmacological basis of therapeutics / Ed. J. G. Hardman et al. Ninth edition. - New York et al.: McGraw-Hill, 1998. - 1905 p.
Katzung B. G. Basic & clinical pharmacology. - Eighth edition / B. G. Katzung. - New York et al.: McGraw-Hill, 2001. - 1217 p.
Konstam M. A. Efficacy of vasopressin antagonism in heart failure outcome study with tolvaptan (EVEREST) investigators. Effects of oral tolvaptan in patients hospitalized for worsening heart failure. The EVEREST outcome trial / M. A. Konstam, M. Gheorghiade, J. C. Burnett et al. // JAMA. - 2007. - Vol. 297. - P. 1319-1331.
MERIT-HF Study Group. Effect ofmetoprolol CR/XL in chronic heart failure: Metoprolol CR/XL Randomised Intervention Trial in Congestive Heart Failure (MERIT-HF) // Lancet. - 1999. - Vol. 353. - P. 2001-2007.
O'Callaghan Р. А. Treatment of arrhythmias in heart failure / Р. А. O'Callaghan, A. J. Camm // Europ. J. Heart Failure. - 1999. - Vol. 1, ? 2. - P. 133-137.
Packer M. Comparative effects of low-dose versus high-dose lisinopril on survival and major events in chronic heart failure: the Assessement of Treatment with Lisinopril And Survival (ATLAS) / M. Packer, P. Poole-Wilson, P. Armstrong et al. // Europ. Heart J. - 1998. - Vol. 19 (suppl.). - P. 142 (abstract).
Packer M. Consensus
recommendations for the management of chronic heart failure / M.
Packer, J. N. Cohn (eds) // Amer. J. Cardiol. - 1999. - Vol.
Remme W. J. Carvedilol protects better against vascular events than metoprolol in heart failure. Results from COMET / W. J. Remme, C. Torp-Pedersen, J. G. F. Cleland
et al. // J. Am. Coll. Cardiol. - 2007. - Vol. 49. - P. 963-971.
Richardson M. Update of recent clinical trials in heart failure and myocardial infarction / M. Richardson, N. Cockburn, J. G. F. Cleland // Europ. J. Heart Failure. - 1999. - Vol. 1, ? 1. - P. 109-115.
The Digitalis Investigation Group. The effect of digoxin on mortality and morbidity in patients with heat failure // New Engl. J. Med. - 1997. - Vol. 336. - P. 525-533.
Young J. B. Superiority of «triple» drug therapy in heart failure: Insight from the PROVED и RADIANCE / J. B. Young, M. Gheorghiade, B. F. Uretsky et al. // JACC. - 1998. - Vol. 32. - P. 686-692.