Клиническая фармакология и фармакотерапия в реальной врачебной практике : мастер-класс : учебник / В. И. Петров. - 2011. - 880 с. : ил.
|
|
|
|
Глава 2. КЛИНИКО-ФАРМАКОЛОГИЧЕСКИЕ ПОДХОДЫ К ВЫБОРУ И ПРИМЕНЕНИЮ САХАРОСНИЖАЮЩИХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Открытие инсулина - одно из величайших достижений XX века. В 1921 г. Фредерик Г. Бантинг и Чарльз Г. Бест, работая в лаборатории Джона Р. Маклеода в университете Торонто, выделили из поджелудочной железы экстракт (как позже выяснилось, содержащий аморфный инсулин), который снижал уровень глюкозы в крови у собак с экспериментальным сахарным диабетом. В 1922 г. экстракт поджелудочной железы ввели первому пациенту - 14-летнему Леонарду Томпсону, больному диабетом, и тем самым спасли ему жизнь. Препарат стали успешно применять у других больных, страдающих сахарным диабетом. В 1923 г. Бантинг и Маклеод за открытие инсулина были удостоены Нобелевской премии по физиологии и медицине.
На протяжении почти шестидесяти лет для лечения больных сахарным диабетом использовали говяжий и свиной инсулин, отличающиеся аминокислотным составом от человеческого (табл. 159).
Таблица 159. Различия аминокислотных последовательностей у некоторых млекопитающих
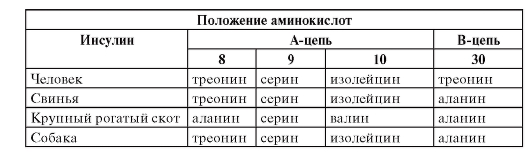
Бычий инсулин отличают от человеческого 3 аминокислотных остатка, вследствие этого он значительно чаще вызывает аллергические реакции, поэтому на сегодняшний день его не применяют.
Свиной инсулин отличает от человеческого одна аминокислота, он реже становится причиной возникновения побочных эффектов, тем не менее от него тоже отказались.
В начале 70-х годов прошлого века национальный консультативный совет по диабету выразил озабоченность по поводу того, что продукции пищевой промышленности США и Европы не может хватить для удовлетворения потребностей в инсулине растущего числа больных сахарным диабетом. Чтобы обеспечить животным инсулином в течение года одного больного сахарным диабетом, необходимо вырастить и забить 14 коров или 70 свиней. Стало ясно, что единственный прогрессивный путь - это синтез человеческого инсулина. Но только в начале 80-х годов было налажено его промышленное производство. В настоящее время только генно-инженерный человеческий инсулин является лекарственным средством выбора для проведения инсулинотерапии.
Инсулины классифицируют по происхождению (человеческий, свиной и бычий инсулины, а также аналоги человеческого инсулина) и продолжительности действия.
КЛАССИФИКАЦИЯ ИНСУЛИНОВ
• Инсулины ультракороткого действия:
- инсулин аспарт;
- инсулин глулизин;
- инсулин лизпро.
• Инсулины короткого действия:
- инсулин растворимый человеческий генно-инженерный;
- инсулин растворимый человеческий полусинтетический;
- инсулин растворимый свиной.
• Инсулины средней продолжительности действия:
- инсулина-цинк (свиного) комбинированного суспензия;
- инсулина-цинк (человеческого генно-инженерного) комбинированного суспензия;
- инсулина-цинк (человеческого полусинтетического) комбинированного суспензия;
- инсулин-изофан свиной;
- инсулин-изофан человеческий полусинтетический;
- инсулин-изофан человеческий генно-инженерный.
• Инсулины длительного действия:
- инсулин гларгин;.
- инсулин детемир;
- инсулина-цинк (человеческого генно-инженерного) кристаллического суспензия;
- комбинированные (двухфазные) инсулины:
• инсулин растворимый человеческий генно-инженерный/ инсулин-изофан человеческий генно-инженерный;
• инсулин аспарт/инсулин аспарт протамин кристаллический;
• инсулин лизпро/инсулина лизпро-цинк кристаллического суспензия.
Генно-инженерный человеческий инсулин является в настоящий момент лекарственным средством выбора для проведения инсулинотерапии.
МЕХАНИЗМ ДЕЙСТВИЯ И ФАРМАКОЛОГИЧЕСКИЕ
ЭФФЕКТЫ
Прямо или косвенно инсулин воздействует на функции практически всех органов или тканей организма. Однако наиболее важные мишени для его действия - печень, мышечная и жировая ткани.
На метаболизм глюкозы инсулин оказывает следующее влияние: с одной стороны, стимулирует ее поглощение (утилизацию) тканями, а с другой - уменьшает эндогенное образование глюкозы, результатом чего становится снижение уровня гликемии.
На метаболизм жиров инсулин оказывает многокомпонентное воздействие. Во-первых, он угнетает липолиз, что приводит к уменьшению высвобождения свободных жирных кислот в кровоток. Во-вторых, инсулин стимулирует липогенез, т.е. превращение свободных жирных кислот и глицерола в триглицериды внутри адипоцитов.
Инсулин активирует синтез белков и ингибирует в организме процессы протеолиза.
ФАРМАКОКИНЕТИКА
Разрешенные в России препараты инсулина вводятся только парентерально. Как правило, это делается подкожно, хотя ИКД можно при необходимости (в ургентных ситуациях, во время оперативных вмешательств и т.д.) вводить внутримышечно и внутривенно. Именно подкожное введение инсулина используется для постоянной инсули-
нотерапии в клинической практике. Основные фармакокинетические параметры препаратов инсулина представлены в табл. 160.
Таблица 160. Некоторые фармакокинетические параметры инсулинов
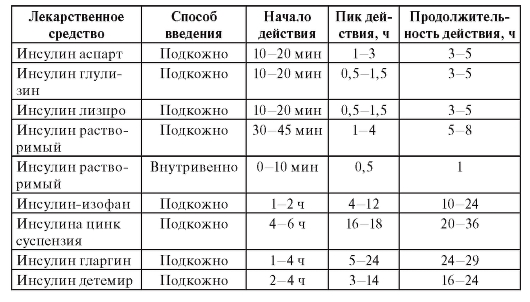
Большая часть поступившего в кровоток инсулина подвергается протеолитическому распаду в печени (около 80%), меньшее количество - в почках, и лишь незначительная часть метаболизируется клетками мышечной и жировой ткани.
МЕСТО В ЛЕЧЕНИИ
В лечении сахарного диабета 1-го типа инсулины играют центральную роль. В настоящее время традиционная инсулинотерапия, основанная на введении ежедневно с помощью минимального количества инъекций одной и той же дозы инсулина, показана лишь лицам пожилого возраста, пациентам, находящимся в тяжелом состоянии и требующим постоянного ухода.
При развитии у пациента кетоацидотической комы (нередкого осложнения сахарного диабета 1-го типа) лечение осуществляется ИКД, вводимыми внутривенно или внутримышечно.
Интенсивная инсулинотерапия в большей степени соответствует физиологической секреции инсулина. При этом базальная потребность в инсулине обеспечивается двумя инъекциями ИСД (утром и вечером),
а пищевая секреция инсулина замещается инъекциями ИКД/инсу- лин ультракороткого действия (ИУД) перед каждым приемом пищи. Следует подчеркнуть, что дозу ИКД/ИУД рассчитывает сам пациент в зависимости от количества углеводов, которые он собирается употребить в пищу, и имеющегося уровня гликемии.
Наиболее часто необходимость применения инсулинов у больных сахарным диабетом 2-го типа возникает тогда, когда с помощью максимальных суточных доз ПССС не удается достичь стойкой удовлетворительной компенсации заболевания.
При проведении хирургических вмешательств, при возникновении острых сердечно-сосудистых нарушений (инфаркт миокарда, инсульт), тяжелых инфекционных заболеваний, гиперосмолярной и лактатацидотической комы или прекомы также следует перевести больного сахарным диабетом 2-го типа на инсулинотерапию. Нередко начать инсулинотерапию вынуждает быстрое прогрессирование поздних осложнений сахарного диабета.
Инсулин - это единственное сахароснижающее средство, которое может использоваться при беременности.
ПЕРЕНОСИМОСТЬ И ПОБОЧНЫЕ ЭФФЕКТЫ
Наиболее частый побочный эффект инсулина - гипогликемия. Как правило, ее развитие связано либо с введением слишком большой дозы, либо происходит в результате незапланированного воздействия различных факторов, уменьшающих потребность организма в инсулине, часто это не спланированная физическая активность.
Другой распространенный побочный эффект препаратов инсулина - увеличение массы тела, однако при соблюдении принципов рационального питания и адекватных физических нагрузок его можно избежать.
С широким распространением генно-инженерных препаратов человеческого инсулина частота аллергических реакций на инсулин значительно сократилась.
К местным реакциям на введение инсулина относятся различные варианты липодистрофии. Для предупреждения развития липодистрофии рекомендуется постоянно менять места инъекций в пределах одной области (живот, бедро или плечо).
Многие больные вскоре после начала инсулинотерапии отмечают нарушение зрения. Это осложнение связано с изменением рефракции
хрусталика и самостоятельно проходит через 2-3 нед, о чем следует предупредить пациентов. В течение первых недель инсулинотерапии нередко возникают также преходящие отеки ног, возникающие в связи с задержкой в организме натрия.
ПРОТИВОПОКАЗАНИЯ
Противопоказание к введению инсулина - гипогликемия у пациента. Кроме того, при наличии аллергии у пациента на данный препарат инсулина или аналог инсулина, необходимо использовать другой препарат инсулина.
ПРЕДОСТЕРЕЖЕНИЯ
В настоящее время инсулин лизпро по риску применения во время беременности относится к классу Б, а опыт применения инсулина аспарт при беременности ограничен, его использование во время беременности продолжает обсуждаться. Возможность применения инсулина глулизин и инсулина гларгин во время беременности находится в процессе изучения.
Инсулин представляет собой единственное средство лечения сахарного диабета в сочетании с тяжелой хронической печеночной и почечной недостаточностью, требуется только индивидуальный подбор дозы в зависимости от характера и активности патологического процесса в печени и почках.
ВЗАИМОДЕЙСТВИЕ
β-Адреноблокаторы подавляют активирующее влияние катехоламинов на гликогенолиз и глюконеогенез и могут способствовать развитию гипогликемии.
Влияние этанола на метаболизм углеводов обусловлено его ингибирующим действием на глюконеогенез в печени. В связи с этим злоупотребление алкогольными напитками на фоне инсулинотерапии чревато высоким риском развития тяжелых гипогликемических состояний.
Целый ряд ЛС вызывает повышение уровня гликемии у здоровых людей и нарушает контроль заболевания у пациентов с сахарным диа-
бетом. Среди них можно выделить препараты контринсулярных гормонов (глюкокортикоиды, эпинефрин), ЛС, ингибирующие секрецию инсулина за счет прямого действия (фенитоин, клонидин, дилтиазем) или за счет снижения концентрации калия (диуретики).
ПЕРОРАЛЬНЫЕ САХАРОСНИЖАЮЩИЕ СРЕДСТВА
В настоящее время арсенал сахароснижающих препаратов, применяемых при лечении сахарного диабета 2-го типа, достаточно большой и продолжает пополняться.
ПССС классифицируют по основному механизму гипогликемического действия. В соответствии с точками приложения действия пероральные сахароснижающие препараты разделяются на три основные группы (рис. 149).
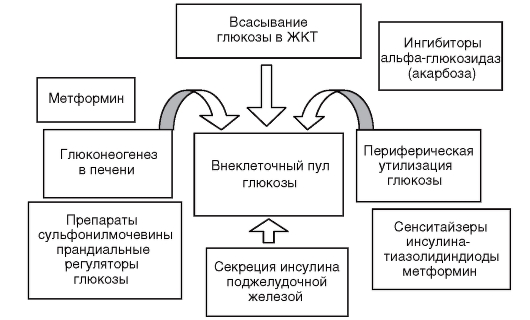
Рис. 149. Точки приложения сахароснижающих препаратов
1. ЛС, повышающие секрецию инсулина (секретагоги). • Производные сульфонилмочевины:
- глибенкламид;
- гликлазид;
- гликвидон;
- глимепирид;
- глипизид;
- хлорпропамид.
• Меглитиниды:
- натеглинид;
- репаглинид.
2. ЛС, преимущественно повышающие чувствительность периферических тканей к инсулину (сенситайзеры).
• Бигуаниды:
- метформин.
• Тиазолидиндионы:
- пиоглитазон;
- росиглитазон.
3. ЛС, нарушающие всасывание углеводов в кишечнике:
- акарбоза;
- миглитол.
1. Средства, повышающие секрецию инсулина
Механизм действия и фармакологические эффекты
Механизм действия ПСМ связан с их влиянием на β-клетки островков поджелудочной железы, поэтому их применение оправдано только у пациентов с функционально сохранными β-клетками.
Результатом активации сульфонилмочевинных рецепторов β-клеток становится высвобождение запасов инсулина из внутриклеточных гранул и его секреция в кровь. Основная часть стимулированного выброса инсулина происходит после приема пищи, когда уровень глюкозы крови закономерно повышается.
Под действием меглитинидов повышается чувствительность β-клеток к стимуляции глюкозой, тем самым увеличивается секреция инсулина в ответ на повышение уровня гликемии. Важная особенность меглитинидов состоит в том, что с их помощью восстанавливается ранняя фаза секреции инсулина, и затем, вследствие короткого периода действия, не развивается гиперинсулинемия.
Фармакокинетические параметры ЛС, повышающих чувствительность периферических тканей к инсулину, приведены в табл. 161.
Место в лечении
ПСМ обладают наиболее выраженным гипогликемическим действием среди всех ПССС: монотерапия ПСМ снижает уровень гликированного гемоглобина (НbА1с) на 1,5-2%.
Таблица 161. Некоторые фармакокинетические параметры лекарственных средств, повышающих чувствительность периферических тканей к инсулину
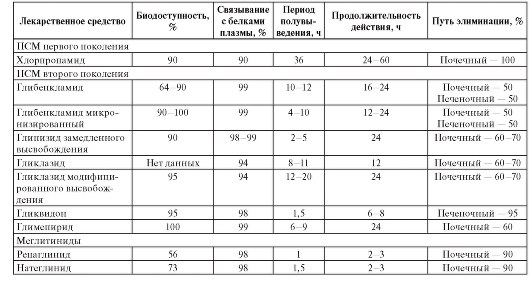
Монотерапия ПСМ показана для компенсации заболевания больным сахарным диабетом 2-го типа с нормальной массой тела. Со временем компенсация заболевания на фоне ПСМ у таких пациентов может утрачиваться из-за развития абсолютной недостаточности инсулина или резистентности к ПСМ.
В качестве комбинированного лечения наиболее часто совместно назначают ПСМ и метформин, как правило, больным с избыточной массой тела, у которых монотерапия метформином не принесла успеха.
По сравнению с ПСМ меглитиниды в большей степени снижают постпрандиальный уровень гликемии, однако в меньшей степени уменьшают уровень гликемии натощак.
Наиболее рациональным выглядит назначение меглитинидов в комбинации с метформином тем больным, у которых монотерапия метформином не позволила добиться удовлетворительной компенсации заболевания, особенно если повышен в первую очередь постпрандиальный уровень гликемии. Меглитиниды могут быть использованы также в качестве монотерапии (эффективность соответствует ПСМ) или в комбинации с тиазолидиндионами.
Переносимость и побочные эффекты
Наиболее частый побочный эффект ЛС описываемой группы (особенно длительно действующих ЛС, таких, как хлорпропамид и глибенкламид) - это гипогликемия.
На фоне приема ПСМ отмечается увеличение массы тела за счет увеличения секреции эндогенного инсулина.
Побочные эффекты со стороны ЖКТ включают тошноту, рвоту, диарею, анорексию и даже холестатическую желтуху, но частота их возникновения довольно низкая. Развитие аллергических реакций на ПСМ также встречается очень редко. Крайне редко ПСМ становятся причиной лейко- и тромбоцитопении, агранулоцитоза, апластической и гемолитической анемии.
Противопоказания
Противопоказания к назначению ЛС, повышающих секрецию инсулина, включают сахарный диабет 1-го типа, беременность, лактацию, печеночную или почечную недостаточность (скорость клубочковой фильтрации <60 мл/мин).
Предостережения
Использование пероральных сахароснижающих препаратов у беременных не рекомендуется, вместо них назначается инсулинотерапия.
Пожилым людям в связи с повышенным риском развития у них гипогликемии лучше использовать короткодействующие ЛС (гликлазид, гликвидон).
Взаимодействие
Большинство ЛС, оказывающих гипогликемическое действие, при совместном приеме с ПСМ способны провоцировать развитие гипогликемических состояний.
2. Средства, повышающие чувствительность периферических тканей к инсулину
Механизм действия и фармакологические эффекты
Метформин, связываясь с фосфолипидами клеточных мембран (возможно, активируя аденозинмонофосфат-протеинкиназу), вызывает целый ряд эффектов, главный из которых - снижение образования глюкозы печенью и увеличение поглощения глюкозы периферическими тканями (прежде всего, скелетными мышцами). В связи с этим действие метформина можно охарактеризовать не как гипогликемическое, а как антигипергликемическое. В итоге под действием метформина происходит уменьшение инсулинорезистентности.
Тиазолидиндионы стимулируют ядерные PPAR-γ, которые регулируют транскрипцию генов, отвечающих за метаболизм углеводов и жиров. Следует отметить, что тиазолидиндионы, по сравнению с метформином, в значительно большей степени снижают инсулинорезистентность тканей, а вот глюконеогенез в печени они подавляют незначительно (табл. 162).
Таблица 162. Некоторые фармакокинетические параметры лекарственных средств, повышающих чувствительность периферических тканей к инсулину
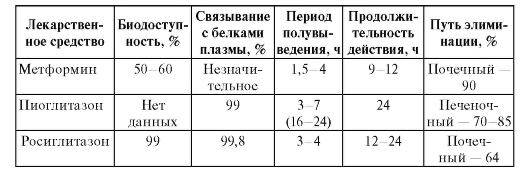
Место в лечении
Метформин является ЛС выбора для начала лечения у больных сахарным диабетом 2-го типа (при условии, что отсутствует нарушение функций почек). Высокая эффективность метформина была неоднократно доказана во многих крупных исследованиях, в том числе в исследовании UKPDS.
Использование тиазолидиндионов наиболее рационально в сочетании с метформином либо в сочетании с ПСМ. Комбинированное воздействие тиазолидиндионы + ИСД (или ИДД) также позволяет улучшить контроль заболевания (уровень НЬА1с может дополнительно снижаться более чем на 1%).
И метформин, и тиазолидиндионы могут успешно сочетаться с ЛС, нарушающими всасывание углеводов в кишечнике (ингибиторами α-глюкозидазы).
Кроме того, у больных сахарным диабетом 2-го типа с ожирением, получающих инсулинотерапию, метформин иногда дополнительно назначается с целью снизить инсулинорезистентность и предотвратить дальнейшее увеличение массы тела пациента.
Переносимость и побочные эффекты
ЛС, повышающие чувствительность тканей к инсулину, не вызывают гипогликемию, в отличие от ПСМ и препаратов инсулина.
В начале лечения метформином около 10-20% пациентов предъявляют жалобы на неприятные ощущения со стороны ЖКТ: снижение аппетита, металлический вкус во рту, тошноту, дискомфорт в эпигастральной области, метеоризм и диарею. Во избежание развития жалоб со стороны ЖКТ, лечение метформином следует начинать с малых доз, а прием ЛС осуществлять вместе с пищей.
Метформин нарушает всасывание витамина В12. Для улучшения всасывания при снижении концентрации витамина В12 в крови следует назначить внутрь препараты кальция. Контроль уровня витамина В12 в крови рекомендуют проводить каждые 2-3 года.
Наиболее грозным побочным эффектом метформина традиционно считается лактат-ацидоз. Это опасное для жизни состояние, вызванное накоплением лактата в организме (возникает при концентрации лактата в плазме крови выше 4 мэкв/л). Развитие лактат-ацидоза при отсутствии каких-либо предрасполагающих факторов возможно лишь при длительной передозировке метформином. На фоне приема метформина рекомендуют определять уровень лактата в крови 2 раза в год, хотя на практике такой частый контроль у большинства пациентов не оправдан.
В первый год приема тиазолидиндионов необходимо регулярно (обычно каждые 2-3 мес) определять уровень АЛТ в сыворотке крови. Если в процессе лечения уровень АЛТ становится в 3 раза выше верхней границы нормы, рекомендуется повторить анализ, и при аналогичном результате прекратить прием ЛС. При появлении желтухи ЛС также отменяются.
В отличие от метформина тиазолидиндионы вызывают увеличение массы тела. Данное явление имеет дозозависимый и времязависимый характер.
Задержка жидкости представляет собой частый побочный эффект тиазолидиндионов. Она, в свою очередь, способствует возникновению не только увеличения массы тела, но и периферических отеков, сердечной недостаточности, а также анемии вследствие гемодилюции.
Противопоказания
Противопоказаниями к использованию всех ЛС, повышающих чувствительность периферических тканей к инсулину, служат сахарный диабет 1-го типа, беременность и лактация.
Помимо этого противопоказаниями к назначению метформина являются все предрасполагающие к развитию лактат-ацидоза факторы: ХПН, сердечная недостаточность, заболевания печени, злоупотребление алкоголем, тяжелые состояния организма, сопровождающиеся гипоксией и (или) ацидозом, оперативное вмешательство, возраст старше 80 лет.
Тиазолидиндионы противопоказаны при III и IV классов NYHA, а также при уровне АЛТ выше верхней границы нормы в 2,5 раза.
Предостережения
Поскольку метформин и, вероятно, тиазолидиндионы за счет снижения инсулинорезистентности способствуют наступлению овуляции у женщин с бесплодием, вызванным синдромом поликистозных яичников, при назначении данных ЛС рекомендуется использовать контрацептивные средства, если женщина не планирует беременность.
Использование пиоглитазона, росиглитазона и метформина в лечении гестационного диабета не рекомендуется. Если женщина принимала эти ЛС до наступления беременности, вместо них следует назначить инсулинотерапию.
Взаимодействие
Несмотря на то что сам метформин не вызывает гипогликемию, при совместном использовании его с ПСМ и инсулином риск гипогликемии возрастает.
Циметидин® конкурентно ингибирует секрецию метформина в канальцах почек, следовательно, при комбинированном применении с ПСМ или инсулином риск гипогликемии возрастает еще больше.
Для предотвращения развития лактат-ацидоза следует отменить метформин за 48 ч до ангиографии и возобновить прием только через 48 ч после окончания процедуры. Это связано с риском развития острой почечной недостаточности на фоне введения рентгеноконтрастных препаратов.
В настоящее время в литературе отсутствуют достоверные данные о взаимодействии пиоглитазона и росиглитазона с другими ЛС.
3. Средства, нарушающие всасывание углеводов в кишечнике
Механизм действия и фармакологические эффекты
Под действием ингибиторов α-глюкозидаз замедляются процессы ферментирования сложных углеводов, и, как следствие, уменьшается скорость всасывания продуктов ферментирования (моносахаридов). Следовательно, не происходит резкого подъема уровня гликемии после еды. На процесс всасывания простых углеводов (глюкоза, фруктоза) ни акарбоза, ни миглитол® не оказывают влияния, поэтому антигипергликемическое действие ингибиторов α-глюкозидаз проявляется лишь при преимущественном употреблении в пищу сложных углеводов (продуктов, содержащих крахмал; декстринов; дисахаридов).
Фармакокинетика
Ингибиторы α-глюкозидаз действуют непосредственно в тонкой кишке. Только 2% поглощенной дозы акарбозы всасывается и попадает в системный кровоток, а основная часть акарбозы в итоге расщепляется населяющими тонкую кишку микроорганизмами. Миглитол®, напротив, полностью всасывается в проксимальной части тонкой кишки.
Т1/2 миглитола® и акарбозы из плазмы крови составляет около 2 ч, элиминация осуществляется почками.
Место в лечении
ЛС, нарушающие всасывание углеводов в кишечнике, применяются для лечения сахарного диабета 2-го типа в основном в комбинации с другими ПССС. При этом используется способность ингибиторов
α-глюкозидаз эффективно снижать постпрандиальный уровень гликемии, а коррекция уровня гликемии натощак обычно достигается с помощью ПСМ или метформина. На фоне приема ингибиторов α-глюкозидаз фармакокинетика ПСМ и метформина не изменяется. Ингибиторы α-глюкозидаз можно комбинировать и с инсулинотерапией.
Переносимость и побочные эффекты
У пациентов часто возникают метеоризм и диарея. Выраженность побочных эффектов можно уменьшить, если начинать лечение с небольших доз и увеличивать дозу постепенно. ЛС необходимо принимать не разжевывая, с небольшим количеством жидкости, непосредственно перед или во время еды.
У пациентов, принимающих акарбозу, особенно в высоких дозах, иногда выявляется повышение активности АЛТ и ACT, однако пока не совсем ясно, по какой причине. В связи с этим в первый год приема ингибиторов α-глюкозидаз необходимо регулярно (обычно каждые 3 мес) определять активность АЛТ и ACT в сыворотке крови.
Противопоказания
Противопоказания к назначению ЛС данной группы включают беременность, лактацию, хронические заболевания кишечника, острые и хронические гепатиты и панкреатиты, а также возраст моложе 18 лет.
Предостережения
При беременности и кормлении грудью использование ингибиторов α-глюкозидаз нецелесообразно.
Безопасность и эффективность применения ЛС у детей не определены.
Взаимодействие
Эффективность ингибиторов α-глюкозидаз может снижаться при совместном назначении с ЛС, содержащими пищеварительные ферменты.
КЛИНИЧЕСКИЙ РАЗБОР
Больная Л., 18 лет, поступила с жалобами на общую слабость, утомляемость, сонливость, сухость во рту, тошноту, жажду, частое мочеиспускание, за последние 5 мес похудела на 10 кг.
Объективно: рост 169 см, вес 60 кг, кожные покровы и видимые слизистые оболочки бледные, сухие. Отмечается рубеоз щек. В выдыхаемом воздухе ощущается запах ацетона. В легких дыхание везикулярное, хрипов нет. ЧДД 18 в минуту. Сердечные тоны ритмичные, приглушены. ЧСС 100 в минуту. АД 110/65 мм рт. ст. Язык сухой, покрыт белым налетом. Живот при пальпации мягкий, умеренно болезненный в эпигастрии. Печень по краю реберной дуги.
При обследовании
Общий анализ крови
Гемоглобин - 112 г/л, эритроциты - 4,3х1012/л, цветовой показатель - 0,85, лейкоциты - 7,8х109/л, палочкоядерные - 2, сегментноядерные - 70, лимфоциты - 19, моноциты - 9, СОЭ - 18 мм/ч.
Биохимическое исследование крови: билирубин общий - 15 мкмоль/л (норма 1,7-21 мкмоль/л); тимоловая проба - 2 ЕД (норма 0-5 ЕД); АЛТ - 25 ЕД/л (норма - ниже 41 ЕД/л); АСТ - 20 ЕД/л (норма - ниже 37 ЕД/л); ОХС - 4 ммоль/л (норма - ниже 5,2 ммоль/л); триглицериды - 1,7 ммоль/л (норма - ниже 2,3 ммоль/л); общий белок - 70 г/л (норма - 66-88 г/л); мочевина - 5 ммоль/л (2,8-8 ммоль/л).
Сахар крови - 17 ммоль/л.
Ацетон в моче - умеренно положительный (++);
Гликированный гемоглобин (НВА1с) - 14% (норма до 6,3%);
С-пептид (базальный) - 0,1 нг/мл (норма 0,5-3,2 нг/мл).
На основании клинических и лабораторных данных больной был поставлен диагноз: сахарный диабет 1-го типа, впервые выявленный, декомпенсация (стадия умеренного кетоацидоза).
Единственный метод лечения сахарного диабета 1-го типа - заместительная инсулинотерапия. Наиболее рациональный вариант инсулинотерапии - интенсифицированная инсулинотерапия (режим многократных инъекций, имитирующий физиологическую секрецию инсулина). Суточная потребность в инсулине в дебюте заболевания рассчитывается: 0,5-0,6 ЕД х масса тела. В данной клинической ситуации суточная потребность в инсулине приблизительно 30 ЕД (0,5 Ед χ 60 кг).
При интенсифицированной инсулинотерапии доза инсулинов пролонгированного действия составляет 30-50%, так как играет роль только базального инсулина. Таким образом, доля продленного инсулина составляет 15 ЕД (8 ЕД утром и 7 ЕД в 21.00-22.00 ч), что составляет 50% суточной дозы. Вечернюю дозу пролонгированного инсулина целесообразно вводить перед сном, для того чтобы максимальный
эффект его не совпадал с часами минимальной гликемии между 1 и 3 ч ночи. Остальные 15 ЕД - это инсулин короткого действия, который вводится непосредственно перед каждым приемом пищи (например, перед завтраком - 4 ЕД, перед обедом - 6 ЕД, перед ужином - 5 ЕД). Следует помнить, что доза инсулина короткого действия будет зависеть от количества употребляемых хлебных единиц (ХЕ). В дальнейшем коррекцию дозы проводят ежедневно на основании данных концентрации глюкозы в крови в течение суток.