Руководство по кардиологии : Учебное пособие в 3 т. / Под ред. Г.И. Сторожакова, А.А. Горбаченкова. - 2008. - Т. 1. - 672 с. : ил.
|
|
|
|
ГЛАВА 20 АРТЕРИАЛЬНАЯ ГИПЕРТОНИЯ
Артериальная гипертония взрослых (АГ) - это стабильное повышение систолического АД до 140 мм рт.ст. и выше и диастолического до 90 мм рт.ст. и выше. Под эссенциальной АГ (ЭАГ) или гипертонической болезнью принято понимать хроническое заболевание, основным проявлением которого является артериальная гипертония, не связанная с наличием других заболеваний или процессов, для которых также характерно повышение АД. В зависимости от величины АД АГ подразделяется на 3 степени: 1 - 140-159/90 -99; 2 - 160-179/100-109; 3 - более 180/110 мм рт.ст.
ЭАГ один из важнейших факторов риска развития атеросклеротических сосудистых заболеваний (инсульт, инфаркт, сердечная и почечная недостаточность). Клинические проявления связаны с сосудистыми и органными поражениями (ангиопатия, энцефалопатия, гипертрофия миокарда левого желудочка, нефропатия). В зависимости от сопутствующих АГ метаболических, сосудистых или органных поражений отечественная классификация предлагает распределение больных на 3 стадии, а также их стратификацию по степени риска. Для постоянной медикаментозной терапии используются препараты шести основных групп: диуретики, бета-адреноблокаторы, антагонисты кальция, ингибиторы АПФ, блокаторы ангиотензиновых рецепторов, агонисты имидазолиновых рецепторов.
Ключевые слова: артериальная гипертония, факторы риска, гипертонический криз, антигипертензивная терапия.
понятие
Согласно современным представления артериальная гипертония (АГ)1 взрослых (лица старше 17 лет) - это стабильное повышение уровня систолического артериального давления до 140 мм рт.ст. и выше и/или уровня диастолического артериального давления до 90 мм рт.ст. и выше. Стабильность АГ подтверждается при трехкратном в течение месяца подтверждении повышения АД.
Настоящая глава будет посвящена главным образом эссенциальной АГ (ЭАГ) или гипертонической болезни (ГБ). Термин «эссенциальная артериальная гипертония» соответствует предложенному в 30-40-х гг. прошлого века Г.Ф. Лангом и широко употребляемому в нашей стране понятию «гипертоническая болезнь». Под ЭАГ или ГБ принято понимать хронически протекающее заболевание, основным проявлением которого является синдром артериальной гипертонии, несвязанный с наличием других заболеваний или патологических процессов, для которых также характерно повышение артериального
1 Гипертония - от греческих υπερ - сверх и τονος - напряжение. Получивший в последнее время распространение термин «гипертензия» следует рассматривать как синоним «гипертонии»
давления (АД). В таблице 20.1 показаны заболевания внутренних органов и сосудов, для которых характерна симптоматическая АГ.
Понятие о факторах риска и механизмах развития ЭАГ
В течение всего ХХ столетия в мире и особенно в СССР и РФ велись жаркие споры, считать ли ЭАГ (ГБ) болезнью или синдромом. Понятие «гипертоническая болезнь» в нашей стране закрепилось благодаря высокому авторитету Г.Ф. Ланга и А.Л. Мясникова. А.Л. Мясников считал, что «ГБ этиологически связана с функциональными нарушениями в деятельности коры головного мозга и подкорковых образований, направленной на регуляцию сосудистого тонуса». Основным этиологическим фактором А.Л. Мясников и его ученики считали «психическую травматизацию и перенапряжение нервной системы отрицательными эмоциями».
В наше время признается, что ЭАГ или ГБ «возникает в ответ на множество факторов, нарушающих внутреннюю уравновешенность и адаптированность кровообращения к условиям жизнедеятельности» (Е.Е. Гогин). С этим положением вполне можно согласиться, как и с тем, что определение гипертонии «эссенциальная» трактовать как сущностная, от устаревшего перевода латинского essentia на русский язык, как сущность.
Наконец, невозможно не признать, что ЭАГ является одним из самых сильных, наряду с курением и дислипопротеидемией, фактором риска таких тяжелейших органных поражений, как мозговой инсульт, ИМ, сердечная и почечная недостаточность. Так, анализ эпидемиологических данных показал, что повышение уровня систолического АД обусловливает около 65% случаев инсульта у мужчин и около 80% - у женщин.
Артериальная гипертония (АГ) взрослых - это постоянное повышение уровня систолического АД до 140 мм рт.ст. и выше и/или уровня диастолического АД до 90 мм рт.ст. и выше. Эссенциальная АГ или гипертоническая болезнь (ГБ) - это хронически протекающее заболевание, основным проявлением которого является синдром артериальной гипертонии, не связанный с наличием других заболеваний или патологических процессов.
Таблица 20.1
Клинические формы артериальной гипертонии и основные методы диагностики
Форма АГ | Основные методы диагностики |
Эссенциальная АГ (гипертоническая болезнь) | Диагноз ставится методом исключения симптоматических АГ |
Симптоматические АГ: | |
Заболевания почек и почечных артерий | |
Реноваскулярная АГ | Инфузионная ренография Сцинциграфия почек Допплеровское исследование кровотока в почечных сосудах Аортография Раздельное определение ренина при катетеризации почечных вен |
Гломерулонефрит | Проба Реберга, суточная потеря белка Биопсия почки |
Хронический пиелонефрит | Инфузионная урография Посевы мочи |
Эндокринные АГ | |
Первичный гиперальдостеронизм (синдром Конна) | Пробы с гипотиазидом и верошпироном Определение уровня альдостерона и активности ренина плазмы Компьютерная или магнитно-резонансная томография надпочечников (КТ, МРТ) |
Синдром или болезнь Кушинга | Определение уровня кортизола в крови Определение уровня экскреции оксикортикостероидов с мочой Проба с дексаметазоном Визуализация надпочечников и гипофиза (УЗИ, КТ, МРТ) |
Феохромоцитома и другие хромафинные опухоли | Определение уровня катехоламинов и их метаболитов в крови и в моче Визуализация опухоли (УЗИ, сцинцигра- фия, КТ, МРТ) |
Продолжение табл. 20.1
Гемодинамические АГ | |
Коарктация аорты | Допплеровское ультразвуковое исследование магистральных сосудов, аортография |
Недостаточность аортальных клапанов | ЭхоКГ |
Синдром нарушения дыхания во сне | Полисомнография |
патофизиология аг
Патофизиология АГ связана главным образом с отклонениями от физиологического равновесия механизмов регуляции уровня АД. Регуляция же АД - это одна из самых сложных функций организма, которая зависит от работы сердечно-сосудистой, нервной, эндокринной систем и почек. Адекватное повышение АД в ответ на физическую или эмоциональную нагрузку является нормальной реакцией организма.
Чрезмерное и особенно хроническое повышение уровня АД в ответ на нагрузки той же интенсивности уже можно трактовать как системную АГ. Так как АД - гемодинамический показатель, опосредованный, с одной стороны, сердечным выбросом (СВ), а с другой стороны, общим периферическим сопротивлением сосудов (ОПСС), повышение уровня АГ может обусловливаться каждым из названных механизмов или их сочетанием. Некоторые авторы отмечали, что для самых ранних стадий ЭАГ характерно умеренное повышение СВ, который с годами снижается, но повышается общее периферическое сопротивление сосудистой стенки. Правда, анализ данных проспективного эпидемиологического исследования, известного как Фрамингемское, сделанный с учетом возраста и базового уровня АД, не подтвердил прогностического значения повышенного сердечного индекса у молодых людей с высоким АД.
Как СВ, так и ОПСС зависят от целого ряда условий. Повышение преднагрузки, т.е. напряжения сердечной мышцы в конце диастолы, и сократительной способности миокарда, приводят к повышению СВ. Функциональное напряжение и гипертрофия гладкомышечно-
го слоя артерий обусловливают повышение ОПСС. В свою очередь, отклонения (функциональные или структурные) как миокарда, так и сосудистой стенки, связаны с врожденными или приобретенными нарушениями в системе регуляции.
Вот основные из известных нарушений регуляции АД.
• Врожденное повышение задержки натрия за счет повышенной его реабсорбции в почечных канальцах. Это особенно характерно для так называемых солечувствительных индивидов.
• Повышение тонуса симпатической нервной системы (СНС), которая в значительной степени находится под воздействием подкорковых сосудодвигательных образований. В свою очередь, СНС тесно связана с другими эндогенными факторами, ответственными за повышение СВ и ОПСС.
• Повышение функции ренин-ангиотензин-альдостероновой системы (РААС), одного из главных гуморальных механизмов регуляции уровня АД.
• Снижение концентрации брадикинина - гуморального фактора, способствующего снижению уровня АД.
• Возможно врожденная, но, безусловно, провоцируемая перееданием и ожирением, резистентность тканей к инсулину и как следствие гиперинсулинемия, которая по принципу замкнутого круга усугубляет ожирение и может инициировать как АГ, так и инсулин-независимый сахарный диабет.
• Также, по-видимому, врожденное нарушение мембранного транспорта для электролитов, в первую очередь ионов натрия и калия, что приводит к увеличению внутриклеточного натрия и, как следствие - внутриклеточного кальция, от чего в значительной степени зависит повышение ОПСС.
• Возникновение эндотелиальной дисфункции, т.е. снижение продукции эндотелий-зависимых сосудорасширяющих факторов (в первую очередь оксида азота, NO) и одновременное повышение эндотелий-зависимых сосудосуживающих факторов (в первую очередь эндотелина-1).
Все названные регуляторные механизмы подвержены влиянию ряда внешнесредовых факторов, в отношении которых особенно уязвимы лица с наследственной предрасположенностью к ЭАГ. К таким внешнесредовым факторам в первую очередь следует отнести повышенное потребление натрия, основным источником которого явля-
ется поваренная соль, недостаточное потребление калия, основным источником которого являются свежие овощи и фрукты, избыточная масса тела, низкая физическая активность и подверженность чрезмерным и частым (иногда постоянным) эмоциональным стрессам.
Определенная генетическая предрасположенность к ЭАГ была продемонстрирована в исследованиях на близнецах и семьях, где АГ и связанные с ней органные поражения наблюдаются достаточно часто. Можно сказать, что факт наличия высоких уровней АД у обоих родителей или хотя бы у матери, а также у сибсов должно настораживать врача относительно возникновения ЭАГ у пробанда. Именно в отношении этих лиц следует проводить наиболее интенсивную профилактику, направленную на коррекцию внешнесредовых факторов риска АГ.
В то же время следует иметь в виду отсутствие доказательств того, что сам факт повышения АД в семьях подчиняется какимлибо закономерностям (например, по Менделю). По-видимому, лишь отдельные регуляторные системы связаны с теми или иными особенностями генотипа. В качестве примеров можно привести случаи наследования доброкачественного альдостеронизма, связанного с нарушениями в хромосоме 8q21, содержащей гены альдостеронсинтетазы и 11Я-гидроксилазы, в результате чего под влиянием АКТГ происходит избыточный синтез альдостерона, что приводит к ранней гипертонии. Другой пример, полиморфизм гена ангиотензинпревращающего фермента (АПФ), располагающегося на хромосоме 17q23, так называемый Insertion/Deletion polymorphism, от английских слов включение и отключение. По указанному признаку возможны сочетания аллелей II, ID, DD. Наибольшая активность АПФ наблюдается при генотипе DD. У этих людей закономерно наблюдаются гипертония и предрасположенность к коронарной болезни сердца. Предрасположенность к ЭАГ также определяется неблагоприятными аллелями М (Т174М - полиморфизм гена ангиотензиногена), а (eNOS4a/b - полиморфизм гена синтазы оксида азота).
Таким образом, можно с большой долей уверенности предположить, что в случае с ЭАГ наследуется не сама патология, а механизмы реагирования систем, определяющих уровень АД. В последнее время внимание привлекают исследования о роли проницаемости клеточных мембран для ионов на тонус гладкомышечных клеток сосудов. В этом плане выделяются исследования, проведенные отечественны-
ми учеными Ю.В. Постновым и С.Н. Орловым, которые предложили мембранную теорию патогенеза ЭАГ. На моделях эритроцитов экспериментальных животных и людей с нормальным АД, ЭАГ и симптоматической АГ было показано увеличение проницаемости мембран. Предварительно насыщенные ионами лития эритроциты специальной линии крыс, склонных к спонтанной гипертонии (SHR), а также больных ЭАГ значительно быстрее замещали ионы лития на ионы натрия, чем эритроциты, полученные от негипертензивных крыс, а также людей с нормальным АД или с симптоматической гипертонией. Предполагается, что такие различия Na'-Li' противотранспорта мембран эритроцитов в полной мере отражают состояние Na'-К' и Na'-Н' противотранспорта и свойственно не только эритроцитам, но и другим клеткам, в том числе гладкомышечным (ГМК) клеткам сосудов. Известно, что нарушения транспорта ионов через клеточные мембраны являются маркерами изменений липидов клеточных мембран, в частности у лиц с ЭАГ. В целом же следует признать, что генетика ЭАГ находится лишь на самых ранних этапах научного поиска.
Значительно лучше изучено влияние внешнесредовых факторов риска, которое часто проявляется уже в раннем детстве. Отмечается даже влияние неблагоприятных факторов на внутриутробное развитие. Так, согласно гипотезе Бреннера (Brenner), небольшой вес плода положительно коррелирует со сниженным количеством нефронов в почках, что в свою очередь является фактором риска повышения АД в детском и подростковом возрасте и ранним возникновением ЭАГ. Основным патогенетическим механизмом заболевания автор считает задержку натрия в результате уменьшения фильтрационной поверхности почек новорожденного.
Роль электролитных нарушений в генезе АГ хорошо известна. В многоцентровых эпидемиологических исследованиях (Intersalt, Cardiac) было установлено, что избыточное потребление натрия является одним из экзогенных факторов риска АГ. Суточное потребление поваренной соли в некоторых популяциях1 достигает 25 г и более в сутки, что значительно превышает минимальную суточную потребность человека. Отмеченная связь между потреблением
1 Например, монголы, уйгуры - исторически кочевые народности, систематически употребляющие «эткин-чай», содержащий очень большое количество поваренной соли, кофеина и животного жира.
поваренной соли населением и частотой АГ в полной мере относится к нашей стране. Так, в рамках программы Intersalt было выявлено, что жители Москвы потребляют в среднем 161 ммоль в день, это примерно соответствует 12 г поваренной соли. В то же время оказалось, что лишь в тех популяциях, которые потребляют менее 60 ммоль натрия за сутки, не происходит увеличения уровня АД с возрастом и практически отсутствует эссенциальная артериальная гипертония1. Снижение суточного потребления натрия ниже 100 ммоль могло бы привести к клинически значимому снижению уровня АД. Для этого достаточно не употреблять заведомо пересоленные продукты, а также не досаливать уже готовую пищу за столом. К сожалению, именно соль применяется в качестве консерванта слишком часто, хотя с появлением современных морозильных установок и методов сублимации без таких больших количеств соли в питании вполне можно было бы обходиться.
В последнее время появились сообщения о том, что пищевой натрий является не только фактором риска АГ, но и независимым фактором риска увеличения массы миокарда, что, в свою очередь, резко увеличивает вероятность коронарной болезни сердца.
Реакция АД у разных лиц на избыточный прием соли неодинакова. Выделяют солерезистентных и солечувствительных лиц. Причем пропорция тех и других в различных этнических группах иногда существенно различается. Если солечувствительные лица получают значительную солевую нагрузку, они реагируют довольно резким повышением ОПСС и АД. Некоторые исследователи именно этим фактом пытаются объяснить значительно больший процент гипертоников среди афроамериканцев по сравнению с белыми американцами. Процент солечувствительных среди первых значительно выше.
Повышенную солечувствительность отдельных индивидов можно связать с гетерогенностью нефронов. Так как в почках присутствуют нефроны, которые ишемизированы или из-за вазоконстрикции афферентных артериол, или от присущего им дефекта клубочковой мембраны, ишемия отдельных участков приводит к гиперсекреции юкстагломерулярным аппаратом почки ренина. Повышение плазменной активности ренина до поры компенсируется нормальными
1 Нельзя не признать, что речь идет о популяциях, ведущих довольно примитивный образ жизни, резко отличный от современного цивилизованного общества.
нефронами. Однако это приводит к расстройству гомеостаза АД (гипотеза Sealy). В конце 60-х годов ХХ в. известный американский исследователь Laragh выдвинул гипотезу, в которой говорилось о прямом патофизиологическом воздействии ренина на клеточные структуры, независимом от его влияния на уровни АД. На основании проспективных наблюдений было показано, если всех больных с ЭАГ подразделить на высокорениновых, норморениновых и низкорениновых, то высокорениновые больные имеют больше шансов получить инфаркт миокарда.
Ренин способствует образованию ангиотензина-1 путем гидролиза образованного в печени ангиотензиногена. Впрочем, декапептид - ангиотензин-1 еще не является активным прессорным фактором, его активация зависит от других ферментов (киназ), важнейшим из которых является ангиотензин-превращающий фермент (АПФ). Именно под действием АПФ неактивный ангио- тензин-1 превращается в активный ангиотензин-II (октапептид), последний является наиболее мощным прессорным агентом.
Многочисленными экспериментами показано, что ангиотензин- II является одним из основных гемодинамических компонентов, определяющих повышение АД. В опытах in vitro было продемонстрировано, что ангиотензин-II способствует гипертрофии сосудистых гладкомышечных клеток, стимулирует рост соединительно-тканного матрикса сосудистой стенки и разрушающе воздействует на эндотелий (Messerli, 1996). В то же время исследования на модели атеросклероза у экспериментальных животных показали, что ингибиторы АПФ могут задерживать развитие атеросклеротического процесса, главным образом препятствуя активации ангиотензина (Chobanian,
1990).
Свое влияние на тонус сосудов ангиотензин-II осуществляет, воздействуя на специфические ангиотензиновые рецепторы. В настоящее время достаточно подробно описаны свойства и функции двух подтипов таких рецепторов АТ1 и АТ2. В дальнейшем будет показано, что наибольших успехов современная антигипертензивная терапия достигла именно благодаря созданию лекарственных средств, ингибирующих активность АПФ и блокирующих АТ1.
Роль АПФ не ограничивается названной функцией, от активности этого же фермента зависит распад мощного гуморального гипотензивного агента брадикинина.
Указанные гуморальные механизмы, регулирующие АД, тесно взаимодействуют с нейрогенными механизмами как центрального, так и вегетативного (главным образом симпатического) звена. Особенно активно симпатическая нервная система (СНС) проявляет себя на ранних стадиях ЭАГ у молодых людей. Это проявляется гиперкатехоламинемией (норадреналинемией), повышением тонуса гладкой мускулатуры сосудов, ЧСС, сердечного выброса. Катехоламины (КА) могут вызывать АГ, непосредственно влияя на α1, α2 -рецепторы сосудистой стенки, вызывая ее сократимость. Вазоконстрикция почечных артериол приводит к нарушению экскреции натрия и воды, а также повышению активности ренина. КА воздействуют на b1-рецепторы, от которых также зависит активность ренина, а также частота сердечных сокращений и, значит, минутный объем сердца. Повышение активности СНС, безусловно, связано с резкой физической нагрузкой и эмоциональным стрессом. Есть современные данные о том, что лицам с ЭАГ и высокой активностью плазменного ренина и наследственной предрасположенностью к АГ свойственны большая тревожность, подавленная агрессивность. Так что роль эмоциональных стрессов в качестве фактора риска ЭАГ, как и нейрогенную теорию в целом нельзя игнорировать, но нельзя в то же время и «догматизировать», как, впрочем, и любую теорию, претендующую на исчерпывающее объяснение процессов поддержания гомеостаза.
Возвращаясь к роли пищевого натрия в развитии АГ, следует сказать, что косвенным подтверждением этого можно считать определенные успехи в профилактике и лечении ЭАГ путем ограничения его (Na) потребления. Успешные попытки в этом плане делались и в нашей стране, и за рубежом (Бритов А.Н. и Молчанова О.В., 1995; Ferrara L.A. et al., 1984; Stamler R., Stamler J. et al., 1989). Причем часто оказывается достаточным ограничить потребление поваренной соли 5-6 г в день и не подсаливать уже готовую пищу. Ограничение соли в рационе дает наилучший эффект у лиц моложе 25 лет c мягкой и умеренной АГ. При ограничении NaCl гипотензивный эффект начинает развиваться на 5-7 день, достигая максимума через 2-3 недели. Уменьшение потребления поваренной соли на 1 г приводит к среднему снижению систолического и диастолического АД примерно на 1 мм рт.ст.
Проблема потребления с пищей, а также обменные процессы в организме ионов натрия и калия тесно взаимосвязаны. Относительно высо-
кое потребление калия с сырыми фруктами и овощами может иметь независимое протективное действие в отношении гипертонии и других сердечно-сосудистых заболеваний. В то же время городское население России потребляет слишком мало овощей и фруктов, особенно в зимние и ранние весенние месяцы года. В рамках программы Intersalt выявилось, что потребление калия москвичами в среднем равнялось 48 ммоль в день, что примерно вдвое меньше физиологической нормы.
У москвичей Na/K коэффициент, определенный методом суточного диетического опроса, колеблется в пределах 1,7-1,5 у мужчин и 1,4-1,5 у женщин. Физиологичное же соотношение названных электролитов должно быть ~1. Представляется, что столь высокое соотношение Na/K - это один из ведущих факторов риска исключительно высокого распространения АГ в нашей стране. Очевидно, что диета с низким содержанием соли приведет к желаемому антигипертензивному эффекту значительно быстрее, если будет подкреплена диетой, богатой калием (Linas SL, 1991).
B последние годы активно изучается роль обмена кальция в развитии АГ. Опубликованы результаты 15 эпидемиологических исследований (McCarron D., Morris C.), в которых продемонстрирована связь между содержанием кальция в пище и уровнем АД. Установлено, что в группе лиц, употребляющих 450-600 мг кальция в день, распространенность АГ составляет 9-12%, а при суточном употреблении кальция 1200-1400 мг - всего 3-6%. Избыточное потребление кальция (1000 мг/сут) приводит к снижению ДАД даже у нормотоников. Введение кальция, направленное на повышение кальциемии и профилактику вторичного гиперпаратиреоза, сопровождается снижением АД и предупреждением АГ.
Говоря о значении характера питания в развитии ЭАГ, нельзя не сказать о нарушении соотношения в пище насыщенных и ненасыщенных жирных кислот. Чрезмерное потребление насыщенных жиров животного происхождения является фактором риска как атеросклероза, так и гипертонии. Рекомендуется суточную потребность в жирах покрывать на 2/3 за счет растительных масел, содержащих преимущественно мононенасыщенные (оливковое масло) и полиненасыщенные (кукурузное, подсолнечное, соевое масла) жирные кислоты. Одновременно следует сокращать потребление животного жира в форме сала, жирных сортов мяса, сливочного масла, сметаны, жирных сортов сыра и других молочных натуральных продуктов.
Пока нет надежных эпидемиологических данных о том, что соблюдение такой рекомендации в отрыве от других рекомендаций по соблюдению здорового образа жизни обладает самостоятельным антигипертензивным эффектом. Но поскольку гипертония редко бывает изолированным фактором риска, а часто сочетается с гиперхолестеринемией и/или гипертриглицеридемией, следование таким рекомендациям оказывается весьма полезным для больных в плане предупреждения атеросклероза. Обнадеживают эпидемиологические данные о превентивном влиянии в отношении сердечно-сосудистых заболеваний так называемой средиземноморской диеты.
Недостаточная физическая активность также является фактором риска ЭАГ. По-видимому, это проявляется как бы через детренированность сердечно-сосудистой системы и ряда регулирующих сосудистый тонус систем, в первую очередь симпатической нервной системы. В ряде работ было показано, что систематические физические нагрузки, тренирующие выносливость, могут предупреждать ЭАГ и даже вызывать ее обратное развитие при мягкой и умеренной степенях. Наоборот, значительные анаэробные нагрузки, такие как поднятие тяжестей, могут провоцировать резкие подъемы уровня АД и приводить к возникновению гипертонии. Поэтому лицам с АГ и высоким риском АГ следует рекомендовать систематическую, достаточно быструю ходьбу, бег трусцой, лыжи, не слишком интенсивные виды плавания.
В настоящее время, когда появилась возможность мониторировать динамику АД в течение суток, можно выделять периоды, когда давление у конкретного пациента достаточно резко повышается. Чаще всего это наблюдается в ранние утренние часы. В указанные периоды не следует рекомендовать сколько-нибудь значительных физических нагрузок. Лучше начинать упражнения в относительно «спокойный» для больного период.
Ведущим фактором риска ЭАГ является избыточное потребление натрия с поваренной солью. Другими факторами риска ЭАГ считают недостаточное потребление калия, малая физическая активность, чрезмерные эмоциональные нагрузки. АД стабильно повышается благодаря ряду регуляторных расстройств: повышению тонуса симпатоадреналовой системы, ренин-ангитензин-альдостероновой системы, а также эндотелиальной дисфункции и нарушению чувствительности тканей к инсулину.
эпидемиология эаг
Распространенность ЭАГ в России, как и во многих других индустриально развитых странах, во второй половине ХХ столетия имела тенденцию к непрерывному и очень быстрому росту. Согласно многочисленным эпидемиологическим данным, распространенность АГ при профилактических осмотрах в 40-50-х гг. прошлого века составила 3-7%. На основании полученных Институтом терапии AMH СССР материалов А.Л. Мясников в 1965 г. оценивал среднюю распространенность гипертонической болезни в СССР как 5-5,5%.
B 70-80-е годы борьба с АГ все шире стала осуществляться на популяционном уровне. За критерий болезни по рекомендациям экспертов BO3 стали принимать уровень АД >160/95 мм рт.ст. Установление четкого критерия повышенного АД, а также единых стандартов эпидемиологических исследований1 в отношении сердечно-сосудистых заболеваний (CCP) позволило сопоставить распространенность АГ в различных странах мира. Так, после проведения многократных обследований было выяснено, что в конце 70-х в начале 80-х годов распространенность АГ в СССР составила у работающих лиц 35-54 лет в среднем 23%. Распространенность АГ среди жителей крупных городов составляла 17-19%. Причем около половины выявленных во время скрининга больных не знали о своем заболевании, а из тех лиц, которые знали, около 50% не лечились или лечились неадекватно. Примерно в те же годы, по данным классического проспективного исследования во Фремингеме (США), АГ была выявлена у 18% мужчин и 16% женщин в возрасте 30-62 лет (Kannel W.B., 1976).
Результаты проведенных в 90-х годах ХХ столетия эпидемиологических исследований показывают, что АГ по критериям: артериальное давление (АД) >160/95 мм рт.ст. + лица, получающие медикаментозное антигипертензивное лечение, выявляется у 25-30% взрослого населения России. Если же взять в качестве критерия принятый в настоящее время уровень АД >140/90 мм рт.ст., то АГ выявляется почти у 40% населения. Причем АГ и ее главное осложнение - мозговой инсульт (МИ), наряду с ишемической болезнью сердца (ИБС), занимают первое место как по величине, так и по темпам роста
1 Речь идет о стандартных правилах формирования репрезентативных выборок, методах опроса, измерения пульса, АД, оценки ЭКГ и других параметров, подходах к статистической обработке полученных данных.
инвалидности и смертности. Это связано с тем, что АГ, во многом обуславливающая высокую сердечно-сосудистую заболеваемость и смертность, характеризуется не только широкой распространенностью, но и явно неадекватным контролем. Сложившуюся ситуацию можно объяснить низкой осведомленностью лиц с повышенными уровнями АД о своем заболевании. По данным Государственного центра профилактической медицины, процент больных, знающих об имеющейся у них гипертонии среди женщин, составляет 58,9%, а среди мужчин - всего 37,1%. Еще более низок охват больных АГ лечением (45,7% у женщин и 21,6% у мужчин), и, наконец, чудовищно низок процент больных АГ, адекватно контролирующих уровни АД (17,5% и 5,7% соответственно). По этому показателю Россия отстает от ряда стран с относительно высоким уровнем организации здравоохранения, где процент больных АГ, адекватно контролирующих уровень АД, достигает 25-29.
Такая ситуация с осведомленностью больных относительно имеющейся у них АГ и низким охватом лечением связана в значительной мере с тем, что в большинстве случаев АГ протекает бессимптомно. По существу, имеющиеся у примерно половины больных ЭАГ субъективные жалобы связаны с сосудистыми или органными поражениями, вызванными АГ (табл. 20.3) или приведшими к симптоматической АГ (табл. 20.1), а также сопутствующими (ассоциированными) заболеваниями (табл. 20.3).
Если взять в качестве критерия уровень АД>140/90 мм рт.ст., то АГ выявляется почти у половины населения. Главное осложнение АГ - мозговой инсульт (МИ), наряду с ишемической болезнью сердца (ИБС), занимают первое место как по величине, так и по темпам роста инвалидности и смертности.
симптомы аг и органных поражений
Принято считать головную боль одним из наиболее частых проявлений ЭАГ. В настоящее время неврологи считают этот симптом, как и потемнение в глазах, мелькание мушек перед глазами,
а также ощущение усталости, дремоту, растерянность, невозможность сосредоточиться проявлениями гипертонической энцефалопатии. Гипертоническая энцефалопатия связана с нарушением ауторегуляции мозгового кровообращения, которое чаще наблюдается при быстрых и значительных подъемах уровня АД. При этом в отдельных участках мозга наблюдается вазодилятация, тогда для поддержания постоянства мозгового кровотока в других участках происходит вазоконстрикция. Называть это спазмом сосудов неверно. Именно сосудистые сегменты, открытые для кровотока, могут повреждаться, что выражается повышенной их проницаемостью для плазмы. Крайним выражением данного феномена может быть отек мозга с клиническими проявлениями эклампсии, которая, впрочем, более типична для ренальной гипертонии, в том числе для нефропатии беременных, а не для ЭАГ.
Возможно, головные боли при АГ можно объяснить ухудшением венозного оттока, что приводит к повышению внутричерепного давления и раздражает чувствительные рецепторы твердой мозговой оболочки. Впрочем, у большей части больных указанных мозговых нарушений не возникает, даже при весьма существенном повышении уровня АД. Однако это обстоятельство не исключает повышенного риска ишемического или геморрагического инсульта.
Отражением сосудистых изменений мозга являются изменения, наблюдаемые на глазном дне при офтальмоскопии. Эти изменения проявляются утолщением артериол глазного дна, геморрагиями, отеком сосочка сетчатки, экссудатами.
Плохим прогностическим признаком является появление транзиторных ишемических атак (ТИА), проявляющихся нарушениями мозгового кровообращения. Главным отличительным признаком ТИА от настоящего инсульта является их кратковременность. ТИА продолжаются, как правило, несколько часов и могут проходить при даже не очень интенсивной терапии.
Другим достаточно частым клиническим проявлением АГ являются загрудинные боли и/или проявления дискомфорта в грудной клетке, а также проявления СН преимущественно в виде одышки при физических усилиях. По существу, эти жалобы связаны с сопутствующими АГ атеросклеротическими поражениями коронарных артерий сердца и сопровождающей АГ гипертрофией левого желудочка сердца.
Отмечается два типа ГЛЖ. Концентрическая гипертрофия, при которой масса миокарда увеличивается одновременно с уменьшением объема полости левого желудочка. Концентрическая ГЛЖ образуется через стадию концентрического ремоделирования миокарда, когда физиологически невыгодное соотношение толщины стенки и внутреннего просвета сосуда уже имеется, но масса миокарда еще не превышает нормальных пределов. Другой вариант ГЛЖ - эксцентрический. При этом указанные пропорции существенно не изменены, но одновременно с увеличением массы миокарда увеличивается внутренний размер ЛЖ, что приводит к значительному повышению его объема.
В условиях ГЛЖ и необходимости для сердца работать против повышенного давления в аорте даже умеренные атеросклеротические изменения в коронарных артериях могут вызывать ситуацию относительной коронарной недостаточности. Часто это выражается типичными приступами стенокардии. Иногда больные отмечают разнообразные неприятные ощущения за грудиной, которые следует рассматривать как эквивалент стенокардии. Имеется ряд многолетних проспективных исследований, показывающих существенное увеличение риска ИМ и смертности от ССЗ у гипертоников с ГЛЖ.
Другим серьезным осложнением гипертонии, сочетающейся с ГЛЖ (особенно при нарушении систолической функции), является хроническая сердечная недостаточность (ХСН). Несколько крупных популяционных исследований, в том числе Фремингемское исследование, показали, что АГ является в настоящее время самой частой причиной ХСН, вызывая систолическую дисфункцию миокарда примерно у 40% мужчин и у 60% женщин с АГ. Появление данного осложнения существенно ухудшает прогноз. При снижении фракции выброса ниже 50% только около 1/3 больных выживают более пяти лет.
Хроническая почечная недостаточность. Функция почек при эссенциальной гипертонии поражается, как правило, очень постепенно и десятилетиями может не проявляться при обычном клиническом обследовании больного. В ряде исследований показано, что ранним признаком структурных и функциональных нарушений со стороны почек при ЭАГ может быть микроальбуминурия, которая отражает повышение внутриклубочкового давления, что приводит к увеличению фильтрации белка через базальную мембрану. Это,
в свою очередь, усугубляет эндотелиальную дисфункцию почечных артериол, вызывая выброс в кровь цитокинов, эндотелина-1 и других вазоактивных медиаторов. В это же время повышается активность ренина. Образовавшийся при этом ангиотензин-II закрепляет системную гипертонию и стимулирует клеточную пролиферацию, в том числе и в приводящих артериолах почек. Создается своеобразный замкнутый круг.
У больных с достаточно длительным течением ЭАГ может наблюдаться снижение концентрационной функции почек, что клинически выражается ноктурией и более выраженной протеинурией (в суточной моче определяется от 1 до 3-х г белка). Лабораторные методы позволяют выявить снижение клиренса креатинина, хотя и в такой степени, которая еще не позволяет диагностировать хроническую почечную недостаточность (ХПН). Уровень креатинина в плазме крови не превышает 2-х мг/дл. Однако в дальнейшем поражение почек может прогрессировать с развитием нефроангиосклероза, т.е. замещением нормальной почечной ткани фиброзными образованиями. Это проявляется усилением протеинурии (>3 г белка за сутки), в осадке мочи появляются гиалиновые, реже зернистые цилиндры. Уровень креатинина крови увеличивается более 2 мг/дл. Наконец, в отдельных случаях развивается развернутая клиническая картина ХПН. Такие случаи в российской клинической практике в настоящее время наблюдаются достаточно редко. Однако в странах, где за последние десятилетия удалось существенно снизить смертность от инсульта и коронарной болезни сердца (не в последнюю очередь благодаря эффективному контролю АГ в популяции) и тем самым продлевать жизнь лицам с гипертонией, частота развития ХПН при ЭАГ значительно возросла. Реализация «Федеральной программы по борьбе с АГ» позволяет предсказывать сходную динамику событий и в России.
Клинические проявления АГ связаны с сосудистыми и органными поражениями мозга, сердца и почек. Не менее чем у половины больных долгое время может не наблюдаться каких-либо субъективных проявлений болезни. АГ остается серьезнейшим фактором риска инсульта, инфаркта миокарда, сердечной и/или почечной недостаточности.
диагностика
Адекватность постановки диагноза ЭАГ имеет важнейшее значение. Может быть, как ни для какого-либо другого хронического заболевания, здесь важно придерживаться согласованных экспертами стандартных подходов. Ведь нередко первичное выявление АГ приходится осуществлять во время массовых осмотров, иногда силами среднего медицинского персонала и даже так называемыми парамедиками. И те, и другие должны быть тщательно подготовлены врачами к этой роли. Данные разделы будут излагаться приближенно к «Рекомендациям по профилактике, диагностике лечению АГ», разработанным экспертами Всероссийского научного общества кардиологов, которые были приняты в 2001-2004 гг. Конгрессами кардиологов России.
Диагностика ЭАГ и обследование пациентов с АГ должна проводиться в строгой последовательности и отвечать определенным задачам:
• определение стабильности повышения АД и его степени;
• исключение симптоматической АГ или идентификация ее вида;
• выявление наличия других факторов риска ССЗ и клинических состояний, которые могут повлиять на прогноз и лечение, а также отнесение больного к той или иной группе риска;
• определение наличия поражений органов-мишеней и оценку их тяжести.
В широкой медицинской практике получил всеобщее признание манжетный метод Рива-Роччи, усовершенствованный Н.С. Коротковым, предложившим в 1905 г. вместо пальпации пульса на лучевой артерии использовать аускультацию артерии дистальнее ее сдавления манжетой, всего удобнее - в локтевой ямке. Это позволяет определять как максимальное (систолическое) давление, так и минимальное (диастолическое) давление по появлению и исчезновению коротковских тонов.
Для измерения АД имеет значение соблюдение следующих условий:
1. Положение больного
• Сидя в удобной позе, рука на столе.
• Манжета накладывается на плечо на уровне сердца, нижний край ее на 2 см выше локтевого сгиба.
Для выслушивания тонов Короткова мембрана фонендоскопа устанавливается в область ямки локтевого сгиба, желательно предварительно пропальпировать лучевую артерию.
2. Обстоятельства
• Исключается употребление кофе и крепкого чая в течение 1 ч перед исследованием.
• Не курить не менее 30 минут.
• Исключается применение симпатомиметиков, включая назальные и глазные капли.
• Измерение проводится в покое после 5-минутного отдыха. В случае, если процедуре измерения АД предшествовала значительная физическая или эмоциональная нагрузка, период отдыха следует продлить до 15-30 минут.
3. Оснащение
• Манжета. Желательно выбрать соответствующий размер манжеты (резиновая часть должна быть не менее 2/3 длины предплечья и не менее 3Д окружности руки).
• Тонометр (сфигмоманометр) должен каждые 6 мес подвергаться проверке, положения столбика ртути или стрелки манометра перед началом измерения должны находиться на нуле.
4. Кратность измерения
Для оценки уровня артериального давления на каждой руке следует выполнить не менее трех измерений с интервалом не менее минуты, при разнице >8 мм рт.ст. производятся 2 дополнительных измерения. За конечное (регистрируемое) значение принимается среднее из двух последних измерений.
Для диагностики заболевания должно быть выполнено не менее 2-х измерений с интервалом не менее недели.
5. Собственно измерение
• Быстро накачать воздух в манжету до уровня давления, примерно на 20 мм рт.ст. превышающего систолическое АД, определяемого по исчезновению пульса.
• АД измеряется с точностью до 2-х мм рт.ст.
• Снижать давление в манжете на 2-3 мм рт.ст. в секунду.
• Уровень давления, при котором появляется 1 тон, соответствует систолическому АД (1-я фаза тонов Короткова).
• Уровень давления, при котором происходит исчезновение тонов (5 фаза тонов Короткова), принимают за диастолическое дав-
ление. У детей и при некоторых патологических состояниях у взрослых невозможно определить 5 фазу, тогда следует попытаться определить 4-ю фазу тонов Короткова, которая характеризуется значительным ослаблением тонов.
• Если тоны очень слабы, то следует поднять руку и выполнить несколько сжимающих движений кистью; затем измерение повторяют. Не следует сильно сдавливать артерию мембраной фонендоскопа.
• При первичном осмотре пациента следует измерить давление на обеих руках.
• В дальнейшем измерения делаются на той руке, где АД выше.
• У больных старше 65 лет, больных с сахарным диабетом и получающих антигипертензивную терапию следует также произвести измерение АД примерно через 2 минуты в положении пациента стоя.
• Целесообразно также измерять давление на ногах, особенно у больных моложе 30 лет. Измерение АД на ногах желательно проводить с помощью широкой манжеты (той же, что и для лиц с ожирением), фонендоскоп располагают в подколенной ямке.
Несоблюдение всех перечисленных выше условий и правил приводит к неверным результатам и трактовкам относительно уровня АД у пациента. Наиболее частые ошибки: однократное измерение АД, измерение АД у людей, находящихся в состоянии физической или эмоциональной усталости, применение стандартной (неширокой) манжеты у лиц с ожирением, измерение АД только на одной руке, измерение АД с точностью до 5 и тем более до 10 мм рт.ст.
Измерение АД на дому
Величины нормального уровня АД и критерии классификации АГ разработаны на основании АД, измеренного на приеме у врача. Показатели АД, измеренного в домашних условиях, могут стать ценным дополнением для контроля эффективности лечения, но не могут быть приравнены к данным, получаемым в клинике, и предполагают применение других нормативов. Так, уровень АД, измеренный на приеме у врача, может превышать уровень, измеренный дома. Следует с осторожностью трактовать данные, полученные с использованием имеющихся в настоящее время автоматических и полуавтоматических приборов для домашнего применения, которыми измеряют АД
на предплечье и на пальцах кисти, в связи с неточностью получаемых при этом значений уровня АД. Приборы, основанные на методе Реклингаузена, т.е. по появлению и исчезновению осцилляций артериальной стенки, могут давать результат, отличный от результатов, полученных по методу Короткова.
В то же время в конкретном случае самоконтроль АД предварительно обученными больными или их родственниками может быть чрезвычайно полезным в достижении адекватного лечения АГ и является неотъемлемой частью образовательных программ.
Суточное амбулаторное мониторирование АД
Суточное амбулаторное мониторирование АД (САМАД) обеспечивает получение важной информации о состоянии механизмов сердечно-сосудистой регуляции, в частности выявляет такие феномены, как суточная вариабельность АД, ночная гипотония и гипертония, динамика АД во времени и равномерность гипотензивного эффекта препаратов. При этом данные 24-часового измерения АД имеют большую прогностическую ценность, чем разовые измерения. Так, лица, имеющие нормальное ночное снижение уровней АД (dippers), имеют лучший прогноз при тех же базовых уровнях давления. Более высоким риском обладают пациенты, у которых в ночные часы уровень АД не отличается от дневных (non-dippers) или даже оказываются выше дневных (night-pickers). САМАД позволяет выявить резкие повышения АД, часто наблюдаемые в ранние утренние часы и протекающие бессимптомно, но существенно повышающие риск органных поражений, особенно инсультов. Наличие чрезмерного снижения АД (over-dippers) также должно привлечь внимание врача, т. к. такие состояния увеличивают риск органных ишемических поражений. Важным является определение так называемого индекса времени повышения систолического и диастолического АД в течение суток, дневного и ночного периодов.
Рекомендуемая программа САМАД предполагает регистрацию АД с интервалами 15 мин в период бодрствования и 30 мин в период сна.
Ситуациями, в которых выполнение САМАД следует считать особенно целесообразным, являются.
• Необычные колебания АД во время одного или нескольких визитов.
• Подозрение на «гипертонию белого халата» у больных с низким риском сердечно-сосудистых заболеваний.
• Подозрение на резкие повышения уровня АД, особенно в ранние утренние часы.
• Больные с синдромом апноэ/гипопноэ во сне.
• Симптомы, которые позволяют заподозрить наличие гипотонических эпизодов.
• Артериальная гипертония, резистентная к проводимому медикаментозному лечению.
Обладая безусловной информативностью, метод САМАД пока не стал общепринятым в основном из-за его высокой стоимости.
Двухэтапное обследование пациента с выявленной АГ
После выявления стабильной АГ следует провести обследование пациента на предмет исключения симптоматических АГ. Далее определяются степень АГ, стадия заболевания и степень риска. Обследование включает 2 этапа.
Первый этап - обязательные исследования, которые проводятся каждому больному при выявлении АГ. Этот этап включает выявление поражения органов-мишеней, диагностику сопутствующих клинических состояний, влияющих на риск сердечно-сосудистых осложнений, и рутинные методы диагностики вторичных АГ.
1. Сбор анамнеза
У больного, особенно с впервые выявленной АГ необходим тщательный сбор анамнеза, который должен включать.
• Длительность существования АГ1 и уровни повышения АД в анамнезе, а также результаты применявшегося ранее лечения немедикаментозными и медикаментозными антигипертензивными средствами, наличие в анамнезе гипертонических кризов.
• Данные о наличии симптомов ИБС, сердечной недостаточности, заболеваний ЦНС, поражений периферических сосудов, сахарного диабета, подагры, нарушений липидного обмена, бронхообструктивных заболеваний, заболеваний почек, сексуальных
1 Практически можно уточнить время, когда пациент впервые узнал о повышении у себя уровня АД, что часто не соответствует истинной длительности патологического процесса.
расстройств и другой патологии, а также сведения о лекарственных препаратах, используемых для лечения этих заболеваний, особенно тех, которые могут влиять на уровни АД.
• Выявление специфических симптомов, которые давали бы основания предполагать вторичный характер АГ (молодой возраст, тремор, потливость, тяжелая АГ, резистентная к лечению; шум над областью почечных артерий, тяжелая ретинопатия, гиперкреатининемия, спонтанная гипокалиемия).
• Тщательная оценка образа жизни, включая потребление поваренной соли, жирной пищи, алкогольных напитков, количественная оценка курения, оценка физической активности, а также данные об изменении массы тела в течение жизни.
• Личностные и психологические особенности, а также факторы окружающей среды, которые могли бы влиять на течение и исход лечения гипертонической болезни, включая семейное положение, ситуацию на работе и в семье, уровень образования.
• Семейный анамнез АГ, сахарного диабета, нарушений липидного обмена, ишемической болезни сердца (ИБС), инсульта или заболеваний почек.
• У женщин - гинекологический анамнез, связь повышения АД с беременностью, менопаузой, приемом гормональных контрацептивов, гормонально-заместительной терапией.
2. Объективное исследование
• Измерение роста и веса с вычислением индекса массы тела (вес в килограммах, деленный на квадрат роста в метрах)1.
• Оценка состояния сердечно-сосудистой системы, в особенности размеров сердца, наличия патологических шумов, проявлений сердечной недостаточности (хрипы в легких, отеки, размеры печени), выявление пульса на периферических артериях и симптомов коарктации аорты (у больных моложе 30 лет необходимо измерение АД на обеих руках и ногах).
• Выявление патологических шумов в проекции почечных артерий, пальпацию почек и выявление других объемных образований.
1 ИМТ или индекс Кетле в норме колеблется от 19 до 26 у мужчин и от 19 до 28 у женщин.
3. Лабораторные и инструментальные обязательные исследования
• Общий анализ мочи.
• Калий, глюкоза натощак, креатинин, общий холестерин крови.
• ЭКГ в покое.
• Рентгенография грудной клетки.
• Осмотр глазного дна.
Если на данном этапе обследования у врача нет оснований подозревать вторичный характер АГ и имеющихся данных достаточно для четкого определения группы риска пациента и, соответственно, тактики лечения, то на этом обследование может быть закончено.
4. Дополнительные исследования
Дополнительные исследования для оценки сопутствующих факторов риска и поражения «органов-мишеней» выполняются в тех случаях, когда они могут повлиять на тактику ведения пациента, т.е. их результаты могут привести к изменению уровня риска.
• Ультразвуковое исследование почек и периферических сосудов.
• Эхокардиография как наиболее точный метод диагностики ГЛЖ. Исследование показано только тогда, когда ГЛЖ не выявляется на ЭКГ, а ее диагностика повлияет на решение вопроса о назначении терапии.
• Холестерин липопротеидов высокой, низкой и очень низкой плотности и триглицериды.
Второй этап предполагает исследования для уточнения вида симптоматической АГ, дополнительные методы обследования для оценки поражения органов-мишеней, выявление дополнительных факторов риска и возможных сопутствующих заболеваний и/или синдромов.
5. Специальные обследования для выявления вторичной (симптоматической) АГ
При подозрении на вторичный характер АГ выполняют целенаправленные исследования для уточнения нозологической формы и, в ряде случаев, характера и/или локализации патологического процесса.
В таблице 20.1 приводятся основные методы уточнения диагноза при различных формах симптоматических АГ. Жирным шрифтом выделены наиболее информативные методы диагностики в каждом случае.
Измерение артериального давления с помощью ртутного или анероидного тонометра (сфигмоманометра) должно проводиться всем пациентам, обратившимся к врачу по любому поводу.
классификация аг
Важным разделом «Рекомендаций по профилактике, диагностике, лечению АГ» являются вопросы классификации АГ и стратификации пациентов по степени риска. В новой классификации в значительной мере учтены рекомендации экспертов ВОЗ и Международного общества по гипертонии. Но не все, в частности, не устранены понятия о формах АГ (легкая, умеренная, тяжелая), которые не всегда соответствуют долговременному прогнозу. Введено понятие «степень» АГ (табл. 20.2), отражающее именно уровень повышения артериального давления (АД). Это особенно важно для больного, у которого повышение уровня АД выявлено впервые и лекарственная антигипертензивная терапия еще не применялась.
Степень повышения АД определяется у лиц, на принимающих антигипертензивные лекарства, что не представляет проблемы при впервые выявленной АГ. В некоторых случаях для уточнения диагноза допускается перерыв в медикаментозном лечении при условии, что это не может серьезно повредить больному.
С учетом того, что в России в течение не менее 50-ти лет применяется классификации ЭАГ (ГБ) по стадиям, было решено сохранить и данную классификацию. ГБ I стадии предполагает отсутствие изменений в органах-мишенях. ГБ II стадии предполагает наличие изменений в одном или нескольких органах-мишенях. Наконец, ГБ III стадии предполагает наличие одного или нескольких, ассоциированных с АГ (сопутствующих), состояний.
В этом разделе отечественная классификация в определенной степени отличается от международной классификации АГ, которая предлагает просто указывать конкретные поражения органов мишеней и/или сопутствующие АГ клинические состояния в качестве критериев для стратификации риска.
Таблица 20.2
Классификация уровней АД
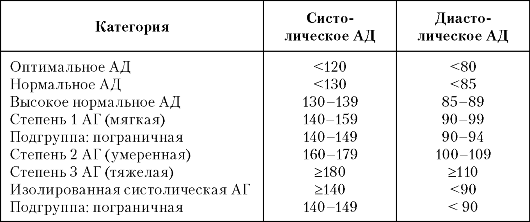 Примечание: (1)
если систолическое и диастолическое АД находятся в разных категориях,
присваивается более высокая (тяжелая) категория, (2) уровни АД
<105/65 мм рт.ст. при определенной симптоматике следует трактовать
как гипотоническое состояние.
Примечание: (1)
если систолическое и диастолическое АД находятся в разных категориях,
присваивается более высокая (тяжелая) категория, (2) уровни АД
<105/65 мм рт.ст. при определенной симптоматике следует трактовать
как гипотоническое состояние.
группы риска
Критерии, определяющие степень риска конкретного больного, представлены в таблице 19.3. Строго говоря, указанные в таблице патологические состояния и определяют клиническую картину ЭАГ, которая зависит, главным образом, от вовлечения в патологический процесс определенной сосудистой области и соответствующих органов-мишеней. Само же по себе постепенное повышение уровня АД чаще всего не манифестируется какими-то субъективными проявлениями. Именно по этой причине выявление АГ часто происходит случайно, а сам пациент вплоть до того момента, когда начинают проявлять себя органные поражения и/или сопутствующие АГ заболевания, не считает себя больным. Естественно, что в этой ситуации вовлечение пациента в процесс лечения затруднителен и врачу следует не только определять группу риска для конкретного больного, но и по возможности разъяснить важность выполнения рекомендаций по немедикаментозному и медикаментозному лечению.
У больных АГ прогноз зависит не только от уровня АД. Наличие сопутствующих факторов риска, степень вовлечения в процесс органов-мишеней, а также наличие ассоциированных клинических состояний имеет не меньшее значение, чем степень повышения АД, в связи с чем в классификацию введена стратификация больных в зависимости от степени риска. Необходимо также учитывать некоторые аспекты личного, клинического и социального положения больного.
Таблица 20.3
Критерии стратификации риска
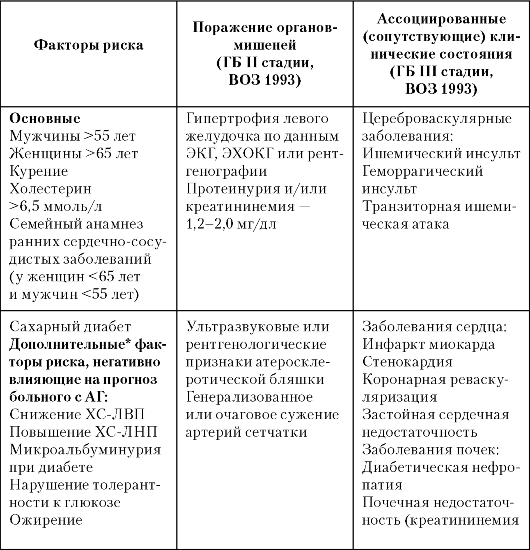
 Примечание: *
Роль этих факторов в настоящее время считается существенной, их наличие
может увеличивать абсолютный риск в пределах одной группы риска,
поэтому их оценка желательна.
Примечание: *
Роль этих факторов в настоящее время считается существенной, их наличие
может увеличивать абсолютный риск в пределах одной группы риска,
поэтому их оценка желательна.
Чтобы оценить суммарное влияние нескольких факторов риска относительно абсолютного риска тяжелых сердечно-сосудистых поражений в будущем, экспертами Всемирной Организации Здравоохранения и Международного общества гипертонии была предложена стратификация риска по четырем категориям: низкий, средний, высокий и очень высокий риск (табл. 19.4). Риск в каждой категории рассчитан исходя из данных об усредненном за 10 лет риске смерти от сердечно-сосудистых заболеваний, о риске нефатальных инсульта и инфаркта миокарда по результатам Фрамингемского исследования.
При формулировке диагноза ГБ у лиц с впервые выявленной и/или нелеченной АГ следует указать степень повышения АД, стадию заболевания и степень риска. Рекомендуется детализация поражений органов-мишеней, факторов риска и сопутствующих клинических состояний.
Таблица 20.4
Стратификация АГ по степени риска
Факторы риска и история заболевания | Норма (САД 120-129 или ДАД 80-84) | Высокое нормальное (САД 130-139 или ДАД 85-89) | 1 степень (САД 140-159 или ДАД 90-99) | 2 степень (САД 160-179 или ДАД 100-109) |
Без факторов риска | Незначительный риск | Незначительный риск | Низкий риск | Средний риск |
1-2 фактора риска | Низкий риск | Низкий риск | Средний риск | Средний риск |
3 фактора риска и более, сахарный диабет, ПОМ | Средний риск | Высокий риск | Высокий риск | Высокий риск |
АКС | Высокий риск | Очень высокий риск | Очень высокий риск | Очень высокий риск |
Примечание: ФР - факторы риска; ПОМ - поражение органов-мишеней;
АКС - ассоциированные с АГ клинические состояния.
Уровни риска (риск инсульта или инфаркта миокарда в ближайшие 10 лет)
Низкий риск (1) - менее 15%;
Средний риск (2) - 15-20%;
Высокий риск (3) - 20-30%;
Очень высокий риск (4) - 30% или выше
гипертонические кризы
У значительной части больных относительно мирное течение ЭАГ нарушается гипертоническими кризами (ГК), которые могут возникать при любой степени АГ и на любой стадии заболевания. ГК - это
обострение ЭАГ, которое характеризуется резким и значительным повышением уровня АД относительно привычных для конкретного больного значений. Как правило, при ГК уровень систолического АД превышает 200 мм рт.ст. и диастолическое - 120 мм рт.ст. Мы разделяем мнение такого авторитетного клинициста, как Norman Kaplan, о том, что скорость повышения АД имеет большее клиническое и прогностическое значение, чем сам по себе высокий уровень АД. Однако неправильно считать любые повышения АД кризами. К ГК следует относить такие связанные с подъемом АД события, которые сопровождаются вегетативными расстройствами, а также появлением или резким усилением связанных с АГ органных нарушений, чаще всего со стороны глаз, мозга, сердца, почек.
ГК чаще возникают у тех больных, у которых уже имеются те или иные функциональные или морфологические отклонения. Например, атеросклероз коронарных артерий сердца, экстракраниальных и интракраниальных артерий, начальные нарушения мозгового кровообращения, диэнцефальный синдром, климактерий у женщин, начальные проявления сердечной недостаточности. К провоцирующим моментам развития криза относят отмену (перерыв в лечении) антигипертензивной терапии, прием алкоголя, большого количества натрия, пищи, воды. Своеобразную вспышку ГК врачи скорой медицинской помощи отмечают в праздничные дни. Другими провоцирующими моментами являются сильный эмоциональный стресс, усталость, метеорологические факторы (в том числе повышенная солнечная активность), смена часовых поясов и климатических зон при перелетах на большие расстояния.
В зависимости от скорости повышения АД, характера изменений гемодинамики и вовлечения тех или иных систем и органов существует ряд классификаций ГК. Наибольшее распространение среди отечественных клиницистов получила классификация, предложенная А.Л. Мясниковым, подразделявшим ГК на два типа. ГК 1 типа характеризуются сравнительно легким и кратковременным течением. Обычно они развиваются на фоне удовлетворительного состояния внезапно. Субъективно больные ощущают головную боль, тяжесть в груди, сердцебиение, ощущение пульсации и дрожи, в тяжелых случаях это воспринимается как озноб. При резком повышении АД отмечается покраснение кожных покровов, особенно сильное на лице и шее. В моче может появляться белок и эритроциты. Нередко такой
криз сопровождается усугублением глазных симптомов («мушки», волны перед глазами, потемнение в глазах).
Возможны носовые кровотечения. В большинстве случаев повышение систолического давления как бы опережает повышение диастолического АД. Тогда пульсовое давление значительно превышает 50 мм рт.ст. На ЭКГ во время криза могут отмечаться изменения конечной части желудочкового комплекса в виде горизонтальной или косовосходящей депрессии интервала ST и/или сглаживания зубца T.
Однако у некоторых больных наблюдается диастолическая «обезглавленная» гипертония, при которой пульсовое АД ниже 30 мм рт.ст. Такой гипертонический криз также тяжело переносится больными. А вот купировать его достаточно сложно, так как большинство антигипертензивных лекарственных препаратов в большей степени влияют на уровень систолического АД, еще более уменьшая пульсовое давление.
В связи с повышением в крови катехоламинов при кризе может наблюдаться отчетливое повышение уровня глюкозы в крови, даже при отсутствии симптомов сахарного диабета. Этот феномен должен побудить врача к выявлению у больного феохромоцитомы, для которой характерны особенно тяжелые ГК.
Кризы 2 типа характеризуются постепенным повышением АД. В то же время таким кризам свойственно тяжелое затяжное течение. Частое возникновение таких трудно купируемых кризов может свидетельствовать о злокачественном течении гипертонии. Больные, как правило, жалуются на сильные головные боли, головокружения, часто сопровождающиеся рвотой, нарушениями со стороны зрения. Характерны также сжимающие боли в области грудной клетки. Как правило, при этом повышается и систолическое, и диастолическое давление.
ГК 2 типа при задержке с оказанием неотложной медицинской помощи часто заканчиваются транзиторными ишемическими атаками и инсультом, а также могут приводить к острому коронарному синдрому или инфаркту миокарда.
Методы купирования ГК будут изложены в разделе «лечение».
Гипертонический криз - это обострение АГ, которое характеризуется резким и значительным повышением уровня АД относительно привычных для конкретного больного значений с высоким риском развития инсульта или инфаркта миокарда.
примеры диагностических заключений
• Эссенциальная АГ или гипертоническая болезнь: степень - 1*; стадия I. Других факторов риска не выявлено. Риск 1 - низкий.
• Эссенциальная АГ или гипертоническая болезнь: степень - 2*; стадия II. Дислипидемия. Очаговое сужение артерий сетчатки. Риск 2 - средний.
• Эссенциальная АГ или гипертоническая болезнь: степень - 3*; стадия II. Дислипидемия. Гипертрофия левого желудочка. Генерализованное сужение артерий сетчатки. Риск 3 - высокий.
• Эссенциальная АГ или гипертоническая болезнь III стадии. Гипертонические кризы 2 типа. ИБС. Стенокардия напряжения II функциональный класс. Риск 4 - очень высокий.
• Эссенциальная АГ или гипертоническая болезнь II. Гипертоническиекризы 1 типа. Атеросклероз аорты, сонных артерий.Риск3 - высокий.
• Эссенциальная АГ или гипертоническая болезнь Степень - 1*. Стадия II. Облитерирующий атеросклероз сосудов нижних конечностей. Перемежающаяся хромота. Риск 4 - очень высокий.
• Эссенциальная АГ или гипертоническая болезнь 1 стадия. Сахарный диабет 2 типа (инсулиннепотребный). Риск 3 - высокий.
• Степень указывается у пациентов, не получающих антигипертензивную терапию. Особенно это важно для пациентов с впервые выявленной ЭАГ.
метаболический синдром и аг
Гипертония нечасто встречается как изолированный фактор риска. По данным Фрамингемского исследования, в 15-50% АГ сопровождается одним или несколькими из указанных в табл. 20.3 факторов риска: ожирение, гиперхолестеринемия (>240 мг%), гипо- α-холестеринемия (< 40 мг%), сахарный диабет II типа, гипертрофия левого желудочка сердца, курение и/или малоподвижный образ жизни. Связь ЭАГ и ожирения известна давно. Еще в 1922 году классик отечественной терапевтической школы Георгий Федорович Ланг указывал на связь гипертонической болезни с нарушениями углеводного обмена, ожирения и подагры. Он писал: «Считается, что гипертония чаще наблюдается у людей крепких, полнокровных, склонных к ожирению и подагре, отличающихся повышенной психической и нервной возбудимостью, обильно питающихся богатой белками (мясными) пищей и злоупотребляющих алкоголем». Тогда же еще молодые его ученики А.Л. Мясников и Д.Л. Гротэль отмечали, что у гипертоников часто повышена мочевая кислота и холестерин крови.
В 1948 году другой выдающийся отечественный клиницист Е.М. Тареев в монографии «Гипертоническая болезнь» указывал: «Представление о гипертонике особенно часто ассоциируется с ожирелым гиперстеником, с нарушением белкового обмена, с засорением крови продуктами неполного метаморфоза - холестерином, мочевой кислотой и т. д.».
В 60-х годах J. Camus предположил взаимосвязь между развитием гиперлипидемии, сахарного диабета 2 типа и подагры, назвав это сочетание метаболическим трисиндромом.
В начале 70-х годов прошлого века автор этих строк, исследуя метаболизм липопротеидов у больных с коронарным атеросклерозом, нашел, что больные с АГ отличаются от больных без АГ именно наличием высокой концентрации липопротеидов очень низкой плотности (пре-р-ЛП) (Бритов А.Н., 1974). В конце 1980-х годов H. Mehnert и H. Kuhlmann, A.R. Christlieb et al., M. Modan и др., L. Landsberg, E. Ferranini, H. Lithell независимо друг от друга отметили взаимосвязь между развитием у пациентов артериальной гипертонии, гиперлипидемии, инсулинорезистентности и ожирения. С 80-х годов подобный вид нарушений стали описывать, как «метаболический синдром».
В 1988 г. американский эндокринолог Gerald М. Reaven в своей актовой лекции, впоследствии опубликованной в журнале «Diabetes», впервые предложил термин «синдром X», в который включал тканевую инсулинорезистентность, компенсаторную гиперинсулинемию, нарушение толерантности к глюкозе, гипертриглицеридемию, снижение ХС-ЛВП и артериальную гипертонию (АГ). Каплан назвал это «смертельным квартетом».
Практически все указанные симптомы связывают с нарушением чувствительности тканей к инсулину. И все чаще стали писать о синдроме инсулинорезистентности, который изначально связывали с инсулин-независимым сахарным диабетом. Оказалось, что как АГ, так и абдоминальное ожирение являются также инсулинорезистентными состояниями.
Указанные выше компоненты метаболического синдрома чрезвычайно часты именно у гипертоников. Так, избыточная масса тела (индекс Кетле >25 кг/м2) встречается у 48% больных АГ, повышенный уровень общего холестерина (>5,2 ммоль/л) - у 85% и нарушения толерантности к глюкозе (включая сахарный диабет) - у 13%. Эти данные получены при метаанализе нескольких эпидемиологических исследований.
Существует несколько предположений, объясняющих частое сочетание АГ и сахарного диабета. Одно из них - нарушенная проницаемость клеточных мембран для ионов как у лиц с наследственной отягощенностью по АГ, так и при сахарном диабете II типа, осложненного нефропатией. Взаимоотношения АГ и сахарного диабета рассматриваются также в контексте полиморфизма гена АПФ. Как недавно было установлено, генотип DD указанного фермента ассоциирован с ИМ, особенно у лиц с изначально низким коронарным риском. Патогенетический механизм этого явления до конца неясен, хотя предполагают увеличение пролиферации и вазоспазма вследствие влияния измененного АПФ на уровень ангиотензина II и брадикинина в коронарных артериях.
Эпидемиологические исследования также подтверждают взаимосвязь высокого АД и нарушений толерантности к глюкозе, независимо от ожирения и массы тела. Причем недавно было показано, что АГ даже у лиц с нормальной массой тела в ряде случаев является инсулинорезистентным состоянием, коррелирующим с тяжестью АГ.
Среди метаболических факторов риска ССЗ сахарный диабет является важнейшим. Кроме того, в настоящее время уже точно установлено, что сахарный диабет II типа и АГ - ассоциированные заболевания (см. табл. 20.3, 20.4). Это обстоятельство следует учитывать при назначении антигипертензивной терапии.
Обычно для оценки массы тела используют так называемый индекс Кетле, который определяют как результат деления веса тела в кг на рост человека в м2. В норме индекс Кетле равен для мужчин 20 - 25, 26-30 считается избыточной массой тела, 30-40 - ожирением, >40 -патологическим ожирением. Критерии для женщин следующие: норма - 19-24, избыточная масса тела - 25-30, ожирение - 30-40, патологическое ожирение - >40.
Индекс Кетле не говорит о распределении жировой ткани и не учитывает два разных типа ожирения - андроидное и гиноидное, поэтому используют подсчет отношения «талия-бедро», которое вычисляется путем деления окружности талии, измеренной ниже грудной клетки над пупком на окружность бедер, измеренную на уровне ягодиц.
Считается, что индекс 0,8-0,9 характеризует промежуточный тип распределения жировой ткани, меньше 0,8 - гиноидный (бедренноягодичный), а 1,0 и больше - андроидный (абдоминальный) тип.
У лиц с «высоким» отношением «талия-бедро» с наибольшей частотой выявляются гиперинсулинемия (в том числе инсулинорезистентность), сахарный диабет, АГ и другие метаболические расстройства, например подагра. Более того, отношение «талия-бедро» считается лучшим предиктором систолической АГ, чем другие весоростовые параметры. В большинстве рекомендаций по АГ предлагается считать верхней границей нормы для объема талии 102 см для мужчин и 88 см для женщин.
С проблемой полиметаболического синдрома, по-видимому, связано взаимоотношение АГ и дислипидемии. Многочисленные исследования демонстрируют у лиц с АГ гиперхолестеринемию, гипертриглицеридемию и снижением холестерина липопротеидов высокой плотности. Часто указанные сочетания носят семейный характер, что, вероятно, связано с особенностями гена липопротеинлипазы.
Наконец, в последнее время ведутся активные поиски взаимосвязи АГ с нарушениями пуринового обмена. Так, по данным Бритова А.Н., Мухина Н.А. и соавт., при популяционном обследовании у 37,4% лиц
выявлены повышенный уровень мочевой кислоты в плазме крови и/или ее повышенная экскреция. Причем среди лиц с нарушениями пуринового обмена повышенное АД зарегистрировано в 2,5 раза чаще, чем в обследованной выборке в целом.
Можно предположить, что АГ у таких больных может быть проявлением уратной нефропатии или хронического тубулоинтерстициального нефрита, который, по данным клиники Н.А. Мухина, инициирует повышение артериального давления у 35% больных, причем у 12% из них развиваются нарушения мозгового кровообращения.
Не вызывает сомнения, что описываемая еще корифеями отечественной кардиологии (Г.Ф. Ланг, А.Л. Мясников, П.Е. Лукомский и др.) тесная связь АГ с атеросклерозом артерий, в значительной степени связана с общностью свойственных этим заболеваниям метаболическим изменениям. В последние десятилетия таким объединяющим патогенетическим фактором называют эндотелиальную дисфункцию. С позиции профилактической кардиологии приведенные данные указывают на необходимость оценки суммарного риска осложнений АГ у каждого больного с регистрацией основных метаболических показателей.
аг при беременности
Особого внимания заслуживает выявление АГ у женщин в период беременности. Согласно рекомендациям экспертов ВОЗ и МОАГ наличие повышенного уровня АД (см. табл. 19.2), как правило, у молодых женщин может быть двоякой природы. Если АГ выявляется на ранних сроках беременности, она расценивается как проявление ЭАГ (в некоторых случаях симптоматической АГ, но не в связи с беременностью). Если же АГ впервые выявляется с 20-й недели беременности, ее расценивают как осложнение беременности (гестоз). Саму эту форму АГ называют гестационной (ГАГ). По данным экспертов ВОЗ, ГАГ является основной причиной материнской и перинатальной смертности. Помимо общепринятого критерия для АГ, а именно уровень АД >140/90 мм рт.ст., для ГАГ предлагается дополнительный критерий - увеличение АД от первого к третьему триместру беременности на >30/20 мм рт.ст.
При ГАГ уровни АД колеблются в пределах 140-170/90- 110 мм рт.ст., в редких случаях отмечаются и более высокие уровни. Не типичным является изолированная систолическая гипертония. Сочетание ГАГ с протеинурией (концентрация белка >0,33 г/л) наблюдается примерно в 1-3% случаев, т.е. даже реже, чем протеинурия при нормальном уровне АД (Е.М. Вихляева, О.М. Супряга). Одним из клинических проявлений ГАГ являются судорожные припадки. По-видимому, именно сочетание ГАГ с протеинурией и эпизодами судорожных припадков следует рассматривать как прогностический фактор возможной эклампсии. К факторам риска эклампсии следует также относить появление гиперурикемии, гипоальбуминемии, повышение активности аланиновой и аспарагиновой трансаминаз, тромбоцитопению, повышение гематокрита за счет снижения объема циркулирующей плазмы.
Помимо эклампсии, ГАГ чревата для беременной задержкой внутриутробного развития плода, преждевременными родами, в редких случаях развитием ДВС-синдрома. Ведение больных с ГАГ осложняется опасностью тератогенных эффектов многих лекарственных антигипертензивных средств.
аг у женщин в постменопаузе
В молодом возрасте, согласно эпидемиологическим данным, ЭАГ у женщин встречается реже, чем у мужчин. Однако характер гипертонии уже в репродуктивном периоде у женщин имеет определенные особенности. Уровень АД, как правило, несколько выше во втором периоде менструального цикла. Значительные повышения АД могут быть одним из клинических проявлений предменструального синдрома.
После 50 лет (средний возраст наступления менопаузы) распространенность АГ у женщин становится существенно выше, чем у мужчин. Значение АГ как фактора риска становится также велико для женщин, как и для мужчин. В настоящее время можно считать доказанным, что снижение АД ведет к уменьшению риска сердечнососудистых осложнений у пациентов с АГ, независимо от пола. На смену первоначально скептическому мнению о пользе гипотензив-
ной терапии у женщин пришло утверждение о равнозначном подходе к стандартам лечения.
Имеющиеся данные свидетельствуют, что у пациентов с эссенциальной гипертонией имеются половые различия гемодинамических показателей. Так, у женщин обнаружены более высокая ЧСС в покое, увеличение сердечного индекса и пульсового давления наряду с более низкими значениями периферического сопротивления по сравнению с этими показателями у мужчин. Ряд исследователей обнаружили меньшую массу миокарда левого желудочка у женщин по сравнению с мужчинами при любом уровне АД. Однако половые различия исчезают после менопаузы. Более того, использование специфичных по полу критериев (134 г/м2 для мужчин и 110 г/м2 для женщин) показало, что ГЛЖ у больных, страдающих АГ, наблюдается среди женщин чаще, чем у мужчин того же возраста, причем у женщин преобладает концентрический тип ГЛЖ.
Использование метода САМАД позволило выявить больше случаев гипертонии «белого халата» у женщин, а также вариабельность АД по сравнению с мужчинами.
Вопрос о том, существуют ли преимущества применения той или иной группы антигипертензивных средств у женщин по сравнению с мужчинами, остается нерешенным. В крупных рандомизированных контролируемых исследованиях по изучению гипотензивных препаратов (TOMHS, MRC и др.), включавших мужчин и женщин, не было выявлено различий в эффективности и переносимости препаратов основных классов.
Большое внимание в настоящее время уделяется изучению влияния менопаузы, которая сопровождает возрастное снижение функции яичников. Женщины в постменопаузе представляют собой категорию высокого риска развития АГ и ИБС. Наступление менопаузы, независимо от возраста, сопровождается повышением уровня холестерина ЛНП и снижением холестерина ЛВП.
Также выявлено, что у женщин в постменопаузе чаще наблюдаются гипертриглицеридемия, нарушение толерантности к углеводам, нарушение параметров гемостаза с увеличением активности коагуляции. Необходимо учитывать, что некоторые факторы риска ИБС имеют большее значение у женщин по сравнению с мужчинами. К ним относятся сахарный диабет, низкий уровень холестерина ЛВП и высокий уровень триглицеридов.
Сочетание этих нарушений обмена и АГ являются основными компонентами метаболического синдрома X. В связи с этим можно предположить, что наличие этого синдрома у женщин сопровождается значительным повышением риска развития атеросклероза.
лечение
Общие принципы ведения больных. Основной целью лечения больного ГБ является достижение максимальной степени снижения общего риска сердечно-сосудистой заболеваемости и смертности. Это предполагает воздействие на все выявленные обратимые факторы риска, такие, как курение, высокий уровень холестерина и диабет, соответствующее лечение сопутствующих заболеваний, равно как и коррекции повышенного АД.
Таблица 20.5
Схема ведения больного с АГ 1-2 степени
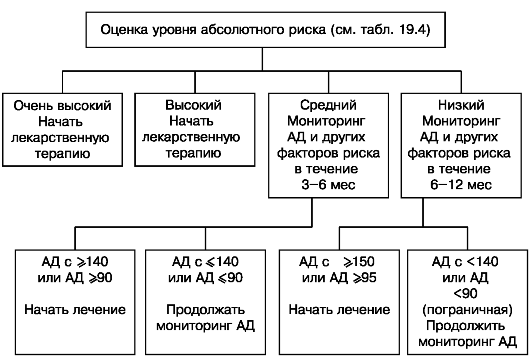 Интенсивность
лечения прямо пропорциональна уровню риска, определяемого по табл.
20.4. Целевым уровнем АД является уровень АД <140/90 мм рт.ст. У
больных сахарным диабетом необходимо снижать АД ниже 130/85 мм рт.ст.,
при ХПН с протеинурией более 1 г/сут ниже 125/75 мм рт.ст.
Интенсивность
лечения прямо пропорциональна уровню риска, определяемого по табл.
20.4. Целевым уровнем АД является уровень АД <140/90 мм рт.ст. У
больных сахарным диабетом необходимо снижать АД ниже 130/85 мм рт.ст.,
при ХПН с протеинурией более 1 г/сут ниже 125/75 мм рт.ст.
Достижение целевого АД должно быть постепенным и хорошо переносимым пациентом. Чем выше абсолютный риск, тем большее значение имеет достижение целевого уровня АД. В отношении сопутствующих АГ других факторов риска также рекомендуется добиваться их эффективного контроля, по возможности нормализации соответствующих показателей. Смена тактики антигипертензивной терапии при условии ее хорошей переносимости рекомендуется не чаще, чем через 4-6 нед. Продолжительность периода достижения целевого АД 6-12 нед.
• В группе низкого риска следует провести длительное наблюдение за больным (6-12 мес) перед принятием решения, назначать ли ему лекарственную терапию (табл. 20.5). Лекарственную терапию в этой группе назначают при сохраняющемся уровне АД более 150/95 мм рт.ст.
• Поскольку группа среднего риска чрезвычайно гетерогенна по уровню АД и характеру факторов риска, то решение о сроке начала медикаментозной терапии врач принимает с учетом всех этих факторов. Допустимо мониторирование АД в течение нескольких недель (при соблюдении рекомендуемой немедикаментозной терапии до 3-6 мес) для принятия решения о назначении лекарственной терапии. Ее следует начать при сохранении уровня АД >140/90 мм рт.ст.
• Если пациент отнесен к группе высокого и очень высокого риска, то следует назначить немедленный прием препаратов по поводу АГ и других факторов риска или сопутствующих заболеваний.
Немедикаментозная профилактика и терапия артериальной гипертонии. Принципы антигипертензивной терапии основываются на современных представлениях о том, что ЭАГ имеет собственные факторы риска. Если такие факторы риска, как возраст, наследственная предрасположенность, не могут быть скорригированы, то в отношении основных внешнесредовых факторов такая коррекция в принципе возможна. Всякая терапия или вторичная профилактика должна начинаться с модификации образа жизни пациента.
Мероприятия по изменению образа жизни рекомендуются всем больным, в том числе и получающим медикаментозную терапию. Они позволяют: снизить АД; уменьшить потребность в антигипертензивных лекарственных препаратах и максимально повысить их эффективность; благоприятно повлиять на другие имеющиеся факторы риска; осуществить первичную профилактику ЭАГ и снизить риск сопутствующих сердечно-сосудистых расстройств.
Немедикаментозные подходы к снижению артериального давления (АД) применимы к гипертоникам при любой степени повышения АД, а также и к тем лицам, чье давление считается нормальным. В последнем случае речь идет о первичной профилактике ЭАГ, поскольку эти подходы направлены не на снижение АД, а на предупреждение его повышений. Коротко говоря, мероприятия по изменению образа сводятся к диетической коррекции, оптимизации двигательной активности, сокращению потребления алкоголя и отказу от курения. Следовать здравому смыслу в соблюдении диеты и двигательной активности - основные составляющие здорового образа жизни, что в равной мере можно советовать не только для контроля ЭАГ, но и для предупреждения ишемической (коронарной) болезни сердца и мозга и для профилактики практически любых хронических неинфекционных заболеваний (ХНИЗ).
Итак, немедикаментозные методы включают.
• Отказ от курения.
• Снижение и/или нормализация массы тела (достижения индекса Кетле <25 кг/м2 у мужчин и <24 кг/м2 у женщин).
• Снижение потребления алкогольных напитков менее чем 30 г алкоголя в сутки у мужчин и менее 20 г/сут у женщин (при ряде сопутствующих заболеваний: заболевания печени, поджелудочной железы, алкоголизме и некоторых других употребление алкоголя следует полностью исключить).
• Увеличение физических нагрузок (регулярные динамические физические нагрузки, такие, как быстрая ходьба, бег трусцой, лыжные прогулки в среднем темпе, плаванье, по 30-40 минут в день, не менее 4-х раз в неделю).
• Снижение потребления поваренной соли до 5 г/сут. Следует помнить, что в большинстве продуктов гастрономии (сыры, колбасные изделия), а также в стандартных сортах хлеба уже содержится указанное (или большее) количество поваренной соли.
• Комплексное изменение режима питания:
1) увеличение употребления растительной пищи, что позволит увеличить потребление растительных волокон, а также калия, магния, содержащихся в овощах, фруктах, зерновых;
2) рекомендуется достаточное потребление обезжиренных молочных продуктов, содержащих полноценные белки и кальций;
3) потребность организма в белке (~100 г/день) рекомендуется также покрывать потреблением рыбы, нежирных сортов птицы и лишь изредка мяса. В морских сортах рыбы помимо полноценного животного белка содержится весьма полезный рыбий жир, богатый ω-3 ненасыщенными жирными кислотами;
4) соотношение насыщенных (животных), мононенасыщенных (оливковое масло) и полиненасыщенных (большинство растительных масел) должно быть, как 1:3,?1:3,?1:3, при 1:3 суточной потребности жира - 80-90 г.
Принципы лекарственной терапии. Если нормализации АД путем модификации образа жизни не достигнуто, то следует назначать пациенту лекарственную терапию, не отказываясь от продолжения немедикаментозного лечения. При этом следует соблюдать следующие принципы:
• Применять низкие дозы антигипертензивных средств на начальном этапе лечения, начиная с наименьшей дозировки препарата с целью уменьшить неблагоприятные побочные эффекты. Если имеется хорошая реакция на низкую дозу данного препарата, но контроль АД все еще недостаточен, целесообразно увеличить дозировку этого препарата при условии его хорошей переносимости.
• Применять препараты длительного действия, обеспечивающие эффективное снижение АД в течение 24 часов при однократном ежедневном приеме. Это снижает вариабельность АД в течение суток за счет более мягкого и продолжительного эффекта, а также улучшает приверженность больного к лечению.
• Использовать эффективные комбинации низких и средних доз антигипертензивных препаратов с целью максимального снижения АД и хорошей переносимости. При неэффективности первого препарата предпочтительнее добавление малой дозы второго препарата, чем повышение дозировки исходного. Перспективно использование фиксированных комбинаций малыми дозами.
• Проводить полную замену одного класса препарата на другой класс препаратов при низком эффекте или плохой переносимости без увеличения его дозировки или добавления другого лекарства.
• Комбинировать антигипертензивные препараты с препаратами, корригирующими другие факторы риска, прежде всего с дезагрегантами, гиполипидемическими и гипогликемическими препаратами.
Рекомендации для индивидуального выбора антигипертензивного препарата. В случаях неосложненной АГ при отсутствии установленных показаний для назначения других гипотензивных препаратов предпочтение следует отдавать диуретикам и β-адреноблокаторам. При наличии установленных показаний для лечения больных АГ можно использовать препараты из современных классов антигипертензивных препаратов, представленных в табл. 20.6. На выбор препарата оказывают влияние многие факторы, среди которых наиболее важными являются следующие:
Таблица 20.6
Алгоритм выбора лекарственной терапии ЭАГ
Особенности клинической картины и выбор лекарственных методов лечения: Неосложненная гипертония и нет сопутствующих заболеваний - диуретики или в-адреноблокаторы Сердечная недостаточность - Ингибиторы АПФ, блокаторы АТ-1, диуретики, карведилол. Метаболический синдром или сахарный диабет II типа с протеинурией - Ингибиторы АПФ, блокаторы АТ-1, диуретик-арифон, агонисты имидазолиновых рецепторов После перенесенного инфаркта миокарда - в-адреноблокаторы, ингибиторы АПФ Изолированная систолическая гипертония - Диуретики или антагонисты кальция Гипертрофия предстательной железы - α-адренергические блокаторы Лечение начинают с малых доз, предпочитая лекарства с длительным эффектом, дающимися один раз в день. Можно использовать комбинации малых доз нескольких препаратов |
• наличие факторов риска у данного больного;
• наличие поражений органов-мишеней, клинических проявлений сердечно-сосудистых заболеваний, болезней почек и сахарного диабета;
• наличие сопутствующих заболеваний, которые могут способствовать или ограничивать использование антигипертензивного препарата того или иного класса;
• индивидуальные реакции больных на препараты различных классов;
• вероятность взаимодействия с препаратами, которые пациент использует по другим поводам;
• социально-экономические факторы, включая стоимость лечения.
В 1993 г. эксперты ВОЗ и Международного общества по изучению гипертонии подтвердили использование на начальном этапе терапии диуретиков и β-адреноблокаторов, а также использование ингибиторов АПФ, антагонистов кальция и α-адреноблокаторов
как альтернативных медикаментов. Эти рекомендации основаны на том факте, что многочисленные многолетние исследования показали эффективность в отношении заболеваемости и смертности от сердечно-сосудистых поражений именно при применении диуретиков и β-адреноблокаторов как у молодых, так и у пожилых больных. К концу 90-х годов были завершены многолетние исследования в отношении других групп медикаментов. В Российских национальных рекомендациях говорится, что антигипертензивными препаратами первой ступени при лечении АГ может быть любой препарат из 6 классов антигипертензивных средств: (1) диуретики, (2) β-адреноблокаторы, (3) антагонисты кальция, (4) α-адреноблокаторы, (5) ингибиторы АПФ и (6) блокаторы рецепторов АТ1. Сюда можно добавить еще один класс - препараты центрального действия.
Проблема, когда начинать медикаментозное лечение, является не только медицинской, но и экономической. Если согласиться с рекомендациями лечить всех больных, чье АД остается на уровне, равном или выше 140/90 мм рт.ст., то в случае безуспешной попытки скорригировать его немедикаментозными подходами придется предписать постоянный прием лекарств дополнительно миллионам людей. Такой подход представляется достаточно радикальным. Стоит ли все это дополнительных средств и усилий?
Важно выявить преимущества, равно как и недостатки раннего медикаментозного вмешательства в процесс лечения гипертонии. Клинические опыты показывают статистически значимое снижение случаев инсульта (на 40-60%), КБС (на 16%), сердечной недостаточности и всей совокупной сосудистой смертности (на 21%) (см. рис. 20.1, 20.2).
Эти данные впечатляют. Но, возможно, некоторые врачи не вполне адекватно оценивают эффективность лечения, они не воспринимают данные о снижении случаев КБС, как результат только антигипертензивного лечения. Наибольшие споры в этом плане касаются гипертонии 1 степени, при которой индивидуальный риск в ближайшие годы оказаться «жертвой» инфаркта миокарда или другого проявления КБС действительно не столь велик.
Хотя, безусловно, этот риск выше, чем у лиц с нормальным АД. В то же время нельзя не учитывать, что гипертония 1 степени настолько массовое явление у мужчин старше 30 лет и у женщин старше 40 лет, что именно на эту часть населения приходятся большинство случаев таких конечных точек, как фатальные и нефатальные ИМ, инсульты, внезапная смерть.
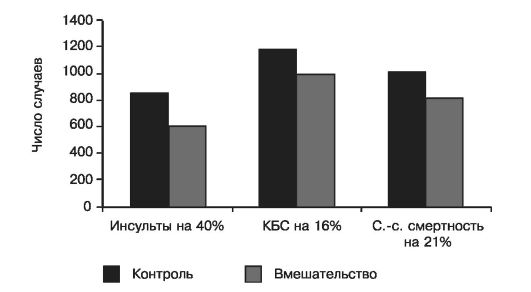 Рис. 20.1. Влияние
антигипертензивной лекарственной терапии на заболеваемость инсультами,
коронарной болезнью сердца и общую сосудистую смертность в семнадцати
многолетних клинических исследованиях. (Herbert P. Et al., Arch. Intern.
Med., 1993)
Рис. 20.1. Влияние
антигипертензивной лекарственной терапии на заболеваемость инсультами,
коронарной болезнью сердца и общую сосудистую смертность в семнадцати
многолетних клинических исследованиях. (Herbert P. Et al., Arch. Intern.
Med., 1993)

Рис. 20.2. Смертность от инсультов в популяциях медикаментозного вмешательства и сравнения. Объединенные данные 5-летней программы борьбы с АГ в организованных популяциях Москвы, Донецка и Чебоксар, 1978-83 годы (Бритов А.Н., Клин. Мед., 1984). Различия, полученные через 3*, 4* и 5** лет статистически достоверны
Специального внимания требуют пациенты с высоким нормальным АД (130-139/85-89 мм рт.ст.), у которых имеется сахарный диабет, почечная недостаточность и/или сердечная недостаточность. В этой группе больных требуется активная ранняя медикаментозная терапия, которая позволяет предупредить прогрессирование осложнений.
Популярным аргументом против широкого охвата медикаментозным лечением больных АГ является утверждение о том, что очень большое число людей должны лечиться с тем, чтобы лишь у небольшого процента из них не случились сердечно-сосудистые поражения. При этом не учитываются случаи прогрессирования гипертонии от менее тяжелой к более тяжелой. На табл. 20.7 показано сравнение плацебо эффекта с активным лечением именно по этому показателю прогрессирования болезни.
Таблица 20.7
Эффект лечения на прогрессирование гипертонии от менее тяжелой к более тяжелой (САД >200-210, ДАД >110-130 мм рт.ст.) в клинических опытах (по данным M. Moser and P. Hebert, 1996)
Группы больных АГ | Число случаев ухудшения | Число наблюдений |
Плацебо | 1493 | 13 342 |
Активное лечение | 95 | 13 389 |
Важным аспектом в лечении больных АГ является раннее выявление и целенаправленное воздействие на пораженные органы-мишени.
Особого внимания и своевременной коррекции требует выявленная у больных АГ микроальбуминурия. Установлено, что она является показателем эндотелиальной дисфункции и независимым фактором риска сердечно-сосудистой смертности. В последнее время пристальное внимание уделяется начальным проявлениям нарушений кровоснабжения мозга у больных АГ. Это органное поражение (в том числе дисциркуляторная энцефалопатия любых степеней) имеется, по нашим данным, у 24% больных АГ. Крайне неблагоприятны в плане возникновения ИМ патологические изменения магистральных сосудов шеи и головы. По данным ультразвуковой допплерографии, они выявляются у 30% больных АГ. К прогностически неблагоприятным проявлениям АГ относят также транзиторные ишемические атаки, изменения сосудов глазного дна и некоторые другие.
Как уже упоминалось, ГЛЖ, будучи не только фактором риска ИБС, но и пораженным органом-мишенью, значимо ухудшает прогноз больного АГ. Предупреждение гипертрофии левого желудочка слишком часто не учитывается при оценке успеха лечения. В клинических опытах на 6098 субъектах, получающих плацебо, ГЛЖ развилась у 216, а из 6150, получающих активное лечение, - у 140, т.е. статистически значимое снижение составило 35%.
Помимо возможности обратного развития гипертрофии левого желудочка, следует также делать акцент и на предупреждении сердечной недостаточности (СН) путем лечения гипертонии (табл. 20.8).
Таблица 20.8
Встречаемость ГЛЖ и СН в клинических опытах лечения гипертонии по данным 17 клинических исследований*
Число опытов | Лечение | Контроль | % снижения | 95% CI | |
ГЛЖ | 4 | 140/6150 | 216/6098 | 35 | 0,52-0,79 |
СН | 12 | 112/6914 | 240/6923 | 52 | 0,38-0,59 |
Примечание: *(М. Moser, 1998)
Другие факторы, на которые только в последние годы стали обращать внимание и учитывать при оценке лечебных программ, это улучшение качества жизни больных. Не говоря уже о немедикаментозных методах терапии, следует сказать, что при адекватной всем особенностям пациента лекарственной антигипертензивной терапии у большинства лиц с повышенным АД качество жизни улучшается.
Диуретики и β-адреноблокаторы - препараты первой медикаментозной ступени.
Каким же лекарственным препаратам должен отдавать предпочтение врач, если он решил лечить пациента с ЭАГ медикаментозно? Прежде чем ответить на такой вопрос, необходимо учесть опыт длительных исследований, посвященных изучению эффективности медикаментозных препаратов в отношении профилактики осложнений АГ. Суммарный анализ 17 таких исследований, проведенный в различных странах мира в 80-х годах прошлого века, свидетельствует о том, что эффективность медикаментозного лечения (в этих исследованиях использовались β-адреноблокаторы короткого действия и диуретики) проявилась только в отношении снижения инсультов (~ на 40%). Вместе с тем снижение смертности от ИБС оказалась значительно скромнее - всего на 14-16% (см. рис. 12.2). Сходные результаты были получены и нами при проведении программы борьбы с АГ в организованных популяциях 23 городов (А.Н. Бритов, 1984). В указанной программе на первой медикаментозной ступени применялся чаще всего тиазидовый диуретик гипотиазид. В конечном счете из всех регистрируемых конечных точек наибольший эффект отмечен в отношении инсультов (см. рис. 12.3), в отношении заболеваемости и смертности от ИМ успехи не были столь впечатляющими, хотя
и было отмечено статистически значимое снижение нефатальных инфарктов миокарда и общей смертности (~ на 16%).
Поскольку ИБС чаще всего ассоциируется с АГ, в целом результаты эффективности ее длительного медикаментозного лечения оцениваются как недостаточные. Объяснение этого феномена сводится к трем главным причинам. Во-первых, применяемые в указанных исследованиях β-адреноблокаторы имеют, как правило, короткое действие (4-6 ч). Такие препараты (например, пропранолол) не обеспечивали стабильного снижения АД в течение суток и прежде всего в утренние и предутренние часы, когда у лиц с АГ наиболее часто развиваются инфаркты миокарда и внезапная смерть. Во-вторых, β-адреноблокаторы короткого действия и диуретики при длительном применении вызывали ряд метаболических нарушений: нарушение липидного обмена, снижение толерантности к глюкозе, снижение чувствительности тканей к инсулину, что могло нивелировать эффект снижения АД. И наконец, медикаментозная профилактика слишком часто не сопровождалась немедикаментозной коррекцией факторов риска, о важности которой говорилось выше. И все же при широком применении диуретиков и/или β-адреноблокаторов, как правило, обеспечивается одна из главных целей терапии - продление жизни. В уже упомянутой отечественной программе было показано, что активное выявление и длительное лечение больных АГ в популяции обеспечивает сохранение 65 жизней за пять лет вмешательства в пересчете на 10 000 взрослого населения.
В этих клинических опытах успех терапии диуретиками отмечался более стабильно (особенно у пожилых) по сравнению с β-адреноблокаторами. Использование β-адреноблокаторов, однако, приводило к более выраженному снижению случаев внезапной смерти, нефатальных инфарктов миокарда, общей смертности. Эти данные учитываются и в международных рекомендациях, где также предлагается начинать антигипертензивную терапию с диуретиков или β-адреноблокаторов, если нет специальных показаний для другой лекарственной терапии.
Диуретики (табл. 20.9) являются одним из наиболее ценных классов гипотензивных средств. Их отличают низкая или умеренная стоимость, высокая эффективность, хорошая переносимость и доказанное положительное влияние на сердечно-сосудистую заболеваемость и смертность.
Клиническая ценность диуретиков подтверждена при сравнении их с новыми классами антигипертензивных средств в ряде многоцентровых исследований: STOP, Нурегtеnsion-2, САРРР, ALLHAT. Большинство нежелательных эффектов, таких, как гипокалиемия, нарушение толерантности к глюкозе, дислипидемия, импотенция, описаны в основном при применении высоких доз диуретиков. Доказанной метаболической нейтральностью обладает индапамид, в ретардной форме эффективный в суточной дозе 1,5 мг. Оптимальная доза наиболее изученного тиазидного диуретика гидрохлортиазида составляет 12,5 мг. В очень низких дозах диуретики повышают эффект других препаратов и не дают нежелательных метаболических эффектов.
Обычное лечение АГ (без сопутствующей сердечной недостаточности) не предполагает использования калийсберегающих и петлевых диуретиков.
При назначении диуретиков рекомендуется контроль содержания калия в сыворотке крови через 3-4 недели после начала лечения. При использовании больших доз рекомендуется также периодический контроль ЭКГ. В качестве препаратов выбора диуретики рекомендуют применять у пожилых людей, больных с изолированной систолической гипертонией, СН.
β-Адреноблокаторы (табл. 20.10) являются эффективными, безопасными и относительно недорогими средствами, которые можно использовать как для монотерапии, так и в комбинации с диуретиками, дигидропиридиновыми антагонистами кальция и α-адреноблокаторами.
β-Адреноблокаторы в первую очередь рекомендуют назначать при наличии стенокардии, перенесенного инфаркта миокарда, а также при тахиаритмии, сердечной недостаточности. В качестве возможных показаний к их преимущественному использованию обсуждаются беременность в 3 триместре и сахарный диабет II типа. При сердечной недостаточности β-адреноблокаторы следует назначать в низкой дозе, которую затем медленно титруют.
Побочные действия β-адреноблокаторов - появление атриовентрикулярной блокады любой степени, появление или обострение бронхообструкции (в меньшей степени свойственно кардиоселективным препаратам), усиление синдрома Рейно, синдрома перемежающейся хромоты, нарушение толерантности тканей к углеводам,
в больших дозах - усугубление застойной сердечной недостаточности, импотенции у мужчин. Препараты противопоказаны при обструктивных заболеваниях легких, заболеваниях периферических сосудов, нарушениях сердечной проводимости. Требуется уточнение целесообразности применения β-адреноблокаторов при дислипидемии, у спортсменов и физически активных лиц.
Таблица 20.9
Диуретики, применяемые для лечения АГ
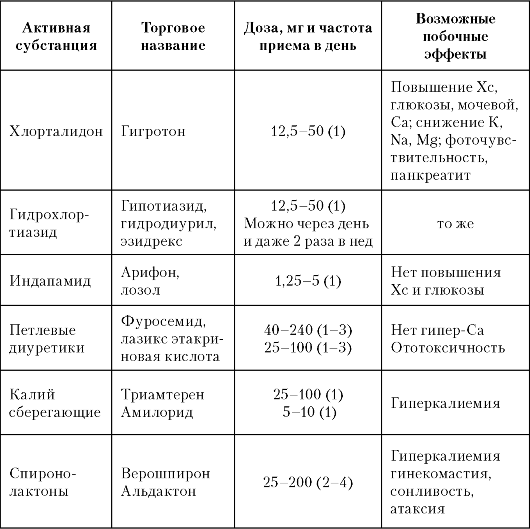 Таблица 20.10 β-Адреноблокаторы, применяемые для лечения АГ
Таблица 20.10 β-Адреноблокаторы, применяемые для лечения АГ
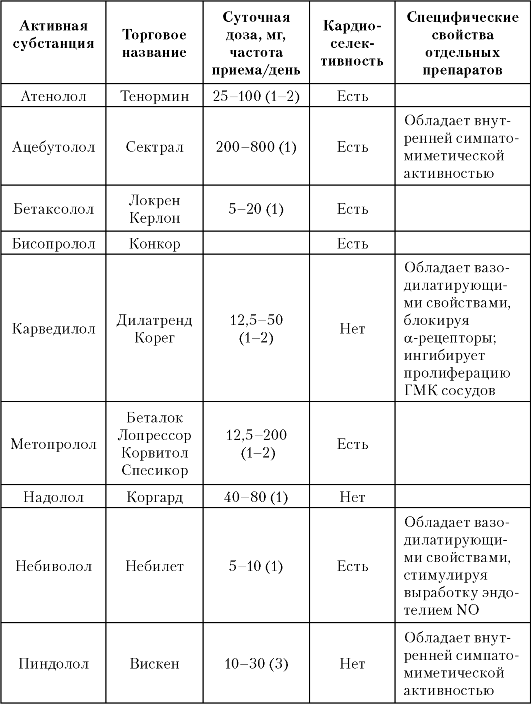
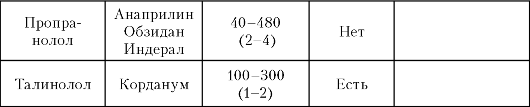 Блокаторы кальциевых канальцев (БКК) (табл. 20.11). БКК -
Блокаторы кальциевых канальцев (БКК) (табл. 20.11). БКК -
широко применяемая группа антигипертензивных лекарств, так как они снижают АД и хорошо переносятся большинством людей. Преобладает представление о том, что БКК являются хорошими вазо- и кардиопротекторами. Недавние исследования показали, что применение БКК у гипертоников урежает случаи смертельных и несмертельных инсультов, однако нет столь же определенных данных в отношении случаев КБС.
В то же время эта группа лекарств вызывает наибольшее число противоречивых оценок, чем любая другая. Есть данные о благоприятном влиянии БКК на сосудистую стенку при экспериментальном атеросклерозе. Большинство врачей, опираясь на данные о благоприятном влиянии на коронарный кровоток, считают их средством выбора у больных с гипертонией и сопутствующей КБС. Тем неожиданнее прозвучали сообщения (Psaty et al, 1995), о том, что у больных гипертонией, получающих БКК, на 60% (!) чаще отмечаются новые случаи инфаркта миокарда по сравнению с больными, леченными диуретиками. Эти публикации основывались на ретроспективном анализе данных американских практических врачей.
Эти неожиданные для врачебной общественности данные вызвали много споров и обсуждений. Так, на конференции Совета по лечению сердечно-сосудистых и почечных заболеваний «Американской администрации по продуктам питания и лекарствам» была констатирована неправомочность обвинений в адрес целого класса лекарств на основании только ретроспективного анализа данных практических врачей, так как весьма вероятно, что последние отдавали предпочтение БКК у больных с уже определенной коронарной болезнью сердца. Кроме того, было отмечено, что назначались преимущественно дигидропиридиновые БКК с коротким периодом действия (нифедипин), которые действительно являются не вполне
подходящими для лечения гипертонии. Alderman с соавт. отметили, что короткодействующие БКК почти в три раза чаще ассоциируются с коронарными конечными точками, чем диуретики. Зато БКК пролонгированного действия в этом отношении оказались примерно на 40% эффективнее.
Таблица 20.11
Блокаторы кальциевых канальцев, применяемые для лечения гипертонии
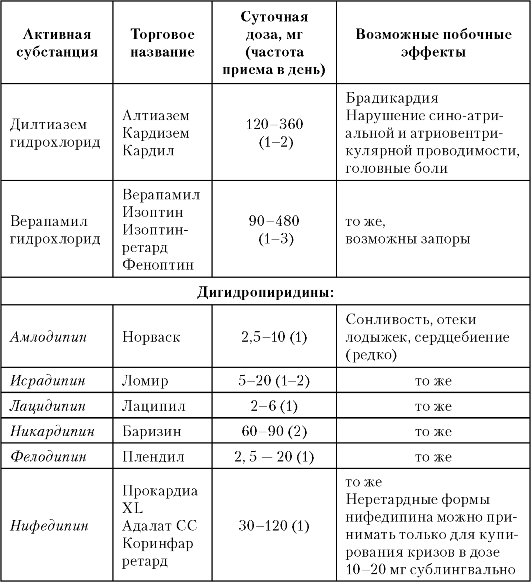 Другие
авторы также подтверждают благоприятный и безопасный эффект
пролонгированных БКК. К таким исследованиям относятся многоцентровое
европейское исследование «Syst Euro Trial» (Staessen et al., 1997), HOT
Study, китайское исследование, проведенное в Шанхае. В этих
исследованиях показано, что БКК в не меньшей степени, чем диуретики и ББ
эффективны в плане профилактики инсультов и других сердечно-сосудистых
конечных точек и могут служить удачной альтернативой для первой
медикаментозной ступени антигипертензивной терапии. Негидропиридиновые
БКК могут снижать частоту повторных инфарктов.
Другие
авторы также подтверждают благоприятный и безопасный эффект
пролонгированных БКК. К таким исследованиям относятся многоцентровое
европейское исследование «Syst Euro Trial» (Staessen et al., 1997), HOT
Study, китайское исследование, проведенное в Шанхае. В этих
исследованиях показано, что БКК в не меньшей степени, чем диуретики и ББ
эффективны в плане профилактики инсультов и других сердечно-сосудистых
конечных точек и могут служить удачной альтернативой для первой
медикаментозной ступени антигипертензивной терапии. Негидропиридиновые
БКК могут снижать частоту повторных инфарктов.
В настоящее время предпочтение при длительном антигипертензивном лечении необходимо отдавать тем препаратам или их лекарственным формам, которые обеспечивают стабильное снижение АД в течение суток и не вызывают метаболических нарушений. К числу таких препаратов прежде всего относятся ретардные формы БКК, в том числе дигидропиридины (амлодипин, фелодипин и другие). При этом указанные препараты, как большинство антагонистов кальция, не вызывают отрицательных метаболических эффектов. Из других антагонистов кальция длительного действия заслуживают внимания изоптин ретард-240 мг, альтиазем - ретардная форма дилтиазема. Основные препараты из группы БКК, применяемые для лечения АГ, представлены в табл. 20.9.
Ингибиторы ангиотензинпревращающего фермента (ИАПФ) (табл. 20.12.). Основой этого класса лекарств послужило открытие, сделанное около 25 лет назад, о том, что РААС тесно связана с сердечно-сосудистым прогнозом больных гипертонией (Brunner, Laragh, Baer et al., 1972).
Какие же результаты мы имеем? Например, относительно больных с застойной сердечной недостаточностью известно, что применение ИАПФ улучшают состояние больных, уменьшают необходимость в госпитализации и, что самое главное, продлевают жизнь. Получены данные при наблюдении за пациентами с ИМ, у которых повреждена сократительная функция левого желудочка. Применение ИАПФ у таких больных не только помогает эффективно лечить СН, но и снижает вероятность развития повторных инфарктов миокарда. Было показано, что новые случаи коронарной болезни сердца у больных АГ при лечении ИАПФ наблюдается на 40 и 50% реже, чем при лечении диуретиками и ББ.
Таблица 20.12 Ингибиторы АПФ, применяемые для лечения АГ
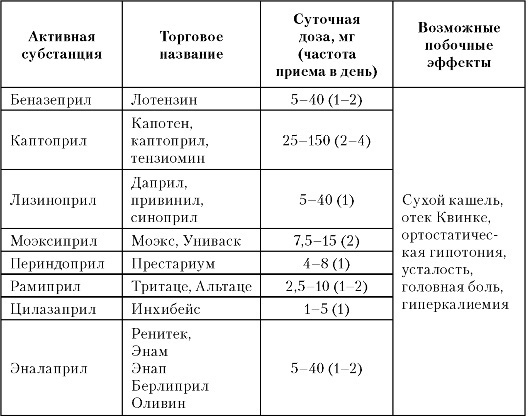 Одна
из труднейших задач, стоящих перед врачом, - профилактика повторных
инсультов при АГ, также у лиц высоким нормальным АД после первого
инсульта. Многоцентровое исследование PROGRESS продемонстрировало
снижение повторных инсультов на 28% при применении периндоприла в дозе 2
или 4 мг в день. У большей части больных ИАПФ применялся в комбинации с
диуретиком индапамидом. Эффективность лечения была достаточной при
любом исходном уровне АД, в том числе при нормотонии. В исследовании
выявлено также достоверное снижение всех сердечно-сосудистых органных
поражений на 26%, риска когнитивных нарушений (в том числе деменции) на
45% и инвалидности на 27%.
Одна
из труднейших задач, стоящих перед врачом, - профилактика повторных
инсультов при АГ, также у лиц высоким нормальным АД после первого
инсульта. Многоцентровое исследование PROGRESS продемонстрировало
снижение повторных инсультов на 28% при применении периндоприла в дозе 2
или 4 мг в день. У большей части больных ИАПФ применялся в комбинации с
диуретиком индапамидом. Эффективность лечения была достаточной при
любом исходном уровне АД, в том числе при нормотонии. В исследовании
выявлено также достоверное снижение всех сердечно-сосудистых органных
поражений на 26%, риска когнитивных нарушений (в том числе деменции) на
45% и инвалидности на 27%.
Антигипертензивная терапия у больных с АГ и сахарным диабетом должна преследовать не только достижение оптимального гипотензивного эффекта (как правило, следует добиваться полной нормализации уровней АД), но и обеспечивать эффективный контроль метаболических нарушений, массы тела, предупреждать свойственные диабету сердечно-сосудистые осложнения. В наибольшей мере этим условиям отвечает применение ИАПФ. У больных с диабетической нефропатией ИАПФ не только осуществляют нефропротекцию, но и показывают тенденцию продлевать жизнь больных.
Таким образом, при наличии сердечной и/или почечной недостаточности или сахарного диабета у пациентов с повышенным АД или с верхней границей нормального АД (130-139/85-89 мм рт.ст.) показано медикаментозное лечение. Накапливается все больше данных исследований, основанных на доказательствах (ABCD, FACET, HOPE, ALLHAT и другие) и свидетельствующих о том, что предпочтение в таких случаях следует отдавать ингибиторам АПФ.
Блокаторы ангиотензиновых рецепторов (БАР). Блокаторы ангиотензиновых рецепторов - АТ-1, в частности, наличествующие на отечественном рынке вальсартан (диован), лозартан (казаар), эпросартан (теветен) и ирбесартан (авапро), являются принципиально новым классом гипотензивных средств. По механизму действия они отличаются от ИАПФ, в противоположность которым при блокаде рецепторов ангиотензина происходит даже увеличение уровня AT II, которые, в свою очередь, стимулируют незаблокированные рецепторы. Результатом этого является вазодилятирующий и антипролиферативный эффект.
Хотя эффективность БАР сопоставима с другими лекарствами, но они очень хорошо переносятся из-за незначительного числа побочных эффектов, которое практически не отличается от эффекта плацебо. Предварительные данные показывают, что БАР, как и ИАПФ, оказывают прямой благоприятный эффект в отношении сосудистых структур. В частности, БАР восстанавливают функцию эндотелия при его исходной дисфункции. Есть работы, опубликованные создателями БАР, о том, что предприняты исследования по оценке их влияния на сердечно-сосудистые конечные точки. Недавно появились данные программы ELITE, в котором лозартан оказался значительно более эффективным, чем один из ИАПФ каптоприл в снижении летальности больных с сердечной недостаточностью (Weber, 1997).
Постсинаптические a1-адреноблокаторы. Постсинаптические a1-адреноблокаторы - празозин (пратсиол, адверзутен), доксазозин (кардура, тонокардин) и теразозин оказались весьма эффективными средствами для лечения ЭАГ практически при любой степени повышения АД и при любой стадии заболевания. Многие авторы особо отмечали то обстоятельство, что данная группа препаратов благоприятно влияла и на липидный обмен, который нередко нарушен при АГ. В частности, α-адреноблокаторы способствовали снижению уровня плазменного холестерина липопротеидов низкой плотности и, наоборот, - повышению холестерина липопротеидов высокой плотности. Другим важным преимуществом является благоприятное влияние на гипертрофию простаты у мужчин. Однако при практическом использовании празозина выявилось одно существенное неудобство. Речь идет об эффекте первой дозы, при назначении которой нередко отмечались приступы резкого ортостатического снижения АД вплоть до коллапса. Причем, если по какой-то причине больной даже на короткое время прерывал лечение, при его возобновлении эти приступы могли возникнуть вновь. Кроме того, a-адреноблокаторы могут неблагоприятно влиять на сократительную функцию миокарда. В 2000 г. комитет по безопасности исследования ALLHAT прервал применение α-адреноблокатора - доксазозина в связи с достоверно большей частотой возникновения смертельно опасных осложнений, в частности развитием застойной сердечной недостаточности по сравнению с таковой при других схемах лечения.
Антигипертензивные препараты центрального действия. Антигипертензивные препараты центрального действия представлены такими старыми средствами, как резерпин, метилдопа (допегит), клонидин (клофелин, катапрессан), а также новым средством - моксонидином. Клонидин и метилдопа действуют как агонисты центральных α2-рецепторов. Моксонидин является агонистом так называемых имидазолиновых рецепторов. В отличие от старых препаратов моксонидин практически не имеет серьезных побочных эффектов. Он оказывает благоприятное влияние на показатели липидного и углеводного метаболизма, что позволяет применять его для лечения АГ при метаболическом синдроме и при сахарном диабете.
Метилдопа наиболее широко применяется при гипертонии беременных, так как это практически единственный из антигипертензивных препаратов, не оказывающих влияния на плод. Резерпин и кло-
нидин в настоящее время не рассматриваются как препараты первой ступени из-за их психотропного воздействия. Клонидин отличает быстрый гипотензивный эффект, поэтому его применяют для купирования гипертонических кризов.
Нельзя не сказать о важном преимуществе резерпина и клонидина, их дешевизне. Это привлекает к названным препаратам многих пациентов. Если у них нет возможности лечиться современными препаратами, то врач может согласиться с таким лечением. Но при условии тщательного контроля за больными. Следует обращать внимание на динамику АД в течение суток, как правило, стабильного антигипертензивного эффекта при такой терапии достичь не удается. Более того, постоянный прием клонидина вызывает толерантность к препарату, это побуждает врача все больше наращивать дозу, увеличивая вероятность побочных эффектов. Нужно помнить, при приеме резерпина и особенно клонидина не допускается одновременный прием алкоголя. Этим больным нельзя управлять транспортными средствами.
Комбинированная антигипертензивная терапия. Исследования последних лет убедительно продемонстрировали необходимость применения двух или более препаратов у большинства пациентов для достижения адекватного контроля АД без ухудшения качества жизни. В исследовании НОТ, в частности, было показано, что для снижения диастолического АД до уровня 80 мм рт.ст. 3/4 пациентов потребовалась комбинированная антигипертензивная терапия.
При наличии АГ 2-3 степени рациональные комбинации препаратов в низких дозах могут быть использованы уже на начальном этапе медикаментозной терапии. Эффективная комбинация препаратов подразумевает использование препаратов из различных классов с разным механизмом действия с целью получения дополнительного гипотензивного эффекта и уменьшения нежелательных явлений. Нерационально комбинирование препаратов с одинаковым механизмом действия (усиление компенсаторных механизмов повышения АД) и сходным спектром нежелательных явлений (табл. 20.13).
Поскольку, как уже указывалось, ЭАГ весьма часто сочетается с другими факторами риска и сопутствующими заболеваниями, то перед врачом встает вопрос о комбинации антигипертензивных средств с другими лекарствами. Сейчас уже не вызывает сомнения целесообразность одновременной коррекции дислипопротеидемии,
нарушенной толерантности к глюкозе, дисгормональных нарушений, например, при климактерическом или посткастрационном синдроме у женщин или лечения таких заболеваний, как хронический бронхит и бронхиальная астма, язвенная болезнь желудка и двенадцатиперстной кишки, заболеваний центральной и периферической нервной системы и т.д. Применение аспирина или других антиагрегантов существенно усиливает профилактический эффект антигипертензивной терапии в плане предупреждения ишемического инсульта и инфаркта миокарда.
Таблица 20.13
Комбинированная терапия артериальной гипертонии
Предпочтительные комбинации: Диуретик + β-адреноблокатор Диуретик + ингибитор АПФ Диуретик + блокатор рецепторов ангиотензина II Антагонист кальция (дигидропиридиновый) + β-адреноблокатор Антагонист кальция + ингибитор АПФ a1-Адреноблокатор + β-адреноблокатор Менее предпочтительные, но допустимые комбинации Антагонист кальция + диуретик β-Адреноблокатор + ингибитор АПФ Недопустимые комбинации: β-Адреноблокатор + верапамил или дилтиазем Антагонист кальция + а1-адреноблокатор |
Клинически значимые последствия комбинированного применения антигипертензивных препаратов с рядом других средств представлены в табл. 12.14.
Таблица 12.14
Клинически значимые взаимодействия антигипертензивных препаратов
Класс препаратов | Усиление эффективности | Ослабление эффективности | Влияние на другие препараты |
Диуретики | Диуретик с иной точкой приложения в нефроне(например, фуросемид + гипотиазид) | Нестероидные противовоспалительные препараты (НПВП) Стероиды | Повышение уровня лития Калийсберегающие диуретики + ингибиторы АПФ: возможное усугубление гиперкалиемии |
β-Адреноблокаторы | Для препаратов, метаболизирующихся в печени: циметидин, хинидин | НПВП Отмена клонидина Препараты, индуцирующие печеночные ферменты (рифампицин, фенобарбитал) | Пропранолол, индуцируя печеночные ферменты, повышает клиренс препаратов с аналогичным метаболизмом Нивелирование и пролонгирование инсулининдуцированной гипогликемии Нарушение проводимости при комбинированном применении с недигидропиридиновыми антагонистами кальция Усиление кокаининдуцированной стенокардии |
Ингибиторы АПФ | Хлорпромазин Клозапин | НПВП Антациды | Может повышаться уровень лития Усиление гиперкалиемии калий-сберегающих диуретиков |
Продолжение табл. 20.14
Антагонисты кальция | Грейпфрутовый сок Циметидин, ранитидин (антагонисты кальция,метаболизирующиеся в печени) | Препараты, индуцирующие печеночные ферменты (рифампицин, фенобарбитал) | Дилтиазем и верапамил повышают уровень циклоспорина Недигидро-пиридины повышают уровень препаратов, метаболизирующихся с участием тех же ферментов систем печени (дигоксин, хинидин, сульфаниламиды, теофиллин) Верапамил - снижение уровня лития |
а-Адреноблокаторы | Для препаратов, метаболизирующихся в печени: циметидин, хинидин | НПВП Отмена клонидина Препараты, индуцирующие печеночные ферменты (рифампицин, фенобарбитал) | Празозин может повышать клиренс верапамила |
Центральные а.2-адренерги- ческие агонисты | Трициклические антидепрессанты и фенотиазины Ингибиторы моноаминоксидазы Симпатомиметики и антагонисты фенотиазинов Соли железа уменьшают всасывание метилдопы | Метилдопа - повышение уровня лития Усиление эффекта отмены клонидина β-адреноблокаторами Клонидин потенцирует действие многих анестетиков |
Продолжительность лечения. Переход на другую ступень лечения. АГ требует постоянного лечения индивидуально подобранным препаратом или их комбинацией. Недопустимо курсовое, прерывистое лечение АГ. Если препарат первого выбора в адекватной дозе не дает достаточного эффекта, то можно добавить препарат другого класса или заменить первый препарат в случае плохой его переносимости на другой. Интервал между ступенями (этапами) лечения должен составлять не менее 4 недель при отсутствии необходимости в более быстром снижении АД или непереносимых нежелательных явлениях, например при аллергических осложнениях.
Препаратом второго ряда обычно является диуретик, если он не был использован на первой ступени, так как он усиливает действие других антигипертензивных средств. Если второй препарат обеспечивает адекватный контроль АД, то можно обсудить возможность отмены первого препарата. Прежде чем изменить терапию, необходимо оценить возможные причины ее недостаточной эффективности. Если АГ удается контролировать в течение, по крайней мере, 1 года, то можно попытаться уменьшить дозы и число антигипертензивных средств. Переходить на более низкую ступень лечения следует постепенно. Чаще это удается сделать пациентам, которые одновременно устраняют факторы риска, следуя немедикаментозной программе лечения.
Частые экстренные и плановые госпитализации больных АГ являются в определенной мере результатом распространенной порочной практики краткосрочного курсового лечения, нерационального комбинирования препаратов, установки на так называемое рабочее АД, которое практически никогда не соответствует целевому АД. Для решения этой крайне обременительной для бюджета проблемы необходим существенный пересмотр тактики амбулаторного ведения больных. В период госпитализации пациентов акцент смещается на решение краткосрочных задач гипотензивной терапии. В связи с этим в госпитальной практике представляется обоснованным преимущественное применение короткодействующих гемодинамически активных препаратов с последующим переходом на прием длительно действующих препаратов в амбулаторных условиях. Целесообразно ориентироваться на краткосрочные, среднесрочные и долгосрочные цели терапии (табл. 20.15).
Таблица 20.15
Цели и критерии эффективности антигипертензивной терапии
Краткосрочные (1-6 мес от начала лечения) |
Достижение целевого уровня АД или снижение систолического и/или диастолического АД на 10% и более Эффективное предупреждение гипертонических кризов Улучшение или сохранение качества жизни Благоприятное влияние на модифицируемые факторы риска |
Среднесрочные (>6 мес от начала лечения) |
Достижение целевых значений АД Отсутствие поражений органов-мишеней или обратная динамика имевшихся осложнений Устранение модифицируемых факторов риска |
Долгосрочные (через 1 год и более) |
Стабильное поддержание АД на целевом уровне Отсутствие прогрессирования поражения органов-мишеней Компенсация имеющихся сердечно-сосудистых осложнений |
Злокачественная АГ и рефрактерность к лечению
Критерием рефрактерности АГ к лечению является снижение САД менее чем на 15% и ДАД менее чем на 10% от исходного уровня на фоне рациональной терапии с использованием адекватных доз трех антигипертензивных препаратов и более.
Отсутствие адекватного контроля АД более чем у 2/3 пациентов обусловлено несоблюдением режима лечения (псевдорефрактерность). Другая наиболее распространенная и легко устранимая причина этого явления - избыточное потребление поваренной соли или явное несоблюдение рекомендаций по немедикаментозной терапии. Причиной истинной рефрактерности к лечению часто бывает перегрузка объемом, связанная с неадекватной диуретической терапией
(табл. 20.16).
Таблица 20.16
Причины неадекватного снижения АД
Псевдорезистентность Отсутствие приверженности лечению Перегрузка объемом Избыточное потребление поваренной соли Неадекватная диуретическая терапия «Гипертония белого халата» Псевдогипертония у пожилых людей Использование обычной манжетки у больного с ожирением | Лекарственные причины: Низкие дозы антигипертензивных средств Нерациональные комбинации препаратов Взаимодействия с другими препаратами (НПВС, симпатомиметики, оральные контрацептивы, антидепрессанты и т.д.) |
Сопутствующие заболевания и состояния: Прогрессирующий нефросклероз Курение Нарастающее ожирение Ночное апноэ Инсулинорезистентность/гиперинсулинемия Злоупотребление алкоголем Поражение головного мозга | |
Истинная рефрактерная к лечению АГ чаще наблюдается при паренхиматозных заболеваниях почек, реже - при гипертонической болезни. Отсутствие желаемого гипотензивного эффекта у некоторых больных с реноваскулярной гипертонией и опухолями коркового или мозгового слоя надпочечников не следует расценивать в качестве истинной рефрактерности к лечению, так как проведение соответствующего оперативного вмешательства улучшает возможности контроля за уровнем АД, а в ряде случаев приводит к полной его нормализации.
Критериями диагностики злокачественной АД (первичной или любой формы вторичной АГ) являются повышение АД до 220/130 мм рт.ст. и выше в сочетании с ретинопатией III-IV степени по КейтуВегенеру, а также фибриноидный артериолонекроз, выявляемый при микроскопии биоптатов почек. Проведение биопсии почки не счита-
ют обязательным, учитывая ее травматичность и отсутствие полного соответствия между морфологическими изменениями в почках, сетчатке и головном мозге.
Из всех случаев выявления злокачественной АГ 40% приходятся на долю больных с феохромоцитомой, 30% - больных с реноваскулярной гипертонией, 12% - больных с первичным альдостеронизмом, 10% - больных с паренхиматозными заболеваниями почек, 2% - больных с гипертонической болезнью, 6% - на долю больных с остальными формами симптоматической АГ (склеродермия, узелковый периартериит, опухоли почек и др.). Особенно часто злокачественную АГ выявляют у пациентов с сочетанными формами АГ и при множественной эмболии мелких ветвей почечных артерий холестериновыми частицами (у 50% таких больных).
Тактика лечения больных с рефрактерной к лечению и злокачественной АГ во многом сходная. Обязательно одновременное назначение этим больным комбинации из 3-5 антигипертензивных препаратов в достаточно высоких дозах: ингибиторов АПФ, антагонистов кальция, β-адреноблокаторов, диуретиков, а в ряде случаев также антагонистов α2- или имидазолиновых рецепторов, блокаторов рецепторов ангиотензина II, αl-блокаторов. При отсутствии адекватного антигипертензивного эффекта на фоне комбинированной терапии проводят курс внутривенных инфузий нитропруссида натрия (3-5 инфузий), простагландина Е2 (2-3 инфузии) или применяют экстракорпоральные методы лечения: плазмофорез, гемосорбцию, ультрафильтрацию (при застойной сердечной недостаточности), иммуносорбцию (при выраженной гиперхолестеринемии), гемофильтрацию (при повышении уровня креатинина в крови до 150-180 мкмоль/л).
С целью предупреждения церебральных и коронарных осложнений и быстрого прогрессирования почечной недостаточности на первом этапе у больных с рефракторной к лечению и злокачественной АГ следует стремиться к снижению АД на 20-25% от исходного уровня. В последующем, также соблюдая предосторожность, следует стараться достигнуть уровня АД 140/90 мм рт.ст. Постепенное снижение АД необходимо для адаптации жизненно важных органов к новым условиям кровоснабжения.
Купирование гипертонических кризов
Гипертонический криз является острой ситуацией, угрожающей тяжелыми органными осложнениями и даже жизни больного, к его лечению (купированию) следует приступать немедленно после установления диагноза ГК.
Врач должен учитывать не только степень и скорость подъема АД, но также проявления и выраженность органных нарушений, нарушений регионального кровообращения.
Подчас такие органные нарушения, как острые нарушения мозгового кровообращения (ОНМК), коронарного кровотока, синдрома сердечной астмы, реже нарушений почечного или абдоминального кровообращения, возникают практически сразу вслед за подъемом АД. Это обстоятельство налагает на врача высокую ответственность за принятие решений, а действовать врачу приходится не всегда в благоприятных для этого условиях.
При оказании экстренной помощи больному необходимо следить за динамикой уровня АД, самочувствием больного. При появлении даже не резко выраженных проявлений ОНМК необходимо неврологическое обследование, при появлении загрудинных болей, приступа удушья или даже затруднения дыхания обязательно необходимо снять электрокардиограмму в 12-ти отведениях.
Необходимо проаускультировать легкие и сердце, определить число сердечных сокращений, их ритмичность.
Пульс и артериальное давление определяются на обеих руках, а при подозрении на сосудистые поражения и на ногах.
Врач должен поинтересоваться мочеиспусканием больного. Острая задержка может быть связана с нарушение клубочковой фильтрации, а при наличии гипертрофии и/или аденомы предстательной железы с патологией мочевыводящих путей.
Для самого купирования резко повышенного АД применяют различные медикаментозные подходы, которые показаны в табл. 20.17.
Как видно из приведенной таблицы, возможностей для купирования, и притом достаточно быстрого, немало. Далеко не всегда следует добиваться очень быстрого эффекта, за исключением случаев, когда явно имеется угроза ОИМ или инсульта. Врач, купирующий гипертонический криз, должен внимательнейшим образом следить за динамикой состояния больного в целом. Особое внимание следует обращать на неврологическую симптоматику. Это связано
Таблица 12.17
Средства, используемые для купирования ГК
Препарат | Доза | Метод введения, начало действия | Возможные побочные эффекты |
Натрия нитропрусид (нанипрус) | 30 мг на 500 мл глюкозы или физиологического р-ра | Внутривенно, капельно. Эффект наступает сразу | Тошнота, рвота, подергивание мышц, потоотделение |
Обзидан (пропранолол) | 1-5 мл 0,1% р-ра | В/в, медленно (!) | A/V-блокада, Бронхоспазм |
Диазоксид | 50-100 мг, иногда до 300 мг | Болюс Эффект через 2-4 минуты | Ортостат. коллапс, головная боль, гипергликемия, отеки, усиление ишемии миокарда |
Клонидин (клофелин) | 0,5-1 мл 0,01% р-ра в 20 мл изотонического р-ра или табл. 0,000075 | В/в, медленно Эффект через 15-20 минут; сублингвально* | Сонливость, заторможенность, ортостатическая гипотония, запоры |
Магнезия сульфат | 5-20 мл 25% р-ра | В/м или в/в медленно (!) | Гиперемия лица, редко угнетение дыхания |
Нитроглицерин | 5-100 мкг в мин | Болюс или в/в капельно | Тахикардия Головная боль, прилив крови к лицу, ортостатическая гипотония |
Дибазол | 5-10 1% р-ра | В/в или в/м | Головокружение, тошнота |
Продолжение табл. 20.17
Фуросемид (лазикс) | 20-100 мг | В/в или в/м | Выраженный мочегонный эффект, слабость, гипотония |
Нифедипин | 10-20 мг | Сублингвально* | Сухость во рту, слабость, гипотония |
Аминазин | 0,5-1, 0 мл 2,5% р-ра | В/м или в/в на 20 мл изотонического р-ра NaCl | Раздражение тканей в месте введения, психическая заторможенность, аллергические проявления, отеки, ортостатическая гипотония |
Ганглиоблокатор - пентамин | 0,5-1,0 мл 5% р-ра | В/в под строгим контролем АД (!) | Ортостатическая гипотония, парез кишечника |
Примечание: *Сублингвальный прием лекарств не одобряется некоторыми неврологами, так как это может способствовать ишемии мозга.
с тем, что при остром инсульте, особенно ишемическом, значительное снижение АД чревато ухудшением регионального кровообращения, в результате чего зона ишемии мозга расширяется. Это приводит к усугублению клиники инсульта и ухудшению прогноза.
Значение образовательных программ для пациентов и населения. Необходимо отметить, что при тяжело протекающей АГ (3 степень) даже неполная нормализация АД сокращает в 2 раза число опасных сердечно-сосудистых осложнений. Особенно важна регулярность лечения. Так, по нашим данным, если в группе больных АГ, лечен-
ных регулярно, заболеваемость инсультом и ОИМ составила 0,4%, то в группе леченных нерегулярно - 6,1%, а в группе отказавшихся от лечения - 9,1%. Значительные усилия медицинских работников по вовлечению населения в осуществление профилактических программ увеличивает число лиц, получающих эффективное лечение, приводящее к нормализации АД. Число лиц, регулярно леченных, увеличивается в 5-6 раз.
Несмотря на это, остается значительная часть лиц, не получающих адекватного лечения. Трудность заключается в нежелании значительной части населения участвовать в такого рода программах, что связано с их психологическими особенностями, бытовыми и профессиональными трудностями. Несмотря на эти трудности, проведение специальных образовательных программ как для пациентов и членов их семей, так и для населения в целом дает реальную возможность повысить эффективность лечения, увеличить осведомленность больных о наличии у них АГ. В конечном счете это позволяет снизить заболеваемость, инвалидность и смертность от сердечно-сосудистых заболеваний. Для практического осуществления таких программ на базе поликлиник, центрах медицинской профилактики создаются к лубы (школы) для больных с АГ и/или высоким риском АГ.
Основными задачами обучения являются доведение в доступной форме основных положений о факторах риска, о связанных с АГ опасностях серьезных поражений сердца, мозга, почек. В то же время слушателям школы сообщается о реальной возможности борьбы с АГ, профилактики органных поражений. Внушается необходимость соблюдения принципов здорового образа жизни, регулярности немедикаментозного и медикаментозного лечения АГ для улучшения качества жизни и ее продления.
В таких школах пациенты и их родственники обучаются правильному измерению АД, адекватной трактовке полученных результатов измерения, определенным правилам коррекции лечения в пределах, в которых это возможно без врачебного вмешательства.