Аналитическая химия. Практикум : учеб. пособие / Харитонов Ю.Я., Григорьева В.Ю. - 2009. - 296 с.
|
|
|
|
Тема III АНАЛИЗ СМЕСИ КАТИОНОВ ВСЕХ ШЕСТИ АНАЛИТИЧЕСКИХ ГРУПП ПО КИСЛОТНО-ОСНОВНОЙ КЛАССИФИКАЦИИ
Занятие 8. Анализ смеси катионов всех шести аналитических групп по кислотно-основной классификации
Цель занятия:
- научиться проводить анализ раствора, содержащего смесь катионов всех шести аналитических групп;
- научиться проводить анализ раствора с осадком, содержащего смесь катионов всех шести аналитических групп;
- научится составлять схему анализа сложных объектов, содержащих все катионы или только часть катионов шести аналитических групп.
Задание для самоподготовки
К занятию надо знать
1. Схему анализа объектов (раствор без осадка, раствор с осадком), содержащих смесь катионов всех шести аналитических групп или только часть из них.
2. Как проводить предварительные наблюдения и испытания.
3. Как проводить дробный анализ смеси катионов.
4. Как проводить систематический анализ смеси катионов.
5. Правила техники безопасности и работы в химико-аналитической лаборатории.
Уметь
1. Выбирать ту или иную схему анализа.
2. Проводить аналитические реакции на катионы всех шести аналитических групп.
3. Проводить разделение катионов с помощью групповых реагентов.
Литература
Харитонов Ю.Я. Аналитическая химия (аналитика). Кн. 1, гл. 13,
с. 336-343.
Лурье Ю.Ю. Справочник по аналитической химии. - М.: Химия,
1989.
Вопросы для самоподготовки
1. Какие катионы отсутствуют в растворе, если раствор - бесцветный?
2. Какие продукты гидролиза могут входить в состав осадка исходного анализируемого раствора с осадком?
3. Какие катионы отсутствуют в растворе без осадка, если значение рН раствора находится в пределах рН = 2-4? Почему?
4. Какие реагенты используют для открытия некоторых катионов в предварительных испытаниях?
5. Как отделяют катионы второй аналитической группы? Напишите уравнения соответствующих реакций.
6. Как переводят сульфаты катионов третьей группы в их карбонаты? Напишите уравнения соответствующих реакций.
7. Как открывают катионы железа(П) и железа(Ш) в предварительных испытаниях? Напишите уравнения соответствующих реакций.
8. Как открывают катионы кобальта(П) и никеля(П)? Напишите уравнения соответствующих реакций.
9. Как отделяют катионы четвертой группы от катионов пятой и шестой групп? Охарактеризуйте основные этапы.
10. Как проводят разделение и открытие катионов пятой и шестой аналитических групп? Охарактеризуйте основные этапы.
11. Каковы основные этапы анализа раствора с осадком?
Лабораторная работа
Реактивы (см. занятия 4- 6) Учебные таблицы
1. Аналитические реакции катионов первой - шестой аналитических групп.
2. Схемы анализа смесей катионов различных аналитических групп.
Анализ смеси катионов всех шести аналитических групп
В зависимости от того, что представляет собой анализируемый объект - водный раствор без осадка или водный раствор с осадком - выбирают ту или иную схему систематического хода анализа.
А. Анализ раствора без осадка. Если анализируемый объект представляет собой водный раствор без осадка, то применяемая схема анализа заключается в следующем (в конкретных случаях отдельные детали анализа могут быть различными).
Анализируемый раствор может быть окрашенным или бесцветным. По окраске раствора высказывают предположения о присутствии или отсутствии катионов, имеющих характерную окраску. Если, например, раствор прозрачный и бесцветный, то можно предположить, что он не содержит катионы Cr3+,Fе3+,Cu2+,Cо2+,Ni2+.
Некоторые предварительные указания можно получить и на основании измерения значения рН раствора (например, с помощью универсальной индикаторной бумаги, которая при разных значениях рН водного раствора окрашивается в различные цвета). Если значение рН раствора находится в пределах рН = 2-4 (и раствор не содержит осадка), то в нем отсутствуют олово(П), олово(ШМ), сурьма(Ш), сурьма(М), висмут(Ш), ртуть(П), железо(Ш), так как в противном случае их продукты гидролиза выделялись бы в форме осадков при указанных значениях рН раствора.
Анализируемый раствор делят на три части. Одну часть используют для предварительных испытаний, другую - для проведения систематического анализа, третью - оставляют для контроля.
а) Предварительные испытания. В отдельных небольших порциях анализируемого раствора (объемом примерно по 0,3-0,5 мл) определяют наличие катионов II-VI аналитических групп действием групповых реагентов - водного раствора хлороводородной кислоты HC1, водного раствора серной кислоты H2S04, водного раствора гидроксида натрия NaOH в присутствии пероксида водорода Н202,водного 25 % раствора аммиака. В отдельных порциях анализируемого раствора предварительно открывают также и некоторые индивидуальные катионы - железа Fe2+ иFе3+, хрома(Ш) Сг3+,медиС1д2+' катионы первой группы и другие действием различных реагентов.
Определив наличие катионов различных групп, приступают к разделению их с помощью групповых реагентов.
б) Отделение и открытие катионов второй аналитической группы. Если в растворе присутствуют катионы второй аналитической группы
(Ag+, Hg2+ ,Pb2+), то их отделяют действием водного раствора хлороводородной кислоты в виде смеси осадков хлоридов AgCl, Hg2Cl2 иРЬС12 белого цвета, в которой затем открывают каждый из указанных катионов, как описано в занятии 3.
в) Отделение и открытие катионов третьей аналитической группы. Маточник, оставшийся после отделения от анализируемого раствора осадков хлоридов катионов второй аналитической группы, медленно обрабатывают водным раствором серной кислоты (с добавлением этанола, если в растворе присутствуют катионы кальция). Выделяются белые осадки сульфатов катионов третьей аналитической группы - кальция CaS04,стронцияSrS04,бария BaS04, а также сульфат свинца PbS04 (катионы свинца Pb2+ были неполностью отделены на предыдущем этапе при обработке раствора хлороводородной кислотой, поскольку хлорид свинца заметно растворим в воде). Убеждаются в полноте осаждения катионов третьей группы (раствор не должен мутнеть при добавлении небольшого количества серной кислоты). Смесь центрифугируют, отделяют осадки сульфатов, а маточник оставляют для дальнейшего анализа.
К осадку сульфатов прибавляют небольшое количество водного 30 % раствора ацетата аммония CН3C00NН4 или натрия СН3С00? при нагревании на водяной бане для удаления примесей сульфата свинца, который в этих условиях переходит в раствор. 0перацию при необходимости повторяют до отрицательной реакции на катионы свинца (проба с дихроматом калия в отдельной порции раствора). В осадке остаются сульфаты кальция, стронция и бария, которые переводят в карбонаты (растворимые в кислотах) для того, чтобы затем растворить эти карбонаты в кислоте и получить раствор, в котором содержались бы катионы кальция, стронция и бария. В растворе открывают эти катионы, как описано в занятии 3.
Для перевода сульфатов в карбонаты к осадку сульфатов кальция, стронция и бария прибавляют небольшое количество насыщенного водного раствора карбоната натрия (соды) ?2С03, смесь перемешивают и нагревают несколько минут на водяной бане. Сульфаты переходят в карбонаты. 0днако однократной обработки обычно бывает недостаточно. Поэтому смесь после нагревания центрифугируют, отделяют центрифугат, и осадок снова обрабатывают насыщенным водным раствором соды, как описано выше. Снова центрифугируют смесь и отделяют центрифугат от осадка. 0перацию обработки осадка раствором соды повторяют до отрицательной реакции на сульфат-ионы в центри-фугате. Промывают осадок дистиллированной водой и к промывным
водам прибавляют раствор хлорида бария. Если при этом не наблюдается образование мути (сульфата бария), то обработку осадка раствором соды прекращают, так как отсутствие сульфат-ионов свидетельствует о том, что сульфаты кальция, стронция и бария полностью перешли в карбонаты.
0ставшийся осадок уже карбонатов кальция, стронция и бария обрабатывают раствором уксусной кислоты (2 моль/л) при нагревании. 0садок растворяется. В полученном растворе затем открывают каждый катион третьей аналитической группы.
г) Предварительное открытие некоторых катионов четвертой, пятой и шестой аналитических групп. Раствор, оставшийся после отделения катионов второй и третьей аналитических групп, может содержать катионы первой, четвертой, пятой и шестой аналитических групп по кислотно-основной классификации. Перед продолжением проведения дальнейшего систематического анализа можно предварительно открыть (хотя это делается не всегда) некоторые катионы в отдельных небольших порциях этого или исходного раствора, например, катионы же-леза(П) Fe2+, железа(Ш) Fе3+, хрома(Ш) Cr3+, меди(П) Cu2^ мышья-ка(\~), сурьмы, марганца(П) Mn2+, кобальта(П) ОН, никеля(П) Ni2+, ртути(П) Hg2+, висмута(Ш) а также катионы первой аналитической группы.
Открытие катионов железа. Катионы железа(П) Fe2+ открывают реакцией с гексацианоферратом(Ш) калия К3[Fе(CN)6] в кислой среде (рН = 2-3). В присутствии катионов Fe2+ образуется темно-синий осадок турнбулевой сини. Если цвет осадка иной, то это свидетельствует об отсутствии катионов железа(П).
Катионы железа(Ш) открывают реакцией с гексацианоферра-том(П) калия K4[Fe(CN)6] (также в кислой среде, рН « 3). При наличии в растворе катионов Fе3+ образуется темно-синий осадок берлинской лазури.
Открытие катионов хрома(Ш) Cr3+. Катионы хрома(Ш) предварительно открывают, окисляя их пероксидом водорода до хромат-ионов в присутствии щелочи.
Открытие катионов меди(Л) Cu2+. Катионы меди(П) Cu2+предварительно открывают в отдельной порции раствора реакцией с концентрированным раствором аммиака, при которой образуется аммиачный комплекс меди(П) [Cu(NН3)4]2+ интенсивно синего цвета.
Если окраска раствора недостаточно характерна, то медь(П) вначале переводят в оксид меди, который затем растворяют в азотной кислоте. Для этого к небольшому количеству анализируемого раствора
прибавляют раствор гидроксида натрия (2 моль/л). Выпадает осадок. Смесь нагревают несколько минут на водяной бане; при этом осадок чернеет вследствие образования оксида меди. 0брабатывают смесь небольшим количеством раствора хлорида аммония (2 моль/л), перемешивают и центрифугируют. 0садок отделяют от центрифугата и прибавляют к нему (по каплям) небольшое количество 2 моль/л раствора азотной кислоты до растворения осадка. 0ксид меди растворяется, и катионы Cu2+ переходят в раствор. Полученный раствор обрабатывают водным 25 % раствором аммиака. 0бразуется аммиачный комплекс меди - раствор принимает интенсивно синюю окраску.
Открытие мышьяка. Мышьяк (V) можно предварительно открыть реакцией с молибдатом аммония в присутствии азотной кислоты. При наличии арсенат-ионов AsO 4~ образуется желтый кристаллический осадок аммонийной соли мышьяковомолибденовой гетерополикисло-ты ^Н4)3[Ая04(Мо03)12].
Открытие сурьмы. Сурьму открывают в отдельной порции раствора в том случае, если исходный раствор без осадка имеет значение рН < 1.
К небольшому количеству (несколько капель) раствора прибавляют несколько капель водного раствора 2 моль/л азотной кислоты НN03, столько же - 3 % раствора пероксида водорода. Смесь нагревают на водяной бане. В этих условиях вся сурьма в растворе оказывается в состоянии высшей степени окисления - сурьма(V) - и выделяется из раствора в форме белого осадка сурьмяной кислоты Н^Ь04 (формулу которой можно представить также в виде Sb0(0^3 или ЖЬ03).
Смесь охлаждают и центрифугируют. 0садок отделяют от центри-фугата и растворяют в концентрированной хлороводородной кислоте. При этом образуется растворимый хлоридный комплекс сурьмы(У) состава [SbC16]- . Раствор разбавляют (примерно в 2 раза) дистиллированной водой и подтверждают присутствие в нем сурьмы(V) реакцией с сероводородной водой или сульфидом аммония (выделяется оранжевый осадок сульфида сурьмы Sb2S5), а также реакцией с органическими реагентами - метиловым фиолетовым или родамином 6Ж. При реакциях комплексов [SbC16]- с указанными органическими реагентами образуются окрашенные ионные ассоциаты состава R+[SbC16]- ,где R+ - органический катион метилового фиолетового или родамина 6Ж, которые экстрагируются из водной фазы бензолом. Экстракт окрашивается в фиолетовый (в случае метилового фиолетового) или розовый (в случае родамина 6Ж) цвет.
Открытие катионов марганца(II). Эти катионы открывают в отдельной порции раствора реакцией окисления Mn2+ до перманганат-
ионов MnO4 висмутатом натрия NaBiO3 вазотнокислойсреде - наблюдается окрашивание раствора в малиново-фиолетовый цвет.
Открытие катионов кобальта(II) ^Ч Если в растворе присутствуют катионы железа(Ш) Fе3+ и меди(П) Cu2+, то катион Cо2+ открывают капельной реакцией на полоске фильтровальной бумаги с 1-нитро-зо-2-нафтолом (реактив Ильинского) в уксуснокислой среде - наблюдается возникновение окрашенной коричневой зоны вследствие образования комплекса кобальта (пурпурно-красного цвета в чистом виде) с органическим реагентом. Большие количества катионов меди(П) Cu2+ мешают определению.
При отсутствии в растворе катионов Fе3+ и Cu2+ кобальт(П) открывают реакцией с тиоцианатами аммония NH4NCS или калия КNCS в присутствии изоамилового спирта (экстрагент) - наблюдается окрашивание органического слоя в ярко-синий цвет вследствие образования синего тиоцианатного комплекса [Cо(NCS)4]2- , экстрагирующегося в органическую фазу.
Мешающее действие железа(Ш) и меди(П) можно устранить путем их восстановления до железа(П) и медиЦ) хлоридом олова(П). Желе-зо(Ш) также маскируют (устраняют его мешающее действие) добавлением фторида натрия NaF - образуется устойчивый бесцветный фто-ридный комплекс железа(Ш) состава [FеF6]3- , не мешающий, как и железо(П), определению кобальта(П).
Открытие катионов никеля(II) Ni2+. Если в растворе отсутствуют катионы железа(П), то никель(П) открывают капельной реакцией с диметилглиоксимом (реактив Чугаева) в аммиачной среде на полоске фильтровальной бумаги - возникает окрашенная розовая зона вследствие образования комплекса никеля с диметилглиоксимом красного цвета.
Катионы железа(П), меди(П) и других металлов, образующих окрашенные аммиачные комплексы, мешают определению.
Открытие катионов ртути(II) Hg2+. Катионы Hg2+ открывают реакцией с хлоридом олова(П) (точнее - с хлоридными комплексами [SnC14]2- ) - наблюдается выпадение белого осадка каломели Hg2C12, который темнеет вследствие выделения тонкодисперсной металлической ртути, образующейся при восстановлении Hg2C12 оловом(П).
Открытие катионов висмута(Ш) Bi3+. Если в растворе отсутствуют катионы сурьмы и ртути(П), то висмут(Ш) открывают реакцией восстановления висмута(Ш) до металлического висмута оловом(П) (точнее, комплексами (Sn(0Н)4]-) - наблюдается образование черного осадка, содержащего металлический висмут.
д) Отделение катионов четвертой аналитической группы от катио-новпятойишестойаналитическихгрупп. После предварительного открытия ряда катионов в отдельных порциях раствора (как описано выше), оставшегося в результате отделения катионов второй и третьей аналитических групп, из основной части этого раствора, содержащего катионы первой, четвертой, пятой и шестой аналитических групп, отделяют сурьму (если предварительные испытания показали ее наличие в растворе). Для этого к раствору прибавляют небольшие количества водного 2 моль/л раствора азотной кислоты и водного 3 % раствора пе-роксида водорода, смесь нагревают несколько минут на кипящей водяной бане. В этих условиях вся сурьма переходит в сурьмяную кислоту ffib03 Выпавший белый осадок сурьмяной кислоты отделяют центрифугированием, а раствор, уже не содержащий сурьмы, подвергают действию щелочи для отделения катионов четвертой аналитической группы.
К центрифугату медленно прибавляют водный 2 моль/л раствор гидроксида натрия до нейтральной реакции среды и затем - дополнительно избыток раствора гидроксида натрия и небольшое количество пероксида водорода. Нагревают смесь на кипящей водяной бане. В этих условиях катионы четвертой аналитической группы, образовавшие соответствующие растворимые гидроксокомплексы, остаются в растворе, а катионы пятой и шестой аналитических групп переходят в осадок (смесь гидроксидов и основных солей).
В случае присутствия в растворе катионов хрома(Ш) смесь продолжают нагревать до изменения цвета раствора из зеленого (цвет катионов Cr3+) до желтого (цвет хромат-ионов CrO4~). При этом весь хром(Ш) окисляется до хрома (VI). После нагревания (непрореагиро-вавший пероксид водорода удаляется) смесь центрифугируют, осадок отделяют от центрифугата.
0садок содержит катионы пятой и шестой аналитических групп, а щелочной центрифугат - катионы первой и четвертой аналитических групп.
В части центрифугата открывают катионы четвертой аналитической группы, как описано ранее.
е) Разделение и открытие катионов пятой и шестой аналитических групп. Полученный свежевыпавший осадок гидроксидов, гидратиро-ванных оксидов и основных солей катионов пятой и шестой аналитических групп обрабатывают при нагревании раствором азотной кислоты (1:1) в присутствии пероксида водорода. В раствор переходят все катионы обеих групп, за исключением сурьмы, которая остается в
осадке в форме метасурьмяной кислоты ЖЬО3 Этот осадок отделяют центрифугированием, растворяют в небольшом количестве концентрированной хлороводородной кислоты и в растворе открывают сурьму реакцией с родамином Б.
Азотнокислый раствор после отделения сурьмы нейтрализуют 1 моль/л раствором соды ?2СО3 до начала помутнения, прибавляют двух-трехкратный объем концентрированного раствора аммиака и нагревают до 40-50 °C. При этом катионы шестой аналитической группы переходят в раствор в виде комплексных аммиакатов состава
I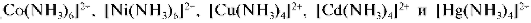 .
.
В осадке остаются гидроксиды катионов пятой группы.
Смесь центрифугируют. Центрифугат, содержащий катионы шестой аналитической группы, отделяют от осадка, содержащего катионы пятой аналитической группы. Центрифугат и осадок анализируют раздельно.
Осадок промывают 2 моль/л раствором аммиака, водой, растворяют в 2 моль/л растворе азотной кислоты и в полученном растворе открывают катионы пятой аналитической группы, как описано ранее.
Аммиачный центрифугат, содержащий катионы шестой аналитической группы, нейтрализуют 1 моль/л раствором серной кислоты до слабокислой реакции, и в полученном растворе открывают катионы шестой аналитической группы.
ж) Открытие катионов первой аналитической группы. Катионы первой аналитической группы, не имеющей группового реагента, открывают дробным методом в отдельных небольших пробах исходного анализируемого раствора или раствора, полученного после отделения катионов второй и третьей аналитических групп.
Б. Анализ раствора с осадком. Если анализируемый объект представляет собой раствор с осадком, то вначале эту смесь центрифугируют, отделяют осадок от раствора и обе фазы анализируют раздельно.
Наличие осадка свидетельствует о возможности присутствия в нем хлоридов катионов второй аналитической группы, сульфатов катионов третьей и второй аналитических групп, продуктов гидролиза соединений олова, сурьмы, висмута, арсенатов и арсенитов.
Раствор, отделенный от осадка, анализируют так, как описано выше (см. «Анализ раствора без осадка»).
Осадок испытывают на растворимость в разбавленных растворах уксусной, хлороводородной, азотной кислот. Если он полностью растворяется в какой-то из этих кислот, то раствор, полученный после
растворения осадка, либо присоединяют к центрифугату и анализируют далее вместе (что делают чаще всего), либо анализируют отдельно на присутствие тех или иных катионов.
Если осадок не растворяется в указанных разбавленных кислотах, то испытывают его растворимость в других растворителях - в более концентрированной (1:1) азотной кислоте, в водном растворе винной кислоты, в водном 30 % растворе ацетата аммония.
В азотной кислоте (1:1) растворяются осадки оксохлорида висмута BiOC1, хлорид свинца PbC12, в водном растворе винной кислоты - ок-сохлориды сурьмы SbOC1 и Sb02C1, в водном растворе ацетата аммония - осадок сульфата свинца. В пробах полученных растворов открывают соответствующие катионы характерными реакциями на эти катионы.
Если осадок нерастворим во всех вышеперечисленных растворителях, то это указывает на возможное присутствие в нем хлоридов катионов второй аналитической группы, сульфатов второй и третьей аналитических групп.
Систематический анализ осадка. 0брабатывают осадок горячей азотной кислотой и центрифугируют полученную смесь. В центрифу-гат переходят мышьяк(Ш), мышьяк(V), висмут(Ш), которые открывают в отдельных пробах центрифугата характерными реакциями.
0тделенный от раствора осадок может содержать смесь хлоридов, оксохлоридов и сульфатов AgC1, Hg2C12,PbSO4,CaSO4,SrSO4,BaSO4, SbOC1, SbO2C1. 0садок обрабатывают кипящей дистиллированной водой. При этом растворяется хлорид свинца PbC12 Катионы свинца Pb2+ открывают в пробе раствора реакциями на эти катионы.
Смесь центрифугируют (или фильтруют), осадок отделяют, промывают горячей водой до отрицательной реакции на катионы свинца Pb2+ (реакция с раствором хромата калия) и прибавляют к нему концентрированный раствор аммиака. Хлорид серебра AgC1 растворяется с образованием аммиачного комплекса [Ag (NН3)2]+. Если в осадке присутствовал хлорид ртути(1) Hg2C12, то при обработке аммиаком осадок чернеет вследствие выделения металлической ртути.
Раствор отделяют от осадка центрифугированием и открывают в нем катионы серебра Ag+ реакциями на этот катион.
0садок промывают дистиллированной водой и прибавляют к нему раствор винной кислоты при нагревании. В раствор переходит сурьма, которую открывают в пробах раствора реакциями на сурьму.
0статок осадка обрабатывают последовательно порциями горячего 30 % раствора ацетата аммония до полного растворения сульфата
свинца PbS04 (отрицательная реакция с раствором хромата калия на катионы свинца Pb2+). В осадке остаются сульфаты катионов третьей аналитической группы, которые переводят в карбонаты обработкой раствором соды, растворяют в уксусной кислоте и в полученном растворе открывают катионы кальция Cа2+,стронцияSr2+ ибария Ва2+.
Контрольные вопросы
1. Какие выводы можно сделать о присутствии тех или иных катионов по внешнему виду раствора без осадка и раствора с осадком?
2. Какие выводы можно сделать о присутствии тех или иных катионов, если известна величина рН раствора?
3. Какие катионы и как можно обнаружить в предварительных испытаниях?
4. Какие окислительно-восстановительные реакции используют при анализе смеси катионов всех шести аналитических групп?
5. Какие аммиачные комплексы металлов используются при анализе смеси катионов?
6. Какие гидроксокомплексы используются при анализе смеси катионов?
7. В какой форме присутствует мышьяк(Ш) и мышьяк(У) в анализируемом растворе - в форме катионов или анионов?
8. Могут ли в анализируемом растворе (с осадком или без осадка), содержащем смесь катионов всех шести аналитических групп, одновременно присутствовать в соизмеримых количествах окислители и восстановители?