Иммунология : учебник. - Хаитов Р. М. - 2009. - 320 с. : ил.
|
|
|
|
ГЛАВА 6 Т-ЛИМФОЦИТЫ
Основное предназначение T-лимфоцитов - распознавание поверхностных структур собственных клеток организма. Если что-то на поверхности своих клеток будет «раздражать» T-лимфоцит (например, примесь вирусных пептидов), то он постарается организовать уничтожение повреждённой клетки.
• В отличие от B-лимфоцитов, T-лимфоциты не продуцируют растворимых форм Аг-распознающих молекул и всегда «работают» собственным «клеточным телом». Более того, большинство T-лим- фоцитов не способны распознавать и связывать растворимые Аг.
• Для того чтобы T-лимфоцит «обратил на Аг своё внимание», другие клетки должны каким-то образом пропустить Аг через себя и выставить его на своей мембране в комплексе с MHC-I/II. Это и есть феномен представления Аг T-лимфоциту. Распознавание такого комплекса T-лимфоцитом - двойное распознавание, или MHC-рестрикция T-лимфоцитов.
рецептор для антигена t-лимфоцитов
Антигенраспознающие Рц T-лимфоцитов - TCR-принадлежат к надсемейству иммуноглобулинов (см. рис. 5.1). Выступающий над поверхностью клетки Аг-распознающий участок TCR - гетеродимер (т.е. состоит из двух разных полипептидных цепей) - аналог одного Fab-фрагмента Ig. Известны два варианта TCR, обозначаемые как TCRαβ и TCRγδ; эти варианты различаются составом полипептидных цепей Аг-распознающего участка. Каждый T-лимфоцит несёт только один вариант Рц. Tαβ стали известны раньше и изучены подробнее, чем Tγδ; поэтому строение Рц T-лимфоцитов для Аг удобнее описывать на примере TCRαβ. Полностью трансмембранно расположенный TCR состоит из 8 или 10 (одна или две пары α + β плюс комплекс «2ε + δ + γ + 2ζ») полипептидных цепей (рис. 6.1).
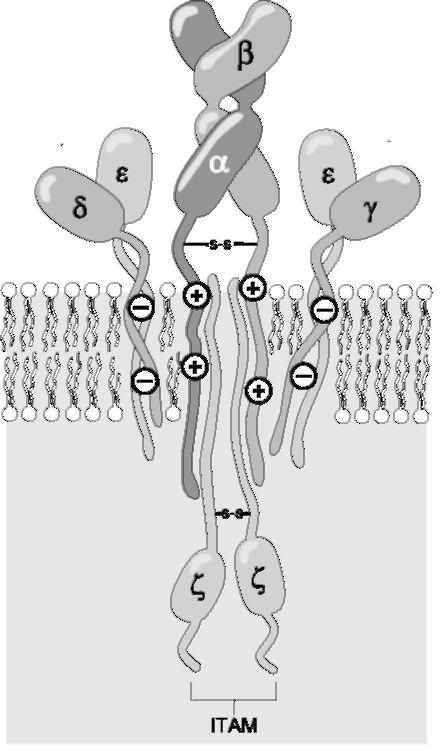 Рис. 6.1. Рецептор TCRap T-лимфоцитов для антигена.
Рис. 6.1. Рецептор TCRap T-лимфоцитов для антигена.
Аг-связывающая область рецептора формируется α- и β-цепями; цепи γ, δ, ε (вместе их называют комплексом CD3) необходимы для экспрессии α- и β-цепей, их стабилизации и, вероятно, проведения сигнала внутрь клетки; ζ-цепь, самая «внутриклеточная», обеспечивает проведение сигнала внутрь клетки.
• Трансмембранные цепи α и β TCR. Это 2 примерно равновеликие полипептидные цепи - α (молекулярная масса 40-60 тыс., кислый гликопротеин) и β (молекулярная масса 40-50 тыс., нейтральный или основный гликопротеин). Каждая из этих цепей имеет по два гликозилированных домена во внеклеточной части Рц, гидрофобную (положительно заряженную за счёт остатков лизина и аргинина) трансмембранную часть и короткий (из 5-12 остатков АК) цитоплазматический участок. Внеклеточные части обеих цепей соединены одной дисульфидной связью.
♦ V-область. Наружные внеклеточные (дистальные) домены обеих цепей имеют вариабельный АК-состав. Они гомологичны V-об- ласти молекул Ig, это V-область TCR. Именно V-области α- и β-цепей вступают в связь с комплексом «MHC-I/II-пептид».
♦ C-область. Проксимальные домены обеих цепей гомологичны константным областям Ig, это C-области TCR.
♦ Короткий цитоплазматический участок (как α-, так и β-цепи) не может самостоятельно обеспечить проведение сигнала внутрь клетки. Для этого служат 6 дополнительных полипептидных цепей: γ , δ, две ε и две ζ.
• Комплекс CD3. Цепи γ, δ, ε (вместе их называют комплексом CD3) необходимы для экспрессии α- и β-цепей, их стабилизации и, вероятно, проведения сигнала внутрь клетки. Комплекс CD3 состоит из внеклеточной, трансмембранной (отрицательно заряженной и
потому электростатически связанной с трансмембранными участками α- и β-цепей) и цитоплазматической частей.
♦ ζ-Цепи соединены между собой дисульфидным мостиком и, будучи по большей частью расположены в цитоплазме, осуществляют проведение сигнала внутрь клетки.
♦ ITAM-последовательности. Цитоплазматические участки полипептидных цепей γ, δ, ε и ζ содержат АК-последовательности ITAM (1 в γ- и δ-цепях, 2 в ε-цепях, 3 в каждой ζ-цепи), которые взаимодействуют с тирозинкиназами цитозоля (активация этих ферментов и составляет начало биохимических реакций по проведению сигнала).
В связывании Аг участвуют ионные, водородные, ван-дер-ваальсовы и гидрофобные силы, конформация Рц при этом существенно изменяется. Каждый TCR потенциально способен связывать порядка 105 разных Аг, причём не только родственные по строению (пере- крёстно реагирующие), но и не имеющие гомологии в структуре.
Гены TCR
• Гены α-, β-, γ- и δ-цепей (рис. 6.2) гомологичны генам Ig и претерпевают при дифференцировке T-лимфоцитов соматическую рекомбинацию ДНК, что теоретически обеспечивает генерацию порядка 1016-1018 вариантов антигенсвязывающих центров (реально это разнообразие ограничено числом лимфоцитов в организме до 109). Гены α-цепи имеют 70-80 V-сегментов, 61 J- и один C-сегмент.
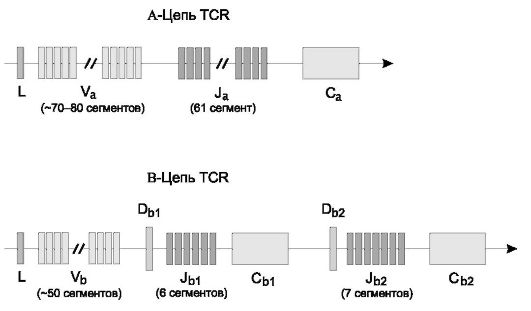 Рис. 6.2. Гены α- и β-цепей рецептора T-лимфоцитов для антигена.
Рис. 6.2. Гены α- и β-цепей рецептора T-лимфоцитов для антигена.
• Гены β-цепи содержат 52 V-сегмента, 2 D-сегмента, 13 J-сегментов, и 2 С-сегмента.
• Гены δ-цепи. Между V- и J-сегментами α-цепи расположены гены D-, J- и С-сегментов δ-цепи TCRγδ. V-сегменты δ-цепи «вкраплены» среди V-сегментов α-цепи.
• Гены γ-цепи TCRγδ имеют 2 С-сегмента, 3 J-сегмента перед первым С-сегментом и 2 J-сегмента перед вторым С-сегментом, 12 V-сегментов.
Перестройка генов
• Рекомбинация ДНК происходит при объединении V-, D- и J- сегментов и катализируется тем же комплексом рекомбиназ, что и при дифференцировке B-лимфоцитов.
• После перестройки VJ в генах α-цепи и VDJ в генах β-цепи, а также присоединения некодируемых N- и P-нуклеотидов с ДНК транскрибируется РНК. Объединение с С-сегментом и удаление лишних (неиспользуемых) J-сегментов происходит при сплайсинге первичного транскрипта.
• Гены α-цепи могут перестраиваться неоднократно при уже правильно перестроенных и экспрессированных генах β-цепи, поэтому есть некоторая вероятность того, что одна клетка может нести более одного варианта TCR.
• Соматическому гипермутагенезу гены TCR не подвергаются.
Корецепторные молекулы CD4 и CD8
Помимо самого TCR, каждый зрелый T-лимфоцит экспрессирует одну из так называемых корецепторных молекул - CD4 или CD8, которые также вступают в связь с молекулами MHC на АПК или клетках-мишенях. Каждая из них имеет цитоплазматический участок, связанный с тирозинкиназой Lck, и, вероятно, вносит свой вклад в проведение сигнала внутрь клетки при состоявшемся распознавании Аг.
• CD4 вступает в связь с инвариантной частью (β2-доменом) молекулы MHC-II (принадлежит к надсемейству Ig, см. рис. 5.1Б). CD4 имеет молекулярную массу 55 тыс. и 4 домена во внеклеточной части. При активации T-лимфоцита одну молекулу TCR «обслуживают» две молекулы CD4 (вероятно, происходит димеризация молекул CD4).
• CD8 связывается с инвариантной частью (α3-доменом) молекулы MHC-I (принадлежит к надсемейству Ig, см. рис. 5.1А). CD8 - гетеродимер цепей α и β, соединённых дисульфидной
связью. В некоторых случаях обнаруживают гомодимер из 2-х α-цепей, который также может взаимодействовать с MHC-I. Во внеклеточной части каждая из цепей имеет по одному иммуноглобулиноподобному домену.
ПРОВЕДЕНИЕ СИГНАЛА С ИММУНОРЕЦЕПТОРОВ ЛИМФОЦИТОВ
Рецепторы лимфоцитов для Аг (TCR и BCR) имеют ряд общих закономерностей регистрации и проведения в клетку активационных сигналов (см. рис. 5.8).
• Кластеризация рецепторов. Для активации лимфоцита необходима кластеризация Рц и корецепторов, т.е. «сшивка» нескольких Рц одним Аг.
• Тирозинкиназы. В проведении сигнала играют значительную роль процессы фосфорилирования/дефосфорилирования белков по остатку тирозина под действием тирозинкиназ и тирозинфосфатаз, ведущие к активации или инактивации этих белков. Эти процессы легко обратимы и «удобны» для быстрых и гибких реакций клетки на внешние сигналы.
• Киназы Src. Богатые тирозином ITAM-последовательности цитоплазматических участков иммунорецепторов подвергаются фосфорилированию под действием нерецепторных (цитоплазматических) тирозинкиназ семейства Src (Fyn, Blk, Lyn в B-лимфоцитах, Lck и Fyn - в T-лимфоцитах).
♦ Активность киназ Src зависит от состояния С-концевого участка молекулы: его фосфорилирование под действием киназы Csk инактивирует, дефосфорилирование трансмембранной тирозинфосфатазой CD45 - активирует фермент.
♦ Другой механизм регуляции активности киназ Src - их ковалентное связывание с убиквитином через адаптерный белок Cb1. Связывание с убиквитином «направляет» всякий белок на деградацию в протеосомах.
• Другие киназы. Киназы Syk (в B-лимфоцитах) и ZAP-70 (в T- лимфоцитах), связываясь с фосфорилированными ITAM-после- довательностями, активируются и начинают фосфорилировать адапторные белки: LAT (Linker for Activation of T cells) и SLP-76 (Syk), BLNK и SLP-65 (ZAP-70).
• Фосфолипаза Cγ (см. рис. 4.3). Киназы семейства Tec (Btk в B- лимфоцитах, Itk - в T-лимфоцитах) связывают адаптерные белки
и активируют фосфолипазу Cγ (PLCγ).
♦ PLCγ расщепляет фосфатидилинозитдифосфат (PIP2) клеточной мембраны на фосфатидилинозиттрифосфат (PIP3) и диацилглицерин (DAG).
♦ DAG остаётся в мембране и активирует протеинкиназу С (PKC) - серин/треониновую киназу, которая активирует эволюционно «древний» фактор транскрипции NFkB.
♦ PIP3 связывается со своим Рц в эндоплазматическом ретикулуме и высвобождает ионы кальция из депо в цитозоль.
♦ Свободный кальций активирует кальцийсвязывающие белки - кальмодулин, который регулирует активность ряда других белков, и кальциневрин, который дефосфорилирует и тем самым активирует ядерный фактор активированных T-лимфоцитов NFAT (Nuclear Factor of Activated T-cells).
• Малые G-белки Ras в неактивном состоянии связаны с ГДФ, но адаптерные белки заменяют последний на ГТФ, чем переводят Ras в активное состояние.
♦ Ras обладает собственной ГТФ-азной активностью и быстро отщепляет третий фосфат, чем возвращает себя в неактивное состояние (самоинактивируется).
♦ В состоянии кратковременной активации Ras успевает активировать очередной каскад киназ, называемых MAP (MitogenActivated Protein kinase), которые в итоге активируют фактор транскрипции АP-1 (Activator Protein-1) в ядре клетки.
ДИФФЕРЕНЦИРОВКА T-ЛИМФОЦИТОВ
Процессы дифференцировки, происходящие в тимусе, изучены достаточно подробно и представляют следующую последовательность событий:
• Тимоциты дифференцируются из общей клетки-предшественника, которая ещё вне тимуса экспрессирует такие мембранные маркёры как CD7, CD2, CD34 и цитоплазматическую форму CD3.
• Коммитированная к дифференцировке в T-лимфоцит клеткапредшественник мигрирует из костного мозга в субкапсулярную зону коры тимуса, где примерно в течение 1 нед происходит медленная пролиферация клеток. На тимоцитах появляются новые мембранные молекулы CD44 и CD25.
• Затем клетки перемещаются несколько вглубь коры тимуса, молекулы CD44 и CD25 исчезают с их мембраны. В этой стадии
начинается перестройка генов β-, γ- и δ-цепей TCR. Если гены γ- и δ-цепей успевают продуктивно (т.е. без сдвига рамки считывания) перестроиться раньше, чем гены β-цепи, то лимфоцит дифференцируется далее как Tγδ. В противном случае происходит экспрессия β-цепи на мембране в комплексе с pTα (инвариантной суррогатной цепью, заменяющей на этом этапе настоящую α-цепь) и CD3. Это служит сигналом к прекращению перестройки генов γ- и δ-цепей. Клетки начинают пролиферировать и экспрессировать одновременно CD4 и CD8 (дважды позитивные тимоциты). При этом накапливается масса клеток с уже готовой β-цепью, но с ещё не перестроенными генами α-цепи, что вносит свой вклад в разнообразие α-β-гетеродимеров.
• На следующем этапе клетки перестают делиться и начинают перестраивать Vα-гены, причём несколько раз в течение 3-4 сут. Перестройка генов α-цепи приводит к необратимой делеции δ-локуса, расположенного между сегментами генов α-цепи.
• Происходит экспрессия TCR с каждым новым вариантом α-цепи, и отбор (селекция) тимоцитов по силе связывания с комплексом «пептид-MHC» на мембранах эпителиальных клеток тимуса.
♦ Позитивная селекция: погибают тимоциты, не связавшие ни одного из доступных комплексов «пептид-MHC». В результате позитивной селекции в тимусе погибает около 90% тимоцитов.
♦ Негативная селекция уничтожает клоны тимоцитов, связывающих комплексы «пептид-MHC» со слишком высокой аффинностью. Негативная селекция элиминирует от 10 до 70% клеток, прошедших позитивную селекцию.
♦ Тимоциты, связавшие какой-либо из комплексов «пептид- MHC» с правильной (т.е. средней по силе) аффинностью, получают сигнал на выживание и продолжают дифференцировку.
• На короткое время с мембраны тимоцитов исчезают обе корецепторные молекулы, а затем экспрессируется одна из них: тимоциты, распознавшие пептид в комплексе с MHC-I, экспрессируют корецептор CD8, а с MHC-II - корецептор CD4. Соответственно, на периферию выходят (в соотношении около 2:1) T-лимфоциты двух типов: CD8+ (или Т8) и CD4+ (или Т4), функции которых в предстоящих иммунных ответах различны.
♦ CD8+ T-лимфоциты выполняют функции цитотоксических T-лимфоцитов (ЦТЛ), или «перфорин-гранзимовых киллеров». Своим «клеточным телом» они непосредственно убивают клетки, на мембране которых они распознали Аг.
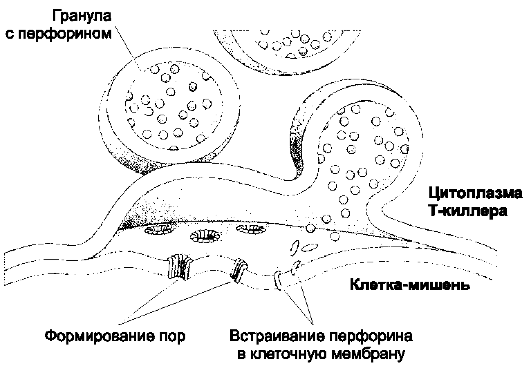 Рис. 6.3. Механизм воздействия цитотоксического T-лимфоцита на клетку-мишень. В
Рис. 6.3. Механизм воздействия цитотоксического T-лимфоцита на клетку-мишень. В
киллере гранулы с перфорином в ответ на увеличение концентрации Са2+ сливаются с клеточной мембраной. Освободившийся перфорин встраивается в мембрану клетки-мишени с последующим образованием пор, проницаемых для гранзимов, воды и ионов. В результате клетка-мишень лизируется.
♦ CD4+ T-лимфоциты. Функциональная специализация иммунных CD4+ T-лимфоцитов более разнообразна. Из них могут развиться перфорин-гранзимовые цитотоксические T- лимфоциты - CD4+ ЦТЛ (в частности, такие T-лимфоциты обнаружены в значительных количествах в коже больных с синдромом Лайелла). По-видимому, существенная часть CD4+ T-лимфоцитов в процессе развития иммунного ответа становится T-хелперами - «профессиональными» продуцентами цитокинов, «нанимающими» для разрушения повреждённых патогеном тканей другие клетки-исполнители.
• Иммунное отклонение. Изменение терминальной дифференцировки иммунных CD4+ T-лимфоцитов в сторону преобладания той или иной субпопуляции в процессе развития иммунного ответа называют иммунным отклонением.
Субпопуляции T-хелперов
С конца 80-х годов XX века было принято выделять две субпопуляции T-хелперов (в зависимости от того, какой набор цитокинов они продуцируют) - Th1 и Th2. В несколько преобразованном варианте эта концепция (несмотря на значительную её условность) «прижилась» среди иммунологов и врачей, и её продолжают использовать, выделяя следующие виды Т4-лимфоцитов:
• Th0 - Т4-лимфоциты на ранних стадиях развития иммунного
ответа, они продуцируют только ИЛ-2 (митоген для всех лимфоцитов);
• Th 1 - дифференцированная субпопуляция иммунных Т4-лимфоци- тов, специализирующаяся на продукции ИФНγ (менеджер осуществляемого активированными макрофагами иммунного воспаления в виде гиперчувствительности замедленного типа - ГЗТ);
• Th2 - дифференцированная субпопуляция иммунных Т4-лимфо- цитов, специализирующаяся на продукции ИЛ-4 и его «дублёра» ИЛ-13 (менеджер иммунного ответа с преобладанием продукции IgE и зависящих от него вариантов иммунного воспаления);
• Th3 - иммунные Т4-лимфоциты на более поздних стадиях развития иммунного ответа, переключившиеся на продукцию трансформирующего фактора роста (ТФРβ) - ингибитора пролиферации лимфоцитов;
• Тг - Т4-регуляторы, продуценты иммуносупрессорных цитокинов - ИЛ-10 (ингибитора активности макрофагов и Th1) и ТФРβ . Возможно также, что на мембране Тг экспрессированы индукторы апоптоза активированных и отработавших лимфоцитов - FasL (Fas-лиганд) и др.
В последующем стало известно, что каждый зрелый иммунный Т4-лимфоцит в каждый момент времени продуцирует только один цитокин (лишь в редких случаях, возможно, два), поэтому в настоящее время большинство авторов предлагают говорить не о разных субпопуляциях иммунных Т4-лимфоцитов, а о разных типах иммунного ответа.
Типы иммунного ответа
Иммунный ответ типа I
• Свойства. Доминируют ИФНγ и активированные макрофаги. Со стороны T-лимфоцитов такому ответу способствуют не только CD4+ Th1, но и другие продуценты ИФНγ - CD8+-лимфоциты и NK.
• Биологические эффекты ИФНγ, направлены на уничтожение клеток, инфицированных изнутри: - прямой противовирусный эффект на уровне ферментов нуклеиновых кислот (2'-5'-оли- гоаденилатсинтетаза и др.); - сильная стимуляция макрофагов, соответственно повышенный синтез токсичных продуктов макрофагов; - стимуляция NK. - ИФНγ поддерживает переключение синтеза иммуноглобулинов в B-лимфоцитах на IgG, что активирует фагоциты (нейтрофилы и макрофаги), т.е. T-лимфо- циты - продуценты ИФН - обеспечивают макрофагальный и
цитотоксический характер иммунного воспаления повреждённых патогеном тканей.
• Патогистология. Иммунное воспаление типа I - это очаги ГЗТ, гранулемы и им подобные изменения в тканях.
Иммунный ответ типа II
• Характеристика. Иммунный ответ типа II - ответ, управляемый другими цитокинами (например ИЛ-4). Продуценты ИЛ-4: CD4+ Th2, «нулевые» (CD4/CD8) T-лимфоциты, тучные клетки.
♦ Th2-лимфоциты поддерживают переключение синтеза изотипов иммуноглобулинов в B-лимфоцитах на IgE, IgG4 и IgА. Клет- ки-партнёры для этих изотипов - тучные клетки, базофилы и эозинофилы. При их активации развиваются воспалительные процессы с выраженным вазоактивным компонентом и экссудацией или характерное эозинофильное воспаление.
♦ За исключением патологических случаев IgE-зависимых аллергических реакций, иммунный ответ типа II принято рассматривать как противовоспалительный.
Примеры иммунного воспаления. Патологические процессы с превалированием иммунного воспаления типа I (Th1) или II (Th2) перечислены ниже.
• Th1 (I) (макрофагальное воспаление - ГЗТ, гранулемы: тиреоидит Хасимото; офтальмопатия; сахарный диабет типа I; рассеянный склероз; ревматоидный артрит; гастрит (Helicobacter pylori); боррелиоз Лайма; хронический гепатит С; острое отторжение аллотрансплантата; острая болезнь «трансплантат против хозяина»; саркоидоз; апластическая анемия; привычные аборты.
• Th2 (II) (Th2-зависящее воспаление - экссудативное, эозинофильное и др.): корь, синдром Оменна, атопические заболевания; хроническая болезнь «трансплантат против хозяина»; аллергический кератоконъюнктивит.
Лимфоциты Tγδ и тимуснезависимые антигены
99% T-лимфоцитов, проходящих лимфопоэз в тимусе, - это Tαβ; менее 1% - Tγδ. Последние в большинстве своём дифференцируются экстратимически, в первую очередь в слизистых оболочках ЖКТ. Среди всех T-лимфоцитов организма их доля оценивается от 10 до 50%. В эмбриогенезе Tγδ появляются раньше, чем Tαβ.
• Tγδ не экспрессируют CD4. Молекула CD8 экспрессирована на части Tγδ, но не в виде αβ-гетеродимера, как на CD8+ Tαβ, а в виде гомодимера из двух α-цепей.
• Функции Tγδ: продуценты цитокинов и/или цитотоксические T-лимфоциты.
• Антигенраспознающие свойства: TCRγδ в большей степени напоминают Ig, чем TCRαβ , т.е. способны связывать нативные Аг независимо от классических молекул MHC - для Tγδ не обязателен или вовсе не нужен предварительный процессинг Аг в АПК.
• Разнообразие TCRγδ больше, чем TCRαβ и Ig, т.е. в целом Tγδ способны распознавать широкий спектр Аг (в основном это фосфолипидные Аг микобактерий, углеводы, белки теплового шока).
• Тимуснезависимые Аг. Вещества подобной химической природы не могут быть процессированы до комплексов с молекулами MHC-I/II из-за своих химических свойств и, следовательно, не могут быть представлены для распознавания и распознаны Tαβ-лимфоцитами. Такие вещества называют тимуснезависимыми Аг и делят на два класса.
♦ Тимуснезависимые Аг 1-го класса (ТН-1) индуцируют поликлональную активацию B-лимфоцитов и продукцию поликлональных иммуноглобулинов. Эти вещества ещё называют B-клеточными митогенами. Участие T-лимфоцитов при этом вообще не требуется.
Иммунный ответ B-лимфоцитов без участия T-лимфоцитов характеризуется рядом свойств: АТ только класса M (нет переключения классов), нет иммунологической памяти, нет «созревания» аффинности. Но у подобного ответа есть и преимущество: он развивается уже в первые 2 суток после проникновения Аг и начинает защищать организм в ранние сроки инфекции, пока тимусзависимого ответа ещё нет.
♦ Тимуснезависимые Аг 2-го класса (ТН-2): полисахариды бактериальных стенок, содержащие много повторяющихся структур. ТН-2 (в отличие от ТН-1) способны активировать только зрелые B-лимфоциты. В незрелых B-лимфоцитах повторяющиеся антигенные эпитопы индуцируют анергию или апоптоз. Именно по ТН-2 «специализируются» преимущественно B1-лимфоциты
(CD5+).
Вероятно, именно в случае Аг ТН-2 имеет место взаимодействие B1-лимфоцитов с Tγδ-лимфоцитами или/и T-лимфоцитами TCRαβ/CD4-/CD8- (дважды негативными). Обе эти разновидности T-лимфоцитов связывают (распознают) полисахаридные Аг в комплексе с MHC-I-подобной молекулой CD1.