Иммунология : учебник. - Хаитов Р. М. - 2009. - 320 с. : ил.
|
|
|
|
ГЛАВА 5 АНТИТЕЛА. B-ЛИМФОЦИТЫ
Антиген
Антиген (Аг) - любое вещество (соединения разной химической природы: пептиды, углеводы, полифосфаты, стероиды), которое потенциально может быть распознано иммунной системой организма как чужеродное («не своё»). Таким образом, Аг - вещество, несущее признаки генетически чужеродной информации. В качестве синонима применяют также термин «иммуноген», подразумевая, что иммуноген (Аг) способен вызвать ответные реакции иммунной системы, в итоге приводящие к развитию приобретённого иммунитета. Способность вызывать такие ответные реакции (т.е. образование АТ и сенсибилизацию - приобретение организмом чувствительности к Аг) присуща не всей молекуле Аг, а только особой его части, её называют антигенная детерминанта, или эпитоп. У большинства белковых Аг такую детерминанту образует последовательность из 4-8 аминокислотных остатков, а у полисахаридных Аг - 3-6 гексозных остатков. Число детерминант у одного вещества может быть различным. Так, у яичного альбумина их не менее 5, у дифтерийного токсина - минимум 80, у тиреоглобулина - более 40. Различают Аг экзогенные (Аг, поступающие в организм извне) и эндогенные (аутоантигены - продукты: собственных клеток организма), а также Аг, вызывающие аллергические реакции, - аллергены.
Антитела
Антитело (АТ) - особый растворимый белок с определённой биохимической структурой (иммуноглобулин, который присутствует в сыворотке крови и других биологических жидкостях и предназначен для связывания Аг).
• Антитела связывают антиген. Существенным и уникальным свойством АТ, отличающим их даже от TCR, является их способность связывать Аг непосредственно в том виде, в каком он проникает
в организм. При этом не требуется времени на предварительную метаболическую обработку Аг, поэтому АТ являются единственным фактором безотлагательной защиты организма (например, от сильных ядов, при укусах змей, скорпионов, пчёл и др.).
• Конкретное антитело синтезирует только и исключительно клон B-лимфоцита. При дифференцировке каждый единичный В-лимфоцит и его митотически возникшие дочерние клетки (клон В-лимфоцитов) становятся способными к синтезу единственного варианта АТ по признаку структуры Аг-связывающего центра молекулы - то есть имеет место клональность биосинтеза иммуноглобулинов.
• Множество антител. В то же время вся совокупность B-лимфоцитов организма способна синтезировать поразительное разнообразие АТ - около 106-109, но точно подсчитать, сколько разных Аг потенциально способно связать одно АТ, принципиально невозможно.
• Иммуноглобулины. Все АТ являются белками, имеющими глобулярную вторичную структуру, поэтому молекулы этого типа и названы иммуноглобулинами. Иммуноглобулины отнесены к надсемейству иммуноглобулинов (рис. 5.1), куда входят также белки MHC, некоторые молекулы адгезии - LFA-2 (CD2), ICAM-1 (CD54), VCAM-1 (CD106) и др. (см. табл. 4.1.), TCR, отдельные Рц для цитокинов - для ИЛ-1 типов I и II, Ил-6, M-CSF, c-kit (CD117), Рц для Fc-фрагментов Ig (FcαR, FcγRI, FcγRII), мембранные молекулы CD3, CD4, CD8, CD80 и др.
ИММУНОГЛОБУЛИНЫ
Иммуноглобулины (международная аббревиатура - Ig) - класс структурно связанных белков, содержащих два вида парных полипептидных цепей: лёгкие (L, от Light - лёгкий), с низкой молекулярной массой, и тяжёлые (H, от Heavy - тяжёлый), с высокой молекулярной массой. Все четыре цепи соединены вместе дисульфидными связями. Принципиальная схема строения молекулы иммуноглобулина (мономер) приведена на рис. 5.2.
Классы иммуноглобулинов
На основании структурных и антигенных признаков H-цепей Ig подразделяют (в порядке относительного содержания в крови) на 5 классов АТ: IgG (80%), IgA (15%), IgM (10%), IgD (менее 0,1%), IgE (менее 0,01%). Заглавная латинская буква справа от Ig обозначает
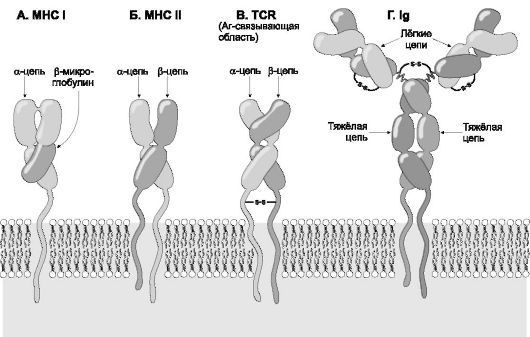 Рис. 5.1. Структура белков надсемейства иммуноглобулинов. А. Молекула MHC I класса состоит из α-цепи, внемембранная её часть связана с короткой цепью β2-
микроглобулина. Б. Молекула MHC II класса состоит из двух субъединиц:
более длинной α-цепи и β-цепи. Часть каждой цепи выступает над
поверхностью клеточной мембраны, цепь содержит трансмембранный участок и
небольшой фрагмент в цитоплазме. В. Аг-связывающая область молекулы TCR
состоит из двух цепей: α и β. Каждая цепь представлена двумя
внеклеточными Ig-подобными доменами, стабилизированными при помощи S-S
связей, вариабельным внеклеточным NH-концом и цитоплазматическим
стабильным COOH-концом. SH-группа, присутствующая в цитоплазматическом
фрагменте α-цепи, может взаимодействовать с мембранными или
цитоплазматическими белками. Г. Мономер молекулы IgM встраивается в
плазматическую мембрану B-лимфоцитов, это рецептор для Аг. Молекулярная
структура TCR весьма сходна со структурой молекул MHC и Ig. Разнообразие
структуры TCR и Ig обеспечивается возможностью сайт-специфической
рекомбинации множества различных генных сегментов, кодирующих отдельные
фрагменты молекулы.
Рис. 5.1. Структура белков надсемейства иммуноглобулинов. А. Молекула MHC I класса состоит из α-цепи, внемембранная её часть связана с короткой цепью β2-
микроглобулина. Б. Молекула MHC II класса состоит из двух субъединиц:
более длинной α-цепи и β-цепи. Часть каждой цепи выступает над
поверхностью клеточной мембраны, цепь содержит трансмембранный участок и
небольшой фрагмент в цитоплазме. В. Аг-связывающая область молекулы TCR
состоит из двух цепей: α и β. Каждая цепь представлена двумя
внеклеточными Ig-подобными доменами, стабилизированными при помощи S-S
связей, вариабельным внеклеточным NH-концом и цитоплазматическим
стабильным COOH-концом. SH-группа, присутствующая в цитоплазматическом
фрагменте α-цепи, может взаимодействовать с мембранными или
цитоплазматическими белками. Г. Мономер молекулы IgM встраивается в
плазматическую мембрану B-лимфоцитов, это рецептор для Аг. Молекулярная
структура TCR весьма сходна со структурой молекул MHC и Ig. Разнообразие
структуры TCR и Ig обеспечивается возможностью сайт-специфической
рекомбинации множества различных генных сегментов, кодирующих отдельные
фрагменты молекулы.
 Рис. 5.2. Молекула иммуноглобулина. L
- лёгкие цепи; H - тяжёлые цепи; V - вариабельная область; С -
константная область; N-концевые области L- и H-цепей (V-область)
образуют два Аг-связывающих центра: (Fab)2-фрагмент.
Fc-фрагмент молекулы взаимодействует со своим рецептором в мембране
различных типов клеток (макрофаг, нейтрофил, тучная клетка).
Рис. 5.2. Молекула иммуноглобулина. L
- лёгкие цепи; H - тяжёлые цепи; V - вариабельная область; С -
константная область; N-концевые области L- и H-цепей (V-область)
образуют два Аг-связывающих центра: (Fab)2-фрагмент.
Fc-фрагмент молекулы взаимодействует со своим рецептором в мембране
различных типов клеток (макрофаг, нейтрофил, тучная клетка).
класс иммуноглобулина - М, G, А, Е или D. Молекулы IgG, IgD и IgE представлены мономерами, IgM - пентамерами; молекулы IgA в сыворотке крови - мономеры, а в экскретируемых жидкостях (слёз- ная, слюна, секреты слизистых оболочек) - димеры (рис. 5.3).
• Подклассы. У иммуноглобулинов классов G (IgG) и A (IgA) имеется несколько подклассов: G1, G2, G3, G4 и A1, A2.
• Изотипы. Классы и подклассы иммуноглобулинов иначе называют изотипами, они одинаковы у всех особей данного вида.
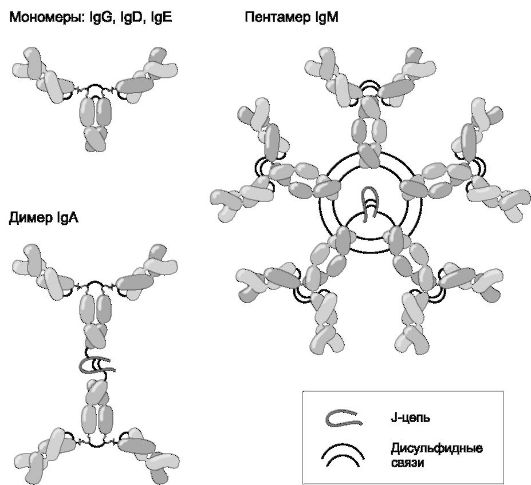 Рис. 5.3. Мономеры и полимеры иммуноглобулинов. J-цепь (от англ. Joint - связь) связывает остатки цистеина на C-концах тяжёлых цепей IgM и IgA.
Рис. 5.3. Мономеры и полимеры иммуноглобулинов. J-цепь (от англ. Joint - связь) связывает остатки цистеина на C-концах тяжёлых цепей IgM и IgA.
• Аллотипы. Индивидуальные аллельные варианты иммуноглобулинов в пределах одного изотипа называются аллотипами.
• Идиотипы. По антигенной специфичности АТ относят к различным идиотипам.
Структура иммуноглобулинов
• Фрагменты молекулы Ig (рис. 5.2). Путём протеолитического расщепления молекулы Ig с последующей ионообменной хроматографией можно получить 3 фрагмента: Fc-фрагмент и 2 Fab- фрагмента.
♦ Fab-фрагменты (Fragment, antigen binding - Аг-связывающие фрагменты) - два одинаковых фрагмента, сохраняющие способность связывать Аг.
♦ Fc-фрагмент (Fragment, constant or crystallizable - константный фрагмент) - непарный, легко кристаллизуется. Fc-фрагменты иммуноглобулинов в пределах одного изотипа строго идентичны (независимо от специфичности АТ по Аг). Они обеспечивают взаимодействие комплексов Аг-АТ с системой комплемента, фагоцитами, эозинофилами, базофилами, тучными клетками. При этом каждый класс иммуноглобулинов взаимодействует только с определёнными «исполнителями» элиминации Аг.
• Тяжёлые цепи определяют различия между классами Ig, поэтому разные типы тяжёлых цепей обозначают греческими буквами соответственно латинской аббревиатуре класса: для IgM - μ, для IgG - γ, для IgA - α, для IgE - ε, для IgD - δ. Каждая из H- цепей молекул IgG, IgD и IgA состоит из 4 доменов (см. рис. 5.2): вариабельного - VH и константных (CH1, CH2, CH3). H-цепи молекул IgM и IgE содержат дополнительный домен - СН4.
• Лёгкие цепи примыкают к N-концу тяжёлых цепей. Каждая L-цепь состоит из двух доменов - VL и CL. Известно два типа лёгких цепей Ig - κ (каппа) и λ (лямбда). Функциональные различия между Ig с лёгкими κ- или λ-цепями не выявлены.
• Домены. Вторичная структура полипептидных цепей представлена доменами (см. рис. 5.1), каждый из которых включает около 110 остатков АК.
♦ V-домены обеих цепей имеют сильно варьирующий АК-состав (отсюда и их обозначение - Variable), что позволяет им связывать разные Аг.
- Гипервариабельные участки. Внутри V-доменов выделяют несколько (3-4) гипервариабельных участков: HV1, HV2, HV3, HV4 (HV - от Hypervariable). Другое обозначение - CDR (Complementarity Determining Regions), т.е. области молекулы Ig, определяющие её комплементарность Аг.
- Каркасные области. Промежутки между гипервариабельными участками HV или CDR обозначают как FR (Framework Regions), т.е. каркасные области. Их также 4: FR1, FR2, FR3 и FR4. Помимо чисто «скелетной», им случается выполнять и другие функции, отличные от связывания с Аг: FR-участки V-области молекул Ig могут обладать ферментативной (протеазной и нуклеазной) активностью, связывать ионы металлов и суперантигены.
• C-домены. Остальные домены имеют строго инвариантный для каждого изотипа иммуноглобулинов АК-состав и называются C-доменами (от Constant).
- В C-доменах и в FR-участках V-доменов содержатся одинаковые АК-последовательности, что рассматривают как молекулярное свидетельство генетической общности. - Гомологичные последовательности АК присутствуют (помимо Ig) и в молекулах других белков, которые объединяют с Ig в одно молекулярное надсемейство - надсемейство иммуноглобулинов (см. выше и рис. 5.1). Большое количество возможных комбинаций L- и H-цепей со- здаёт многообразие АТ каждого индивидуума.
• Формы иммуноглобулинов. Молекулы Ig одной и той же специфичности по Аг присутствуют в организме в 3 формах: растворимой, трансмембранной и связанной.
• Растворимая. В крови и других биологических жидкостях (секретируемый клеткой Ig).
• Трансмембранная. На мембране В-лимфоцита в составе Рц В- лимфоцитов для Аг - BCR (B-Cell Receptor). Трансмембранные формы всех классов Ig (включая IgM и IgA) - мономеры.
• Связанная, т.е. в связи с клетками (макрофагами, нейтрофилами, эозинофилами), но не в трансмембранном варианте, а связанные FCR клетки за Fc-конец. Все АТ, кроме IgE, могут фиксироваться FcR клеток только в комплексе с Аг.
Связывание антигена
Гипервариабельные участки V-области АТ (как и TCR) непосредственно и комплементарно связывают Аг с помощью ионных, ван-дер-ваальсовых, водородных и гидрофобных взаимодействий (сил, связей).
• Эпитоп (антигенная детерминанта - см. выше) - участок молекулы Аг, который непосредственно вступает в ионные, водородные, ван-дер-ваальсовы и гидрофобные связи с активным центром Fab-фрагмента.
• Сродство между Аг и АТ количественно характеризуют понятиями «аффинность» и «авидность».
• Аффинность. Силу химической связи одного антигенного эпитопа с одним из активных центров молекулы Ig называют аффинностью связи АТ с Аг. Аффинность количественно принято оценивать по константе диссоциации (в моль-1) одного антигенного эпитопа
с одним активным центром.
Так как у цельных молекул мономерных Ig имеется по два потенциально равнодееспособных симметрично расположенных активных центра для связывания Аг, у димерного IgA - 4, а у пентамерного IgM - 10, скорость диссоциации цельной молекулы Ig со всеми связанными эпитопами меньше, чем скорость диссоциации одного из активных центров.
• Авидность. Силу связи цельной молекулы АТ со всеми антигенными эпитопами, которые ей удалось связать, называют авидностью связи АТ с Аг.
ГЕНЫ ИММУНОГЛОБУЛИНОВ
Зародышевые гены иммуноглобулинов. У здорового человека B-лим- фоциты в течение жизни создают несколько миллионов вариантов АТ, связывающих разные Аг (потенциально 1016 Аг). Никакой геном физически не несёт столько различных структурных генов. Количество наследуемого от родителей генетического материала (ДНК), определяющего биосинтез АТ, не так уж и велико - немногим более 120 структурных генов. Это наследуемое множество генов - зародышевые гены Ig (зародышевая конфигурация генов).
Гены вариабельных доменов
Во всех соматических клетках, включая СКК, гены Ig находятся именно в зародышевой конфигурации, где гены V-участков представлены в виде отдельных сегментов, расположенных друг относительно друга на уловимом расстоянии и сгруппированных в несколько кластеров: собственно V (вариабельный), J (связующий), а у тяжёлых цепей также D (от англ. Diversity - разнообразие).
Процесс генерации разнообразия структурных генов для миллионов вариантов V-участков молекул Ig продолжается в течение всей жизни в процессе дифференцировки B-лимфоцитов и является запрограммированно случайным. В его основе лежат три механизма, свойственные только генам Аг-связывающих молекул (Ig, TCR): соматическая рекомбинация, неточность связи V-D-J и гипермутагенез.
• Соматическая рекомбинация. Феномен соматической рекомбинации ДНК заключается в том, что на самом раннем этапе дифференцировки лимфоцитов начинается сложный генетический процесс объединения сегментов ДНК, предназначенных для коди-
рования разных частей молекулы Ат-связывающих молекул - V- и C-доменов. В непрерывную последовательность ДНК соединяются по одному сегменту из V-, D- и J-областей, при этом в каждом отдельном B-лимфоците возникает уникальная комбинация VDJ для тяжёлой цепи и VJ - для каждой из лёгких цепей. Вся остальная ДНК зародышевого гена выбрасывается из генома в виде кольцевых ДНК.
♦ Число возможных комбинаций можно подсчитать. Для κ-цепи из 40 V-сегментов и 5 J-сегментов может получиться 40*5 = 200 вариантов V-области; для λ-цепи - 30*4 = 120 вариантов; всего для лёгких цепей 320 вариантов; для тяжёлой цепи 50V*30D*6J = 9000 вариантов Аг-связывающих областей. В цельной молекуле Ig разные лёгкие и тяжёлые цепи объединяются в тетрамер также случайным образом (по крайней мере теоретически). Число случайных сочетаний из 320 и 9000 - около 3x106.
♦ Рекомбиназы. Рекомбинацию ДНК Ig катализируют специальные ферменты - рекомбиназы. Они же катализируют рекомбинацию ДНК генов TCR в T-лимфоцитах, т.е. рекомбиназы - уникальные ферменты лимфоцитов. Но в B-лимфоцитах эти ферменты не «трогают» гены TCR, а в T-лимфоцитах «обходят» гены Ig. Следовательно, до начала процесса перестройки ДНК в клетке уже существуют регуляторные белки - различные у T- и B-лимфоцитов.
• Неточность связи V-D-J. Под неточностью связи V-D-J понимают тот факт, что при формировании этих связей происходит добавление лишних нуклеотидов. Их два «сорта»: P-нуклеотиды и N-нуклеотиды.
♦ Нуклеотиды P (от англ. Palindromic sequences - зеркальные последовательности) возникают на концах сегментов при вырезании одноцепочечных петель ДНК и «достройки хвостов» ферментами репарации ДНК.
♦ Нуклеотиды N (от Nontemplate-encoded - нематрично кодируемые), характерные только для тяжёлых цепей, случайным образом пристраиваются к ДНК специальным ферментом - терминальной дезоксинуклеотидилтрансферазой.
♦ С учётом присоединения N- и P-нуклеотидов число вариантов антигенсвязывающих областей цельных молекул Ig оказывается порядка 1013. Если учесть аллельные варианты V-, D- и J-сегментов, то мыслимое разнообразие составит около 1016 (в
действительности это число меньше, так как в организме нет
такого количества лимфоцитов). ♦ «Платой» за эти попытки увеличить разнообразие Аг-связы-
вающих областей АТ в 2/3 случаев является непродуктивная
рекомбинация генов, т.е. сдвиг рамки считывания, делающий
• невозможной трансляцию белка. Гипермутагенез - запланированное повышение частоты точечных мутаций - отличает гены иммуноглобулинов даже от генов TCR. Гипермутагенез имеет место только в В-лимфоцитах во время иммуногенеза (т.е. после состоявшегося распознавания Аг и начавшегося иммунного ответа) в лимфоидных фолликулах периферических лимфоидных органов и тканей (лимфатических узлов, селёзенки, диффузных скоплений). Частота точечных мутаций в генах V-Ig достигает одного нуклеотида из 1000 на один митоз (т.е. каждый второй В-лимфоцит клона в зародышевом центре приобретает точечную мутацию в V-Ig), тогда как для всей остальной ДНК она на 9 порядков ниже.
Гены константных доменов
Структурные гены константных частей полипептидных цепей Ig расположены в тех же хромосомах, что и V-, D- и J-гены, «ниже по течению», т.е. к 3'-концу от J-сегментов.
 Завершившие
лимфопоэз B-лимфоциты (независимо от Аг-специфичности) экспрессируют
иммуноглобулины только классов M и D (IgM и IgD). При этом мРНК
транскрибируется в виде непрерывного первичного транскрипта с
перестроенных генов VDJ и Cμ-Cδ. При этом ДНК остальных C-генов других изотипов остаётся целой и невредимой. В
результате альтернативного сплайсинга первичного транскрипта образуются
мРНК отдельно для тяжёлых цепей IgM и IgD, которые и транслируются в
белок. Этим процессом заканчивается полноценный лимфопоэз В-лимфоцитов.
Завершившие
лимфопоэз B-лимфоциты (независимо от Аг-специфичности) экспрессируют
иммуноглобулины только классов M и D (IgM и IgD). При этом мРНК
транскрибируется в виде непрерывного первичного транскрипта с
перестроенных генов VDJ и Cμ-Cδ. При этом ДНК остальных C-генов других изотипов остаётся целой и невредимой. В
результате альтернативного сплайсинга первичного транскрипта образуются
мРНК отдельно для тяжёлых цепей IgM и IgD, которые и транслируются в
белок. Этим процессом заканчивается полноценный лимфопоэз В-лимфоцитов.
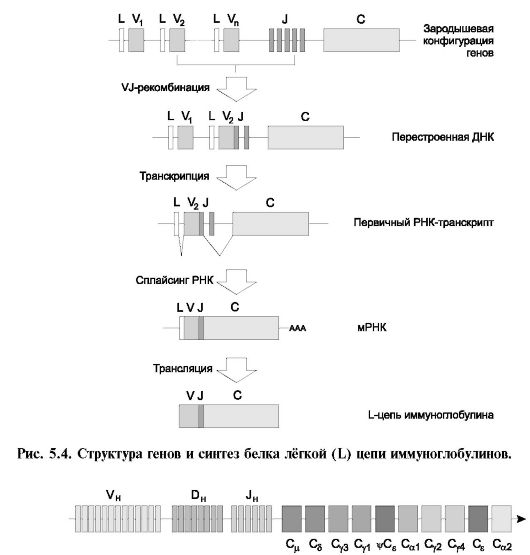 Рис. 5.5. Структура генов тяжёлой (Н) цепи иммуноглобулинов человека.
Рис. 5.5. Структура генов тяжёлой (Н) цепи иммуноглобулинов человека.
Переключение изотипов иммуноглобулинов
• В процессе развития иммунного ответа, т.е. после распознавания Аг и под воздействием определённых цитокинов и молекул клеточной мембраны T-лимфоцитов может происходить переключение синтеза Ig на другие изотипы - IgG, IgE, IgA (рис. 5.6). Переключение изотипа тяжёлой цепи тоже идёт по механизму рекомбинации ДНК: к ранее перестроенной комбинации VDJ присоединяется один из C-генов тяжёлой цепи (либо Сγ1, либо Сγ2, либо Сγ3, либо Сγ4, либо Сε, либо Сα1, либо Сα2). При этом ДНК разрывается по областям переключения - SR (Switch Region),
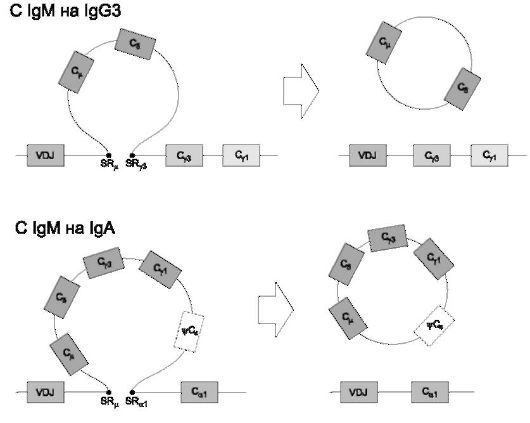 Рис. 5.6. Рекомбинация ДНК при переключении изотипов иммуноглобулинов B-лимфо- цитов.
Рис. 5.6. Рекомбинация ДНК при переключении изотипов иммуноглобулинов B-лимфо- цитов.
расположенным в интронах перед каждым C-геном (за исключением Сδ).
ДНК C-генов, предшествующих задействованному, элиминируется в виде кольцевых структур, поэтому дальнейшее переключение изотипа возможно только по направлению к 3'-концу.
B-ЛИМФОЦИТЫ Рецептор BCR
Молекула Ig способна связывать Аг как в растворе, так и будучи связанной с клеткой, но для формирования полноценного клеточного Рц для Аг (BCR) необходимы ещё два полипептида, называемые (на наш взгляд, неудачно) Igα (CD79a) и Igβ (CD79b). Все шесть полипетидньгх цепей BCR показаны на рис. 5.7.
• Внеклеточный домен. Igα и Igβ имеют по одному внеклеточному домену, которым они прочно, но нековалентно связаны с тяжёлыми цепями иммуноглобулинового компонента BCR.
• Цитоплазматические активирующие последовательности. В цитоплазматических участках Igα и Igβ присутс-
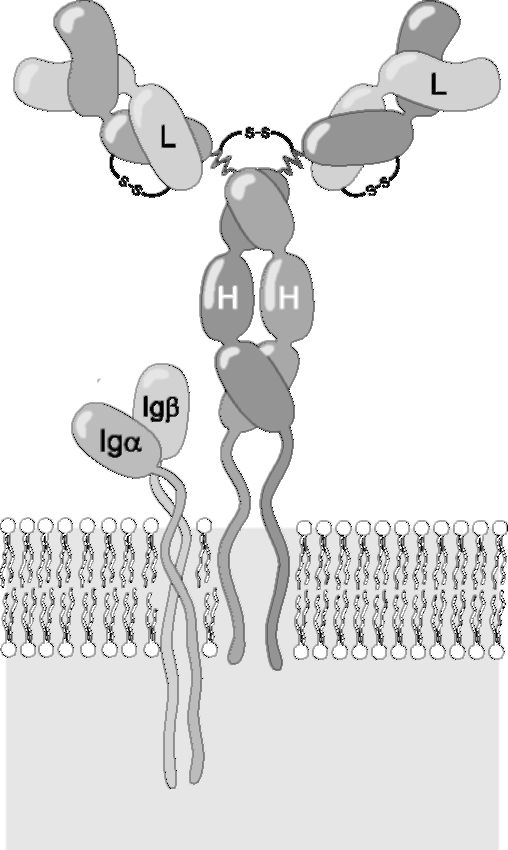 Рис. 5.7. Рецептор для антигена B-лимфоцита.
Рис. 5.7. Рецептор для антигена B-лимфоцита.
твуют характерные последовательности АК-остатков, называемые иммунорецепторными тирозинсодержащими активирующими последовательностями (ITAM - Immunoreceptor Tyrosine-based Activation Motif); такие же последовательности присутствуют в проводящих сигнал компонентах Рц T-клеток для Аг. Активация B-лимфоцита. Для эффективной активации В-клетки через BCR необходима перекрёстная «сшивка» Аг нескольких BCR. Для этого молекула Аг должна иметь повторяющиеся эпитопы на своей поверхности. Дальнейшие события активации B-лимфоцита показаны на рис. 5.8.
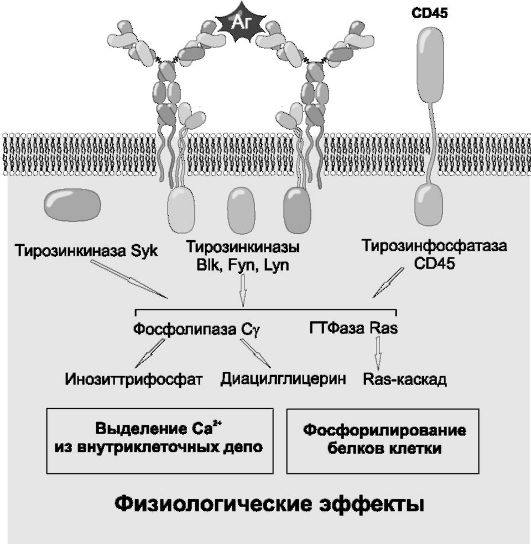 Рис. 5.8. Активация B-лимфоцита: внутриклеточная передача «сигнала».
Рис. 5.8. Активация B-лимфоцита: внутриклеточная передача «сигнала».
Корецепторный комплекс
Повторяющиеся эпитопы есть не на каждом Аг; следовательно, не каждый Аг способен вызвать перекрёстную сшивку BCR, поэтому необходим дополнительный корецепторный комплекс мембранных молекул, связанных с внутриклеточными системами проведения сигналов. В этот комплекс входят по крайней мере три мембранные
молекулы: CD19, CR2 (CD21) и TAPA-1 (CD81).
• CR2 - Рц для компонентов комплемента. Связывание Рц с продуктами деградации C3b, C3dg и C3bi вызывает фосфорилирование молекулы CD19 ассоциированными с BCR киназами.
• CD19. Фосфорилированная молекула CD19 активирует фосфати- дилинозит-3-киназу и молекулу vav (многофункциональная молекула проведения внутриклеточных сигналов), которые усиливают активационные реакции, инициированные BCR (рис. 5.8).
• TAPA-1 (Target of Antiproliferative Antibody - мишень для антипролиферативных АТ) в мембране физически примыкает к CD19 и CR2, но роль этой молекулы неизвестна.
Дифференцировка B-лимфоцитов
Дифференцировка B-лимфоцитов из общей лимфоидной клетки-предшественника (потомка СКК) состоит из следующих этапов и процессов: - перестройка генов Ig и интеграция их продуктов в клеточный метаболизм; - экспрессия генов молекул, обеспечивающих проведение сигнала с BCR внутрь клетки; - экспрессия генов мембранных молекул, необходимых для взаимодействия с другими клетками (в первую очередь с T-лимфоцитами и ФДК); - экспрессия на мембране корецепторных комплексов.
B2-лимфоциты
• Этапы B2-лимфопоэза. В лимфопоэзе B2-лимфоцитов выделяют 6 этапов: общая лимфоидная клетка-предшественник → ранняя про-B-клетка → поздняя про-B-клетка → большая пре-B-клет- ка → малая пре-B-клетка → незрелая B-клетка → зрелая неиммунная B-клетка (выходит из костного мозга в периферическую лимфоидную ткань).
♦ Общая лимфоидная клетка-предшественник. Экспрессируется несколько молекул адгезии, обеспечивающих оседлость в течение необходимого периода времени в костном мозгу, среди них VLA-4 (Very Late Activation Antigen-4 - очень поздний активационный Аг 4), лигандом которого на клетках стромы является VCAM-1 (Vascular Cell Adhesion Molecule-1 - моле- кула-1 адгезии к стенке сосуда).
♦ Ранняя про-B-клетка. Происходит перестройка D-J в генах тяжёлых цепей, причём на обеих гомологичных хромосомах. В этой стадии (помимо молекул адгезии) экспрессируется Рц c-kit (CD117) для первого фактора роста - мембранной молекулы клеток стромы SCF - стволовоклеточного фактора.
Это взаимодействие обеспечивает надлежащее число митозов предшественников B-лимфоцитов, ещё не поделённых на клоны по Рц для Аг.
♦ Поздняя про-B-клетка. Происходит рекомбинация ДНК V-DJ сначала на одной из гомологичных хромосом. Если она окажется непродуктивной, то та же попытка делается на второй гомологичной хромосоме. Если перестройка на первой хромосоме продуктивна, вторая хромосома использована не будет.
- Как только в клетке происходит трансляция полипептида тяжёлой цепи, он экспрессируется на мембране в составе так называемого пре-B-Рц. Его экспрессия транзиторна, но абсолютно необходима для правильной дифференцировки B-лимфоцитов.
- На поздней про-B-клетке также экспрессируются Рц для цитокинов ИЛ-7 и SDF-1, секретируемых клетками стромы и вызывающих пролиферацию и накоплению «полуклонов» B-лимфоцитов (про-B- и больших пре-B-клеток) с уже известной специфичностью по тяжёлой цепи, но ещё неизвестной - по лёгкой. Это тоже увеличивает разнообразие молекул Ig: с одной и той же тяжёлой цепью будет сочетаться больше разных вариантов лёгких цепей.
♦ Пре-B-клетка. Происходит перестройка V-J лёгких цепей (сначала одной из цепей - κ или λ) на одной из гомологичных хромосом. Если продуктивная перестройка не получится с первой попытки, предпринимаются следующие. Клетки, в которых не получилось ни одной продуктивной перестройки в генах тяжёлых и лёгких цепей, погибают по механизму апоптоза - явления, весьма распространённого среди лимфоцитов.
♦ Незрелый B-лимфоцит. Уже экспрессируется дефинитивный BCR состава: L-цепь + μ-цепь + Igα + Igβ.
• Развитие толерантности. На стадии незрелых B-лимфоцитов начинается также развитие толерантности к собственным тканям организма. Для этого предусмотрено три механизма: делеция аутореактивных клонов, ареактивность (анергия) и «редактирование» Рц по антигенной специфичности. Первые два механизма продолжают действовать и по выходе лимфоцита из костного мозга, т.е. при контакте со значительными количествами аутоантигенов.
♦ Делеция клонов. Связывание мембранного Аг незрелой B-клеткой (имеется Аг-распознающий Рц с IgM, но ещё нет Рц с IgD) является сигналом для апоптоза. Таким образом удаляются
B-лимфоциты, несущие Рц, способные связывать белки собственных тканей.
♦ Ареактивность. Связывание незрелого B-лимфоцита с растворимым Аг не приводит к апоптозу, но лимфоцит приходит в состояние анергии, т.е. вместо активации лимфоцита к иммунному ответу блокируется проведение сигнала.
♦ «Редактирование» рецепторов происходит в небольшой части незрелых B-клеток, в которых ещё активны рекомбиназы. В этих клетках связывание IgM в составе BCR на поверхности незрелого B-лимфоцита с Аг является сигналом для запуска нового процесса рекомбинации VDJ/VJ на второй из двух гомологичных хромосом: если «повезёт», новая комбинация не будет аутореактивной.
• Маркёр завершения B-лимфопоэза (образования зрелого неиммунного B-лимфоцита, готового к выходу из костного мозга в периферическую лимфоидную ткань) - одновременная экспрессия (коэкспрессия) на мембране 2-х типов BCR - с IgM и IgD (причём IgD больше, чем IgM).
• Иммуногенез. После распознавания Аг и вступления в иммунный ответ B-лимфоцит проходит в фолликулах периферических лимфоидных органов и тканей ещё две стадии додифференцировки, которые называют иммуногенезом.
♦ Пролиферация центробластов. В фолликулах B-лимфоциты, называемые на этой стадии центробластами, интенсивно пролиферируют, удерживаясь связями со специальными клетками стромы - дендритными клетками фолликулов (ФДК).
о На ФДК экспрессированы необычные Рц для иммуноглобулинов (FcR), способные продолжительное время (дни, месяцы, возможно, годы) удерживать комплекс Аг-АТ на мембране клетки.
о В центробластах происходит возрастание аффинности АТ в отношении своего Аг по механизму гипермутагенеза, так как на этом этапе дифференцировки выживают те из вновь мутировавших B-лимфоцитов, у которых аффинность BCR к Аг на поверхности ФДК выше.
♦ Выбор дальнейшего пути. На второй стадии иммуногенеза происходит выбор: B-лимфоцит становится либо B-лимфоцитом памяти (дифференцированный резерв на случай повторной встречи с тем же Аг), либо плазмоцитом - терминальным продуцентом больших количеств секретируемых АТ заданной специфичности
(рис. 5.9).
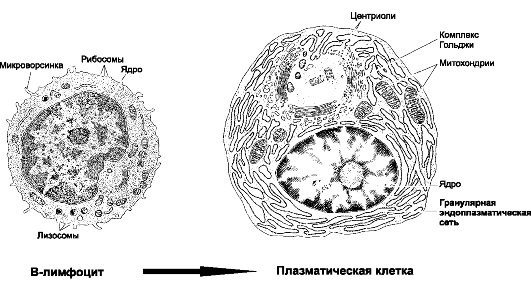 Рис. 5.9. B-лимфоцит и плазматическая клетка. Активированные
B-лимфоциты, т.е. получившие информацию о структуре конкретной
антигенной детерминанты и сигнал к пролиферации, размножаются и
додифференцируются. Совокупность окончательно дифференцированных
потомков B-лимфоцита составляет клон плазматических клеток,
синтезирующих АТ (Ig) именно к этой и только к этой антигенной
детерминанте. Обратите внимание, что в цитоплазме плазматической клетки
находится огромное количество синтезирующего белок (Ig) аппарата -
гранулярной эндоплазматической сети. На мембране плазмоцита уже нет ни
Ig, ни MHC-II, в них прекращается переключение классов Ig и
гипермутагенез, а продукция АТ уже не зависит от контакта с Аг и
взаимодействий с T-лимфоцитами.
Рис. 5.9. B-лимфоцит и плазматическая клетка. Активированные
B-лимфоциты, т.е. получившие информацию о структуре конкретной
антигенной детерминанты и сигнал к пролиферации, размножаются и
додифференцируются. Совокупность окончательно дифференцированных
потомков B-лимфоцита составляет клон плазматических клеток,
синтезирующих АТ (Ig) именно к этой и только к этой антигенной
детерминанте. Обратите внимание, что в цитоплазме плазматической клетки
находится огромное количество синтезирующего белок (Ig) аппарата -
гранулярной эндоплазматической сети. На мембране плазмоцита уже нет ни
Ig, ни MHC-II, в них прекращается переключение классов Ig и
гипермутагенез, а продукция АТ уже не зависит от контакта с Аг и
взаимодействий с T-лимфоцитами.
Описанный путь дифференцировки характерен для B2-лимфоцитов, которые давно известны и хорошо изучены. Однако, существует и другая субпопуляция B-лимфоцитов - B1-клетки.
B1-лимфоциты
• Клетки-предшественники B1-лимфоцитов отселяются из кроветворной ткани в брюшную и плевральную полости ещё в эмбриональном периоде, поэтому их пул у взрослых за счёт костного мозга не пополняется.
• Предназначение B1-лимфоцитов - быстрая реакция на «просачивающиеся» в прибарьерные полости инфекционные микроорганизмы из числа широко распространённых.
• АТ B1-лимфоцитов не очень разнообразны, но полиспецифичны. Почти все они относятся к IgM, распознаваемые ими Аг - наиболее распространённые соединения клеточных стенок бактерий.
• Преобладающая часть Ig сыворотки крови здорового человека синтезируется именно B1-лимфоцитами.
Конститутивные иммуноглобулины
Ещё до встречи с каким бы то ни было внешним Аг, в крови и биологических жидкостях организма уже присутствуют так называемые нормальные (конститутивные) иммуноглобулины. У взрослых большинство из них относится к IgG, но есть также IgA и IgM. Эти АТ способны связывать множество Аг (как ауто-, так и экзогенных). Мишенями для нормальных Ig могут быть: другие иммуноглобулины; TCR; молекулы CD4, CD5 и HLA-I; FcγR; лиганды для молекул межклеточной адгезии и др.
Функции нормальных АТ. Есть основания полагать, что нормальные АТ выполняют ряд весьма важных для здоровья организма функций: - «первая линия обороны» против инфекций; - удаление из организма отживших клеток и продуктов катаболизма; - представление Аг для T-лимфоцитов; - поддержание гомеостаза аутоиммунной реактивности; - противовоспалительное действие (нейтрализация суперантигенов; индукция синтеза противовоспалительных цитокинов; аттенуация комплементзависимого повреждения тканей и др.).