Гигиена с основами экологии человека : учебник - Архангельский В.И. и др.; под ред. П.И. Мельниченко. 2010. - 752 с.: ил.
|
|
|
|
ГЛАВА 7 ПИТАНИЕ И ЗДОРОВЬЕ ЧЕЛОВЕКА
Питание определяет продолжительность и качество жизни человека. Ошибки в структуре питания становятся одной из причин многих тяжелых заболеваний, в том числе самых распространенных - сердечно-сосудистых и онкологических. Гигиенические мероприятия по профилактике алиментарно-зависимых заболеваний основаны на современных знаниях о сущности процессов обмена веществ и поддержания гомеостаза.
Всасывание (ассимиляция) пищевых веществ в желудочно-кишечном тракте человека осуществляется включением механизмов полостного (внеклеточного) и мембранного пищеварения в виде лишенных видовой специфичности мономеров - аминокислот, моносахаридов, жирных кислот. Помимо питательных веществ, в процессе ассимиляции принимают участие также витамины, минеральные вещества, гормоны и другие физиологически активные соединения, продукты жизнедеятельности микрофлоры кишечника и чужеродные для организма вещества (ксенобиотики).
Сохранение постоянства внутренней среды является важнейшим условием нормального обмена веществ в организме. Даже при случайном выборе пищевых продуктов, когда количество и соотношения нутриентов варьируют в значительных пределах, состав питательных веществ, поступающих во внутреннюю среду, изменяется незначительно. В тонкой кишке наряду с транспортом веществ из ее полости в кровь постоянно существует и противоположно направленный поток - из крови в полость.
Увеличение содержания какого-либо компонента в рационе сказывается на всасывании не только этого, но и других компонентов. Так, повышение концентрации углеводов увеличивает всасывание всех остальных веществ. Увеличение содержания жиров и азотистых веществ сопровождается увеличением всасывания только их самих и незначительным уменьшением всасывания других компонентов.
Благодаря секреции белков плазмы в просвет кишечника и их протеолитическому расщеплению аминокислотный состав среды при поступлении с пищей неполноценных белков нормализуется.
Более 80% массы аминокислот, используемых ежедневно организмом для синтеза белков, поступает не из пищи, а освобождается в организме при реакциях гидролиза собственных белков.
7.1. ЗНАЧЕНИЕ ПИЩЕВЫХ ВЕЩЕСТВ В ОБЕСПЕЧЕНИИ ЖИЗНЕДЕЯТЕЛЬНОСТИ ОРГАНИЗМА
К пищевым веществам относят белки, жиры, углеводы, витамины и минеральные вещества.
Белки являются главной составной частью всех органов и тканей организма, с ними тесно связаны все жизненные процессы: обмен веществ, сократимость, раздражимость, способность к росту, размножению и мышлению. Основное назначение белков пищи - участие в построении новых клеток и тканей, обеспечение роста и развития молодых растущих организмов и регенерация изношенных, отживших клеток в зрелом возрасте.
Из белков пищи постоянно синтезируются белки организма, ферменты, гормоны, антитела. Белки участвуют в транспорте кровью кислорода, липидов, углеводов, некоторых витаминов, гормонов. Организм человека не имеет резервов белка. Белок поступает с пищей и относится к незаменимым компонентам рациона.
Критерием биологической ценности белков является их аминокислотный скор, которым выражают процентное отношение количества незаменимой аминокислоты в белке продукта к количеству этой же аминокислоты в стандартном белке с идеальной аминокислотной шкалой:
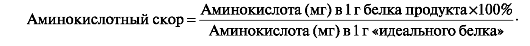 Лимитирующей
биологическую ценность аминокислотой является та, скор которой имеет
наименьшее значение. По этому показателю белки пищи животного
происхождения имеют высокую биологическую ценность. Растительные белки
лимитированы по ряду незаменимых аминокислот, и прежде всего по
треонину, изолейцину и лизину. Идеальным белком считают такой белок, в 1
г которого содержится 40 мг изолейцина, 70 мг лейцина, 55 мг лизина, 35
мг серосодержащих соединений (в сумме), 60 мг ароматических соединений,
10 мг триптофана, 40 мг треонина, 50 мг валина.
Лимитирующей
биологическую ценность аминокислотой является та, скор которой имеет
наименьшее значение. По этому показателю белки пищи животного
происхождения имеют высокую биологическую ценность. Растительные белки
лимитированы по ряду незаменимых аминокислот, и прежде всего по
треонину, изолейцину и лизину. Идеальным белком считают такой белок, в 1
г которого содержится 40 мг изолейцина, 70 мг лейцина, 55 мг лизина, 35
мг серосодержащих соединений (в сумме), 60 мг ароматических соединений,
10 мг триптофана, 40 мг треонина, 50 мг валина.
Биологическая ценность белков определяется также доступностью отдельных аминокислот, которая может снижаться в присутствии ингибиторов протеолитических ферментов (например, в бобовых), а также в процессе кулинарной обработки. Доступность белков определяется их усвояемостью пищеварительной системой.
Для удовлетворения потребности в аминокислотах целесообразно использовать комбинации пищевых продуктов по принципу взаимного дополнения лимитирующих аминокислот, например зерновых и молочных продуктов. Суточная потребность в белках составляет 58-87 г для женщин и 65-117 г для мужчин, причем 50% должны составлять белки животного происхождения. Это количество белка обеспечивает 11-12% энергетической потребности организма.
Жиры обладают высокой энергетической ценностью и выполняют важную роль в биосинтезе липидных структур, прежде всего мембран клеток. Жиры пищевых продуктов представлены триглицеридами и липоидными веществами. Жиры животного происхождения состоят из насыщенных жирных кислот с высокой температурой плавления. Растительные жиры содержат значительное количество полиненасыщенных жирных кислот (ПНЖК).
Животные жиры содержат свиное сало (90-92% жира), сливочное масло (72-82%), свинина (до 49%), колбасы (20-40% для разных сортов), сметана (20-30%), сыры (15-30%). Источниками растительных жиров являются растительные масла (99,9% жира), орехи (53-65%), овсяная крупа (6,1%), гречневая крупа (3,3%).
Природные жирные кислоты делятся на насыщенные, мононенасыщенные (с 1 двойной связью) и полиненасыщенные (с 2 двойными связями и более). Насыщенные жирные кислоты (пальмитиновая, стеариновая и др.) используются организмом в основном в качестве энергетических веществ. ПНЖК входят в состав клеточных мембран и других структурных элементов тканей, участвуют в синтезе простагландинов, способствуют удалению холестерина из организма. Количество ПНЖК в пересчете на линолевую кислоту должно обеспечивать около 4% общей энергетической ценности рациона. Оптимально соотношение 10% ПНЖК, 30% насыщенных и 60% мононенасыщенных жирных кислот.
Качество жировых компонентов пищевых продуктов определяется показателем биологической эффективности, отражающим содержание в них полиненасыщенных жирных кислот.
В рационе должны быть представлены жиры как животного, так и растительного происхождения. Жиры должны обеспечивать в среднем 30% энергетической ценности рациона. В физиологически полноценном рационе растительные жиры составляют 30% общего количества жиров.
Углеводы являются основной составной частью рациона человека. Около 60% углеводов поступает с зерновыми продуктами, от 14 до 26% - с сахаром и кондитерскими изделиями, до 10% - с клубнями и корнеплодами, 5-7% - с овощами и фруктами.
Углеводы делятся на усвояемые и неусвояемые. К усвояемым углеводам относятся глюкоза, фруктоза, сахароза, лактоза, мальтоза и альфа-глюконовые полисахариды - крахмал, декстрины и гликоген. Неусвояемые углеводы (целлюлоза, гемицеллюлоза, пектиновые вещества, лигнин и др.) не расщепляются ферментами желудочнокишечного тракта, но подвергаются расщеплению под действием микрофлоры кишечника.
Моносахариды в питании человека представлены глюкозой, галактозой, маннозой, ксилозой и фруктозой, олигосахариды - лактозой и сахарозой.
Полисахариды представлены растительным крахмалом, гликогеном и клетчаткой растительных продуктов. Содержание растительного крахмала достигает в хлебопродуктах 40-73%, в бобовых - 40-45%, в картофеле - 15%. Усвояемый полисахарид животного происхождения - гликоген содержится главным образом в печени (2-10%). В мышечной ткани содержание гликогена не превышает 1%.
Клетчатка растительных продуктов состоит из пищевых волокон и других недоступных для ассимиляции углеводов. Пищевые волокна представляют собой смесь различных полисахаридов и лигнина, но могут также иметь в своем составе белки, жиры и микроэлементы. В значительных количествах пищевые волокна присутствуют в неочищенных злаках, хлебе, овощах. В зависимости от количества клетчатки все продукты - носители углеводов - делят на содержащие «защищенные углеводы» (клетчатка в количестве более 0,4%) и рафинированные (клетчатки менее 0,4%).
Пищевые волокна влияют на интенсивность абсорбции и метаболизма жиров, углеводов и белков, а также способны менять обмен стеринов и баланс минеральных веществ.
В целом клетчатка способствует продвижению пищи в кишечнике. Под влиянием клетчатки снижается абсорбция кальция, магния,
цинка, меди, железа, редуцируется всасывание глюкозы, усиливаются абсорбция холестерина и экскреция стероидов. Пищевые волокна, в частности пектиновые вещества, способны адсорбировать вредные вещества и выводить их из организма.
Основным источником пищевых волокон являются зерновые продукты, фрукты, орехи и овощи. В суточном рационе должно содержаться около 20 г клетчатки. При традиционном питании большая часть клетчатки поступает с хлебом и крупой (10 г), картофелем (7 г), овощами (6 г), фруктами (2 г).
Углеводы рациона взрослого человека должны обеспечивать 50-60% энергетической потребности организма. Оптимальный состав углеводов: крахмал - 75%, сахара - 20%, пектиновые вещества - 3%, клетчатка -2%.
Современные представления о роли пищевых веществ в обеспечении жизнедеятельности и здоровья человека позволяют их обозначить как макронутриенты и микронутриенты (табл. 7.1).
Макронутриенты участвуют в структурном и энергетическом обеспечении организма. Потребность в них выражается в граммах, и за жизнь человек съедает около 30 тонн белков, жиров и углеводов. Большинство микронутриентов присутствует в пище в минимальных концентрациях, составляющих миллиграммы и даже микрограммы. Соответственно, масса важных для здоровья микронутриентов в течение жизни едва ли превышает 30 кг, т.е. около 1 г в день. Биологическая роль микронутриентов - регуляция чрезвычайно широкого спектра важнейших функций организма. Большинство из микронутриентов относится к разряду незаменимых пищевых веществ, необходимых для поддержания гомеостаза и жизнедеятельности организма.
Базовые физиологические функции микронутриентов:
• регуляция жирового, углеводного, белкового и минерального обмена;
• оптимизация активности ферментных систем;
• вхождение в структурные компоненты клеточных мембран;
• противодействие окислительному стрессу (антиоксидантная защита);
• участие в процессах клеточного дыхания;
• обеспечение электролитного баланса;
• поддержание кислотно-щелочного равновесия;
• участие в синтезе гормонов;
• регуляция репродуктивной функции и процессов эмбриогенеза;
Таблица 7.1. Модифицированная классификация пищевых веществ (Гичев Ю.Ю., Гичев Ю.П., 2006)
Макронутриенты | Микронутриенты |
Белки Жиры Углеводы | Витамины Витаминоподобные вещества Макроэлементы Микроэлементы Микронутриенты белковой природы: - аминокислоты - полипептиды Микронутриенты липидной природы: - омега-3 полиненасыщенные жирные кислоты - гамма-линоленовая кислота - фосфолипиды и липотропные вещества - фитостерины Микронутриенты углеводной природы: - пищевые волокна - неусваиваемые олигосахариды (пребиотики) - полисахаридные адъюванты Живые кишечные микроорганизмы (пробиотики) Пищеварительные ферменты растительного происхождения Парафармацевтики - гликозиды - алкалоиды - индолы и изотиоционаты - органические полисульфиды - фитоэстрогены - сапонины - фитостерины - терпены и др. (всего около 1000 парафармацевтиков, обнаруживаемых непосредственно в пищевых продуктах) |
• поддержание функциональной активности различных звеньев иммунной системы;
• участие в процессах кроветворения и регуляции свертываемости крови;
• регуляция функционального состояния центральной и периферической нервной системы;
• регуляция возбудимости миокарда и сосудистого тонуса;
• обеспечение жизнедеятельности нормальной (аутохтонной) микрофлоры кишечника;
• структурное и функциональное обеспечение опорно-двигательного аппарата;
• участие в синтезе соединительной ткани;
• участие в процессах детоксикации и биотрансформации ксенобиотиков;
• адаптогенный эффект при неблагоприятном воздействии факторов среды обитания.
Витамины жизненно необходимы организму человека, они не синтезируются (или синтезируются в недостаточном количестве) в организме и выполняют функции катализаторов обменных процессов. Витамины поступают в организм с пищей и относятся к незаменимым факторам питания (табл. 7.2).
Таблица 7.2. Классификация витаминов
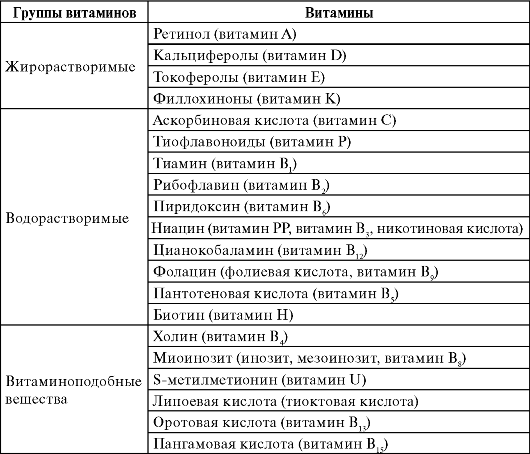 Ретинол (витамин
А) регулирует функцию нормального зрения, роста, дифференциации клеток,
поддерживает воспроизводство и целостность иммунной системы.
Ретинол (витамин
А) регулирует функцию нормального зрения, роста, дифференциации клеток,
поддерживает воспроизводство и целостность иммунной системы.
Основными источниками ретинола являются продукты животного происхождения. Содержание витамина в печени животных и морских рыб может достигать 15 000 мг/100 г. Много ретинола в молоке и молочных продуктах, яйцах, мясе птицы. Мясо животных и рыба бедны ретинолом (0-30 мг%). При адекватных запасах ретинола в печени (более 20 мкг/г) значительная часть адсорбированного витамина переносится в звездчатые клетки печени. У рационально питающегося человека запасы витамина А в печени составляют более 90% всех запасов организма.
Провитамин А в продуктах представлен пигментами, каротиноидами, превращающимися в организме в витамин А. Каротиноиды находятся в зеленых частях растений. В группу каротиноидов входят α-, β-, γ-каротины и криптоксантин. Наиболее распространенным и активным каротиноидом является β-каротин. В отличие от ретинола каротиноиды накапливаются преимущественно в жировой ткани. Содержание провитамина А в моркови достигает 2-7 мг%, в лиственных овощах - 2-3 мг%, в томатах - 0,7-1 мг%. Оранжевый цвет овощей и фруктов не обязательно свидетельствует о высоком содержании β-каротина. Биологически активна только 1/6 часть β-каротина, содержащегося в пищевых продуктах. Степень усвоения каротина из растительной пищи зависит от полноты разрыва клеточных оболочек. Каротин, содержащийся в пюре из моркови, усваивается лучше, чем из целой вареной и сырой моркови. Физиологическая потребность в витамине А выражается ретиноловым эквивалентом и составляет от 400 до 1000 мкг/сут для детей разных возрастных групп и 900 мкг/сут для взрослых.
Кальциферол (витамин D) необходим для регуляции всасывания кальция. Основными представителями витаминов группы D являются эргокальциферол (витамин D2) и холекальциферол (витамин D3). Потребность детей и взрослых в кальцифероле составляет 10 мкг/сут, для лиц старше 60 лет - 15 мкг/сут. Обеспеченность организма витамином D определяют по содержанию в сыворотке кальция (в норме 0,1 г/л), фосфора (в норме 0,05% г/л), кальциферола и повышенной активности щелочной фосфатазы сыворотки крови.
Значительное количество кальциферола содержат рыбий жир, икра, красная рыба и куриные яйца, его небольшие количества присутствуют в сливках и сметане.
Токоферол (витамин Е) является одним из основных алиментарных антиоксидантов, предотвращающим усиление перекисного окисления липидов. Токоферол необходим для нормального развития и функционирования мужской и женской половой системы, влияет на репродуктивные органы как непосредственно, так и через гипоталамо-гипофизарный комплекс. Физиологическая потребность в токофероле составляет от 3 до 15 мг/сут для ребенка и 15 мг/сут для взрослых. С пищей человек получает от 20 до 30 мг токоферола, но в кишечнике всасывается не более 50% витамина.
Витамин Е не синтезируется в организме человека. Ассимиляция витамина зависит от присутствия в пище жиров и нарушается при недостаточной секреции желчи. Источниками токоферола являются растительные масла, особенно кукурузное, хлопковое и из пшеничных зародышей, хлеб и крупы, в которых содержание витамина Е около 2- 6 мг%, облепиха (10 мг%), грецкие орехи (23 мг%), майонез (32 мг%).
Критерием обеспеченности организма витамином Е является содержание его в сыворотке крови (в норме 0,006-0,008 г/л) и креатина в моче. Косвенным показателем может служить устойчивость эритроцитов к гемолизу.
Филлохиноны (витамин К) необходимы для синтеза в печени функционально активных форм протромбина, а также других белков, участвующих в регуляции процессов свертывания крови. Витамин К входит в состав биологических мембран. Физиологическая потребность в витамине К составляет 120 мкг/сут для взрослых и от 30 до 75 мкг/сут для детей. Основными источниками филлохинонов являются овощи (капуста, томаты, тыква) и печень. Причинами дефицита витамина К чаще всего становятся нарушения его всасывания в желудочно-кишечном тракте, обусловленные хроническими поражениями кишечника (колиты, энтероколиты) и гепатобилиарной системы (гепатит, цирроз, желчнокаменная болезнь, дискинезия желчных путей). До 50% потребности в витамине может обеспечить эндогенный синтез бактериальной флорой кишечника. Нормальная свертываемость крови сохраняется при потреблении 0,4 мкг витамина К на 1 кг массы тела в день. Основным критерием обеспеченности организма витамином К является поддержание концентрации протромбина в плазме на уровне 80-120 мкг/ мл.
Тиамин (витамин В1) непосредственно участвует в обмене углеводов. При его недостаточности нарушается процесс окисления пировиноградной кислоты и развивается полиневрит, исторически известный как
болезнь бери-бери. Дефицит витамина В1 может развиться при питании рафинированными углеводами, у больных хроническим алкоголизмом из-за повышенной потребности в этом витамине и при потреблении продуктов, содержащих антивитаминный фактор тиаминазу (рыба).
Источниками тиамина являются хлебопродукты из муки грубого помола, большинство круп, бобовые, печень и другие субпродукты, пивные дрожжи. Суточная потребность составляет для взрослых 1,5 мг/сут, для детей - от 0,3 до 1,5 мг/сут. Критерием обеспеченности организма тиамином является содержание витамина В1 и пировиноградной кислоты в моче.
Рибофлавин (витамин В2) входит в состав ряда окислительно-восстановительных ферментов и участвует в регуляции белкового, жирового и углеводного обмена. Основными причинами недостаточности рибофлавина являются хронические заболевания желудочно-кишечного тракта и недостаток в рационе молока и молочных продуктов. Суточная потребность в витамине В2 составляет 1,8 мг/сут для взрослых и 0,4-1,8 мг/сут для детей. Основными источниками рибофлавина, помимо молока и молочных продуктов, считают мясо, яйца, рыбу, печень, хлеб, гречневую и овсяную крупы, дрожжи. Критерием обеспеченности организма рибофлавином является его количество в суточной моче (норма 300-1000 мкг/л), эритроцитах (норма 200 мкг/л), сыворотке крови (норма 25-30 мкг/л), лейкоцитах (норма 2000-2500 мкг/л).
Ниацин (витамин РР) играет роль переносчика электронов в окислительно-восстановительных реакциях в организме. При недостатке ниацина развивается пеллагра с упорной диареей, дерматитом кожи лица и открытых частей тела, а в тяжелых случаях - с деменцией (три Д). Нарушаются секреция желудочного сока, чувствительность кожных рефлексов, появляются атаксия, адинамия, раздражительность и психозы. Пеллагра может возникнуть при одностороннем питании кукурузой либо при недостатке триптофана как важного источника этого витамина: из 60 мг триптофана образуется 1 мг ниацина. Суточная потребность в витамине PP составляет 20 мг/сут для взрослых и от 5 до 20 мг/сут для детей. Основные источники ниацина - дрожжи, крупы, хлеб грубого помола, пшеничные зародыши, бобовые, субпродукты, мясо, рыба, сушеные грибы.
Пиридоксин (витамин В6) в качестве кофермента участвует в функционировании ферментных систем углеводного и липидного обмена.
Пиридоксин присутствует во многих пищевых продуктах. Источниками витамина В6 являются печень, дрожжи, цельные зерна
злаковых культур, фрукты, овощи и бобовые. Суточная потребность в витамине В6 прямо зависит от потребления белка. Взрослому человеку требуется 2 мг/сут витамина В6. Потребность в пиридоксине увеличивается во время беременности и лактации, при воздействии ионизирующего излучения, приеме некоторых лекарств и при сердечной недостаточности. Суточная норма пиридоксина для детей составляет 0,4-2 мг.
Критерием обеспеченности организма витамином В6 является содержание 4-пиридоксиловой кислоты в суточной моче (норма 3- 5 мг), содержание пиридоксина в цельной крови (норма 100 мкг/л) и сыворотке (норма 70 мкг/л).
Цианокобаламин (витамин В12) участвует в построении ряда ферментных систем, являясь промежуточным переносчиком метильной группы, влияет на процессы кроветворения.
Источниками цианокобаламина являются говядина, субпродукты (печень, сердце), мясо кур, яйца. Алиментарная недостаточность цианокобаламина возможна у вегетарианцев, беременных, при хроническом алкоголизме, нарушении синтеза внутреннего фактора Кастла, наследственном дефекте синтеза белков, участвующих в транспорте витамина В12.
Суточная потребность в витамине В12 у взрослых составляет 3 мкг, у беременных - 4 мкг и от 0,3 до 3 мкг у детей. Критерием обеспеченности организма витамином В12 является уровень его ренальной экскреции, который в норме должен быть не ниже 0,02 мкг/сут, и содержание в сыворотке крови (в норме 200-1000 нг/мл).
Аскорбиновая кислота (витамин С) участвует во многих биохимических процессах, способствует регенерации и заживлению ран, поддерживает устойчивость к стрессам и обеспечивает иммунобиологическую резистентность по отношению к вредным биологическим агентам внешней среды. Особую роль аскорбиновая кислота играет в обеспечении нормальной проницаемости сосудистой стенки. Участие в поддержании гомеостаза способствует сохранению работоспособности, предупреждению утомления и раздражительности.
Аскорбиновая кислота не синтезируется и не депонируется в организме, поэтому потребность в витамине С обеспечивается только ее поступлением с пищей. Естественными источниками аскорбиновой кислоты являются овощи и фрукты, в первую очередь шиповник, черная смородина, облепиха, сладкий перец, укроп, петрушка, цитрусовые, рябина и др. В картофеле немного аскорбиновой кислоты,
но его можно считать основным источником витамина С благодаря традиционно высокому потреблению картофеля жителями РФ.
Суточная потребность в аскорбиновой кислоте у взрослых составляет 90 мг, у детей - от 30 до 90 мг.
Критериями обеспеченности организма аскорбиновой кислотой являются ее экскреция с мочой (в норме 20-30 мг/сут), содержание в плазме крови (в норме 0,007-0,012 г/л), лейкоцитах (в норме 0,2-0,3 г/л), тесты на проницаемость сосудов.
Биофлавоноиды (витамин Р). Во взаимодействии с аскорбиновой кислотой уменьшают проницаемость и повышают прочность капилляров, стимулируют тканевое дыхание. Недостаточность их вместе с недостаточностью аскорбиновой кислоты приводит к ломкости и повышенной проницаемости капилляров, общей слабости, склонности к кровоизлияниям. Потребность - 50 мг в сутки. Содержатся во фруктах, ягодах и овощах, особенно в черноплодной рябине, черной смородине, апельсинах, лимонах, бруснике, клюкве, винограде.
Инозит (витамин В8). Обладает липотропным и седативным действием, влияет на функцию половых желез, участвует в обмене углеводов, стимулирует двигательную функцию желудка и кишечника, оказывает липотропное действие. Суточная потребность для взрослых составляет 500 мг, для детей 4-6 лет - 80-100 мг и для детей
17-18 лет от 200 до 500 мг.
Липоевая кислота. Влияет на обмен углеводов и холестерина, обладает липотропным действием. Суточная потребность у взрослых составляет 30 мг. Содержится в большинстве пищевых продуктов. Как лечебный препарат применяют при атеросклерозе, болезнях печени, диабете.
Оротовая кислота (витамин В13). Участвует в обмене белков и витаминов. Как лечебное средство используется при болезнях печени (ускоряет регенерацию печеночных клеток), инфаркте миокарда, сердечной недостаточности. Рекомендуемый уровень потребления для взрослых - 300 мг/сут.
Пангамовая кислота (витамин В15). Повышает окислительные процессы и усвоение кислорода тканями. Содержится в пищевых продуктах. Как лечебный препарат применяют при атеросклерозе, болезнях печени, сердечной недостаточности.
S-Метилметионин (витамин U). Улучшает тканевое дыхание, стимулирует окислительные процессы, нормализует секрецию пище-
варительных желез, ускоряет заживление язвы желудка и двенадцатиперстной кишки, дает липотропный эффект. Содержится в овощах и фруктах, особенно в капусте. Рекомендуемый уровень потребления для взрослых - 200 мг/сут.
Холин (витамин В4). Участвует в образовании лецитина и ацетилхолина. Обладает липотропным действием, влияет на обмен белков и холестерина. При недостатке холина жир накапливается в печени, так как при этом нарушается переход его в фосфолипиды. При болезнях печени потребность в холине повышается. Содержится в треске, печени, почках, капусте, шпинате. В организме образуется из метионина. Рекомендуемый уровень потребления для взрослых - 500 мг/сут, для детей 4-6 лет - от 100 до 200 мг/сут, с 7 до 18 лет - от 200 до 500 мг/сут.
Минеральные вещества в адекватном количестве обеспечивают поддержание гомеостаза, участвуют в обеспечении жизнедеятельности, а их дефицит приводит к специфическим нарушениям или заболеваниям. Минеральные вещества содержатся в костной ткани в виде кристаллов, а в мягких тканях - в виде истинного или коллоидного раствора в соединении с белками.
Натрий содержится во всех органах, тканях и биологических жидкостях. Основное поступление натрия в организм обеспечивается поваренной солью. Суточная потребность в натрии у взрослых составляет 1300 мг, у детей - от 200 до 1300 мг.
В организме натрий присутствует преимущественно во внеклеточных жидкостях - лимфе и сыворотке крови. Натрий играет важную роль в процессах внутриклеточного и межтканевого обмена, участвуя в формировании буферной системы крови, обеспечивает поддержание кислотно-щелочного равновесия. Соли натрия участвуют в поддержании осмотического давления цитоплазмы и биологических жидкостей. Основным регулятором содержания натрия в крови и тканевой жидкости являются почки.
При избыточном потреблении поваренной соли из-за перегрузки регуляторных механизмов стойко повышается артериальное давление и формируется гипертоническая болезнь. Ограничение потребления поваренной соли остается одним из главных профилактических мероприятий предупреждения артериальной гипертензии и в дальнейшем инфаркта миокарда.
Калий вместе с натрием участвует в формировании буферных систем, предотвращающих сдвиги реакции среды. Соединения калия
влияют на коллоидное состояние тканей, уменьшая гидратацию тканевых белков и способствуя выведению жидкости. В этом случае калий выступает как антагонист натрия, что используется в терапии заболеваний почек. В норме отношение натрия и калия при рациональном питании должно составлять 2 : 1. Смешанный рацион полностью удовлетворяет потребность в калии. Физиологическая потребность для взрослых - 2500 мг/сут, для детей - от 400 до 2500 мг/сут.
Источниками калия являются преимущественно растительные продукты, вследствие чего возможны сезонные колебания поступления вещества: весной около 3 г/сут, осенью - 5-6 г/сут.
Кальций необходим не только для правильного формирования костной ткани. Около 1% кальция организма входит в состав всех органов, тканей и биологических жидкостей. Кальций участвует в поддержании нервно-мышечной возбудимости, влияет на процессы свертывания крови, проницаемость клеточных оболочек. Потребность в кальции для взрослых - 1000 мг/сут, для лиц старше 60 лет - 1200 мг/сут, для детей - от 400 до 1200 мг/сут. У женщин во время беременности потребность в кальции увеличивается до 1300 мг/сут и до 1400 мг/сут в период грудного вскармливания новорожденных.
Кальций присутствует в разных продуктах, но его усвояемые формы содержатся преимущественно в молоке и молочных продуктах. При потреблении около 500 мл молока человек получает около 1000 мг кальция.
Диетические продукты, приготовленные с добавлением костной муки, рыбно-витаминных концентратов, порошка яичной скорлупы и шрота пантов, содержат кальций с биодоступностью около 88%.
Алиментарный кальций в повышенных дозах, по-видимому, играет важную роль в защите организма от действия ионизирующего излучения, поддержке баланса субстратов антиоксидантной системы (токоферола и селена), повышает резистентность к чужеродным химическим веществами.
Усвоение кальция из других продуктов и питьевой воды незначительно.
По поводу нарушений при недостаточном потреблении кальция нет единого мнения. Недостаток кальция не всегда приводит к остеопорозу, а его лечение солями кальция не всегда эффективно. Большинство болезней, рассматриваемых как следствие недостатка кальция (остеопороз, рахит, остеомаляция, кариес), могут возникать на фоне дефицита других пищевых веществ (белки, фтор, кальцифе-
рол, другие витамины и их метаболиты). Нарушения обмена кальция при этих заболеваниях следует считать вторичными.
Фосфор в обменных процессах тесно связан с обменом кальция. Всасывание из кишечника кальция и фосфора и окостенение идут параллельно, а в сыворотке крови они являются антагонистами. Соединения фосфора играют особенно важную роль в деятельности головного мозга, скелетных и сердечной мышц, потовых желез. Наиболее интенсивно обмен фосфора осуществляется в мышцах. Фосфорная кислота участвует в построении многих ферментов. Неорганический фосфор совместно с кальцием составляет твердую основу костной ткани и является обязательным компонентом реакций превращения углеводов. Суточная потребность для взрослых 800 мг, для детей - от 300 до 1200 мг.
Наиболее богаты фосфором молоко и молочные продукты, яйца, мясо теплокровных животных и рыба. В продуктах, содержащих фитиновые соединения (бобовые, хлебобулочные и крупяные изделия), фосфор находится в малоусвояемой форме. Для эффективного усвоения фосфора из пищевых продуктов необходимо соотношение фосфора и кальция, равное 1 : 1,5.
Магний оказывает антиспастическое и сосудорасширяющее действие, стимулирует перистальтику кишечника и повышает желчеотделение. Имеются данные о снижении концентрации холестерина под влиянием этого элемента. Ионы магния участвуют в регуляции углеводного и фосфорного обмена. Физиологическая потребность для взрослых - 400 мг/сут, для детей - от 55 до 400 мг/сут. О влиянии других микроэлементов см. также главы 6 и 8.
7.2. ЗДОРОВОЕ ПИТАНИЕ
Здоровым (рациональным) называют физиологически полноценное питание здоровых людей с учетом их пола, возраста, характера трудовой деятельности, особенностей действия климата и других факторов. Рациональное питание должно обеспечивать постоянство внутренней среды организма (гомеостаз) и поддерживать жизнедеятельность (рост, развитие, функции органов и систем) на высоком уровне.
Общие требования к пищевому рациону можно сформулировать следующим образом:
1. Суточный рацион питания должен соответствовать по энергетической ценности энерготратам организма. Потребность в энергии
зависит от возраста и связанной с ним величины основного обмена (ВОО), соотношения роста и массы тела, профессиональной и непрофессиональной деятельности человека, качества и условий жизни, климата. Потребность в энергии определяется также физиологическим состоянием (беременность, кормление грудью).
2. Физиологические потребности организма должны обеспечиваться пищевыми веществами в количествах и пропорциях, которые оказывают максимум полезного действия.
Суть этого положения рационального питания представляет балансовый подход, характеризующий качество рациона: состав нутриентов, соотношение незаменимых и заменимых веществ (белки животного и растительного происхождения; жирные кислоты; пропорции углеводов, витаминов и минеральных веществ). Этот постулат лежит в основе построения пищевых рационов для различных групп населения.
3. Химическая структура пищи должна максимально соответствовать ферментным пищеварительным системам организма (правило соответствия).
Соблюдение правила соответствия («энзиматической констелляции») играет важную роль в поддержании ферментных систем организма, ответственных за ассимиляцию пищи и сохранение гомеостаза. Всякое нарушение соответствия химической структуры пищи ферментным констелляциям ведет к расстройству обмена веществ и формированию различных патологических состояний (схема 7.1).
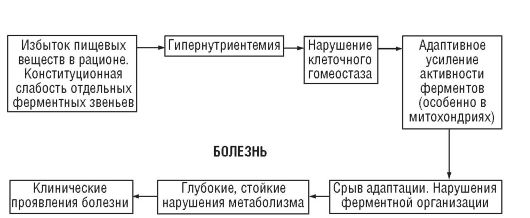 Схема 7.1. Влияние пищевых веществ на развитие болезней избыточного питания (Покровский А.А.)
Схема 7.1. Влияние пищевых веществ на развитие болезней избыточного питания (Покровский А.А.)
4. Пищевой рацион должен быть правильно распределен в течение дня. Правильный режим питания обеспечивает эффективность работы пищеварительной системы, усвоение пищевых веществ и регулирует обменные процессы. Физиологически обоснованным является 3-4-разовое питание с интервалами между приемами пищи от 4 до 5 ч. При 3-разовом питании завтрак должен обеспечивать 30% суточной энергетической ценности рациона, обед - 45%, ужин - 25%. При 4-разовом питании на первый завтрак должно приходиться 25%, на второй завтрак - 15%, на обед - 35% и на ужин - 25% энергетической ценности.
Режим питания может изменяться в соответствии с национальными традициями, характером трудовой деятельности, культурой, привычками в питании, климатом.
5. Здоровое питание должно быть безупречным в санитарно-эпидемиологическом отношении. Продукты не должны представлять опасности для здоровья из-за наличия физических, химических или биологических контаминантов или процессов порчи (окисление, брожение, осаливание и т.п.) при неправильном хранении и реализации.
Организацию здорового питания затрудняют экономические факторы, сложность обеспечения набором продуктов и недостаточная первичная профилактика, а именно - неудовлетворительное состояние дел в вопросах гигиенического воспитания и обучения правилам здорового питания не только населения, но и врачей.
Резкое сокращение энерготрат современного человека требует уменьшения потребления пищи. Однако снижение потребности в энергии не сопровождается аналогичным снижением потребности в других жизненно важных пищевых веществах, в частности в микронутриентах. Поскольку источниками энергии и биологически активных веществ остаются неизменившиеся традиционные пищевые продукты, возникают своеобразные «ножницы»: адекватный по энергетической ценности рацион не обеспечивает потребностей в микронутриентах (витамины, микроэлементы и др.). И наоборот, при адекватном поступлении с традиционной пищей микронутриентов формируется избыточное по макронутриентам и энергии питание.
Другой причиной формирования дефицита микронутриентов является применение интенсивных технологий в производстве пищевых продуктов: выращивания сырья, его хранения и переработки. По данным английской статистики, качество пищи значительно ухудшилось с 40-х годов прошлого века. За 60 лет содержание железа
в среднем бифштексе уменьшилось на 55%, кальция - на 4%, магния - на 7%. Содержание железа в молоке снизилось на 62%, кальция - на 21%. В сыре стало меньше магния - на 38%, кальция - на 9%, железа - на 47%.
Предпочтение населением использования в пищевом рационе высокоочищенных (рафинированных) продуктов повседневного применения (мука, крупы, сахар) усугубляет ситуацию, поскольку в этих продуктах содержание микронутриентов в десятки раз ниже по сравнению с исходным (витамины, минеральные вещества, микроэлементы, пищевые волокна).
Наконец, при различных видах кулинарной обработки продуктов, консервировании и длительном хранении происходит разрушение или потеря свойств микронутриентов, особенно термолабильных.
Перечисленные выше особенности питания современного человека являются основными причинными факторами нарушения второго постулата здорового питания, согласно которому нормальную жизнедеятельность организма должен обеспечивать пищевой рацион, сбалансированный не только по макронутриентам и энергетической ценности, но и по многочисленным незаменимым факторам питания, каждому из которых в обмене веществ принадлежит специфическая роль.
Несоответствие фактического питания фундаментальному признаку здорового питания - сбалансированности - является фактором риска для развития почти 70% наиболее распространенных неинфекционных заболеваний.
7.3. ОСОБЕННОСТИ ЗДОРОВОГО ПИТАНИЯ РАЗЛИЧНЫХ ГРУПП НАСЕЛЕНИЯ
Питание пожилых людей и долгожителей
Правильно организованное питание является важным средством воздействия на процессы старения, поскольку в пожилом возрасте снижаются обменные процессы.
В старости возникает энергетический дисбаланс, сопровождающийся ожирением, снижением двигательной активности и замедлением нейрогуморальной регуляции гомеостаза, а также нарушением липидного обмена, в частности холестеринового. Тучность предрасполагает к атеросклерозу, сахарному диабету и другим заболеваниям.
Рациональное питание людей пожилого и старческого возраста основано на принципах, сформулированных академиком А.А. Покровским:
• энергетическая ценность рациона должна быть адекватной фактическим энерготратам в течение дня;
• рацион должен иметь антисклеротическую направленность;
• в рационе в сбалансированном соотношении должны присутствовать все основные незаменимые факторы питания;
• в рационе в оптимальном количестве должны присутствовать вещества, стимулирующие активность ферментных систем организма;
• в привычном питании должны быть представлены продукты и блюда, обладающие достаточной ферментной доступностью.
Умеренное ограничение питания пожилых людей должно быть разумным, не в ущерб биологической ценности рациона (табл. 7.3). Большинство продуктов нужно употреблять в небольших количествах и с определенной частотой в течение недели.
Таблица 7.3. Рекомендуемые количества энергии, белков, жиров и углеводов в рационе лиц пожилого возраста*
Возрастные группы, годы | Энергия, ккал | Белки, г | Жиры, г | Углеводы, г | |
всего | в том числе животные | ||||
Мужчины старше 60 лет | 2300 | 68 | 34 | 77 | 335 |
Женщины старше 60 лет | 1975 | 61 | 30,5 | 66 | 284 |
* Нормы физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации: Методические рекомендации МР 2.3.1.2432-08. - М., 2008.
Около 50% белка должно приходиться на белки животного происхождения, причем половина этих белков должна быть представлена молочным белком (молоко, творог, кефир), а другая половина - белками мяса и рыбы. Потребность в белке для пожилых составляет в среднем 1 г/кг массы тела.
Жировая часть рациона должна состоять на четверть из жиров животного и на четверть - из жиров растительного происхождения. Остальные жиры могут содержаться в продуктах или применяться
для кулинарной обработки. Важное значение имеет соотношение ПНЖК/насыщенные жирные кислоты. Если в рационе здорового человека это соотношение должно быть 0,3-0,4, то в противоатеросклеротических диетах оно рекомендуется от 1 до 2.
В углеводной составляющей рациона доля сахара ограничивается 10% от калорийности суточного рациона, что соответствует приблизительно 50 г/сут. Не менее 25% общего количества углеводов целесообразно получать с овощами и фруктами. Таким образом, в сбалансированном рационе лиц пожилого возраста соотношение основных питательных веществ будет у мужчин 1 : 1,1 : 4,9 и у женщин 1 : 1,1 : 4,7. Людям пожилого возраста показано разумное ограничение энергетической ценности рациона, прежде всего за счет углеводов - сахара и кондитерских изделий и жиров животного происхождения. Однако ограничение количества жиров возможно только до определенного предела, поскольку жиры влияют на устойчивость организма к воздействию низких температур и возбудителям инфекционных заболевания. Недостаток жира в рационе препятствует использованию жирорастворимых витаминов (ретинола, кальциферола, токоферола и филлохинона).
Следует также учитывать, что жиры являются источниками некоторых естественных антисклеротических факторов (ПНЖК, фосфолипиды, токоферолы и др.).
Наиболее изученный естественный антисклеротический фактор лецитин относится к группе фосфолипидов. В яичном желтке содержится до 90 г/кг лецитина, в печени - 25 г/кг. В достаточном количестве фосфатиды присутствуют в нерафинированных растительных маслах, где также имеются фитостерины. Высокой биологической активностью отличается бета-фитостерин, который способствует нормализации холестеринового обмена, понижая растворимость холестерина в жире и ограничивая его всасывание.
Антисклеротической активностью обладают также холин, инозит и цианокобаламин. Источниками холина можно считать яйца, мясо, рыбу, бобовые, капусту; инозита - апельсины, зеленый горошек и дыни; цианокобаламина - мясо, субпродукты, яйца. Уровень холестерина в сыворотке крови снижает также фолиевая кислота, источником которой являются зеленые листовые овощи, цветная капуста, картофель, свекла, куриное мясо, печень. При правильно организованном питании потребность организма в фолиевой кислоте и цианокобаламине полностью удовлетворяется.
К противосклеротическим веществам можно отнести калий и магний. Калий содержится во многих продуктах растительного происхождения, его особенно много в картофеле. Однако значительная энергетическая ценность этого продукта заставляет рекомендовать лицам пожилого возраста не более 200 г картофеля в день. Основные источники магния - мясо, рыба, молоко, картофель, овощи и фрукты. Много магния в овсяной крупе (133 мг%), кураге (105 мг%), миндале (154 мг%).
В питании пожилых должны присутствовать витамины - антиоксиданты (витамины Е и С), препятствующие перекисному окислению липидов и ожирению печени. Наибольшее количество токоферолов содержится в зародышах хлебных злаков (до 250 мг/кг), поэтому хлебобулочные изделия из цельного зерна, в частности хлеб из обойной муки, предпочтительны в пожилом возрасте.
В рационе должно содержаться 90 мг аскорбиновой кислоты, желательно в комплексе с рутином. Витамин С и рутин присутствуют вместе в черной смородине, черном винограде, вишне, черноплодной рябине, чернике, бруснике.
Для нормализации микрофлоры кишечника в пожилом возрасте целесообразно использовать кисломолочные продукты (простоквашу, кефир, ацидофилин и др.) и включать в рацион продукты, содержащие пищевые волокна, в частности пектиновые вещества.
Наиболее рациональным следует признать четырехразовый прием пищи со следующим примерным распределением ее в течение дня: первый завтрак - 25%, второй завтрак - 15%, обед - 35% и ужин - 25%.
Питание детей и подростков
Все аспекты организации здорового питания школьников представлены во вступивших в действие с 1 октября 2008 г. СанПиН 2.4.5.2409-08 «Санитарно-эпидемиологические требования к организации питания обучающихся в общеобразовательных учреждениях, учреждениях начального и среднего профессионального образования» (см. гл. 10, приложение к главе учебника на электронном носителе).
Питание беременных и кормящих матерей
Адекватное питание беременных обеспечивает не только правильное развитие и созревание внутриутробного плода, но и сложные физиологические перестройки, которые связаны со становлением лактационных механизмов. Рост плода, существенное увеличение массы
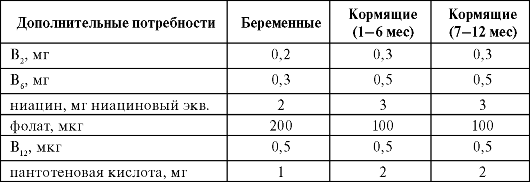
матки, изменения молочных желез - все это напряженные пластические процессы, требующие обеспечения. Приблизительно 2/3 прибавки массы тела во время беременности приходится на массу плода и новообразованных тканей половых органов, крови и амниотической жидкости, а 1/3 составляет «материнский резерв», или запас питательных веществ, необходимых для послеродового периода и обеспечения лактации. Питание беременной должно быть рассчитано прежде всего на покрытие повышенной потребности во всех основных его ингредиентах. Для беременных и кормящих определены дополнительные потребности в энергии и пищевых веществах (табл. 7.4).
Таблица 7.4. Дополнительные к норме, соответствующей физической активности и возрасту, потребности в питательных и биологически активных веществах для беременных и кормящих (Методические рекомендации МР 2.3.1.2432-08)
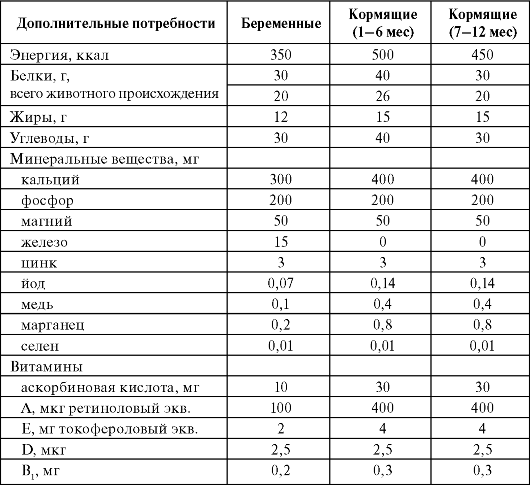
 Адекватный пищевой рацион беременных женщин должен:
Адекватный пищевой рацион беременных женщин должен:
• покрывать физиологические потребности плода в основных пищевых веществах и энергии, необходимых для его правильного роста и развития;
• удовлетворять физиологические потребностей беременной женщины в пищевых веществах и энергии, необходимых для сохранения ее здоровья и работоспособности;
• обеспечивать комфортное самочувствие, хорошее настроение и высокую активность женщины на всех этапах беременности.
Питание работников умственного труда
Все профессии, связанные с умственной деятельностью, относятся к 1-й группе интенсивности труда с минимальными энергетическими затратами, которые не превышают в возрастной группе 18-29 лет 2000 ккал у женщин и 2450 ккал у мужчин. Умственный труд связан с высоким нервно-эмоциональным напряжением в сочетании с выраженной гипокинезией. У работников умственного труда широко распространены избыточная масса тела и ожирение (31-36%), заболевания органов кровообращения и пищеварения.
Питание работников умственного труда, как правило, избыточно по энергетической ценности, не сбалансировано по основным пищевым веществам и дефицитно по ряду незаменимых пищевых веществ (серосодержащие аминокислоты, растительные жиры, аскорбиновая кислота, ретинол и др.).
При организации питания работников умственного труда следует руководствоваться следующими положениями:
1. Энергетическая ценность пищевого рациона должна соответствовать 2000-2450 ккал, за счет белков должно обеспечиваться
244-288 ккал, за счет жиров - 630-730 ккал и за счет углеводов - 1028-1432 ккал.
2. В рационе должно содержаться 58-72 г белка, 60-81 г жиров и 257-358 г углеводов. Соотношение между ними (по массе) будет 1 : 1,1 : 4,9 в возрастных группах 18-29 и 30-39 лет для мужчин и 1 : 1,1 : 4,7 для женщин.
В старшей возрастной группе (40-59 лет) уменьшается потребность в углеводах, и это соотношение будет 1 : 1,1 : 4,7 для мужчин и 1 : 1 : 4,4 для женщин.
3. Количество белка животного происхождения составляет не менее 50% всего белка суточного рациона. До половины этого количества белка обеспечивает молочный белок. На долю сливочного масла должно приходиться не более 1/4 общего количества жира. Такое же количество жиров должно быть представлено растительными маслами, а половина жиров рациона - в продуктах и при кулинарной обработке.
4. Прием пищи должен осуществляться 4 раза в день. По первому варианту на 1-й завтрак приходится 25% энергетической ценности рациона, на 2-й завтрак - 20%, на обед - 35% и на ужин - 20%. По второму варианту вместо 2-го завтрака включается полдник, тогда на завтрак должно приходиться 25%, на обед - 35%, на полдник - 15% и на ужин - 25% энергетической ценности. Питание лиц умственного труда при общей умеренности должно
быть биологически полноценным и иметь антисклеротическую и липотропную направленность.
При высоком нервно-эмоциональном напряжении, нагрузке на аналитические функции мышления в связи с большим потоком информации, дефиците времени и ответственности за принимаемые решения потребность в витаминах группы В увеличивается на 25-30%, в аскорбиновой кислоте - на 30%. В связи с этим в рацион включают субпродукты, хлеб из муки грубого помола, фрукты, свежую зелень. Для обеспечения высокой работоспособности зрительного анализатора должно быть увеличено количество ретинола (печень, яйца, сливочное масло, морковь).
Питание студентов как представительной социальной группы существенно не отличается от такового у работников умственного труда в целом. Наиболее значимой проблемой является нарушение режима питания студентов. Так, от 25 до 47% студентов не завтракают, 17-30% - едят 2 раза в день, около 40% - не обедают или обедают
нерегулярно и около 22% - обходятся без ужина. Студенты редко едят горячее и поздно ужинают.
Питание спортсменов
Потребность в энергии в дни соревнований и напряженных тренировок составляет у мужчин 4500-5000 ккал, у женщин -
3500-4000 ккал.
Интенсивная мышечная работа сопровождается повышенной потребностью в белке. Среднее количество белка в рационе спортсмена определяется из расчета 2 г/кг. При длительных тренировках из-за значительных потерь азота количество белка увеличивается до 2,5 г/кг. В дни соревнований количество белка должно составлять для мужчин 154-171 г/сут, из которых 77-86 г должны быть представлены белками животного происхождения. Белковое питание необходимо в скоростных и силовых видах спорта. Из-за опасности развития жировой инфильтрации печени у спортсменов при длительных максимальных и средних нагрузках в рацион вводят метионин (творог, печеночный паштет, мясо, рыбу, птицу).
Потребность в жирах в дни тренировок и соревнований для мужчин составляет 145-161 г, в том числе 44-48 г растительного масла, для женщин - 113-129 г, в том числе 34-39 г должны быть представлены растительными жирами.
Потребность в углеводах у спортсменов повышена. Только смесь сахаров (моно- и дисахаридов) и крахмалсодержащих углеводов позволяет поддерживать достаточный уровень глюкозы в крови и усиливать гликогенолиз в печени. В дни интенсивных тренировок и соревнований потребность в углеводах равна 8-10 г/кг, что соответствует приблизительно 615-683 г углеводов для мужчин и 477-546 г для женщин. Не менее 1/3 суточного количества углеводов должны составлять легкоусвояемые углеводы (сахара), а остальные 2/3 могут быть представлены крахмалом.
Таким образом, оптимальное соотношение питательных веществ в рационе спортсменов 1 : 0,7: 4. Рекомендуется 4-разовый прием пищи. Завтрак содержит 30-35%, обед - 35-40%, полдник - 5-10% и ужин - 25-30% энергетической ценности рациона.
Потребность в витаминах, особенно водорастворимых, у спортсменов повышена. В частности, потребность в аскорбиновой кислоте может достигать 150-250 мг/сут. Из жирорастворимых витаминов особенно важен токоферол, стимулирующий мышечную деятель-
ность и, в частности, работу сердечной мышцы. Большие потребности в витаминах трудно удовлетворить обычными пищевыми продуктами, поэтому спортсмены часто используют поливитаминные препараты и витаминизированные продукты.
Для профилактики ацидоза в рацион спортсменов включают продукты с щелочным эквивалентом (молоко, овощи и фрукты). Повышенная потребность в фосфоре (в 1,5-2 раза по сравнению с человеком, не занимающимся спортом) удовлетворяется всеми продуктами животного происхождения. Фосфор из продуктов растительного происхождения, особенно из зерновых, усваивается плохо. Большая кислородная емкость крови, быстрое образование миоглобина возможны при адекватном поступлении с пищевыми продуктами железа, потребность в котором также увеличена в среднем на 20%. Несколько повышена потребность в магнии, который обладает ощелачивающими свойствами и участвует в образовании катализаторов реакций гликолиза. Из-за больших потерь хлоридов с потом в 1,5-2 раза увеличивается суточная потребность в поваренной соли, достигая 20-25 г/сут.
Таким образом, построенное на общих принципах сбалансированности базовое питание спортсменов в условиях обычных тренировочных занятий должно полностью покрывать повышенную потребность в белках, углеводах, витаминах и минеральных веществах при некотором ограничении количества жиров. Используют различные мясные и рыбные продукты с оптимальным аминокислотным составом белка. Рекомендуется включать в рацион мясо молодых животных, молочные продукты и яйца (до 2 штук в день). Особое значение в питании спортсменов имеют свежие овощи и фрукты, доля которых может достигать 15-20% энергетической ценности суточного рациона.
В дни интенсивных тренировок и соревнований в питании спортсменов следует ограничивать жареные блюда, жирные сорта мяса, копчености, бобовые, квашеную капусту и ржаной хлеб. Для питания на дистанции во время длительных соревнований рекомендуются шоколад, глюкоза и сахар, обогащенные аскорбиновой кислотой.
По окончании напряженных соревнований для предупреждения жировой инфильтрации печени рекомендуется как можно быстрее принять 150 г легкоусвояемых углеводов (глюкозы), а в течение последующих нескольких дней уменьшить в пищевом рационе жиры и одновременно увеличить количество творога, сыра, яиц.
В дни соревнований есть нужно за 3,5 ч до старта и через 15-20 мин после тренировок.
Особенности питания в районах высоких широт с экстремальными климатическими условиями
Почти 2/3 территории Российской Федерации относится к районам Крайнего Севера и местностям, приравненным к ним. У человека, проживающего в таких экстремальных климатических условиях, формируется так называемый полярный метаболический тип с повышением энергетической значимости белков и жиров и снижением углеводов. У аборигенов Севера повышенное поступление белка (до 15% общей энергетической ценности рациона) поддерживает высокую иммунореактивность, а большая доля жиров (до 35%) позволяет покрывать увеличенные потребности в энергии.
Набор продуктов жителей Арктики и Субарктики ограничен, в нем преобладают мясо и рыба и почти полностью отсутствуют молочные продукты, овощи и фрукты местного производства. С пищей поступает холестерина более 600-700 мг/сут, но в силу особенностей обмена атеросклероз и его осложнения (инфаркт миокарда, инсульт) занимают скромное положение (до 10%) в структуре патологии коренного населения Крайнего Севера.
Питание пришлого населения является составной частью акклиматизации и зависит от централизованных поставок пищевых продуктов, обогащенных витаминами, завоза и хранения овощей и фруктов, молочных продуктов. В районы Крайнего Севера завозят сахар-рафинад с аскорбиновой кислотой, молочный порошок с аскорбиновой кислотой и кальциферолом, пищевые жиры с ретинолом, муку с тиамином, рибофлавином и ниацином, овощные и фруктовые консервы с аскорбиновой кислотой и ретинолом. Питание на Севере, согласно рекомендациям Комитета ФАО/ВОЗ, с понижением среднемесячной температуры на каждые 10 °С, начиная с +10 °С, должно увеличивать энергетическую ценность на 5%.
В среднем потребность жителей Севера в энергии на 15% выше потребности жителей других климатических зон. Нормами физиологических потребностей в энергии и пищевых веществах для различных групп населения Российской Федерации (2008) предусматривается покрывать повышенную потребность в энергии жителей Крайнего Севера пропорциональным увеличением количества белков, жиров и углеводов.
Питание в условиях жаркого климата
Отсутствие знаний о механизмах адаптации и акклиматизации в регионах с жарким климатом может представлять опасность для здоровья, особенно для приезжающих в субтропики и тропики из умеренного климата. В низких широтах возможно формирование как специфических болезней - тепловых поражений, так и увеличение числа случаев заболеваний, встречающихся во всех климатических зонах, в частности нервно-психических расстройств, болезней кожи, травм, мочекаменной болезни, болезней сердечно-сосудистой системы, особенно у лиц старше 45 лет, а также ОРВИ.
В комплексе мер по адаптации к действию высокой температуры важное место занимает рациональное питание. Физиологический предел накопления организмом человека тепла - 600 кДж, что примерно в 10 раз меньше предельной теплоотдачи. Биологический резерв теплонакопления быстро расходуется при температуре окружающего воздуха 32-35 °С, т.е. когда механизмы физической терморегуляции выключены из обмена энергией с окружающей средой. Механизмы терморегуляции истощаются особенно быстро в жарком влажном климате, где неэффективен такой механизм терморегуляции, как испарение пота с поверхности тела.
Современными исследованиями установлено увеличение энергетического обмена при краткосрочной адаптации к высокой температуре окружающей среды. При долгосрочной адаптации к жаркому климату в натурных исследованиях получены противоречивые результаты. Существует концепция о снижении энергетического обмена в этих условиях. С учетом рекомендаций экспертов Продовольственной программы ФАО/ВОЗ принят постулат о понижении потребности людей в энергии на 5% при повышении температуры воздуха на каждые 10 °С по сравнению со стандартным уровнем 20 °С. Однако такой подход не имеет удовлетворительного физиологического обоснования, так как невозможно подтвердить снижение энергообмена в жарком климате при повышении температуры кожи, усилении потоотделения, повышении частоты сердечных сокращений, указывающих на усиление деятельности систем жизнеобеспечения, а следовательно, на накопление тепла в организме.
У военнослужащих на жаре в состоянии покоя метаболизм в течение дня увеличивается на 35%. В соответствии с этим в армии США при выполнении физической работы в условиях жары энергетическая
ценность рациона повышается на 5% на каждый градус повышения температуры воздуха в интервале между 30 и 40 °С.
Жара вызывает сложные изменения в деятельности системы гипо- физ-кора надпочечников. Увеличение в крови количества альдостерона и антидиуретического гормона приводит к торможению диуреза, уменьшению содержания натрия и увеличению содержания калия в моче. Стероиды коры надпочечников мобилизуют белковый и углеводный обмен. Увеличение выделения калия с мочой прямо связано с увеличением белкового катаболизма. В организме человека белковый и калиевый обмен имеет однонаправленные изменения. Распад 1 г азота сопровождается выведением 3 ммоль калия. В эксперименте на добровольцах показано, что увеличению экскреции азота соответствует повышение энерготрат за счет белка с 13,9 до 21,3%.
Следовательно, при построении рациона питания в жарком климате следует учитывать особенности метаболизма белка и минеральных веществ. Увеличение потерь калия может быть обусловлено его недостаточным поступлением с пищей, поскольку под действием высокой температуры в первые дни часто теряется аппетит.
Рацион в условиях жаркого климата должен содержать оптимальное количество полноценных белков, водорастворимых витаминов и минеральных веществ и меньше насыщенных жиров. Свежие овощи и фрукты, а также минеральная вода позволяют уменьшить дефицит водорастворимых витаминов и нормализовать водно-электролитный баланс. Жажду лучше утолять 200-300 мл воды через 1-2 ч. После приема пищи и во время отдыха лучше пить натуральные фруктовые соки, чай, кофе, компоты.
Хлорид натрия добавляют к питью для здоровых людей только при потерях жидкости с потом, превышающих 5 л/сут. Желательно перенести прием пищи на менее жаркое время суток, поэтому энергетическая ценность завтрака и обеда равняется 25%, а остальные 50% суточной энергетической ценности рациона приходятся на ужин.
Здоровое питание населения, проживающего на территориях с повышенным уровнем радиационного воздействия
На территории России радиоактивные загрязнения местности образовались в результате аварий на Чернобыльской АЭС и взрыва на радиохимическом заводе «Маяк» (Челябинская обл.).
На территории, загрязненной радионуклидами в результате аварии на Чернобыльской АЭС, в 1991 г. проживало, по данным Госкомстата,
4,87 млн человек, в том числе на территории России 1,553 млн, в Украине - 1,462 млн и в Беларуси - 1,86 млн. Для профилактики вредного воздействия радиации разработаны нормы питания (табл. 7.5).
Питание детей и взрослых в этих районах должно быть направлено на полное удовлетворение потребностей организма в пищевых веществах и энергии, профилактику возможных неблагоприятных биохимических нарушений (усиление перекисного окисления липидов, нарушение стабильности и проницаемости биологических мембран) и заболеваний, связанных с этими нарушениями.
Основными принципами построения рационов питания взрослого и детского населения являются:
• увеличение доли белков до 15% энергетической ценности рациона, в основном за счет белков животного происхождения;
• относительное ограничение поступления ПНЖК при общем содержании жира в рационе не более 30% энергетической ценности;
• содержание витаминов-антиоксидантов (А, Е, С), повышенное на 20-50% по сравнению с возрастными нормами;
• увеличение на 20-30% содержания растительных волокон, обеспечивающих нормальную моторику кишечника и неспецифическую адсорбцию радионуклидов;
• повышение содержания кальция и калия, способствующих выведению радионуклидов стронция и цезия соответственно;
• достаточное содержание в рационе йода, направленное на компенсацию его дефицита в биогеохимических провинциях со сниженным содержанием йода в почве, воде и пищевых продуктах.
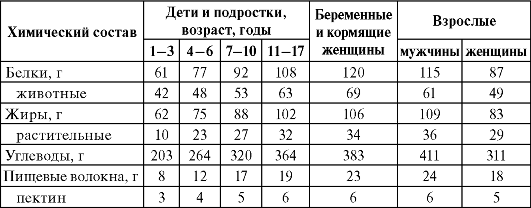
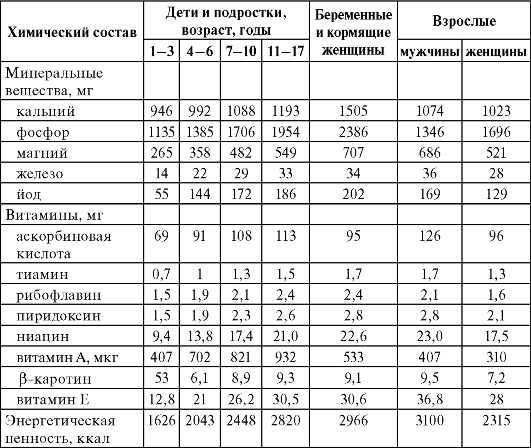
Таблица 7.5. Рекомендуемые нормы потребления пищевых веществ и энергии для населения территорий, загрязненных радионуклидами
 В
рацион включают мясо, птицу, рыбу, субпродукты (белок с высокой
биологической активностью и витамин А), молоко, творог и сыр
(полноценный белок и легкоусвояемый кальций), овощи и фрукты,
натуральные соки с мякотью (витамин С, каротин, калий, пектин,
клетчатка). Для обеспечения потребностей в йоде и пищевых волокнах в
рацион следует вводить морепродукты.
В
рацион включают мясо, птицу, рыбу, субпродукты (белок с высокой
биологической активностью и витамин А), молоко, творог и сыр
(полноценный белок и легкоусвояемый кальций), овощи и фрукты,
натуральные соки с мякотью (витамин С, каротин, калий, пектин,
клетчатка). Для обеспечения потребностей в йоде и пищевых волокнах в
рацион следует вводить морепродукты.
Для наиболее полного обеспечения организма витаминами рекомендуется регулярный прием поливитаминных препаратов.
7.4. ПИЩЕВОЙ СТАТУС КАК ПОКАЗАТЕЛЬ ЗДОРОВЬЯ
Термином «пищевой статус» характеризуется состояние здоровья, сложившееся на фоне конституциональных особенностей организма под воздействием фактического питания.
Изучение пищевого статуса основано на изучении состояния здоровья как показателя адекватности индивидуального питания. Обобщенная характеристика состояния здоровья и особенностей питания конкретного человека необходима для определения объема и характера лечебно-диагностических, диетических и гигиенических мероприятий. Оценка пищевого статуса включает определение показателей функции питания, пищевой адекватности (выявление признаков пищевой недостаточности, избыточности или несбалансированности рациона) и заболеваемости (схема 7.2). Под функцией питания понимают систему обменных процессов, нейрогуморальная регуляция которых обеспечивает относительное постоянство внутренней среды организма (гомеостаз). Функцию питания оценивают по показателям процессов пищеварения и обмена веществ: белкового, жирового, углеводного, витаминного, минерального, водного.
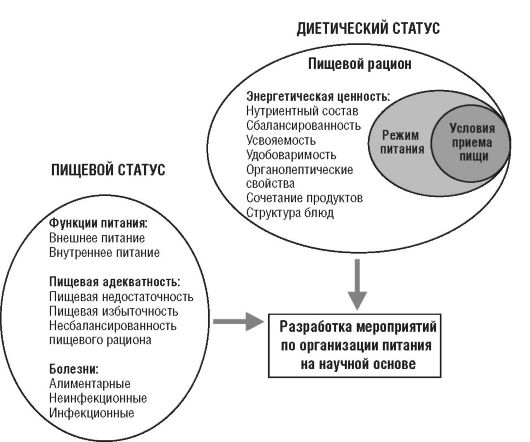 Схема 7.2. Анализ и коррекция пищевого статуса
Схема 7.2. Анализ и коррекция пищевого статуса
Оценку пищевой неадекватности проводят на основании показателей роста, массы тела и массо-ростового показателя, обмена веществ (конечные продукты обмена в моче, содержание специфических метаболитов в крови, активность ферментов и др.); функционального состояния отдельных систем организма (нервная, пищеварительная, сердечно-сосудистая и др.). На основании исследований выявляют ранние симптомы пищевой неадекватности.
Заболеваемость характеризует процесс возникновения и распространения патологии среди населения в результате взаимодействия настоящих и предшествующих поколений людей с окружающей средой (в широком понимании этого слова), проявляющейся в различных формах в конкретных условиях существования общества.
Заболеваемость тесно связана с пищевым статусом и обусловлена различными нарушениями питания, в частности недостаточным или избыточным питанием. Ценные косвенные данные о влиянии питания получают при анализе распространенности важнейших неинфекционных заболеваний (болезни сердечно-сосудистой системы и желудочно-кишечного тракта). Однако следует помнить, что и заболеваемость большинством инфекционных и паразитарных заболеваний тесно связана с фактическим питанием отдельного человека или популяции.
Пищевой статус подразделяется на обычный, оптимальный, избыточный и недостаточный. При обычном пищевом статусе структура и функции организма не нарушены, адаптационные резервы организма достаточны для обычных условий жизнедеятельности. Оптимальный пищевой статус формируется при использовании специальных рационов для обеспечения высокой резистентности к экстремальным (стрессовым) ситуациям, что позволяет организму выполнять работу в необычных условиях без каких-либо заметных сдвигов в гомеостазе.
Избыточный пищевой статус связан с избыточным поступлением пищевых веществ и энергии, а недостаточный формируется соответственно при количественной и особенно качественной недостаточности питания. Как при избыточном, так и при недостаточном статусе питания происходит нарушение структур и функций организма, что находит выражение в парциальном нарушении работоспособности и состояния здоровья, а в тяжелых случаях - в формировании соматической патологии.
Недостаточный пищевой статус по выраженности нарушений функций и структур делится на неполноценный, преморбидный и патологический. Неполноценный статус проявляется в снижении адаптационных возможностей организма в обычных условиях существования; симптомы алиментарной недостаточности еще не проявляются. При преморбидном статусе на фоне снижения функциональных возможностей и изменения биохимических показателей появляются микросимптомы пищевой недостаточности. Патологический статус проявляется явными признаками алиментарной недостаточности с выраженными нарушениями структур и функций организма.
Оценка здоровья как показателя адекватности питания основана на выявлении различных видов алиментарной недостаточности. Используются данные медицинской документации (амбулаторные или диспансерные карты), социально-демографические показатели (заболеваемость по статистической отчетности, продолжительность жизни, смертность, производительность труда и трудопотери), клинические показатели, результаты функциональной диагностики и биохимических исследований.
Клинические симптомы витаминной недостаточности
Комитетом экспертов ВОЗ для оценки пищевого статуса рекомендованы следующие симптомы неадекватности питания. Глаза:
• ксероз конъюнктив. Сухость, утолщение, пигментация конъюнктивы открытой части глазного яблока и потеря ею блеска и прозрачности. Симптом легко обнаружить, оттянув веки. Проявляется при недостаточности витамина А;
• бляшки Искерского (пятна Бито). Четко очерченные поверхностные сероватые, серебристые или белые, как мел, пенистые бляшки, имеющие треугольные или неправильно округлые очертания и чаще локализующиеся снаружи от роговицы. Бляшки представляют собой остатки ороговевших эпителиальных клеток, всегда сочетаются с ксерозом конъюнктивы, свидетельствуют о гиповитаминозе А и чаще обнаруживаются у детей раннего и дошкольного возраста. Иногда наблюдаются у школьников и взрослых как изолированный симптом авитаминоза А при отсутствии каких бы то ни было других признаков;
• нарушение темновой адаптации. Может быть признаком недостаточности витаминов А, В2 и С.
Губы:
• ангулярный стоматит. Эрозии и трещины в углах рта. При гиповитаминозе поражены оба угла рта. Проявляется при недостаточности витаминов В и В ?
2 6'
• хейлоз. Вертикальные трещины губ с отечностью и гиперемией, а также изъязвление по всей поверхности губ. Чаще поражается центральная часть нижней губы. Признак недостаточности витаминов В2, В6 и РР. Иногда поражение в этой части губы обусловлено низкой температурой воздуха и ветром.
Язык:
• отек языка. Отпечатки зубов по краю языка. Признак недостаточности витаминов В, В, РР;
26
• атрофия сосочков. Исчезают нитевидные сосочки, поверхность языка становится совершенно гладкой. Признак недостаточности витаминов В2 и РР;
• гиперемия и гипертрофия сосочков. Сосочки гипертрофированы, красного или розового цвета, поверхность языка кажется зернистой (землянично-красной). Признак недостаточности витаминов В2 и РР;
• ярко-красный язык, отпечатки зубов и чувство жжения языка могут быть признаками недостаточности витамина РР;
• глоссит - гиповитаминоз В6. Необходимо помнить, что поражения в полости рта иногда бывают следствием местной травмы твердой пищей или зубным протезом.
Десны:
• рыхлые кровоточащие десны, фиолетовые или красные. Отечные межзубные сосочки и края десен, кровоточащие при легком надавливании. Авитаминоз С. Этот симптом отсутствует у детей раннего возраста (детская цинга), даже при случаях тяжелого авитаминоза С.
Зубы:
• частота развития кариеса зубов достаточно заметно связана с характером пищи, особенно с содержанием в ней сахара, муки тонкого помола и других легкоусвояемых углеводов.
Кожа:
• ксероз. Общая сухость кожи с шелушением - симптом недостаточности витамина А. При рассмотрении этого и других кожных симптомов следует иметь в виду факторы внешней среды, такие как грязь, сухой, жаркий, ветреный климат. Необходимо исключить генетический фактор, например врожденный ихтиоз;
• фолликулярный гиперкератоз. Бляшки шипообразной формы вокруг шейки волосяного фолликула. Симптом легко обнаружить по характерному ощущению (кожа как бы колется при проведении рукой по пораженному участку). Локализация - область ягодиц, бедер и локтей. Признак недостаточности витаминов А и С;
• петехии. Мелкие пятна геморрагий на коже и слизистых оболочек. Если наложить жгут, иногда появляются дополнительные геморрагии. Симптом недостаточности витаминов Р и С.
Ногти:
• койлонихия. Двусторонняя ложковидная деформация ногтей у детей старших возрастных групп и у взрослых. Симптом недостаточности железа.
Органы пищеварения:
• диспепсический синдром - запах изо рта, неприятный привкус во рту, отрыжка, изжога, тошнота, рвота, метеоризм. Необходимо исследование желудка, двенадцатиперстной кишки, кишечника, определение границ печени.
Нервная система:
• психомоторные изменения. Апатия часто определяется у лиц старческого возраста, но чаще как признак белково-энергетической недостаточности питания отмечается у маленьких детей при развитии квашиоркора. У детей симптом не поддается точной оценке и приблизительно может быть определен по реакции ребенка на яркие предметы и цвет. Повышение утомляемости, снижение работоспособности, раздражительность, общая слабость могут быть признаками недостаточности витаминов В1, В6, РР и С;
• бессонница и боли в мышцах отмечаются при недостаточности витамина В1.
Для подтверждения связи патологических процессов с состоянием питания особое внимание придается определению заболеваний, в этиологии которых существенную роль играют нарушения питания: алиментарная дистрофия, болезни органов пищеварения, печени, обмена веществ (ожирение, подагра), сердечно-сосудистой системы (атеросклероз, гипертоническая болезнь). Во всех случаях необходимо иметь результаты общего анализа мочи и крови. В связи с неспецифичностью большинства клинических симптомов для подтверждения связи между нарушениями здоровья и нарушениями питания необходимо проводить антропометрические исследования и избранные биохимические тесты для характеристики состояния обмена веществ.
Антропометрические показатели физического развития
Показатели физического развития являются наиболее информативным критерием соответствия энергетической и биологической ценности рациона питания потребностям организма. Уровень и гармоничность физического развития взрослых и детей определяются антропометрическими исследованиями с использованием региональных стандартов физического развития. Если стандарты для данного региона не разработаны, следует использовать индекс массы тела (ИМТ):
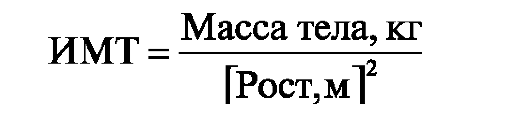 Этот
росто-массовый показатель меньше связан с ростом и больше зависит от
массы тела, вследствие чего хорошо отражает содержание жира в теле. В
качестве референтных интервалов рассматривается как нормальное значение
ИМТ - 18,5-25 кг/м2; недостаточная масса тела - ИМТ < 18,5 кг/м2 (признак белково-энергетической недостаточности); избыточная масса тела - ИМТ от 25 до 30 кг/м2, ожирение - ИМТ > 30 кг/м2.
Этот
росто-массовый показатель меньше связан с ростом и больше зависит от
массы тела, вследствие чего хорошо отражает содержание жира в теле. В
качестве референтных интервалов рассматривается как нормальное значение
ИМТ - 18,5-25 кг/м2; недостаточная масса тела - ИМТ < 18,5 кг/м2 (признак белково-энергетической недостаточности); избыточная масса тела - ИМТ от 25 до 30 кг/м2, ожирение - ИМТ > 30 кг/м2.
Массу тела взрослых следует сравнивать с идеальной, т.е. статистически коррелирующей с наибольшей ожидаемой продолжительностью жизни для лиц данного пола, возраста и роста. Признаком ожирения считается увеличение массы тела по отношению к идеальной на 15% и более, т.е. ИМТ > 30 кг/м2.
Антропометрический статус оценивается по соответствию возрастным региональным стандартам показателей роста, массы тела, толщины кожной складки, окружности мышц плеча, а также по экскреции креатина.
Биохимические критерии адекватности питания
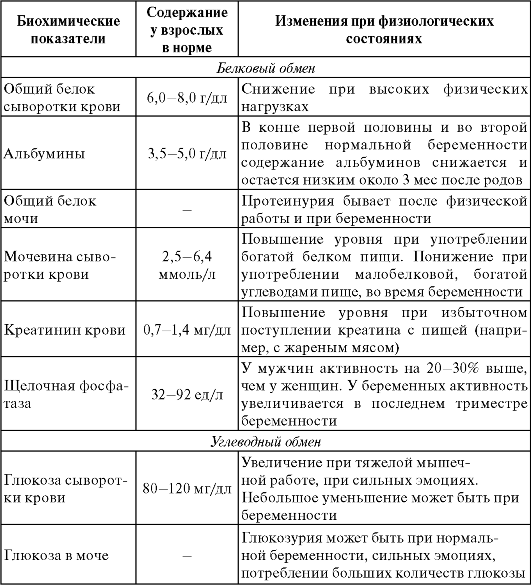
Как недостаточный, так и избыточный пищевой статус проявляется изменениями обменных процессов. Преморбидное состояние объективно проявляется изменениями биохимических показателей, связанных с обменными процессами основных пищевых веществ. Количественные изменения биохимических показателей в этом случае выполняют роль маркеров нарушений питания. В комплексе с данными объективного медицинского исследования и гигиенической оценки типичного пищевого рациона они позволяют выявлять ранние изменения структур и функций организма. В табл. 7.6. представле-
ны избранные биохимические показатели, которые могут указывать как на алиментарный генез их изменений, так и на особенности обменных процессов при некоторых физиологических состояниях. Нормы биохимических показателей приведены для умеренного климата Европейской территории России. Для районов с экстремальными климатическими условиями используются региональные стандарты, соответствующие генетической и социальной адаптации населения.
Таблица 7.6. Важнейшие клинико-биохимические константы
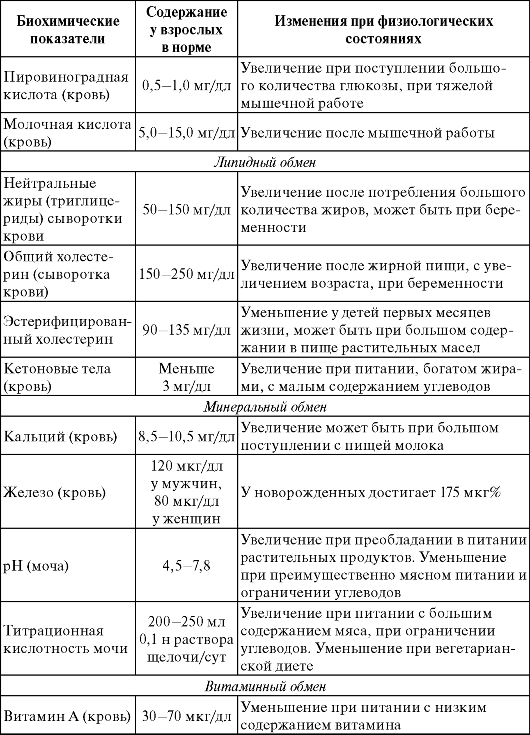
 Оценка
пищевого статуса конкретного человека позволяет сформулировать
индивидуализированные рекомендации по количеству и пропорциям пищевых
компонентов с учетом особенностей метаболизма, возможной
предрасположенности к определенным заболеваниям, реального
функционального состояния организма, пола, возраста, рода занятий,
климатических условий проживания и других факторов, формирующих качество
жизни.
Оценка
пищевого статуса конкретного человека позволяет сформулировать
индивидуализированные рекомендации по количеству и пропорциям пищевых
компонентов с учетом особенностей метаболизма, возможной
предрасположенности к определенным заболеваниям, реального
функционального состояния организма, пола, возраста, рода занятий,
климатических условий проживания и других факторов, формирующих качество
жизни.
7.5. ЗАБОЛЕВАНИЯ ПРИ НЕДОСТАТОЧНОМ ПИЩЕВОМ СТАТУСЕ
При питании, неадекватном потребностям организма, возникают нарушения метаболизма клеток. Алиментарная недостаточность существенно снижает способность организма синтезировать специфические антитела, фагоцитарную активность микро- и макрофагов, неспецифическую резистентность к бактериальным токсинам, является причиной ослабления воспалительной реакции, замедляет заживление ран и образование коллагена, изменяет микрофлору кишечника.
Болезни пищевой недостаточности сопровождаются стойкими изменениями биохимических констант внутренней среды организма. Чувствительность к дефициту пищевых веществ тем выше, чем моложе организм и чем интенсивнее его рост.
Длительное одностороннее (ограниченное по какому-либо питательному веществу) питание приводит к глубоким изменениям в клетках, вплоть до явлений дистрофии, которые проявляются раньше, чем будут использованы собственные запасы питательных веществ организма. Болезни недостаточности питания связаны с недостатком в рационе белков, витаминов, минеральных веществ и микроэлементов.
Белково-энергетическая недостаточность
Белково-энергетическая недостаточность в клинической практике встречается в виде квашиоркора и алиментарного маразма.
Квашиоркор бывает у детей в возрасте 2-3 лет. Главной причиной заболевания является несбалансированное питание, особенно по белкам животного происхождения. Как правило, энергетическая составляющая рациона обеспечена легкоусвояемыми углеводами. Вместе с тем практически никогда квашиоркор не имеет исключительно пищевую этиологию: в его возникновении очень часто участвуют инфекционные, психологические, культурные, религиозные факторы.
Переход от грудного вскармливания к общему столу представляет для ребенка критический период. На 2-3-м году жизни потребность в белках (незаменимых аминокислотах) особенно велика из-за быстрого роста и развития мышечной ткани. Эксперты ФАО/ ВОЗ определяют потребность в белке у ребенка 1-3 лет равной 0,88-1,76 г/кг. Недостаточное поступление полноценного белка приводит к появлению отеков. Нарушение синтеза ферментов поджелудочной железы сопровождается нарушениями процессов пищеварения и абсорбции (мальабсорбция), в результате чего возникает диарейный синдром.
Различают постоянно встречающиеся симптомы квашиоркора: отек (отсутствие отека позволяет исключить квашиоркор, это главный признак); отставание роста от возрастных норм; мышечная гипотония с сохранением подкожной клетчатки и психомоторные нарушения (апатия, грусть, инертность, индифферентное отношение к окружающему и потеря аппетита).
Среди не обязательных для диагностики, но часто встречающихся симптомов следует назвать изменения цвета и формы волос («красные мальчики»); депигментацию кожи («змеиная кожа»); лунообразную форму лица (отек и гормональные нарушения), анемию, неоформленный стул, содержащий непереваренные пищевые частицы.
Непостоянными симптомами считают десквамационный дерматоз с участками гиперпигментации; сплено- и гепатомегалию; кератомаляцию как следствие авитаминоза А; глоссит, хейлит и ангулярный стоматит как следствие недостаточности витамина В2.
Второй важный синдром белково-энергетической недостаточности - алиментарный маразм (кахексия). Возникновение алиментарного маразма связано с недостатком одновременно и белков, и энергетической ценности пищи. Это состояние может развиться во
всех возрастных группах, включая и взрослых, но чаще встречается у детей первого года жизни. Причинами являются социально-экономические факторы (голод), раннее прекращение грудного вскармливания без адекватного искусственного питания. Маразм часто сочетается с диареей инфекционной этиологии и туберкулезом.
Алиментарный маразм сопровождается отставанием физического развития (отставание массы тела от возрастной нормы достигает 60%, происходит задержка роста) и мышечной дистрофией при отсутствии подкожного жира. Потеря подкожной клетчатки вызывает появление морщин (лицо «маленького старичка» или «обезьяны»).
При маразме не изменяются форма и цвет волос, никогда не бывает депигментации кожи, нет отеков. Психические нарушения выражены гораздо менее значительно, чем при квашиоркоре: ребенок подвижен и имеет хороший аппетит.
Признаки белково-энергетической недостаточности в России в середине 90-х годов ХХ века встречались у 6-8% детей раннего возраста и у 2% взрослых.
Гипо- и авитаминозные состояния
Под авитаминозами понимают состояние полного истощения витаминных запасов в организме, при гиповитаминозе резко снижено содержание того или иного витамина. В последние годы выделяют еще одну форму дефицита витаминов - субнормальную обеспеченность, обозначаемую как маргинальная (биохимическая) недостаточность. Она проявляется до клинических симптомов недостаточности и обусловливает только биохимические нарушения.
Причины развития гипо- и авитаминозных состояний
(по Самсонову М.А. и Покровскому А.А., 1992)
I. АЛИМЕНТАРНАЯ НЕДОСТАТОЧНОСТЬ ВИТАМИНОВ
1. Низкое содержание витаминов в рационе питания.
2. Разрушение витаминов вследствие технологической переработки продуктов, их длительного и неправильного хранения и нерациональной кулинарной обработки.
3. Действие антивитаминных факторов, содержащихся в продуктах.
4. Присутствие в продуктах витаминов в малоусвояемой форме.
5. Нарушение сбалансированности рационов и оптимальных соотношений между витаминами и другими веществами и между отдельными витаминами.
6. Пищевые извращения и религиозные запреты, налагаемые на ряд продуктов.
7. Анорексия.
II. УГНЕТЕНИЕ НОРМАЛЬНОЙ КИШЕЧНОЙ МИКРОФЛОРЫ, ПРОДУЦИРУЮЩЕЙ ВИТАМИНЫ
1. Болезни желудочно-кишечного тракта.
2. Нерациональная химиотерапия.
III. НАРУШЕНИЯ АССИМИЛЯЦИИ ВИТАМИНОВ
1. Нарушения всасывания витаминов в желудочно-кишечном тракте: заболевания желудка и кишечника, поражения гепатобилиарной системы, конкурентные отношения с абсорбцией других витаминов и пищевых веществ, врожденные дефекты транспортных и ферментных механизмов абсорбции витаминов.
2. Утилизация поступающих с пищей витаминов кишечными паразитами и патогенной кишечной микрофлорой.
3. Нарушение метаболизма витаминов и образования их биологически активных форм при наследственных аномалиях или приобретенных заболеваниях, под действием токсических или инфекционных агентов.
4. Нарушения образования транспортных форм витаминов (наследственные, приобретенные).
5. Антивитаминное действие лекарственных препаратов, ксенобиотиков.
IV. ПОВЫШЕННАЯ ПОТРЕБНОСТЬ В ВИТАМИНАХ
1. Особые физиологические состояния организма (интенсивный рост, беременность, лактация).
2. Особые климатические условия.
3. Интенсивная физическая нагрузка.
4. Интенсивная нервно-психическая нагрузка, стресс.
5. Инфекционные состояния и интоксикации.
6. Действие вредных производственных факторов.
7. Заболевания внутренних органов и желез внутренней секреции.
8. Повышенная экскреция витаминов.
Субнормальная обеспеченность витаминами широко распространена (беременные и кормящие женщины, дети различных возрастных групп, студенты, лица пожилого возраста и др.). Распространенность этого состояния сопряжена с падением уровня доходов, изменением
структуры питания, широким использованием рафинированных продуктов, потерявших витамины в процессе приготовления, хранения, нерациональной кулинарной обработки. При субнормальной обеспеченности витаминами снижается устойчивость организма к простудным и инфекционным заболеваниям, психоэмоциональному стрессу, действию неблагоприятных (вредных) факторов окружающей среды.
Гиповитаминоз А. Дефицит витамина А часто обнаруживается у детей дошкольного возраста в виде специфических поражений глаз. Это прогрессирующее поражение конъюнктивы и роговицы глаза (ксерофтальмия), нарушение сумеречного зрения (гемералопия, «куриная слепота») и цветовосприятия. Среди других признаков гиповитаминоза А следует назвать кожные поражения в виде гиперкератоза, повышенную восприимчивость к инфекционным заболеваниям, метаплазию и кератинизацию покровных клеток дыхательных путей.
Недостаточность ретинола в организме человека сопровождается рядом иммунологических нарушений. Отмечают лимфопению с атрофией лимфоидных органов, ослабление иммунного ответа на воздействие различных антигенов, подавление трансплантационного иммунитета, реакций гиперчувствительности замедленного типа, репродукции Т- и В-лимфоцитов. В эпидемиологических исследованиях установлена обратная связь между обеспеченностью ретинолом и β-каротином и частотой рака толстой кишки. Считается, что точкой приложения действия ретиноидов является система Т-хелперов. Дефицит витамина А сопровождается нарушением иммунного контроля за постоянством антигенного состава клеток, что вызывает снижение антибластомной резистентности и создает условия для развития опухолевого процесса.
Недостаточность витамина D (рахит) отмечается у многих детей раннего возраста, особенно проживающих в крупных городах. В начальной стадии рахита наблюдаются нехарактерные нарушения: повышенная нервная возбудимость ребенка, слабость, потливость, особенно головы, запоздалое прорезывание зубов, легкая спазмофилия, склонность к бронхитам. Через несколько месяцев, когда ребенок начинает садиться и стоять, проявляются искривления позвоночника, деформация бедер, голеней и - в значительно меньшей степени - верхних конечностей.
У взрослых авитаминоз встречается редко и проявляется в форме остеопороза и остеомаляции. В группу риска по развитию дефицитных по витамину D состояний входят также беременные, лица,
долго лишенные солнечного света и потребляющие много углеводов и пищу с дисбалансом кальция и фосфора; пожилые люди, исключающие из питания продукты животного происхождения; жители Крайнего Севера.
Гиповитаминоз Е у человека встречается крайне редко. У грудных детей это состояние связывают с недостаточным плацентарным транспортом токоферола, обусловленного низким уровнем β-липопротеидов в крови плода. Недоношенные дети больше подвержены формированию гиповитаминозных состояний, так как всасывание токоферола нарушено при морфофункциональной незрелости желудочно-кишечного тракта и организма ребенка в целом. Одной из причин развития гиповитаминозных состояний у детей может стать искусственное вскармливание смесями без добавок витамина. У взрослых проявления недостаточности токоферола могут быть связаны с перегруженностью пищевого рациона ПНЖК, у спортсменов - большой физической нагрузкой, а также с поражением системы пищеварения, включающим нарушение всасывания жиров.
При дефиците токоферола повышается подверженность простудным заболеваниям, наблюдается преждевременное старение кожи.
Гиповитаминоз Е считают фактором риска по атеросклерозу и его осложнениям - ишемической болезни сердца и стенокардии. Недостаточность токоферола играет важную роль в возникновении различных заболеваний печени и желчных путей.
Дефицит тиамина (гиповитаминоз В1) возникает при питании с большим удельным весом рафинированных углеводов. Формированию гиповитаминоза В1 способствует повышенная потребность в тиамине (жаркий и холодный климат, интенсивная физическая работа, нервнопсихическое напряжение, беременность и лактация).
Эндогенная недостаточность может возникать при эндокринных и инфекционных заболеваниях, отравлениях тяжелыми металлами и органическими растворителями, интоксикации сульфаниламидами и антибиотиками, у злостных курильщиков и алкоголиков.
Клинические симптомы выражаются головной болью, повышенной утомляемостью, нарушениями сна, раздражительностью, депрессией. Для гиповитаминоза характерны мышечная астения, боли и судороги в икроножных мышцах, нарушения деятельности сердечнососудистой системы и обмена веществ.
Периферические полиневриты (болезнь бери-бери) характерны для выраженного авитаминоза В1.
Гиповитаминоз В2 чаще проявляется изменениями со стороны слизистой оболочки рта, кожи и глаз. Для гиповитаминоза характерны ангулярный стоматит с трещинами в углах рта («заеда»); поражение слизистой губ с вертикальными трещинами и десквамацией эпителия (хейлоз); поражение кожи носогубных складок, век, ушных раковин, волосистой части головы (себорейный дерматит).
При арибофлавинозе язык становится пурпурно-красным и отечным, имеет мелкозернистую поверхность («географический язык»), возникают симптомы поражения глаз (конъюнктивит, блефарит, васкуляризация и помутнение роговицы, нарушение световой и цветовой чувствительности).
Большие дозы аскорбиновой кислоты предотвращают или задерживают развитие арибофлавиноза. При недостаточности рибофлавина развивается гипохромная микроцитарная анемия.
Дефицит рибофлавина в пищевом рационе беременных женщин является фактором риска по недонашиванию плода и разрешению мертворожденным. Чаще всего гиповитаминоз у беременных встречается в последнем триместре беременности. Появление трещин на сосках у кормящих женщин также связано с недостаточностью рибофлавина.
Недостаточность витамина В2 часто сочетается с дефицитом витамина В, и никотиновой кислоты.
Гиповитаминоз В2 может возникнуть при отсутствии в рационе молока и молочных продуктов, дефиците полноценного белка (квашиоркор), из-за повышенной потребности в витамине в условиях холодного и жаркого климата, интенсивной физической нагрузки, при беременности и лактации, а также при болезнях печени и желудочно-кишечного тракта.
Недостаточность пиридоксина (гиповитаминоз В6) встречается редко, поскольку этот витамин широко представлен в различных продуктах. Симптомы гиповитаминоза В6 возможны при хронических заболеваниях желудочно-кишечного тракта, при наследственных дефектах пиридоксинзависимых ферментов, лечении антагонистами пиридоксина (изониазид, гидралазин, пеницилламин, дезоксипиридоксин, диоксифенилаланин и др.), у женщин при применении оральных контрацептивов и у лиц, страдающих алкоголизмом.
Недостаточность пиридоксина проявляется нарушениями ЦНС (раздражительность, сонливость, заторможенность, полиневриты), поражениями кожных покровов и слизистых оболочек (себорейный дерматит, ангулярный стоматит, глоссит, хейлоз, конъюнктивит).
Авитаминоз В12 может возникать у вегетарианцев, у беременных, при хроническом алкоголизме, нарушениях синтеза внутреннего фактора Кастла и наследственных дефектах транспортных белков, участвующих в переносе цианокобаламина. Симптомы недостаточности витамина В12: раздражительность, повышенная утомляемость, дегенерация и склероз задних и боковых столбов спинного мозга сначала с парестезиями, а затем с параличами и нарушениями функций тазовых органов, потеря аппетита, нарушения моторики кишечника, глоссит и ахилия.
Дефицит фолиевой кислоты является наиболее распространенной формой витаминной недостаточности. Алиментарная недостаточность витамина обусловлена его плохим усвоением из пищи. Высокое содержание фолацина обнаружено в печени, листовых овощах, бобах и дрожжах. При кулинарной обработке количество доступного для всасывания витамина существенно снижается.
Гиповитаминоз чаще встречается у пожилых людей с низким достатком и страдающих алкоголизмом, у беременных и кормящих матерей. Недостаточность фолиевой кислоты сопровождается развитием мегалобластической гиперхромной анемии с явлениями лейко- и тромбоцитопении, гастритов, стоматитов и энтеритов. Беременные представляют особую группу риска, так как гиповитаминоз способствует появлению тератогенных эффектов и может привести к нарушениям психического развития новорожденных. При потребности взрослых 400 мкг/сут у беременных суточное поступление фолиевой кислоты должно быть на уровне 600 мкг. Симптомы гиповитаминоза возникают тогда, когда с пищей длительное время в организм поступает менее 5 мкг/сут фолиевой кислоты (см. также раздел «Витамины»).
Болезни, обусловленные нарушениями поступления микроэлементов
Болезни и симптомы, обусловленные дефицитом, избытком или дисбалансом микроэлементов, называются микроэлементозами. В зависимости от количества поступающих микроэлементов выделяют гипо- и гипермикроэлементозы.
Гипомикроэлементозы могут иметь экзо- и эндогенное происхождение. Экзогенные гипомикроэлементозы встречаются примерно у 20% местного населения биогеохимических провинций с недостаточным содержанием микроэлементов в окружающей среде. К эндогенным относятся гипомикроэлементозы, обусловленные наследственными
или врожденными заболеваниями. Особую и малоизученную группу представляют вторичные эндогенные микроэлементозы, возникающие при инфекционных заболеваниях, ревматизме, туберкулезе, хронических заболеваниях пищеварительной системы, почек и ЦНС. Гипомикроэлементозы в этом случае развиваются, несмотря на поступление микроэлементов в организм в адекватных количествах и соотношениях. По количеству дефицитных микроэлементов гипомикроэлементозы разделяют на моно- и полигипомикроэлементозы.
Гипермикроэлементозы связаны с избыточным содержанием микроэлементов в окружающей среде естественного (геохимические провинции) или искусственного (техногенное загрязнение местности) происхождения.
Недостаточность железа является распространенным следствием неадекватного питания и наиболее частой причиной алиментарной железодефицитной анемии, которая, по оценкам экспертов ВОЗ, составляет около 80% всех алиментарных анемий. Дефицит железа особенно часто встречается у детей и женщин детородного возраста, потребляющих пищу относительно низкой энергетической ценности.
Причины дефицита железа: недостаточное поступление с пищевыми продуктами, увеличенные потери железа (обильные менструации, хроническая потеря крови при язвенной болезни желудка, заболеваниях желудочно-кишечного тракта и мочеполовой системы, хроническая гемоглобинурия, паразитозы), мальабсорбция железа (заболевания тонкой кишки, состояние после гастрэктомии), увеличенная потребность в железе (дети, беременные и кормящие женщины).
Алиментарная профилактика железодефицитных состояний должна строиться с учетом не только содержания железа в пищевых продуктах, но и его биологической доступности. У здоровых людей усвоение железа колеблется от 1% при растительном рационе до 10-25% при употреблении мяса. На всасывание железа влияют многие составные части пищи. Из пищи всасывается преимущественно железо, входящее в состав гема, в меньшей степени двухвалентное и почти не всасывается трехвалентное. Вещества, повышающие усвоение железа из негемоглобинового источника, кроме мяса, содержатся в рыбе, птице и печени. Утилизацию негемоглобинового железа усиливает аскорбиновая кислота.
Недостаточность хрома. Трехвалентный хром является активной составной частью глюкозотолерантного фактора и необходим для образования и активации инсулина. Симптомы дефицита хрома
отмечены у детей с белково-энергетической недостаточностью, у пожилых людей и беременных. Недостаточность хрома снижает толерантность к глюкозе.
Физиологическая потребность в хроме для взрослых составляет 50 мкг/сут, для детей - от 11 до35 мкг/сут. Хром встречается в составе многих соединений, различающихся как по физиологической активности и степени абсорбции в кишечнике, так и по устойчивости при кулинарной обработке, поэтому расчетное определение хрома в рационах может ввести в заблуждение. Так, максимальное количество хрома содержится в яичном желтке и устрицах, но максимальной физиологической активностью обладают пивные дрожжи, а наименьшей - мясо кур и сухое молоко. В яичном желтке, так же как и в овощах, хром биологически недоступен. Практически значимыми источниками активного хрома являются дрожжи, печень, мясо, хлеб, сухие грибы и пиво.
Недостаточность йода встречается в биогеохимических провинциях многих стран мира. В России дефицит йода встречается на Кавказе, Горном Алтае, Урале, в Чувашии, Мордовии, Марий-Эл и др. Биологическое значение йода связано с развитием эндемического зоба, проявляющегося в гипофункции и компенсаторном диффузном увеличении щитовидной железы. Физиологическая потребность в йоде у взрослых - 150 мкг/сут, у детей - от 60 до 150 мкг/сут.
В эндемических по зобу районах распространены железодефицитные анемии, отклонения в физическом развитии детей, нарушения процессов окостенения и полового созревания, снижение умственной работоспособности и иммунного статуса. При наиболее выраженной форме дефицита йода развивается кретинизм с выраженным слабоумием, задержкой роста, непропорциональностью физического развития. В зонах йодной недостаточности довольно часто регистрируются всевозможные врожденные уродства. Патогенное действие дефицита йода усугубляется при недостаточном поступлении в организм ионов меди, кобальта и избытке марганца. Процессы метаболизма йода ухудшаются на фоне неадекватного питания (дефицит белков при избытке углеводов, избыток жиров, дисбаланс витаминов).
Заболеваемость населения эндемическим зобом снижают комплексные оздоровительные мероприятия: йодная профилактика в сочетании с оптимизацией геохимического состава почвы и повышением качества жизни. Йодированная поваренная соль содержит 25 г йодида калия на 1 т соли и позволяет обеспечить ежедневное поступ-
ление около 200 мкг йода. Однако йодированная соль нестойка при хранении и через 6 мес ее используют уже как обычную поваренную соль. Кроме того, потери йода при тепловой обработке блюд, приготовленных с использованием йодированной соли, достигают 60%.
Недостаточность селена. Первые прямые доказательства незаменимости селена для человека получены в 1979 г. на больных ювенильной кардиомиопатией (так называемая болезнь Кешана). В китайской провинции Кешан с низким содержанием селена в почве и воде было зарегистрировано множество случаев кардиомиопатии. Механизмы возникновения заболевания до конца не изучены, но дефициту селена отводят основное место, поскольку селенопрофилактика (назначение селенита натрия или обогащенных селеном дрожжей либо богатых селеном морских продуктов) позволяет успешно предотвращать заболевание. Потребность в селене определена на уровне 55 мкг/сут для женщин, 70 мкг/сут - для мужчин, от 10 до 50 мкг/сут - для детей и зависит от активности системы цитохрома Р-450, обеспеченности организма цинком, медью, марганцем, железом и витамином Е. Замечено, что в обычных дозах селен проявляет защитные свойства при отравлениях афлатоксинами, гепатите В, раке печени и кожи. Источниками селена являются морепродукты, почки, печень, мясо, чеснок, растительное масло, орехи.
Недостаточность цинка в организме человека бывает острой, подострой и хронической. Клинические проявления дефицита цинка обусловлены нарушениями гомеостаза. Из 2-3 г общего количества цинка в организме человека большая часть сосредоточена в костях и коже. Наиболее высокое содержание цинка - в сперме и предстательной железе.
Биологическая роль цинка определяется его необходимостью для нормального роста, развития и полового созревания; поддержания репродуктивной функции и адекватного иммунного статуса; обеспечения нормального кроветворения, вкуса и обоняния, заживления ран. Острая форма дефицита цинка, как правило, возникает у больных, 5-10 нед находящихся на парентеральном питании, и встречается крайне редко. Чаще встречается хронический и особенно подострый дефицит цинка. Наиболее значимыми симптомами гипоцинкоза являются резкое замедление роста, гипогонадизм и выраженная задержка полового развития. Как правило, притупляются вкусовые ощущения, появляются вкусовые извращения, а также снижается порог обоняния.
Первичный гипоцинкоз является следствием недостатка цинка в пище, когда рацион состоит преимущественно из бездрожжевого хлеба, приготовленного из цельной пшеницы. Фитиновые вещества пшеницы и клетчатка, особенно в присутствии кальция, образуют нерастворимый комплекс с цинком, который не всасывается в тонкой кишке. Избыточное содержание в пище антагонистов цинка - меди и кадмия может усиливать дефицит цинка в организме.
Вторичные формы недостаточности цинка в организме связаны с мальабсорбцией или гиперцинкурией. Они возникают у больных сахарным диабетом, при поздних токсикозах беременности и перенашивании плода, тяжелых ожогах (15-53% поверхности тела).
При смешанном питании взрослый человек должен получать с пищей цинк в количестве 12 мг/сут, беременные и кормящие женщины - 15 мг/сут, дети - от 3 до 12 мг/сут. Всасывается только 20-40% поступившего цинка. Основными пищевыми источниками цинка являются мясо, твердые сыры, зернобобовые и некоторые крупы. Много цинка в орехах и креветках.
Недостаточность марганца. В организме взрослого человека содержится 15-20 мг марганца, в основном в головном мозге, печени, почках и поджелудочной железе. Марганец участвует в процессах роста, поддержании репродуктивной функции и остеогенеза, нормального метаболизма соединительной ткани, регуляции липидного и углеводного обмена.
Недостаточность марганца вызывает симптомы гипохолестеринемии, похудание, тошноту и рвоту. В геохимических провинциях с низким содержанием марганца у людей замедляется рост и нарушается формирование скелета (утолщение и укорочение костей нижних конечностей, деформация суставов).
Физиологическая потребность в марганце у взрослых - 2 мг/сут. Марганец содержится в мясных, молочных продуктах, яйцах, рыбе и других продуктах моря. Особенно много марганца в грецких орехах (1,9 мг%), какао и молочном шоколаде (4,6 и 3,1 мг% соответственно). Усвоение марганца из богатых этим элементом злаковых затруднено из-за присутствия фитатов. Чрезвычайно богат марганцем чай, чашка которого содержит 1,3 мкг марганца, но усвоение элемента тормозит танин. Кишечной абсорбции препятствуют также оксалаты, кальций, фосфаты и железо.
Недостаточность кобальта. Клинические симптомы недостаточности кобальта в организме обусловлены в основном нарушениями кроветворения вследствие не столько дефицита самого микроэлемен-
та, сколько недостаточности кобаламина (витамина В12). Соединения кобальта, оказывая гемостимулирующее действие, изменяют и физико-химические свойства эритроцитов. Суточная потребность для взрослых - 10 мкг.
Наибольшие количества кобальта обнаружены в зернобобовых и овощах, но дефицит кобальта может возникнуть при питании преимущественно растительной (вегетарианской) пищей. Источниками кобаламина являются исключительно продукты животного происхождения (см. Витамин В12). Следствием недостаточности может стать анемия Аддисона-Бирмера. К ранним симптомам дефицита кобаламина относятся расстройства менструального цикла, дегенеративные изменения в спинном и костном мозге. Причинами анемии, помимо алиментарной недостаточности микроэлемента, могут быть снижение усвоения кобаламина из-за дефицита мукопротеина, синтезируемого слизистой оболочкой желудка (результат гастрэктомии), и паразитозы.
Фтор неравномерно распределен в различных тканях организма. Его концентрация в зубах составляет 246-560 мг/кг, в костях - 200-490 мг/кг, а в мышцах не превышает 2-3 мг/кг. Имеет значение содержание микроэлемента в суточном рационе, а не в отдельных пищевых продуктах. Суточная потребность во фторе установлена на уровне 4 мг/сут для взрослых и от 1 до 4 мг/сут для детей. Основным источником фтора является питьевая вода, с которой поступает 1-1,5 мг/сут микроэлемента. С пищей поступает 0,25-0,33 мг/сут. В качестве источников фтора можно рассматривать рыбу (особенно треску и сома), орехи и печень. Достаточно много элемента в баранине, телятине и овсяной крупе. Обобщенные величины потребности в микроэлементах представлены в табл. 7.7.
Таблица 7.7. Физиологическая потребность в микроэлементах взрослых (МР 2.3.1.2432-08)
Микроэлементы | Потребность, мг | Микроэлементы | Потребность, мг |
Железо | 10 для мужчин | Селен | 0,055 для женщин |
18 для женщин | 0,07 для мужчин | ||
Медь | 1 | Кремний | 30 |
Марганец | 2 | Хром | 0,05 |
Цинк | 12 | Йод | 0,15 |
Кобальт | 0,01 | Фтор | 4 |
Молибден | 0,07 | Хром | 0,05 |
Недостаточность пищевых волокон
Производство рафинированных пищевых продуктов способствовало росту потребления высокоочищенных от пищевых волокон хлебопродуктов, сахара, растительных масел, мясопродуктов. Такое питание стало одной из важнейших причин распространения так называемых болезней цивилизации, в частности заболеваний сердечно-сосудистой системы, кишечника, диабета, желчнокаменной и почечнокаменной болезней, некоторых форм рака.
Недостаточное потребление клетчатки приводит к развитию дивертикулезной болезни толстой кишки. Заболевание диагностируется у 20% населения в возрасте от 40 лет и у 70% людей старше 70 лет в США и Великобритании. Возникновение заболевания обусловлено продолжительностью транспорта пищи в кишечнике, уменьшением массы стула и сопровождается повышением давления в толстой кишке. При включении в пищевой рацион продуктов, содержащих клетчатку, симптоматика заболевания при неосложненной форме уменьшается, функция кишечника улучшается.
7.6. СОСТОЯНИЕ ЗДОРОВЬЯ ПРИ ИЗБЫТОЧНОМ ПИЩЕВОМ СТАТУСЕ
С избыточным по энергетической ценности или какому-либо пищевому веществу питанием связано распространение атеросклероза, желчнокаменной болезни, ожирения, подагры, сахарного диабета, гипервитаминозов, почечной недостаточности, гиперлипопротеидемии, гиперхолестеринемии, гипергликемии, азотемии, уратемии. Перечисленные выше формы патологии следует рассматривать как мультифакторные, для развития которых необходимо сочетание наследственных факторов с факторами окружающей среды (нерациональное питание, гиподинамия, психоэмоциональный стресс, вредные привычки).
Несбалансированное по энергетической ценности и качественному составу питание приводит к ожирению, которое ассоциируется с факторами риска возникновения гипертензии, атеросклероза, ишемической болезни сердца, инсулинонезависимого сахарного диабета и др. (рис. 7.1).
Избыточное питание в первые месяцы и годы жизни (и даже в эмбриональный период) способствует образованию в подкожных депо
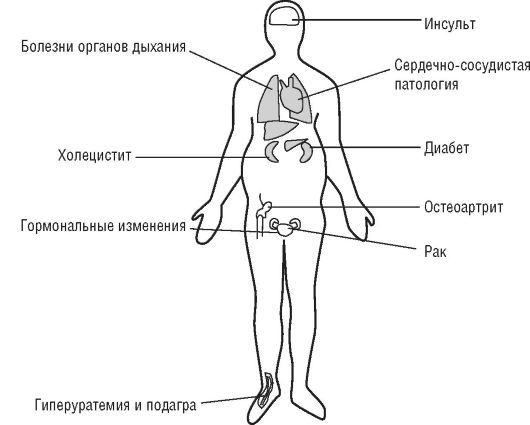 Рис. 7.1. Сопутствующие ожирению заболевания (адаптировано по Campbell I.W., 2007)
Рис. 7.1. Сопутствующие ожирению заболевания (адаптировано по Campbell I.W., 2007)
повышенного количества жировых клеток, в связи с чем на всю жизнь остается предрасположенность к накоплению значительных количеств жира. Возникает особенно устойчивая к лечению гиперцеллюлярная форма ожирения. По мнению К.С. Петровского, жировая ткань весьма активная и даже «агрессивная». «Агрессивность» проявляется неудержимым стремлением образовывать себе подобную ткань во все возрастающих количествах. Этот процесс происходит как при усилении поглощения жира из крови, так и при образовании триглицеридов в результате избыточного поступления углеводов с пищей.
Ожирение - хроническое многофакторное заболевание, развивающееся под влиянием физиологических и генетических факторов и факторов внешней среды. Нарастание МТ в 30-50% случаев зависит от генетического компонента.
Признание ВОЗ ожирения новой «неинфекционной эпидемией» XXI века свидетельствует о появлении новой серьезной угрозы обществен-
ному здоровью. Более 1 млрд людей в мире страдают избыточным весом и ожирением (ВОЗ, 2005). Рост количества тучных людей отмечается не только в странах Америки и Европы, но и в Японии, Китае и Корее, где проблема ожирения еще недавно не была столь актуальной. При сохранении таких высоких темпов роста заболеваемости к 2025 г. ожидается двукратное увеличение числа страдающих ожирением.
В городах России 10-20% мужчин и 30-40% женщин трудоспособного возраста имеют ожирение, т.е. ИМТ > 30 (см. Пищевой статус). В Москве избыточная масса тела отмечается у каждого 4-го мужчины и почти у каждой 2-й женщины в возрасте 35-64 лет.
К числу факторов риска развития ожирения, помимо генетических, относятся внешнесредовые факторы:
• избыточное потребление калорийной пищи, богатой жирами и легкоусвояемыми углеводами, хаотичный режим питания с преобладанием обильного питания в вечернее и ночное время, гипокинезия. Избыток 50 ккал в сутки, источником которых могут быть потребление 1/3 железной баночки кока-колы, горсти чипсов или 25 г мороженого, приводит к увеличению МТ на 2,25 кг в год.
Около трети всех углеводов в диете среднестатистического американца приходится на различные заменители сахара, половину из которых потребитель получает из газированных напитков. Основным подсластителем, входящим в состав большинства прохладительных напитков, является кукурузный сироп, в избытке содержащий фруктозу. В отличие от глюкозы, этот моносахарид не способен стимулировать выработку организмом инсулина, участвующего в метаболизме углеводов, и, кроме того, подавляет выработку лептина, ответственного за чувство насыщения;
• перекармливание грудных детей. По мнению экспертов ВОЗ, идеальный вес для 2-3-летних детей завышен на 15-20%. В этом они видят одну из причин «эпидемии» ожирения у взрослых нынешнего поколения;
• гипокинезия. Риск развития ожирения увеличивается в 2 раза при ежедневном просмотре телевизионных программ 3 часа и более, часто сопровождающегося необоснованным приемом калорийной пищи (например, чипсов) и сладких газированных напитков. Показано, что физическая активность приводит к умеренному повышению энергозатрат и способствует изменению энергетического баланса. Физическая активность уменьшает количество висцерального жира, что чрезвычайно важно для снижения
риска развития сопутствующей патологии и улучшения прогноза жизни;
• недостаток сна. По мнению ученых, повышенный аппетит, развивающийся при нарушениях и недостатке сна, связан с гормональным дисбалансом и потребностью компенсировать нехватку энергии за счет питания;
• влияние так называемых эндокринных дизрапторов - химических соединений, входящих в состав пластмасс и пестицидов. Эти вещества нарушают работу эндокринной системы, регулирующей обмен веществ, что может привести к накоплению жировых отложений;
• широкое распространение кондиционеров. В условиях постоянной комфортной температуры уменьшается расход энергии на функционирование механизмов физической терморегуляции (излучение, испарение, конвекцию);
• рост числа старородящих женщин с избыточной массой тела и избирательное формирование тучных семейных пар, что увеличивает риск формирования у детей изначального избытка жировой ткани и становления злокачественного метаболического синдрома, который в дальнейшем обозначается как «адипозус-генотип».
Основной задачей профилактики ожирения является постепенное изменение неправильного образа жизни пациента, исправление нарушенного пищевого стереотипа, снижение доминирующей роли пищевой мотивации, ликвидация неправильных связей между эмоциональным дискомфортом и приемом пищи. Очень важно выработать в детском возрасте долговременные навыки пищевого поведения и физической активности, которые должны оставаться на всю жизнь.
Лиц с избыточной массой тела надо научить различать низко-, умеренно- и высококалорийные продукты. Продукты, рекомендуемые к потреблению без ограничения, должны обеспечить чувство насыщения (нежирные сорта мяса, рыбы), удовлетворить потребности в сладком (ягоды, чай с сахарозаменителем), создать ощущение наполнения желудка (фрукты, овощи). Рацион питания следует обогащать продуктами с липолитическими свойствами (огурец, ананасы, лимон) и увеличивающими термогенез (зеленый чай, негазированная минеральная вода, морепродукты).
Избыточное поступление пищевых белков также небезразлично для организма, так как вызывает усиленную работу пищеварения, значительную активацию процессов межуточного обмена аминокислот и синтеза мочевины. Усиление экскреции конечных продуктов азотис-
того обмена может привести к функциональному истощению почек. При избыточном поступлении с пищей белков увеличивается развитие гнилостных процессов в кишечнике, что может вызвать интоксикацию продуктами гниения и неполного расщепления белков.
Другие формы болезней избыточного питания часто возникают при использовании пищевых рационов избыточной энергетической ценности, включающих жиры (преимущественно насыщенные) и углеводы (преимущественно легкоусвояемые) в количествах, превышающих физиологические потребности организма (табл. 7.8).
Таблица 7.8. Болезни и синдромы, связанные преимущественно с избыточным питанием (Уголев А.М., 1991)
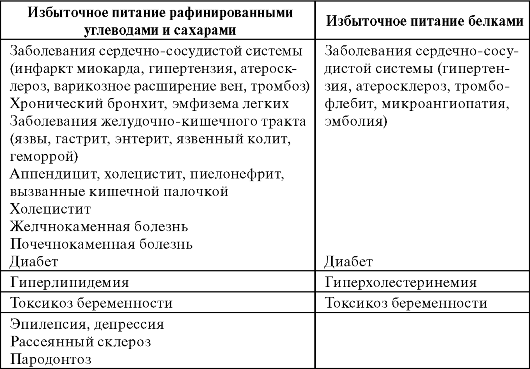 Ожирение
считается самостоятельным фактором риска развития атеросклероза и
ишемической болезни сердца. Кроме того, оно способствует развитию
дислипидемии, артериальной гипертензии, сахарного диабета, которые также
являются факторами риска атеросклероза.
Ожирение
считается самостоятельным фактором риска развития атеросклероза и
ишемической болезни сердца. Кроме того, оно способствует развитию
дислипидемии, артериальной гипертензии, сахарного диабета, которые также
являются факторами риска атеросклероза.
Согласно данным Фремингемского исследования (Framingham Heart Study), у мужчин и женщин в возрасте до 50 лет с избыточной массой тела частота развития сердечно-сосудистых заболеваний возрастает в 2-2,5 раза по сравнению с лицами с нормальной мас-
сой тела. Результаты этого исследования с позиций доказательной медицины (Evidence-based medicine) считаются в настоящее время наиболее достоверными.
Фактором риска развития дислипидемии является нерациональное высококалорийное питание с большим употреблением насыщенных жиров и холестерина. Проведенные в разных странах мира проспективные эпидемиологические исследования на больших группах людей показали, что повышение уровня общего холестерина является независимым фактором риска развития ИБС как у мужчин, так и у женщин.
Повышение уровня холестерина в крови по сравнению с нормой на 10% увеличивает риск развития сердечно-сосудистых заболеваний на 20-30%. При снижении уровня общего холестерина в крови на 10% риск развития ИБС уменьшается у пациентов в возрасте до 40 лет на 50%, 50 лет - на 40%, 60 лет - на 30%, 70-80 лет - на 20%.
В формировании сердечно-сосудистых заболеваний, помимо генетически обусловленных изменений обменных процессов, принимают участие факторы риска, связанные с характером и образом жизни человека. Наиболее убедительные результаты получены в клинических наблюдениях с использованием методов доказательной медицины в отношении ИБС.
При избыточном пищевом статусе с атрибутами нарушений липидного обмена фактором, устранение которого достоверно уменьшает риск развития ИБС, является курение. Составные части табачного дыма (никотин, бензол, оксид углерода, аммиак) вызывают развитие тахикардии, артериальной гипертензии, повышают агрегацию тромбоцитов, усиливают выраженность атеросклеротического процесса, снижают уровень антиатерогенных липопротеинов высокой плотности, повышают содержание фибриногена в крови и способствуют развитию спазма коронарных артерий. Отказ от курения достоверно уменьшает риск развития и прогрессирования ИБС.
С большой вероятностью снижает риск развития ИБС и атеросклероза устранение гиподинамии. Благоприятное действие физической нагрузки объясняется снижением массы тела и артериального давления, улучшением метаболизма глюкозы и снижением уровня атерогенных липидов. С целью первичной профилактики достаточная физическая нагрузка достигается ежедневными физическими упражнениями в течение 30 мин в умеренном темпе. Для вторичной профилактики ИБС двигательная активность подбирается индивидуально.
Клинические исследования влияния алкоголя на риск развития ИБС не проводились. Однако имеются сведения, что эффект воздействия на сердечно-сосудистую систему зависит от дозы алкоголя: чрезмерное употребление алкоголя увеличивает риск общей и сердечно-сосудистой смертности, а употребление умеренных доз алкоголя оказывает протекторный эффект, проявляющийся в повышении уровня липопротеинов высокой плотности (антиатерогенное действие), увеличении фибринолитической активности и снижении агрегации тромбоцитов. Согласно концепции факторов риска, разработанной Американским кардиологическим колледжем (1996), употребление алкоголя является фактором риска, воздействие на который с меньшей вероятностью снижает риск развития ИБС.
К этой же категории факторов риска относится психосоциальный стресс, тип личности (стресс-коронарный профиль). Речь идет о таких чертах и состояниях личности, как гнев, депрессия, ощущение тревоги, агрессивность, чрезмерное тщеславие. Среди психосоциальных факторов следует назвать частые психологические стрессы, отсутствие семейной поддержки, взаимопонимания. Указанные особенности характера и психоэмоциональный стресс сопровождаются высоким выбросом катехоламинов в кровь, что вызывает повышение потребности миокарда в кислороде, увеличивает частоту сердечных сокращений, повышение артериального давления и коагулянтной активности крови.
К факторам риска, которые не могут быть модифицированы, относятся пожилой возраст, мужской пол, семейный анамнез раннего развития ИБС (в частности, инфаркт миокарда). Эти факторы обычно сочетаются с другими факторами риска - артериальной гипертензией, атерогенной дислипидемией, избыточной массой тела и др., что необходимо учитывать при организации мероприятий первичной и вторичной профилактики.
Принципы питания, способствующие предупреждению заболеваний сердечно-сосудистой системы, см. в разделе «Питание пожилых людей и долгожителей».
Гипервитаминозы возникают при употреблении некоторых натуральных продуктов, содержащих исключительно большие количества витаминов, преимущественно жирорастворимых, либо при передозировке витаминных препаратов, особенно у детей.
Гипервитаминоз А. Обычно возникает в случаях длительного приема суточных доз, превышающих физиологические потребности приблизительно в 10 раз. Описанные в литературе случаи гипервитамино-
за А обусловлены в основном употреблением печени птицы, которой в корм в качестве стимуляторов роста добавляли ацетат ретинола.
Гипервитаминоз А проявляется головокружением, головной болью, недомоганием, пересыханием слизистых оболочек и десквамацией эпителия кожных покровов. При значительных дозах отмечаются рвота, диплопия, облысение, спутанность сознания, изменения костной ткани и повреждения печени. Потенциальная токсичность витамина заставляет отказаться от назначения беременным даже терапевтических доз (0,5-1,5 мг/кг) 13-цис-ретиноевой кислоты, так как это существенно увеличивает риск самопроизвольных абортов и врожденных уродств. Гипервитаминоз А вероятен при питании продуктами с повышенным содержанием витамина у алкоголиков и наркоманов, так как возможен синергизм алкоголя, наркотических веществ и ретинола.
Гипервитаминоз D. В больших дозах кальциферол оказывает токсическое действие. В реальных условиях отравления возможны только при случайном использовании фальсифицированных продуктов (растительное масло, предназначенное для корма животных и искусственно обогащенное витамином D). Гипервитаминоз D сопровождается изменением проницаемости клеток для ионов кальция, что проявляется обызвествлением мягких тканей и артерий, а также сморщиванием почек. Предполагают, что отложение кальция в коронарных сосудах у детей при гипервитаминозе D является фактором риска инфаркта миокарда в зрелом возрасте. У наиболее чувствительных к кальциферолу детей явления интоксикации могут возникать при приеме 25-37 мкг витамина в день. Тяжелые формы гипервитаминоза развиваются обычно после приема более 75 мг витамина D.
Одна чайная ложка витаминизированного рыбьего жира содержит 21 мкг витамина D2. Чрезмерный прием витамина детьми может привести к преждевременному окостенению скелета и костей черепа, нарушениям сосудистого тонуса и кардиосклерозу.
Заболевание начинается с изменений функций ЦНС, отмечаются раздражительность, вялость, нарушения сна, затем ухудшается аппетит и появляется потливость. Эти симптомы нередко рассматриваются как активный рахит, что служит поводом к дальнейшему увеличению дозы витамина вместо его отмены. На высоте гипервитаминоза появляются тошнота, рвота, дизурические расстройства, в моче обнаруживаются белок, гиалиновые цилиндры, лейкоцитоз, в крови - снижение гемоглобина и гиперкальциемия. На рентгенограммах часто отмечают изменения костной ткани. Чувствительность детского организма к
токсическим дозам витамина повышают различные интеркуррентные заболевания (экссудативный диатез, гипотрофия), недоношенность, погрешности вскармливания, одновременный прием препаратов кальция, рыбьего жира и ультрафиолетовые лучи.
Гипервитаминоз С. При современном недостаточном использовании в рационах продуктов - носителей аскорбиновой кислоты развитие гипервитаминоза С маловероятно. Причиной гипервитаминоза С может быть систематическое использование больших количеств синтетического витаминного препарата для профилактики простудных заболеваний и гриппа.
Длительный прием аскорбиновой кислоты в дозах более 1 г/сут приводит к активизации симпатико-адреналовой системы и проявляется ощущением беспокойства, бессонницей, ощущением жара, головными болями, повышением артериального давления. При этом увеличивается продукция эстрогенов, что может неблагоприятно сказаться на течении беременности. Избыточное применение аскорбиновой кислоты может вызвать также некротические изменения в поджелудочной железе и способствовать появлению сахара в моче у здоровых людей.
Прием витамина С в дозе 1 г не должен превышать 3 дней и рекомендуется лишь в экстремальных ситуациях, при резком переохлаждении и заболевании гриппом.
7.7. ЗДОРОВОЕ ПИТАНИЕ В ПРОФИЛАКТИКЕ РАКА
Ежегодно в Российской Федерации 300 тыс. человек умирают от рака, а число случаев заболеваний злокачественными новообразованиями постоянно увеличивается.
По современным представлениям, не менее половины случаев рака связано с неправильным питанием, курением и потреблением алкоголя. За возникновение рака считают ответственным чрезмерное употребление жирной пищи при недостаточном количестве белков, овощей и свежих фруктов (табл. 7.9).
Факторы питания в зависимости от их роли в патогенезе рака можно разделить на инициаторы канцерогенеза и коканцерогены и ингибиторы канцерогенеза. Коканцерогенами называются химические вещества, усиливающие действие канцерогенных веществ. Существуют инициаторы, которые превращают нормальные клетки в дремлющие опухолевые, и промоторы - вещества, превращающие дремлющие латентные опухолевые клетки в видимую опухоль.
Таблица 7.9. Причины заболевания раком (Смоляр В.И., 1991)
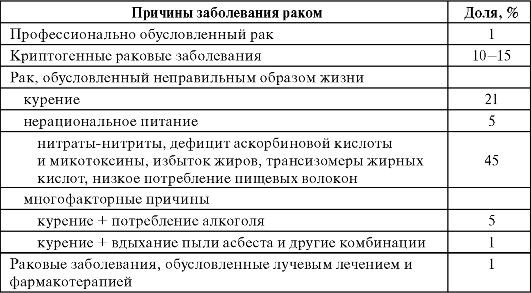 Влияние
избыточного количества жиров на канцерогенез осуществляется,
по-видимому, по типу коканцерогенеза. Конечные продукты окисления и
переокисления ненасыщенных жирных кислот являются сильными мутагенами и
канцерогенами. Трансизомеры жирных кислот снижают активность
цитохромоксидазы, играющей ключевую роль в процессах обезвреживания
канцерогенов.
Влияние
избыточного количества жиров на канцерогенез осуществляется,
по-видимому, по типу коканцерогенеза. Конечные продукты окисления и
переокисления ненасыщенных жирных кислот являются сильными мутагенами и
канцерогенами. Трансизомеры жирных кислот снижают активность
цитохромоксидазы, играющей ключевую роль в процессах обезвреживания
канцерогенов.
Наиболее распространенные локализации рака (толстой и прямой кишки, молочной железы и предстательной железы) чаще встречаются у людей, потребляющих много жиров. Опухоли печени могут возникать при белково-энергетической недостаточности (квашиоркор). Повышенный риск рака толстой и прямой кишки ассоциируется с недостаточным содержанием клетчатки. Избыточное потребление алкоголя связано с риском развития рака полости рта, глотки, гортани, печени. Считается, что алкоголь и продукты горения табака оказывают синергическое канцерогенное действие и стимулируют активность другого фактора канцерогенеза - Helicobacter pylori.
Канцерогенными свойствами обладают и химические вещества, находящиеся в пищевых продуктах. К ним относятся нитрозамины, которые образуются из нитратов и нитритов, поступающих в продукты либо в пищевых цепях, либо в результате технологической обработки мясных и рыбных изделий. Наибольшее количество нит-
розаминов обнаруживается в копченых мясных изделиях, ветчине, мясных консервах, соленой и копченой рыбе.
Канцерогенное действие оказывают токсины плесневых грибов - микотоксины, продуцируемые плесенью при неправильном хранении продуктов. К ним относятся афлатоксины и патулин. Афлатоксины встречаются в арахисе и кукурузе, а патулин - в заплесневелых яблоках, облепихе, а также других фруктах, плодах и овощах, ягодах или соках, джемах, приготовленных из заплесневевших плодов и ягод.
Сильное канцерогенное действие оказывают полициклические ароматические углеводороды. Наиболее изучен 3,4-бенз(а)пирен. Он появляется при копчении домашним способом рыбы и мяса, использовании пережаренных жиров во время кулинарной обработки, а также в результате миграции по пищевым цепям в районах производства сельскохозяйственной продукции с неблагоприятной экологической обстановкой.
Ситуация с определением химических веществ с канцерогенными свойствами постоянно меняется. В 1958 г. в США были запрещены добавки в пищу любых веществ, провоцирующих развитие рака у животных или людей, а 20 лет спустя обнаружили еще 500 канцерогенов. Концентрация этих химических веществ оказалась на 5 порядков ниже той, которая поддавалась определению в 1950-е годы. Следовательно, исходя из беспороговости действия канцерогенов, достичь абсолютной безопасности невозможно даже при условии соблюдения гигиенических нормативов.
Антимутагенными и антиканцерогенными свойствами обладают зеленый и черный чай, кофе, красное вино, пиво, большинство овощей. Ингибиторами процесса канцерогенеза являются витамины и микроэлементы (табл. 7.10).
Длительное время считалось, что β-каротины снижают риск развития рака. Однако исследования последних лет, в том числе эпидемиологические, этого не подтвердили. Более того, представители Международного агентства по исследованию рака указывают на увеличение риска развития рака легких и смертности от сердечнососудистых заболеваний у курильщиков, принимавших добровольно в качестве профилактического средства β-каротин.
Аскорбиновая кислота препятствует образованию канцерогенных нитрозосоединений из нитратов и аминов. Токоферол в качестве антиоксиданта ингибирует процесс канцерогенеза. Антиканцерогенным свойством обладают селен и пищевые волокна.
Таблица 7.10. Природные антиканцерогены
Ингибиторы канцерогенеза | Основные источники |
Аскорбиновая кислота | Овощи, фрукты |
Ароматические изотиоцианаты | Капуста, листовые овощи |
Кумарин, лактоны | Капуста |
Пищевые волокна | Зерновые, фрукты, овощи |
Флавоноиды | Чай, цитрусовые (кожура), шиповник, черноплодная рябина, красный перец, черная смородина, земляника, малина, вишня, облепиха, яблоки, сливы, виноград, бобовые |
Индол | Капуста брокколи, кольраби, цветная капуста, редис, редька |
Фенольные кислоты | Чай, кофе, бобовые, овес, яблоки, картофель |
Протеазные ингибиторы | Бобовые, грецкие орехи |
Соединения селена | Морепродукты, почки, печень, мясо, чеснок, растительное масло, орехи |
α-Токоферол | Растительное масло, зеленый горох, кочанный салат, овес, кукуруза, рожь, пшеничные зародыши, обойная мука, спаржа |
Профилактике рака способствует санитарно-ветеринарный контроль образования нитрозаминов, потребление зелени, овощей и фруктов, разумные ограничения энергетической ценности и жировой составляющей пищевого рациона.
7.8. ПИЩЕВАЯ И БИОЛОГИЧЕСКАЯ ЦЕННОСТЬ ПИЩЕВЫХ ПРОДУКТОВ
Термином пищевая ценность обозначается вся полнота свойств пищевых продуктов, включая обеспечение данным продуктом физиологических потребностей человека в основных пищевых веществах и энергии.
Термином биологическая ценность обозначается степень соответствия аминокислотного состава пищевого белка потребностям организма. Биологическая ценность характеризуется показателем аминокислотного скора.
Качество жировых компонентов пищевых продуктов определяется показателем биологической эффективности, отражающим содержание в них полиненасыщенных жирных кислот.
Характеристику пищевой ценности основных групп сырья и продуктов см. в приложении к главе на электронном носителе.
Функциональные пищевые продукты
Этим термином обозначается широкий круг пищевых продуктов с заданными свойствами, а именно - продукты, обогащенные пищевыми волокнами; пребиотиками (бифидобактерии и другие микроорганизмы, неперевариваемые олигосахариды, отдельные витамины и их производные, биологически активные иммунные белки лактоглобулины и гликопептиды); пробиотиками (микроорганизмы нормальной микрофлоры кишечника и некоторые транзиторные микроорганизмы); антиоксидантами (витамины А, Е, С, β-каротин, селен и др.); минеральными веществами (кальций и др.); микроэлементами (железо, цинк, фтор, йод, селен и др.) и флавоноидами (фитоэстрогены, кварцетины и др.).
Функциональные пищевые продукты относятся именно к пищевым продуктам и не являются фармакологическими средствами. В отличие от клинического применения этих биологически активных веществ (пилюли, капсулы и т.п.) в пищевых продуктах с заданными свойствами они содержатся в пределах физиологических потребностей человека (от 20 до 100% потребностей), в то время как в лечебных целях они применяются в дозах, в 10-100 раз превышающих физиологические потребности.
Основное предназначение функциональных пищевых продуктов - усиление резистентности организма к действию факторов окружающей среды и повышение энергетического обмена человека. Функциональные пищевые продукты обладают выраженным физиологическим эффектом, положительно влияют на состояние структуры и функции организма, улучшают состояние здоровья и продолжительность жизни и/или сокращают риск возникновения болезней, в том числе алиментарно обусловленных.
С физиологических позиций функциональные пищевые продукты оказываются наиболее полезными в следующих направлениях:
• отимизация роста и развития организма;
• стабилизация (нормализация) основных метаболических процессов;
• защита против окислительного стресса;
• влияние на физиологию сердечно-сосудистой системы;
• влияние на деятельность желудочно-кишечного тракта;
• познавательная деятельность и умственная работоспособность;
• физическая работоспособность и фитнес;
• стимуляция иммунитета.
В настоящее время предприятиями пищевой промышленности выпускается достаточно большой ассортимент функциональных пищевых продуктов. На рынке в странах Европейского союза до 25% пищевых продуктов являются функциональными.
Биологически активные добавки
Биологически активные добавки (БАД) - природные (идентичные природным) биологически активные вещества, предназначенные для употребления одновременно с пищей или введения в состав пищевых продуктов.
Биологически активные добавки не отождествляются с пищевыми добавками, которые, также являясь природными соединениями и химическими веществами, сами по себе обычно не употребляются в пищу, но в ограниченных количествах преднамеренно вводятся в продовольственные товары на различных этапах производства, хранения и транспортировки для придания заданных свойств, повышения стойкости продуктов к различным видам порчи, сохранения структуры, внешнего вида и т.д.
БАД подразделяются на 3 группы: нутрицевтики, парафармацевтики и пробиотики.
Нутрицевтики представляют собой эссенциальные нутриенты - природные ингредиенты пищи: витамины и их близкие предшественники (например, β-каротин и другие каротиноиды), полиненасыщенные жирные кислоты (ω-3 и другие ПНЖК), минеральные вещества и микроэлементы (кальций, железо, цинк, йод, селен, фтор), отдельные аминокислоты, некоторые моно- и дисахариды, пищевые волокна.
Использование нутрицевтиков позволяет:
• достаточно легко и быстро ликвидировать дефицит эссенциальных пищевых веществ;
• индивидуализировать питание конкретного здорового человека в соответствии с его потребностями;
• удовлетворить измененные потребности в пищевых веществах у больного человека, а также - по принципу метаболического шунтирования - обойти поврежденное патологическим процессом звено метаболического цикла;
• повысить неспецифическую резистентность организма к действию неблагоприятных факторов среды обитания;
• усилить и ускорить конъюгацию и элиминацию ксенобиотиков из организма;
• активизировать ферментные системы метаболизма ксенобиотиков. С помощью нутрицевтиков осуществляется профилактика ряда
хронических заболеваний, таких как ожирение, атеросклероз, других сердечно-сосудистых заболеваний, злокачественных новообразований и иммунодефицитных состояний.
Наиболее употребляемыми в мировой практике нутрицевтиками являются комплексные витаминно-минеральные БАД, в которые наряду с витаминами включены многие эссенциальные минеральные вещества и микроэлементы в высокоусвояемых, в том числе биотрансформированных, формах. В настоящее время прослеживается тенденция создания БАД, включающих все виды нутрицевтиков, т.е. являющихся источниками белка и энергии, витаминов и минеральных веществ, липидного комплекса, пищевых волокон.
Недавняя публикация в Кохрановской библиотеке (Cochrane Database of Systematic Reviews, 2008) свидетельствует, что профилактическое значение витаминов-антиоксидантов, очевидно, преувеличено. Мета-анализу были подвергнуты 67 случаев рандомизированных клинических наблюдений с общим числом 232 550 человек. 46 проанализированных наблюдений включали 68 111 человек с различными заболеваниями и 21 наблюдение охватывало 164 439 здоровых людей. Все проанализированные случаи сопровождались приемом антиоксидантов (витамина А, бета-каротина, витамина Е, витамина С и селена) в виде пищевых добавок для целей первичной и вторичной профилактики.
Главное заключение авторов исследования: применение пищевых добавок с витаминами-антиоксидантами не приводит к снижению смертности, также не очевидна их польза для целей первичной (здоровых) и вторичной (больных) профилактики. «Кроме того, бетакаротин, витамин А и витамин Е, судя по всему, увеличивают риск преждевременной смерти». В исследовании установлено, что добавленный риск преждевременной смерти от витамина А составляет 16%, бета-каротина - 7%, витамина Е - 4%.
Прием пищевых добавок с витамином С и селеном, по-видимому, не отражается на смертности и, по мнению ученых, нужны дополнительные исследования в отношении их влияния на состояние здоровья.
Парафармацевтики представлены в основном минорными компонентами: органическими кислотами, биофлавоноидами, кофеином, биогенными аминами, регуляторными ди- и олигопептидами, некоторыми олигосахаридами и другими так называемыми натурпродуктами.
Эти вещества получаются из природного сырья и используются для регуляции или стимуляции некоторых функций организма: пищеварительной, выделительной, секреторной и др. Фармакологическая активность минорных веществ позволяет относить их к БАД, если они используются в дозах от 20 до 100% физиологических потребностей человека, регуляция и стимуляция функций организма осуществляется в границах физиологической нормы и если их применяют только орально - с пищей во время еды.
Функционально парафармацевтики выполняют следующую роль:
• регулируют в физиологических границах функциональную активность органов и систем;
• нормализуют деятельность нервной системы;
• поддерживают нормальную микрофлору ЖКТ;
• проявляют адаптогенный эффект к экстремальным условиям внешней среды.
Минорные компоненты пищи, содержащиеся в растениях, употребляемых в пищу (овощи, бобовые, фрукты, ягоды) и не употребляемых в пищу (лекарственные растения), обладают хемопротекторными и хемопревенторными свойствами. Например, биофлавоноиды участвуют в поддержании нормальной проницаемости и структуры кровеносных сосудов, предупреждают развитие склероза. Эти соединения, обладая спазмолитическим действием на гладкую мускулатуру кровеносных сосудов, способствуют нормализации артериального давления, а также проявляют противоотечное и антиоксидантное действие. Биофлавоноиды обладают также противовоспалительным и антиаллергическим действием, регулируют активность ферментов метаболизма ксенобиотиков. Доказанная физиологическая активность биофлавоноидов позволяет отнести пищевые продукты с их высоким содержанием к разряду функциональных.
Другие фенольные соединения, присутствующие в пищевых продуктах, могут оказывать антимикробное, адаптогенное, тонизирующее, спазмолитическое, диуретическое, седативное, желчегонное, кровоостанавливающее, гипотензивное действие.
Выраженной физиологической активностью обладают сапонины и фитостеролы. Сходство структуры фитостеролов с холестери-
ном позволяет использовать продукты с их высоким содержанием (растения и морепродукты) для конкурентного снижения уровня свободного и связанного с атерогенными липопротеинами низкой плотности холестерина.
Таким образом, БАД-парафармацевтики могут использоваться как для первичной, так и для вторичной профилактики.
Пробиотики и пребиотики. Пробиотиками называются живые микроорганизмы или продукты их жизнедеятельности, которые регулируют деятельность желудочно-кишечного тракта. К ним относятся бактерии, входящие в состав нормальной микрофлоры ЖКТ: постоянные обитатели кишечника - бифидобактерии и молочнокислые микроорганизмы рода Lactobacillus и транзиторные микроорганизмы - молочнокислые палочки и кокки, грамположительные пропионбактерии Bacillus, грамотрицательные Echerechia coli, другие бактерии, дрожжи, грибы.
Пробиотики играют функциональную роль:
• оптимизация пищеварения и моторной деятельности кишечника;
• антогонизм в отношении условно-патогенных и патогенных микроорганизмов: бактерий, вирусов, грибов и дрожжей;
• устранение дисбиозов и дисбактериозов;
• продукция витаминов К, биотина, ниацина, пиридоксина, фолиевой кислоты;
• гидролиз желчных кислот и регуляция уровня холестерина;
• участие в рециркуляции женских половых гормонов;
• детоксикация и защита от ксенобиотиков, канцерогенов, эндогенных токсических субстратов, непривычной и экзотической пищи;
• участие в морфогенезе и функционировании иммунокомпетентных тканей в качестве носителей иммуногенов и защитных антигенов.
Пищевые продукты и БАД могут содержать микроорганизмы в виде чистых монокультур или в комбинациях до 6-8 пробиотиков и более.
Пребиотики выполняют роль промоторов пробиотиков. К ним относятся вещества или диетические добавки, которые не усваиваются в кишечнике, но активно стимулируют рост и метаболизм пробиотиков. К группе пребиотиков относятся:
• бифидобактерии;
• неперевариваемые олигосахариды - коротко- и среднецепочные олигомеры из остатков фруктозы, глюкозы, галактозы, а также олигосахариды;
• отдельные витамины и их производные, селективно стимулирующие рост бифидобактерий (пантотеновая кислота, пантетин, S- сульфопантетеин);
• биологически активные иммунные белки - лактоглобулины и гликопептиды.
Для коррекции пищевого статуса естественным способом получения пробиотиков является использование в питании молочнокислых продуктов с использованием различных микроорганизмов в качестве заквасок или стартерных культур.
Генетически модифицированные продукты
Генная инженерия представляет собой совокупность методов и технологий, в том числе технологий получения рекомбинантных рибонуклеиновых и дезоксирибонуклеиновых кислот, по выделению генов из организма, осуществлению манипуляций с генами и введению их в другие организмы. Трансгенными организмами являются животные, растения, микроорганизмы, вирусы, генетическая программа которых изменена с использованием методов генной инженерии. Эта технология в настоящее время широко применяется для создания высокоурожайных сортов, обладающих более высокими показателями пищевой ценности (рис. 7.2). Параллельно решается задача более стабильного обеспечения населения доступным по стоимости продовольствием.
К началу XXI века во всем мире официально зарегистрировано более 1700 мутантных сортов растений, среди которых доминируют хлебные злаки (рис, ячмень, пшеница, кукуруза, пшеница твердых сортов), а также соя.
Создание генетически модифицированных продуктов является ускоренной селекцией генетических свойств растений, отличающейся от традиционных способов селекции значительным сокращением времени и более прогнозируемыми результатами. Основными свойствами, ради которых выводятся новые сорта растений, являются низкорослость, холодо- и жароустойчивость, солеустойчивость, резистентность к гербицидам и болезням. Приобретение растениями этих свойств позволяет снизить химическую нагрузку пестицидами и инсектицидами на сельскохозяйственные угодья в процессе выращивания урожая и вредное воздействие ядохимикатов на работников сельского хозяйства, а также уменьшить содержание остаточных количеств пестицидов в пищевых продуктах.
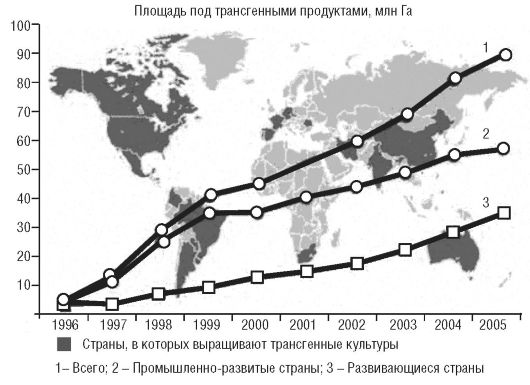 Рис. 7.2. Динамика производства трансгенных сельскохозяйственных культур (Образцов П., Елдышев Ю., 2006)
Рис. 7.2. Динамика производства трансгенных сельскохозяйственных культур (Образцов П., Елдышев Ю., 2006)
Большинство генетически модифицированных культур, используемых на продовольственном рынке, обладают такими свойствами, как высокая урожайность, облегчение уборки, переработки и хранения урожая. Перспективным направлением применения технологии генетической модификации пищевых продуктов является улучшение показателей пищевой ценности, таких как устранение или снижение уровней антинутриентов, токсинов и аллергенов; введение или повышение уровней биологически активных веществ; изменение соотношения витаминов и минеральных веществ.
В соответствии с рекомендациями ВОЗ, директивами Европейского союза, законодательством Российской Федерации пищевая продукция из генетически модифицированных организмов относится к категории «новой пищи» и на основании этого подлежит обязательной оценке на безопасность и последующему мониторингу за оборотом. Пищевые продукты, полученные из генетически модифицированных организмов, прошедшие санитарно-эпидемиологическую
экспертизу и не отличающиеся по полученным свойствам от своих аналогов, полученных традиционными методами, являются безопасными для здоровья человека и могут применяться без ограничений при
организации питания и в производстве пищевых продуктов в пищевой промышленности.
По СанПиН 2.3.2.1078-01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов» маркировка генетически модифицированных источников пищи является обязательной. Маркировке подлежат все пищевые продукты, содержащие в своем составе более 0,9% генетически модифицированных компонентов. К таким продуктам относятся все продукты, содержащие соевый белок, продукты из кукурузы, томатов, картофеля, кабачков, дыни, папайи, цикорий, пищевые добавки и биологически активные добавки к пище с ГМ-компонентами.
В РФ зарегистрированы без ограничений в применении 3 сорта сои, 7 сортов кукурузы, 4 сорта картофеля, 1 сорт сахарной свеклы, 1 сорт риса, а также 5 видов генетически модифицированных микроорганизмов.
Не требуется нанесение на потребительскую этикетку сведений о применении технологии генетической модификации для продуктов из этого сырья, не содержащих ДНК и белка (табл. 7.11).
Таблица 7.11. Пищевые продукты, полученные из генетически модифицированных организмов, не требующие маркировки на содержание ГМП
Продовольственное сырье | Пищевые продукты |
Соя | Соевое масло рафинированное; соевый лецитин; фруктоза |
Кукуруза | Кукурузное масло рафинированное; кукурузный крахмал; мальтодекстрины; сиропы из кукурузного крахмала; глюкоза; фруктоза; патока и другие олигосахара |
Сахарная свекла | Сахар; глюкоза; фруктоза |
Картофель | Картофельный крахмал; глюкоза; патока и другие олигосахара |
Рапс | Рапсовое масло и продукты, его содержащие |
Лен | Льняное масло и продукты, его содержащие |
Хлопок | Хлопковое масло и продукты, его содержащие |
Содержание в пищевых продуктах 0,9% и менее компонентов, полученных с применением генетически модифицированных организмов, является случайной или технически неустранимой примесью, и такие продукты не считаются полученными с применением ГМО.
В 2008 г. в России введена новая маркировка пищевых продуктов, содержащих генно-модифицированные микроорганизмы (ГММ). На этикетках продуктов, содержащих живые ГММ, должно быть написано: «Продукт содержит живые генно-инженерно-модифицированные микроорганизмы», а на этикетках продуктов с нежизнеспособными ГММ: «Продукт получен с использованием генно-инженерно-модифицированных микроорганизмов».
7.9. БЕЗОПАСНОСТЬ ПИЩЕВЫХ ПРОДУКТОВ
Под безопасностью пищевых продуктов понимается отсутствие токсического, канцерогенного, мутагенного или иного неблагоприятного действия продуктов на организм человека при употреблении их в общепринятых количествах.
Пищевые инфекции и инвазии
Через пищу распространяются возбудители эндогенных инфекционных заболеваний животных, которые при определенных условиях могут передаваться человеку (зоонозы), и микроорганизмы, широко распространенные в окружающей среде, которые способны вызвать инфекционные заболевания. От больных животных могут передаваться туберкулез, бруцеллез, ящур, иерсиниозы и другие инфекции, а также гельминтозы. От больного человека или бактерионосителя, а также при контакте с объектами окружающей среды, загрязненных выделениями больных и носителей, возможно алиментарное заражение брюшным тифом, дизентерией и другими инфекционными заболеваниями. В 2007 г., по статистике ВОЗ, наиболее частыми инфекционными заболеваниями, передающимися с пищевыми продуктами, были сальмонеллез, кампилобактериоз, листериоз и заражения энтерогеморрагическими штаммами E. coli O157.
Источниками сальмонелл являются домашние и дикие животные, а также птица, особенно водоплавающая, и яйца. Инфицирование мяса может быть прижизненным, а также в результате неправильного забоя скота, разделки туши, нарушения условий хранения, транспортировки и кулинарной обработки сырья (схема 7.3).
В контексте рекомендаций по увеличению в структуре питания количества свежих овощей, зелени, фруктов и ягод эксперты ФАО/ВОЗ (Meeting Report 26, 2008) указывают на микробиологические риски при использовании в сыром виде листовой зелени, томатов, бахчевых, зеленого лука, капусты, проросших зерен, зерновых и корнеплодов от широкого спектра патогенных микроорганизмов, таких как: энтерогеморрагические штаммы Escherichia coli, Salmonella enteritidis, Shigella, Yersinia pseudotuberculosis, вирусы гепатита А, norovirus, Cyclospora cayatenensis, Cryptosporidium parvum.
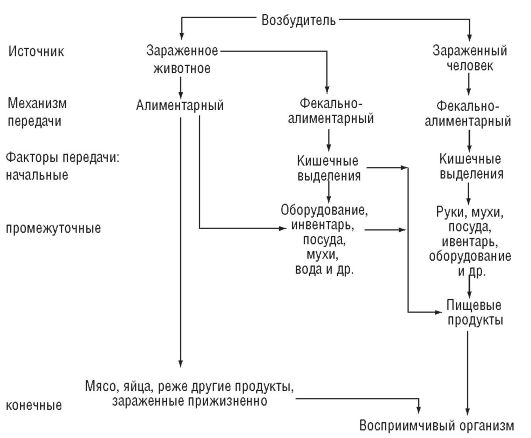 Схема 7.3. Источник, механизмы и факторы передачи возбудителей кишечных сальмонеллезов (по К. С. Петровскому)
Схема 7.3. Источник, механизмы и факторы передачи возбудителей кишечных сальмонеллезов (по К. С. Петровскому)
Причиной глистных инвазий является употребление в пищу мяса, зараженного личинками ленточных паразитов Taeniarinchus saginatus и Taenia solium, нематодой Trichinella spiralis и эхинококком (E. granulosus, E. sibiricensis). Рыба может стать причиной заражения человека дифил-
лоботриозом (Diphyllobothrium latum, D. tungussicum, D. skrasbini, D. minus, D. strictum), описторхозом (Opistorchis felineus), другими глистными инвазиями.
На территории РФ зарегистрировано 52 вида гельминтов: 24 вида нематод, 19 - цестод и 9 - трематод. Из них 24 являются патогенными для человека.
В распространении паразитозов по пищевой цепи имеют значение:
• географический фактор - различное распространение гельминтов в разных географических зонах, обусловленное температурой, влажностью, характером почвы и растительностью, а также наличием и распространенностью промежуточных хозяев;
• условия быта и некоторые традиции и привычки: употребление в пищу строганины из мяса и некоторых сортов рыбы, недостаточно прожаренного или проваренного мяса, рыбы, жареной на вертеле, свежепосоленной щучьей икры. Эти привычки в питании способствует заражению цепнем бычьим от говядины, цепнем свиным и трихинеллами - от свиного мяса, разными видами дифиллоботриид и некоторыми трематодами - от определенных видов рыб. Удобрение огородов необезвреженными фекалиями ведет к распространению аскаридоза и трихоцефалеза.
Пищевые отравления
Пищевые отравления - острые, редко - хронические заболевания, возникающие в результате употребления пищи, массивно обсемененной микроорганизмами определенного вида или содержащей токсичные для организма вещества микробной или немикробной природы.
Пищевые отравления объединяются рядом признаков:
• внезапное острое начало с коротким инкубационным периодом;
• каждый случай пищевого отравления связан с употреблением какого-то одного вида пищевого продукта;
• вне зависимости от этиологии пищевые отравления не передаются от больного человека здоровому.
К пищевым отравлениям не относятся заболевания, вызванные преднамеренным введением в пищу какого-либо яда с целью убийства, самоубийства, алкогольное опьянение. Не являются пищевыми отравлениями случаи ошибочного использования в быту какоголибо ядовитого вещества вместо пищевого, пищевые аллергии и гипервитаминозы.
Пищевые отравления микробной этиологии и их профилактика
Биологические контаминанты пищи являются наиболее часто встречающейся в практике причиной пищевых отравлений, имеющих вид либо токсикоинфекций, либо интоксикаций. В первом случае продукты массивно обсеменены микроорганизмами, во втором случае в пище находятся токсины - продукты жизнедеятельности микроорганизмов. Возможны случаи массовых вспышек пищевых отравлений, если пораженный продукт употребляется группами людей, например на предприятиях общественного питания, либо единичные (семейные) случаи, когда в качестве пострадавших выступает одна семья или один человек.
Пищевые отравления бактериальной этиологии, как правило, протекают остро с коротким инкубационным периодом и бурной клинической картиной поражения различных отделов желудочнокишечного тракта и даже систем жизнеобеспечения (сердечно-сосудистой, нервной) (табл. 7.12).
Таблица 7.12. Выраженность клинических симптомов при некоторых пищевых отравлениях микробной этиологии (Петровский К.С. , 1982)
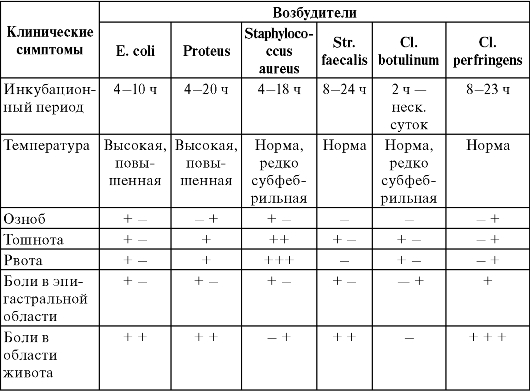
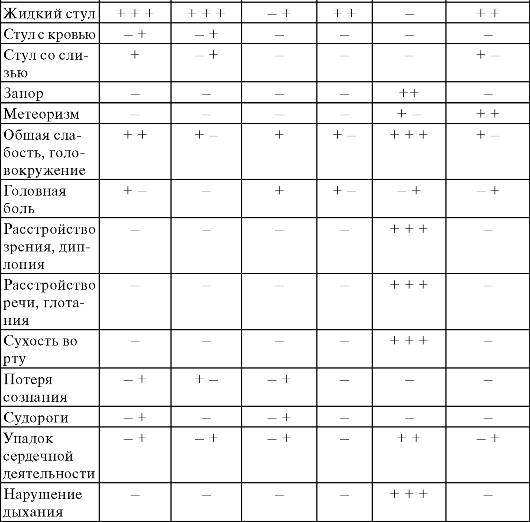 Условные
обозначения, принятые в таблице: +++ симптомы выражены резко; ++
симптомы выражены сильно; +- симптомы наблюдаются редко; -+ симптомы
наблюдаются очень редко; - симптомы не наблюдаются.
Условные
обозначения, принятые в таблице: +++ симптомы выражены резко; ++
симптомы выражены сильно; +- симптомы наблюдаются редко; -+ симптомы
наблюдаются очень редко; - симптомы не наблюдаются.
Пищевые токсикоинфекции
Пищевые токсикоинфекции распространены повсеместно. Восприимчивость к заболеваниям очень высока. Как правило, забо-
леваемость повышается в теплое время года, когда из-за нарушений правил хранения и сроков реализации пищевых продуктов создаются благоприятные условия для быстрого и массивного обсеменения микроорганизмами. Источником возбудителей могут быть животные и люди. Механизм передачи заболевания - фекально-оральный. Путь передачи - пищевой.
Заболевания вызываются разными микроорганизмами, которые могут размножаться на пищевых продуктах. Наиболее распространенными являются Proteus vulgaris, P. mirabilis, S. faecalis, B. cereus, C. perfringens, бактерии родов Hafnia, Klebsiella, Pseudomonas, Vibrio (V. parahaemolyticus).
Основным условием возникновения заболевания является массивное обсеменение пищевых продуктов. В результате гибели возбудителей в желудочно-кишечном тракте высвобождаются эндотоксины - липополисахариды, содержащиеся в клеточной стенке бактерий. Видовые особенности микроорганизмов мало отражаются на особенностях патогенеза и клинической картине, поэтому ответ организма стереотипен: развиваются как местные процессы в желудочно-кишечном тракте (воспаление, дисбактериоз, нарушение моторики), так и общетоксические проявления (головная боль, подъем температуры, нарушение деятельности сердечно-сосудистой и нервной систем).
Пищевым токсикоинфекциям свойственны внезапное развитие заболевания (вспышки) при коротком инкубационном периоде (6-24 ч) почти одновременно у всех потреблявших одну и ту же пищу; связь заболевания с приемом пищи, приготовленной или реализованной при тех или иных санитарных нарушениях; территориальная ограниченность заболевания, обусловленная ареалом реализации загрязненного микроорганизмами продукта (не обязательна в крупных урбанизированных центрах с выраженными миграционными потоками населения в течение рабочего дня); быстрое прекращение вспышки после изъятия опасного продукта.
Пищевые интоксикации
К пищевым интоксикациям относятся ботулизм и стафилококковая интоксикация, возникающие при употреблении пищи, загрязненной микробными токсинами. К возникновению пищевых интоксикаций приводят все условия, которые способствуют токсинообразованию.
Стафилококковые интоксикации. Возникновение заболевания обусловлено энтеротоксинами золотистого стафилококка (S. aureus).
Источниками микроорганизмов являются люди, работающие на пищевых предприятиях и имеющие гнойную инфекцию стафилококковой этиологии (фурункулы, панариции, ангины, нагноившиеся раны и ожоги и др.), резидентные носители золотистых стафилококков, больные маститом животные (козы, коровы).
Стафилококковые интоксикации чаще возникают при использовании в питании обсемененного стафилококком молока и молочных продуктов (крем, сметана, творог, мороженое, а также сыр и брынза). Кроме молочных продуктов, стафилококки размножаются и образуют токсины в готовых мясных и рыбных блюдах, особенно приготовленных из фарша.
Профилактику стафилококковых интоксикаций обеспечивают ветеринарно-санитарный надзор на молочных фермах, строгое соблюдение санитарно-противоэпидемических мероприятий на предприятиях общественного питания, соблюдение правил хранения и реализации готовой продукции.
Ботулизм. Это тяжелый пищевой токсикоз, развивающийся после короткого (2-12 ч) инкубационного периода в результате употребления продуктов, содержащих токсины возбудителя Cl. botulinum.
В клинической картине преобладают офтальмоплегический и бульбарный синдромы (см. табл. 7.12).
Ботулинический токсин - наиболее сильный из известных биологических ядов. При кипячении разрушается в течение 10 мин. Может продуцироваться микроорганизмами в любых продуктах, имеющих анаэробные условия (овощные, грибные, рыбные, мясные консервы, прежде всего домашнего приготовления). Споры устойчивы к кипячению, низкой температуре, различным видам консервирования.
Профилактика ботулизма заключается в соблюдении санитарных правил на рыбных промыслах и бойнях при разделке туш, технологии консервирования и условий хранения консервов. Важным мероприятием по профилактике ботулизма является просветительная работа среди населения по технологии приготовления домашних консервов.
Основные принципы профилактики пищевых отравлений микробной этиологии:
• Изоляция источника возбудителя инфекции. С этой целью необходимы: - своевременное выявление среди работников предприятий питания не только больных с клинически выраженными формами
заболеваний, но и носителей патогенных серотипов микроорганизмов с отстранением от работы в контакте с пищевыми продуктами и санацией; - тщательный ветеринарно-санитарный контроль за состоянием здоровья животных и птицы на сельскохозяйственных фермах с целью выявления больных и носителей (см. также «Гигиенические основы организации лечебного питания»).
• Прерывание путей обсеменения пищевых продуктов возбудителями пищевых отравлений. Соблюдение правил забоя скота, птицы, обработки рыбы и полуфабрикатов, условий транспортировки, соблюдения технологии приготовления пищи на предприятиях питания, контроль за состоянием здоровья персонала пищеблоков.
• Предупреждение размножения микроорганизмов и токсинообразования. Соблюдение условий хранения, консервирования и сроков реализации готовой продукции.
• Утилизация (уничтожение) потенциально опасных в эпидемическом отношении продуктов.
Пищевые микотоксикозы
Пищевые микотоксикозы развиваются в результате употребления в пищу продуктов переработки зерновых и бобовых культур (кукуруза, злаковые, рис, арахис, горох), содержащих токсичные вещества определенных видов микроскопических грибов. Инкубационный период и интенсивность клинических симптомов зависят от свойств грибов, концентрации токсина в продукте и абсорбированной дозы.
Эрготизм вызывается употреблением в пищу зерновых (рожь, реже пшеница), пораженных склероциями гриба Claviceps purpurea.
Действующим токсическим началом при отравлении являются алкалоиды спорыньи, концентрация которых зависит от погодных условий и практически не снижается при выпечке хлеба из загрязненной муки. Клиническая симптоматика обусловлена блокадой адренергических систем организма.
В настоящее время случаи возникновения эрготизма крайне редки.
К фузариотоксикозам относят отравления при использовании в пищу зерновых, пораженных грибами рода Fusarium, почти все разновидности которого токсичны для человека. Развитие грибов рода Fusarium на зерновых происходит при высокой температуре и относительной влажности воздуха. К фузариотоксикозам относятся отравления «пьяным хлебом» и алиментарно-токсическая алейкия.
Отравление «пьяным хлебом» обусловлено заражением зерновых грибом Fusarium graminearum. Даже в случае однократного употребления хлеба, содержащего токсины этого гриба, проявляются симптомы, характерные для тяжелого алкогольного опьянения.
Алиментарно-токсическая алейкия встречается при употреблении в пищу хлеба, приготовленного из перезимовавшего в поле зерна (просо, пшеница, рожь, ячмень, овес). Действующим токсическим началом отравления является токсин грибов Fusarium sporotrichella. Болезнь развивается через 1-2 нед после употребления хлеба, выпеченного из муки, содержащей токсины. Главным признаком заболевания является некротическая ангина, развивающаяся при явлениях алейкии, снижении количества гранулоцитов и гемоглобина, лимфоцитозе. Единственная мера профилактики - не допускать применения в питании муки из перезимовавшего зерна.
Афлатоксикоз. Афлатоксины являются высокотоксичными вторичными метаболитами микроскопических грибов Aspergillus flavus Link ex Fries, которые образуются на различных пищевых продуктах, пищевом сырье и кормах практически повсеместно, наиболее часто и в наибольших количествах на арахисе, кукурузе, семенах хлопчатника.
Афлатоксины являются одними из наиболее сильных гепатотропных ядов, обладающих также выраженной способностью вызывать отдаленные последствия, в том числе канцерогенный эффект. Для афлатоксинов доказаны мутагенная активность, цитотоксическое действие, влияние на нервную систему, иммунотоксичность, влияние на репродуктивную функцию, тератогенная активность.
Токсические свойства афлатоксинов усиливаются при питании с недостаточным количеством белка, полиненасыщенных жирных кислот, витамина А, холекальциферола и при употреблении этилового спирта.
Профилактика микотоксикозов включает борьбу с сельскохозяйственными вредителями и гигиенический мониторинг уровня загрязнения сырья и пищевых продуктов.
Пищевые отравления немикробной этиологии
Немикробные отравления продуктами, ядовитыми по своей природе или становящимися ядовитыми при определенных условиях
Такие отравления нечасто встречаются в клинической практике, но имеют широкий диапазон этиологических факторов, разнообразную картину патогенетических механизмов и тяжелые клинические
проявления. Отравления зоотоксинами или растительными ядами возникают при употреблении в пищу незнакомых животных (как правило, морских рыб) или растений.
Отравления ядами животного происхождения возможно при употреблении печени и мяса ядовитых акул. Отравления скумбриевыми рыбами (тунец, пеламида, ставрида, макрель) объясняется высоким содержанием в мясе этих рыб гистидина, который при нарушении условий и сроков хранения превращается в активное гистаминоподобное вещество заурин.
От растительных ядов наиболее часто страдают дети, которых привлекают красивый вид и яркий цвет ягод и растений. Возможно отравление настойками и отварами из трав с целью самолечения.
К наиболее распространенным ядовитым растениям на территории Российской Федерации относятся:
• растения, вызывающие преимущественно поражение нервной системы: аконит (борец, голубой лютик, иссык-кульский корень); белена; белладонна (красавка); болиголов пятнистый; вех ядовитый (цикута, водяной болиголов, водяной омег); дурман; конопля индийская; чина посевная; чистотел; чилибуха (рвотный орех);
• растения, вызывающие преимущественно поражения желудочно-кишечного тракта: безвременник, волчье лыко, клещевина (турецкая конопля, касторка), крушина, молочай, паслен;
• растения, вызывающие преимущественно поражение сердца: ландыш, наперстянка, чемерица;
'растения, вызывающие преимущественно поражение печени: гелиотроп, горчак розовый, крестовник.
Профилактика острых отравлений включает гигиеническое воспитание и обучение населения, в частности детей в детских садах и школах.
Отравления грибами
Массовые отравления грибами (в том числе со смертельным исходом) в Российской Федерации приходятся на 3-ю декаду июля - начало октября. Причиной отравления обычно становится употребление ядовитых грибов вместо съедобных. Более 90% отравлений со смертельным исходом приходится на долю бледной поганки (Amanita phalloides), возможно отравление ложными опенками и строчками.
При отравлении грибами различают: 1. Желудочно-кишечный синдром (острый гастроэнтерит), вызываемый практически всеми ядовитыми и условно-ядовитыми гриба-
ми при их неправильной кулинарной обработке вследствие раздражающего действия грибных пептидов на слизистую оболочку желудочно-кишечного тракта.
2. Печеночный синдром, чаще называемый фаллоидиновым, так как вызывается α-, β-, δ- и σ-аманитинами бледной поганки (Amanita phalloides).
3. Почечный синдром, обусловленный содержащимся в ядовитых грибах токсином ореланином.
4. Психоневрологический (мозговой) синдром при действии нейротоксинов псилоцибина, гирометрина, атропина и др. Отравления не связаны с массовыми мутациями грибов из съедобных в ядовитые и, скорее, вызваны ошибочным сбором ядовитых двойников съедобных грибов.
Грибы, собранные в экологически неблагополучных районах с интенсивно развитой промышленностью и сетью автодорог, могут накапливать ксенобиотики и должны рассматриваться в этом случае как причина отравлений химической этиологии, а не как вариант грибной интоксикации.
Профилактика массовых отравлений грибами должна строиться на активной воспитательной работе среди населения.
Отравления химическими веществами антропогенного происхождения
Из загрязненных в результате хозяйственной деятельности объектов окружающей среды по пищевым (трофическим) цепям различных экосистем в организм человека поступают чужеродные химические вещества (ксенобиотики). Считается, что из ядов, регулярно попадающих в организм человека, около 70% поступают с пищей, 20% - из воздуха и 10% - с водой.
Механизмы биотрансформации ксенобиотиков в наземной и водной трофических цепях существенно различаются. Защитные (антидотные) механизмы у теплокровных наземных животных при однократном поступлении загрязнителя способствуют снижению его концентрации в каждом звене наземной трофической цепи. Однако вредные вещества способны накапливаться в организме (материальная кумуляция) при хроническом поступлении с пищевыми продуктами.
При миграции ксенобиотиков по водным пищевым цепям они не подвергаются процессам биотрансформации во внутренней среде, и в каждом последующем звене концентрация вредных веществ увеличивается. Так, непосредственно из водной среды планктон извлекает
остатки растворенных или взвешенных пестицидов и происходит 10-кратное увеличение их концентрации в микроорганизмах. При утилизации планктона дафниями и мелкими ракообразными происходит дальнейшее 50-кратное увеличение концентрации ксенобиотиков. В организме мелких рыб, питающихся ракообразными, увеличение составляет 5 раз, в крупных хищных рыбах - в 2 раза и в организме птиц, питающихся рыбой, - еще в 25 раз. В результате концентрация хлорорганических пестицидов в тканях щуки увеличивается в 26 тыс. раз, а в тканях бакланов, питающихся рыбой, в том числе и щуками, - в 528 тыс. раз.
Путь ксенобиотиков от источников эмиссии до органа-мишени представлен на схеме 7.4.
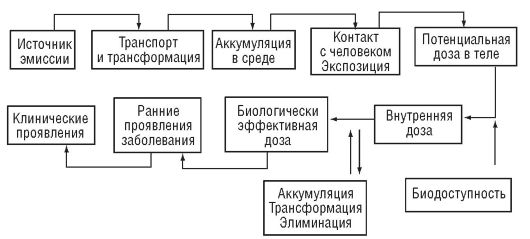 Схема 7.4. Схема воздействия контаминанта на здоровье человека
Схема 7.4. Схема воздействия контаминанта на здоровье человека
Среди ксенобиотиков, поступающих алиментарным путем, для человека опасны пестициды, тяжелые металлы, полихлорированные и полибромированные углеводороды, нитраты и нитриты.
Отравления пестицидами
Пестициды (ядохимикаты) представляют собой основное ядро ксенобиотиков, поступающих в организм человека алиментарным путем. Их химический состав разнообразен и представлен соединениями 12 классов. Наиболее распространены хлорорганические (типа гексахлорциклогексана), фосфорорганические (типа метафоса, хлорофоса), карбоматы (типа севина), ртутьорганические (типа гранозана). На территории Российской Федерации разрешены к применению в сельском хозяйстве 66 различных пестицидов. Помимо специфического действия
на сельскохозяйственных вредителей, они отличаются неблагоприятными отдаленными последствиями (тератогенным, эмбриотоксическим, гонадотропным, канцерогенным и др.). Эпидемиологическими исследованиями установлена прямая корреляционная связь между ухудшением состояния здоровья сельского населения (особенно детей) и территориальными нагрузками пестицидами.
Для диагностики пищевого отравления пестицидами необходимо знать конкретную номенклатуру применяемых в районе пестицидов, их токсикологические характеристики, патогенетические механизмы интоксикаций и клинические симптомы отравления. Основными причинами отравлений ядохимикатами являются нарушения правил обработки растений, вследствие чего остаточные количества пестицидов в продукции растениеводства превышают максимально допустимые уровни (МДУ).
Пищевые отравления пестицидами обусловлены их высокой токсичностью, устойчивостью во внешней среде, в том числе в почве, воде и пищевых продуктах, выраженными кумулятивными свойствами, способностью накапливаться в некоторых системах и тканях, достигая значительных концентраций, длительным пребыванием в организме (большой период полувыведения), способностью проникать в молоко кормящих матерей, а также образовывать стойкие масляные эмульсии и длительно сохраняться в этих эмульсиях при обработке овощей и фруктов.
Профилактика хронических отравлений пестицидами базируется на строгом соблюдении агротехнических приемов использования пестицидов с учетом их токсикологических характеристик и контроле содержания остаточных количеств пестицидов в пищевых продуктах. Использование продуктов с содержанием остаточных количеств пестицидов, превышающих МДУ, запрещается.
На здоровье населения могут влиять и примеси, содержащиеся в пестицидах. К таким наиболее токсичным примесям относятся диоксины, которые в качестве трудно отделимого побочного продукта и в незначительных количествах содержатся в препаратах трихлорфеноксиуксусной кислоты (2,4,5-Т). Источниками загрязнения объектов окружающей среды диоксинами являются также целлюлозно-бумажные комбинаты, мусоросжигательные технологии. Опасность диоксинов заключается в чрезвычайно высокой мутагенной активности и канцерогенном действии. Около 90% диоксинов, поступающих в организм человека, ассоциируются с загрязнением пищевых продуктов (ВОЗ, 2007).
Отравления тяжелыми металлами, полихлорированными и полибромированными углеводородами
Болезнь Минамата впервые была официально зарегистрирована в 1956 г. у людей, проживающих около залива Минамата в юго-западной части Японии. В 1959 г. было доказано, что это заболевание связано с употреблением рыбы, загрязненной ртутью. Ртуть поступала в морской залив со сточными водами химического завода по производству ацетальдегида и поливинилхлорида. В морской воде и в водных организмах неорганическая ртуть в результате метилирования переходила в метилртуть (рис. 7.3).
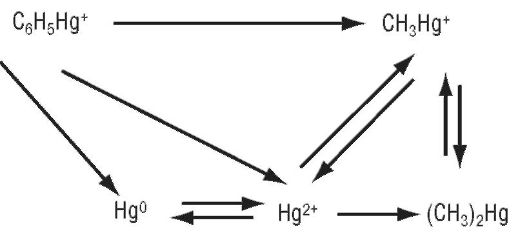 Рис. 7.3. Упрощенная схема превращений ртути в воде (W. Eichler, 1993)
Рис. 7.3. Упрощенная схема превращений ртути в воде (W. Eichler, 1993)
Содержание хлорида метилртути в рыбе, выловленной в загрязненной морской зоне, достигало 50 мг/кг, в креветках - 85 мг/кг. В результате употребления морских продуктов в общей сложности пострадало 17 тыс. человек, у 121 пострадавшего наблюдалось острое тяжелое отравление, 46 человек скончались. Всего с 1956 г. от отравления погибло 1022 человек. У собак, кошек, свиней, крыс и птиц, обитавших вблизи залива, развились классические клинические симптомы отравления, и многие из этих животных погибли.
У пострадавших отмечались нарушения координации движений, слабость и тремор, замедление и неясность речи, атаксия, ухудшение зрения и слуха. Эти симптомы постепенно усиливались, и в дальнейшем к ним присоединялись общий паралич, деформация конечностей, затруднение глотания, конвульсии. При тяжелом отравлении наступала смерть. Врожденная болезнь Минамата по клинической картине сходна с детским церебральным параличом. Только спустя 40 лет рыба и моллюски в заливе Минамата были признаны безопасными для здоровья.
С воздействием полихлорированных бифенилов (ПХБ) связано развитие таких заболеваний, как болезнь Юшо (Япония, 1968) или болезнь
Ю- Ченг (Ю-Уенг, болезнь рисового масла, о. Тайвань, 1979). В Японии воздействию подверглось 1800 человек, употреблявших в пищу рис, загрязненный трансформаторным маслом. У пострадавших наблюдалось только развитие хлоракне.
Общее число лиц, подвергнутых воздействию на о. Тайвань, составило около 2000 человек. Поражение населения было вызвано употреблением в пищу загрязненного Канехлором-400 рисового масла с концентрацией 2000-3000 мг/кг. ПХБ, использовавшиеся в качестве теплопроводного материала, попали в продукт при производстве рисового масла через мельчайшие отверстия в трубах. Ранними признаками заболевания были: увеличение и гиперсекреция мейбомиевых желез глаз, набухание век, пигментация ногтей и слизистых оболочек, слабость, тошнота, рвота. Затем обычно развивался гиперкератоз и потемнение кожи с увеличением кожных фолликулов и появлением угреподобной сыпи (хлоракне), часто осложнявшихся вторичной стафилококковой инфекцией. Дети, родившиеся у матерей с болезнью Юшо, отставали от сверстников в физическом развитии. Нейротоксическое действие на плод проявилось у родившихся детей в снижении интеллекта, гиперактивности, нарушениях поведения.
ПХБ, а также полибромированные бифенилы обладают канцерогенным действием и оказывают влияние на репродуктивную функцию. Период выведения ПХБ из организма составляет 58 лет. ПХБ могут переходить через плацентарный барьер, а также поступать в организм ребенка с материнским молоком.
Отравления нитратами, нитритами и нитрозаминами возникают при поступлении этих ксенобиотиков с пищевыми продуктами в значительных количествах. Источниками пищевых нитратов являются преимущественно продукты растениеводства. Животные продукты (мясо, молоко) содержат их в незначительном количестве. Нитраты при участии нормальной микрофлоры кишечника и ферментов восстанавливаются до нитритов. Нитраты и нитриты при хроническом поступлении в больших количествах приводят к образованию метгемоглобина, в результате чего может развиться хроническая алиментарная нитратно-нитритная метгемоглобинемия.
Нитриты (в частности, нитрит натрия) широко используются при консервировании мяса, производстве колбас и деликатесных продуктов, а также рыбных консервов для улучшения потребительских свойств продукта, придания специфических «ветчинных» аромата и вкуса и повышения стойкости продукта при хранении.
Большие абсорбированные дозы нитратов или нитритов приводят к появлению симптомов интоксикации. Через 4-6 ч появляются тошнота, рвота, признаки кислородного голодания (одышка, синюшность слизистых оболочек и кожных покровов), понос. Все это сопровождается слабостью, болями в затылочной области, сердцебиением.
Нитрозамины в отличие от нитритов и нитратов обладают выраженной канцерогенной активностью.
Пищевые добавки, классификация, требования к применению в производстве пищевых продуктов
В настоящее время на продовольственном рынке России резко возрос ассортимент пищевых продуктов с пищевыми добавками или собственно пищевых добавок. Согласно определению ВОЗ, пищевые добавки - это природные соединения и химические вещества, которые сами по себе обычно не употребляются в пищу, но в ограниченных количествах преднамеренно вводятся в продовольственные товары на различных этапах производства, хранения и транспортировки для придания товарам заданных свойств, повышения стойкости продуктов к различным видам порчи, сохранения структуры, внешнего вида и т.д. Пищевые добавки могут находиться в продуктах полностью или частично в неизменном виде или в виде веществ, образующихся в результате химического взаимодействия добавок с компонентами пищевых продуктов.
В разных странах используются около 500 пищевых добавок, не считая разновидностей, комбинированных добавок, отдельных душистых веществ и ароматизаторов. На упаковке большинства пищевых продуктов стоят буквенные и цифровые индексы, которые и обозначают пищевые добавки.
Разрешение на применение добавок выдается специализированной международной организацией - Объединенным комитетом экспертов ФАО/ВОЗ по пищевым добавкам и контаминантам. Комиссией «Кодекс алиментариус» закодированы все пищевые добавки в виде Международной цифровой системы (International Numbering System - INS). В странах Европейского сообщества используется региональная система цифровой кодификации с литерой «Е».
Согласно этой системе каждой пищевой добавке присвоен цифровой код из 3 или 4 цифр с предшествующей литерой «E». Коды, или идентификационные номера используются только в сочетании с названиями функциональных классов, отражающих группиров-
ку пищевых добавок по технологическим функциям (подклассам). Например, аскорбиновая кислота может быть обозначена на этикетке продукта как «антиокислитель E300», а изоаскорбиновая кислота - как «антиокислитель E315».
В некоторых случаях после индекса может стоять некоторая величина, например 50 ppm, которая обозначает, что на 1 млн массовых или объемных частей продукта приходится не более 50 частей пищевой добавки (ppm - part per million). В целом пищевая добавка в продукте, согласно «Кодекс алиментариус», будет поступать в организм человека в соответствии с максимально допустимым количеством вещества для животных, уменьшенным по отношению к человеку в
100, 500 и даже в 1000 раз.
Согласно системе «Кодекс алиментариус», классификация пищевых добавок выглядит следующим образом:
• Е100 - Е182 - красители, применяемые для окраски пищевых товаров в различные цвета;
• Е200 и далее - консерванты, способствующие длительному хранению продуктов;
• Е300 и далее - антиокислители (антиоксиданты), замедляющие окисление и предотвращающие порчу. По действию схожи с консервантами;
• Е400 и далее - стабилизаторы, сохраняющие заданную консистенцию продукта;
• Е500 и далее - эмульгаторы, поддерживающие структуру продуктов. По действию схожи со стабилизаторами;
• Е600 и далее - усилители вкуса и аромата;
• Е700 - Е800 и далее - запасные индексы;
• Е900 и далее - антифламинги, противопенные вещества (понижают пену, например при розливе соков);
• Е1000 и далее - вновь формируемая группа, куда входят глазирующие вещества, подсластители, добавки, препятствующие слеживанию сахара, соли, для обработки муки, крахмала и др.
7.10. ГИГИЕНИЧЕСКИЕ ОСНОВЫ ЛЕЧЕБНОГО
И ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОГО ПИТАНИЯ
В основу диетотерапии положена концепция сбалансированного питания. Питание больного человека строится на основе данных о
физиологических потребностях в пищевых веществах и энергии здорового человека. В пропорции пищевых веществ вносятся коррективы, соответствующие особенностям патогенеза, клинического течения, стадии болезни и метаболических нарушений. Сочетание диетотерапии с фармакологической, с одной стороны, повышает эффективность лечения, а с другой - смягчает или предупреждает побочные действия лекарственных препаратов, которые при этих условиях дают нужный терапевтический эффект при меньших дозах. Считается, что под влиянием адекватной диеты происходит реадаптация ферментных систем. Лечебное питание является важным элементом вторичной профилактики, поскольку препятствует переходу начальных форм заболевания в хронические и способствует выздоровлению и реабилитации.
Лечебное питание используется при всех без исключения заболеваниях желудочно-кишечного тракта, болезнях обмена веществ, заболеваниях сердца, легких, печени, почек, опорно-двигательного аппарата и др. Нередко лечебное питание дает хорошие результаты в тех случаях, когда другие методы лечения неэффективны.
Успешное лечение в современном лечебном учреждении возможно при правильном сочетании диеты, соответствующей характеру и тяжести заболевания, и лечебных процедур (лекарственная терапия, физиотерапия, лучевая терапия). В лечебном питании применяются дополнительные операции при обработке продуктов, в том числе измельчение продукта, вплоть до полной гомогенизации, приготовление блюд на пару и запекание.
Технологическая обработка сырья при приготовлении рационов лечебного питания позволяет сохранить пищевую и биологическую ценность пищи. При различной термической обработке потери энергетической ценности и пищевых веществ существенно различаются. Потери белков и жиров в животных продуктах выше, чем в растительных. Потери минеральных веществ больше в 2 раза в продуктах животного происхождения, за исключением кальция, который при некоторых видах обработки рыбы и птицы частично переходит из костей в мясо. Витамины разрушаются при воздействии высокой температуры, что составляет не менее 50% всех потерь витаминов, а для аскорбиновой кислоты эта величина достигает 75%. Общие потери энергетической ценности составляют 10%.
Потери при варке зависят от способа термической обработки. Если варка производится без слива жидкости, то потери всех пищевых веществ минимальны: 2-5% белков, жиров, углеводов и минеральных
веществ. Потери витамина С достигают 60%, разрушается 10-15% витаминов группы В и β-каротина. Если отвар после приготовления большинства овощей и некоторых каш (рисовая), макаронных изделий сливают, потери белков, жиров, витаминов и минеральных веществ увеличиваются в 2-3 раза и приближаются к потерям при жарке.
В больничных учреждениях существуют 2 основные системы приготовления пищи: централизованная и децентрализованная. При централизованной системе пища готовится в пищеблоке и доставляется в лечебное отделение. При децентрализованной системе централизованно производится лишь заготовка полуфабрикатов, а в корпусах организуются доготовочные кухни.
Первым звеном централизованной системы является пищеблок. К пищеблоку относятся складские помещения, помещения для подготовки продуктов к кулинарной обработке, варочные цехи, раздаточные и ряд вспомогательных помещений. В крупных многопрофильных больницах пищеблок располагается в отдельном здании либо на верхних этажах корпусов. Размещение пищеблоков в подвальных помещениях и на первых этажах гигиенически нецелесообразно.
Второе звено - транспортировка готовой пищи и сухих продуктов из пищеблока по палатным отделениям и далее по палатам, сбор и мытье использованной посуды и доставка ее в пищеблок.
Преимущества централизованной системы заключаются в возможности применять высокопроизводительное технологическое оборудование и в улучшении контроля со стороны диетврачей и диетсестер. Недостатками централизованной системы являются удлинение путей транспортирования пищи в палатные отделения, увеличение времени доставки пищи.
Для приготовления высококачественного диетического питания и профилактики пищевых инфекций и отравлений на пищеблоке предусматриваются:
• полный набор помещений и оборудования цехов;
• рациональная планировка помещений;
• недопущение встречных или пересекающихся «чистых» и «грязных» процессов (сырых и готовых продуктов, чистой и грязной посуды);
• обязательная маркировка всего оборудования пищеблока и использование этого оборудования в строгом соответствии с маркировкой;
• соблюдение технологического режима тепловой обработки продуктов, особенно мяса и рыбы;
• соблюдение правил хранения продуктов и сроков реализации пищи;
• строгое соблюдение персоналом правил личной гигиены;
• соблюдение санитарного режима работы пищеблока с обеспечением тщательного мытья посуды и рабочих поверхностей, рук и оборудования с применением дезинфицирующих и моющих средств.
Качество готовых блюд (бракераж) оценивается во время опробования пищи, которое производит дежурный врач в присутствии повара и медицинской сестры по диетпитанию непосредственно перед выдачей готовой пищи в отделение. При этом оценивается:
• правильность выбора блюд на диеты (сопоставление с меню-порционником и семидневным меню);
• органолептические свойства готовых блюд (готовность, вкус, доброкачественность);
• температура блюд при раздаче;
• соответствие выхода готовых блюд расчетным данным (при раздаче порционных мясных и рыбных блюд во время взвешивания 5-10 порций допускается отклонение не более ± 3%);
• санитарное состояние пищеблока.
В зависимости от качества приготовленных блюд в бракеражном журнале ставится оценка: «отлично» - блюдо приготовлено вкусно, соответствует диете, красиво оформлено; «хорошо» - блюдо соответствует рецептуре и диете, но имеет некоторые устранимые дефекты, например недосолено; «удовлетворительно» - блюдо имеет существенные отклонения от требований кулинарии; «неудовлетворительно», когда блюдо имеет низкие вкусовые качества, несвойственные запах и вкус, значительный пересол, недоварено или недожарено, подгорело и т.п.
Существенным дефектом, заставляющим признать блюдо «неудовлетворительным», является несоответствие его диете. Например, образование зажаренной корочки на котлетах при диете ? 2 (хронический гастрит с секреторной недостаточностью) или использование соли в блюдах диет ? 7 и 10 (диета ? 7 - острый нефрит в период выздоровления, хронический нефрит вне обострения и недостаточности почек; диета ? 10 - заболевания сердечно-сосудистой системы с недостаточностью кровообращения I-IIA степени).
Одновременно со снятием пробы отбирают образцы всех блюд, которые сохраняют до следующего дня в чистой отдельной посуде в холодильном шкафу, запертом на замок (суточная проба). В случае возникновения
пищевого отравления в лечебном учреждении отобранные продукты суточной пробы отправляют в лабораторию для исследования.
Непосредственно перед раздачей пищи в больницах осуществляется С-витаминизация готовой пищи, которую при централизованной системе питания проводит медицинская сестра по диетпитанию, а при децентрализованной системе - старшие медицинские сестры отделений. Сведения о проведенной С-витаминизации заносятся в меню-раскладку или специальный журнал.
В раздаточных отделениях пища не должна храниться более 2 ч (овощные блюда - более 1 ч), исключая время, затраченное на перевозку.
Медицинские осмотры, обследования и личная гигиена персонала пищеблока являются важными противоэпидемическими мероприятиями. Лица, поступающие на работу в пищеблок, обязаны пройти медицинский осмотр в лечебно-профилактических учреждениях по месту жительства у терапевта, дерматовенеролога, обследование на бактерионосительство, гельминтоносительство, на венерические и заразные кожные заболевания. В дальнейшем медицинский осмотр проводится ежеквартально, а обследование на бактерио- и глистоносительство - по эпидемиологическим показаниям в зависимости от анализа эпидемиологом заболеваемости инфекционными и паразитарными заболеваниями на обслуживаемой территории и санитарно-гигиенического состояния пищеблока, оцениваемого врачом по гигиене питания учреждения Роспотребнадзора.
Не допускаются к работе лица, переболевшие брюшным тифом, паратифом, дизентерией и оказавшиеся носителями этих инфекций, а также больные активной формой туберкулеза легких и внелегочными формами туберкулеза (костей, суставов и т.д.), имеющие гнойничковые заболевания кожи. Отстраняются от работы и те лица, которые проживают совместно с заболевшими (болеющими) острыми кишечными инфекционными заболеваниями до окончания проведения специальных мероприятий в квартирах и предоставления справки из территориальной организации Роспотребнадзора.
Временно отстраняются от работы с готовыми продуктами лица, страдающие ангинами, гнойничковыми заболеваниями кожи, с порезами и нагноившимися ожогами. Для выявления лиц с гнойничковыми заболеваниями необходимо ежедневно перед работой проверять руки персонала; о результатах проверки и принятых мерах делается соответствующая запись в журнале осмотров на наличие гнойничковых заболеваний.
Факторы риска возникновения пищевых отравлений и кишечных инфекций на пищеблоке представлены в табл. 7.13.
Таблица 7.13. Санитарно-эпидемические факторы риска в общественном питании (Ванханен В.Д., Лебедева Е.А.)
Фактор риска | Оценочный коэффициент, балл |
Нарушение правил транспортировки продуктов | |
Отсутствие в накладных сведений о сроках изготовления и реализации скоропортящихся продуктов | |
Отсутствие клейма на мясных тушах, заключения ветеринарного надзора | |
Использование сомнительных по качеству продуктов | |
Нарушение порядка реализации нестандартных продуктов | |
Нарушение температурных условий хранения, сроков реализации и товарного соседства продуктов | 5 |
Нарушение правил холодной и тепловой обработки продуктов | 5 |
Нарушение поточности обработки продуктов в пространстве и во времени | 5 |
Нарушение технологических схем кулинарной обработки продуктов | 10 |
Нарушение сроков реализации готовых блюд | 20 |
Несоблюдение температурного режима блюд при раздаче | 10 |
Нарушение сроков реализации и температурных условий хранения буфетной продукции | 20 |
Несоблюдение санитарных правил содержания территории | 1 |
Несоответствие планировки предприятия и оборудования санитарным нормам и правилам | 2 |
Нарушение правил содержания помещений предприятия | 2 |
Несоблюдение санитарных требований к технологическому оборудованию, инвентарю и посуде | 3 |
Наличие на предприятии тараканов, мух, грызунов | 2 |
Невыполнение правил личной и производственной гигиены | 4 |
Несвоевременное проведение медицинских осмотров и профилактических обследований, прививок; выявление больных и лиц, имеющих в семье (квартире) больных кишечными инфекциями | 6 |
Лечебно-профилактическое питание назначается рабочим, имеющим профессиональный контакт с вредными физическими или химическими факторами. Питание предназначено для здоровых людей трудоспособного возраста и поэтому основывается на принципах рационального питания с учетом особенностей обмена ксенобиотиков и роли отдельных компонентов пищи, оказывающих защитный эффект. Химический состав пищи способствует уменьшению вредного действия ксенобиотиков или продуктов их метаболизма. Это задержка абсорбции вредных веществ из желудочно-кишечного тракта, ускорение выведения из организма ксенобиотиков или продуктов их метаболизма, повышение общей резистентности, защита отдельных систем от вредного действия токсичных веществ.
Превращение ксенобиотиков в организме осуществляется путем метаболической трансформации и конъюгацией. К метаболической трансформации относятся все процессы превращения ксенобиотиков: окисление, восстановление, гидролиз, отщепление химических групп от их молекулы. В биотрансформации участвуют многие ферменты, из которых главная роль принадлежит микросомальным ферментам эндоплазматической сети клеток, в первую очередь гепатоцитов.
Конъюгация представляет собой биосинтетический процесс, в котором ксенобиотики или их метаболиты, образовавшиеся при метаболической трансформации, соединяются с легко доступными эндогенными субстратами: глюкуроновой кислотой, глутатионом, аминокислотами, ацетильными и метильными группами, сульфатом и др.
При метаболической трансформации и конъюгации ксенобиотики превращаются в более полярные и более растворимые метаболиты и конъюгаты, что способствует их более быстрому и полному выведению из организма экскреторными системами (преимущественно с мочой и желчью).
При функциональной недостаточности механизмов обезвреживания активные промежуточные метаболиты ксенобиотиков могут вступать во взаимодействие с молекулами клетки-мишени (белки, РНК, ДНК, липиды), приводя к образованию свободных радикалов эндогенных молекул и проявлению гепатотоксического, нефротоксического, мутагенного, сенсибилизирующего, тератогенного, канцерогенного действия. Рационы лечебно-профилактического питания - см. главу «Гигиена труда» и приложение к главе 7 учебника на электронном носителе.