Клиническая фармакокинетика: теоретические, прикладные и аналитические аспекты: руководство / Под ред. В.Г. Кукеса. - 2009. - 432 с
|
|
|
|
ГЛАВА 15 ПРИКЛАДНЫЕ АСПЕКТЫ ФАРМАКОКИНЕТИКИ ВИТАМИНОВ
Е.В. Ших
Молекулярные механизмы абсорбции водорастворимых витаминов
В последнее время изучен молекулярный механизм абсорбции и распределения ряда водорастворимых витаминов. Показана роль транспортёров в абсорбции и распределении некоторых водорастворимых витаминов. Изучена так же регуляция этого процесса на генном уровне.
Аскорбиновая кислота
Сайты абсорбции аскорбата были обнаружены на всем протяжении тонкого кишечника. Абсорбция аскорбата осуществляется при помощи Na+/аскорбатного котран- спортёра. Это пример вторично активного транспорта, так как захват аскорбата осуществляется по градиенту концентрации Na+, который поддерживается работой Na+-/К+-АТФазы. На перемещение 2 ионов Na+ приходится 1 аскорбат-анион, таким образом, электрохимический градиент натрия создаёт энергию, необходимую для захвата аскорбат-аниона.
Известно, что большие дозы аскорбата абсорбируются не полностью, в отличие от малого количества вещества, вероятно, это связано с ограниченной способностью энтероцитов к использованию Na+/аскорбатного котранспортёра. Многие исследователи отмечают снижение абсорбции аскорбата при взаимодействии с некоторыми пищевыми продуктами и ЛС. По-видимому, гипергликемия может снижать биодоступность аскорбата, из-за снижения кишечной абсорбции. Такие результаты были получены in vitro.
Na+/аскорбатный котранспортёр обладает стереоселективностью, более высокую его аффинность наблюдали по отношению к L-аскор- бату, чем к D-аскорбату.
Были клонированы 2 изоформы Na/аскорбатного котранспортёра: SVCT1 и SVCT2, закодированные в генах SLC23a1 и SLC23a2 соответственно. SVCT1 и SVCT2 обладают значительно большей субстратной специфичностью к L-аскорбату, чем к D-изоаскорбату.
У людей старшего возраста выявлена более низкая экспрессия SVCT, вследствие чего отмечают ухудшение клеточной способности к захвату аскорбата с возрастом.
Контроль Na/аскорбатного котранспорта может осуществляться путём посттрансляционных модификаций и перераспределения SVCT-белков.
Биотин
Na-зависимый мультивитаминный транспортёр (SMVT), с одинаковой аффинностью участвует в переносе биотина, пантотеновой, липоевой кислот. Предполагают, что SMVT содержат 2 сайта фосфорилирования протеинкиназы C, по-видимому, участвующих в регуляции захвата биотина. Были клонированы и изучены 5'-регулятор- ные отрезки SMVT-гена. Несмотря на важную роль SMVT в переносе биотина, накоплены данные, что есть иные транспортёры витамина. Захват биотина лимфоидными клетками человека осуществляет монокарбоксилатный транспортёр 1 (MCT1).
Фолаты
Доказано, что кишечная абсорбция фолата регулируется внеклеточным уровнем субстрата, внутриклеточной протеинкиназой и онтогенетически. Пищевой дефицит фолиевой кислоты ведёт к значительному повышению транспорта фолата с помощью переносчиков. Этот процесс осуществляется через увеличение Vmax транспорта фолата и параллельным повышением уровня кишечного RFC-проте-
ина и РНК. Последние данные позволяют предполагать участие механизмов регуляции транскрипции в повышении транспорта фолата. У человека промотор B, по-видимому, управляет экспрессией варианта I, основной формой hRFC кишечника. Учёными идентифицированы молекулярные детерминанты, ответственные за экспрессию hRFC в плазматических мембранах, а так же механизмы распределения белков-переносчиков на клеточной поверхности.
Тиамин
Исследования молекулярной природы транспортной системы тиамина в кишечнике позволили клонировать 2 транспортёра SLC19A2 и SLC19A3. Данные транспортёры тиамина разделяют друг от друга на 48% - по идентичности и 64% - по сходству. Их также различают на 40 и 39% по идентичности уровня аминокислот с hRFC соответственно. По данным ряда исследователей, SLC19A2 и SLC19A3 не транспортируют фолат, а hRFC не участвует в переносе тиамина.
Тиамин-зависимая мегалобластная анемия (синдром Роджерса) - аутосомно-рецессивное заболевание со следующими клиническими проявлениями: мегалобластная анемия, нейросенсорная тугоухость и сахарный диабет. В настоящее время считают, что причина тиаминзависимой мегалобластной анемии - генетический дефект недавно клонированного транспортёра тиамина SLC19A2.
Открытие большого числа транспортёров витаминов позволяет осуществлять научные исследования в направлении поиска мутаций этих переносчиков, объясняя наследственно обусловленную мальабсорбцию некоторых витаминов, а так же открывая пути её коррекции и возможность изучения различных видов взаимодействия витаминов, макро- и микроэлементов в организме.
Фармакокинетика витаминов
Витамин B1
Витамин В1 (тиамин) хорошо всасывается в кишечнике и проникает в кишечный эпителиоцит при помощи переносчика путём активного транспорта, а при больших дозах всасывается путём диффузии. Определённое количество витамина циркулирует из эпителиальных клеток тонкой кишки в её полость и обратно.
Через 15 мин тиамин обнаруживают в плазме крови, а через 30 мин - в тканях. Витамин накапливается в мозге, сердце, почках,
надпочечниках, печени, скелетных мышцах. Около 50% всего тиамина в организме содержится в мышечной ткани. Максимальную концентрацию при приёме внутрь тиамин достигает приблизительно через 1,5 ч как при использовании в виде монопрепарата, так и в составе витаминных комплексов. Значения максимальной концентрации тиамина приблизительно равны в обоих случаях. При приёме тиамина в той же дозе в составе витаминоминерального комплекса максимальная концентрация существенно ниже. Аналогичные данные получены и для AUC тиамина.
При приёме внутрь из витаминоминерального комплекса всасывается значительно меньше витамина В1, чем при его приёме в той же дозе в виде монопрепарата или поливитаминного комплекса (табл. 15-1). В печени витамин В1 превращается в активные метаболиты - дифосфо- и трифосфотиамин. Элиминация тиамина осуществляется за счёт метаболизма в печени со средней скоростью 1 мг в сутки. Период полувыведения эндогенного тиамина составляет 9-18 сут. Период полувыведения тиамина при приёме его в виде витаминных препаратов колеблется от 4 до 5,5 ч.
В связи с введением в настоящее время понятия «профилактические и терапевтические дозы» для витаминов представляет интерес исследование фармакокинетических параметров НД, сопоставление их с количеством выводимого витамина для определения наиболее оптимальной дозы.
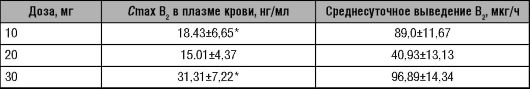
При приёме здоровыми добровольцами 10 мг тиамина однократно Cmax определяли через 2 ч после начала исследования, она составила 33,63±6,2. При приёме 20 мг тиамина однократно здоровыми добровольцами Cmax при определении её через 2 ч после приёма препарата составила 39,73±4,7 нг/мл. При однократном приёме здоровыми добровольцами 30 мг тиамина Cmax составило 56,63±13,6 нг/мл и также определялось через 2 ч от начала исследования.
Таким образом, увеличение дозы принимаемого витамина В1 (тиамина) коррелирует с величиной значения максимальной концентрации его в плазме крови. Коэффициент корреляции составил 0,96.
Увеличение принимаемой дозы тиамина приводит к статистически достоверному увеличению его среднесуточной экскреции. При этом существует прямая корреляционная зависимость между дозой принятого тиамина и величиной его среднесуточной экскреции с мочой (r=0,93). Приём НД тиамина приводит также к возрастанию выведения рибофлавина с мочой в течение суток.
Таблица 15-1. Показатели значения максимальной концентрации и среднесуточной экскреции тиамина при однократном приёме в нагрузочных дозах здоровыми добровольцами
 Известно,
что биодоступность назначенных внутрь водорастворимых солей тиамина
ниже, по сравнению с жирорастворимыми аналогами. В 1954 году была
открыта группа жирорастворимых дериватов тиамина, с соответствующим
названием «аллитиамины», поскольку они в натуральном виде содержатся в
овощах семейства Allium - в чесноке, луке, луке-порее и т.д.
Среди этих веществ бенфотиамин обладает наиболее выраженной клинической
эффективностью и хорошей переносимостью.
Известно,
что биодоступность назначенных внутрь водорастворимых солей тиамина
ниже, по сравнению с жирорастворимыми аналогами. В 1954 году была
открыта группа жирорастворимых дериватов тиамина, с соответствующим
названием «аллитиамины», поскольку они в натуральном виде содержатся в
овощах семейства Allium - в чесноке, луке, луке-порее и т.д.
Среди этих веществ бенфотиамин обладает наиболее выраженной клинической
эффективностью и хорошей переносимостью.
В отличие от тиамина, структура бенфотиамина имеет открытое тиазоловое кольцо, которое закрывается при абсорбции, продуцируя биологически активный тиамин. Фармакокинетические исследования показали, что абсорбция бенфотиамина значительно превышает абсорбцию водорастворимых солей тиамина, при этом практически во всех точках фармакокинетической кривой концентрация при при- ёме бенфотиамина выше концентрации при приёме соответствующей дозы тиамина. Бенфотиамин абсорбируется путём пассивной диффузии через слизистую кишечника и быстро превращается в биологически активный тиамин. Пиковая концентрация тиамина в плазме после назначения бенфотиамина внутрь в 5 раз выше, чем при приёме водорастворимых солей тиамина. Период полувыведения бенфотиамина такой же, как и у солей тиамина, однако биодоступность бенфотиамина примерно в 3 раза выше, чем при приёме солей тиамина.
Витамин B6
Все три формы витамина В6 (пиридоксин, пиридоксаль и пиридоксамин) легко всасываются путём простой диффузии в желудочно-кишечном тракте. В крови происходит неферментативное превращение пиридоксина в пиридоксамин, после чего образуется часть конечного продукта обмена - 4-пиридоксиловая кислота. В тканях пиридоксин превращается путём фосфорилирования в пиридоксинфосфат, пиридоксальфосфат и пиридоксаминфосфат. Конечные
продукты превращения пиридоксаля - 4-пиридоксиловая и 5-фос- фопиридоксиловая кислоты. Оба эти продукта выделяются с мочой. Использование для перорального приёма комплексов витамина В6 с другими витаминами у добровольцев не приводит к уменьшению максимальной концентрации и площади под кривой концентрация - время. Использование для перорального приёма комплексов витамина В6 с другими витаминами в сочетании с добавлением макро- и микроэлементов у добровольцев приводит к уменьшению максимальной концентрации и AUC. Время достижения максимальной концентрации при приёме витамина В6 в составе комплексов несколько больше, чем при приёме его в той же дозе в виде монопрепарата (табл. 15-2). Наибольшие концентрации витамина обнаруживают в печени, миокарде, которые, по-видимому, представляют собой его депо, также достаточно много витамина В6 в почках.
Витамин В2
Витамин В2 из кишечника всасывается путём активного транспорта в проксимальной части тонкой кишки. В связи с тем, что в пище этот витамин находится в фосфорилированном состоянии и связан с белками, для всасывания в кишке он должен расщепиться и дефосфорилироваться. Применение синтетического рибофлавина внутрь в избыточных дозах не ведёт к увеличению его всасывания, однако содержание свободного витамина в жёлчи и просвете кишки возрастает. Рибофлавин подвергается в организме энтерогепатической циркуляции. Наибольшее количество рибофлавина обнаруживают в миокарде, печени, почках, мозге. На величину параметров, характеризующих всасывание витамина В2, не влияет состав витаминного препарата. Использование для перорального приёма витаминоминеральных и поливитаминных комплексов не приводит к уменьшению максимальной концентрации и площади под кривой «концентрациявремя». Метаболизм начинается в стенке кишечника, где витамин В2 подвергается фосфорилированию. Затем в печени образуется рибоф- лавин-5'-монофосфат, после чего - флавинадениндинуклеотид. За сутки выделяется с мочой около 10% принятой дозы, остальная часть подвергается канальцевой реабсорбции. Фармакокинетические параметры представлены в (табл. 15-2). Изучение фармакокинетических параметров НД рибофлавина (10 и 20 мг) при однократном приёме волонтерами не выявило статистически достоверного отличия в величине значения максимальной концентрации рибофлавина в плазме крови. При приёме рибофлавина в дозе 30 мг величина Cmax статис-
тически достоверно превышает эту величину в случае его приёма в дозах 10 и 20 мг.
Таблица 15-2. Показатели значения максимальной концентрации и среднесуточной экскреции тиамина при однократном приёме в нагрузочных дозах здоровыми добровольцами
 Витамин C
Витамин C
Витамин C (аскорбиновая кислота) всасывается в тонкой кишке. Время достижения максимальной концентрации витамина С в плазме крови, по данным различных авторов, колеблется от 1,5 до 4 ч, при этом большие значения соответствуют исследованиям с приёмом аскорбиновой кислоты в составе комплексных препаратов. Рядом авторов установлено, что всасывание витамина C зависит от количества компонентов в препарате: чем меньше компонентов, тем лучше всасывание. Назначение аскорбиновой кислоты в лечебных целях требует коррекции режима дозирования в сторону увеличения дозы при использовании многокомпонентных лекарственных форм. Для насыщения тканей требуется превращение кислоты в дегидроаскорбиновую форму, которая легко проникает через мембраны энтероцита без затрат энергии. В клетках дегидроаскорбиновая кислота быстро восстанавливается, превращаясь вновь в аскорбиновую кислоту при участии тиоловых и дисульфидных групп. Витамин C избирательно накапливается в задней доле гипофиза и надпочечниках. Метаболизируется он главным образом в печени, преобразуясь в дезоксиаскорбиновую и дикетогулоновую кислоты. Последняя превращается затем в щавелево-уксусную кислоту. Метаболиты аскорбиновой кислоты выделяются почками. Скорость метаболизма аскорбиновой кислоты - 5-20 мг в сутки. При приёме аскорбиновой кислоты в сверхвысоких дозах она сразу выводится почками в неизменённом виде.
Витамин E
Свойствами витамина E обладают 8 различных токоферолов естественного происхождения. Из кишечника всасывается приблизительно половина витамина E, принятого с пищей. Его абсорбция требует
присутствия жирных кислот. Витамин E проникает в кровь через лимфу, связываясь сначала с хиломикронами, а затем с β-липопротеинами плазмы крови. Приблизительно 3/4 выводимого из организма витамина (α-токоферола) экскретируется в жёлчь, а остальное количество - в мочу в виде глюкуронидов. Основным путём выведения из организма γ-токоферола - выделение с мочой в виде конъюгированного глюкуронида. Депонируется витамин в гипофизе, семенниках, надпочечниках и ряде других органов. Имеются данные, указывающие на то, что биодоступность натурального витамина E против искусственного токоферола составляет 1,36.
Имеющаяся в литературе информация по фармакокинетическим параметрам витаминов ограничена данными о путях биотрансформации и выведения витаминов, о месте основного депонирования, о времени достижения максимальной концентрации и имеет отношение исключительно к монопрепаратам витаминов.
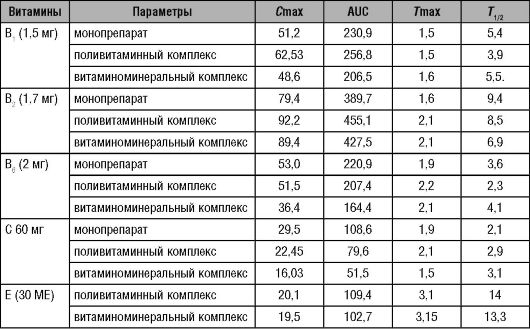
Учитывая тенденцию последнего времени, - назначение преимущественно многокомпонентных или витаминоминеральных комплексов, в табл. 15-3 приведены данные по фармакокинетике витаминов B1, B2, B6, C, E при приёме их в одинаковой дозе в виде монопрепарата, поливитаминного комплекса и витаминоминерального комплекса.
Таблица 15-3. Фармакокинетические параметры витаминов
 Витамин B12
Витамин B12
Витамин В12 (цианкобаламин) - единственный водорастворимый витамин, обладающий способностью к кумуляции, в связи с чем достаточно высок риск развития передозировки при использовании его как в виде монопрепарата, так и в составе различных комплексов.
Сложная пространственная конфигурация молекулы цианкобаламина делает её абсорбцию одной из наиболее сложных среди аналогичных процессов в пищеварительном тракте. Для успешного всасывания B12 требуется присутствие и адекватное функционирование микрофлоры пищеварительного тракта, двух специфических рецепторов и двух трансмембранных транспортёров.
В связи с исключительно низкой биодоступностью, в лечебных целях используют лекарственные формы цианкобаламина в инъекциях. Инъекционный путь введения обладает целым рядом недостатков, а в некоторых случаях его применить невозможно. Затруднено также использование лечения инъекционными препаратами в амбулаторных условиях. С другой стороны, патологические состояния, обусловленные дефицитом витамина В12, требуют длительной курсовой терапии и, практически, пожизненного поддерживающего лечения.
В связи с этим во всем мире достаточно высок интерес к фармакокинетическим исследованиям биодоступности цианкобаламина при альтернативных путях введения.
Введение цианкобаламина ректально мелким и крупным лабораторным животным показало достаточно высокую степень его всасывания при данном способе введения.
При сравнении фармакокинетических параметров, полученных при введении однократно, равной дозы цианкобаламина 18 здоровым добровольцам, в виде внутримышечной инъекции и ректально в той же дозе, установлено, что величина значения максимальной концентрации при ректальном введении в 1,98 раза превысила величину значения максимальной концентрации цианкобаламина при внутримышечном введении и составила соответственно 12120±840,3 и 6098,9±708,5 пг/мл. Площадь под кривой «концентрация-время» при ректальном введении также статистически достоверно превышает аналогичный показатель при внутримышечном введении: для AUC0-t эти показатели составили соответственно 29187+2451,3 и 16122+922,4 пгхч/мл; для AUC0-00, соответственно 141430+10674,2 и 55246,09+834,5 пгхчхмл.
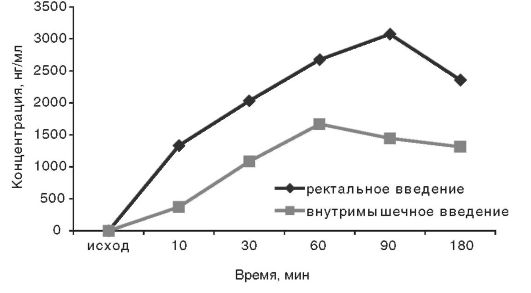 Рис. 15-1 Сравнительная
динамика изменения концентрации цианкобаламина при внутримышечном и
ректальном введении в равной дозе одним и тем же добровольцам
Рис. 15-1 Сравнительная
динамика изменения концентрации цианкобаламина при внутримышечном и
ректальном введении в равной дозе одним и тем же добровольцам
Время достижения максимальной концентрации соответственно составило 1,5+0,1 и 1,0+0,05 ч при ректальном и внутримышечном введении. Период полувыведения при ректальном введении статистически достоверно превышает период полувыведения при парентеральном применении: 8,6+1,1 и 5,6+0,9 ч.
Относительная биодоступность цианкобаламина при ректальном введении по отношению к парентеральному составила 181%.
Таблица 15-4. Фармакокинетические параметры цианкобаламина при ректальном и внутримышечном введении добровольцам
 *
Полученное значение при ректальном пути введения статистически
достоверно отличается от полученного значения при парентеральном
введении той
*
Полученное значение при ректальном пути введения статистически
достоверно отличается от полученного значения при парентеральном
введении той
же дозы.
MRT, ч - среднее время удержания препарата в организме, ч.
Литература
Конюхова О.С. Роль магния и витаминов группы B в лечении хронической сердечной недостаточности: Автореф. дис. ... канд. мед. наук. - М., 2007.
Моргунова Л.А. Фармакокинетика, фармакодинамика и клиническая эффективность новой лекарственной формы витамина В12: Автореф. дис. . канд. мед. наук. - М., 2006.
Ших Е.В. Витаминный статус и его восстановление с помощью фармакологической коррекции витаминными препаратами: Дис. ... д-ра мед. наук. - М., 2002.
Ших Е.В., Красных Л.М., Хашан И., Демидова О.А. Методика определения водорастворимых витаминов в таблетках // Материалы итоговой научной работы Института Клинической фармакологии ФГУ НЦ ЭСМП за 2000. - С. 36.
Ших Е.В., Раменская Г.В., Хашан И., Линквист А.Ю. Использование высокоэффективной жидкостной хроматографии (ВЖЭХ) для совместного определения витаминов А, Е и D3 в плазме крови: Тезисы Х национального конгресса «Человек и лекарство». - С. 465.
Amin M., Reusch J. High-performance Liquid Chromatography of watersoluble Vitamins. // Analyst. - 1987. - Vol. 112. - ? 7. - P. 989-991.
Dawson E.B., Evans D.R., Conway M.E., McGanity W.J. Vitamin B12 and folate bioavailability from two prenatal multivitamin/multimineral supplements // Am. J. Perinatol. - 2000. - Vol. 17. - ? 4. - P. 193-199.
Frank T., Bitsch R., Maiwald J. et al. Alteration of thiamine pharmacokinetics by end-stage renal disease // Int. J. Clin. Pharmacol. Ther. - 1999. -
Vol. 37. - ? 9. - P. 449-455.
Garcia-Arieta A., Torrado-Santiago S., Goya L., Torrado J.J. Spray-dried powders as nasal absorption enhancers of cyanocobalamin // Biol. Pharm. Bull. - 2001, Dec. - Vol. 24. - ? 12. - P. 1411-1416.
Levine M. New Concepts in the Biology and Biochemistry of Vitamin C // N. Engl. J. Med. - 1986. - Vol. 314. - P. 892-902.
Madigan S.M., Tracey F., Mc Nulty H. et al. Riboflavin and vitamin B6 intakes and status and biochemical response to riboflavin supplementation in free-living elderly people // Am. J. Clin. Nutr. - 1998 . - Vol. 68. - ? 2. - Р. 389-395.
Martin A., Janigian D., Shukitt H. B. et al. Effect of vitamin E intake on levels of vitamins E and C in the central nervous system and peripheral tissues: implications for health recommendations. // Brain. Res. - 1999. -
Vol. 845. - ? 1. - Р. 50-59.
Sampson D.A., OConner D.K. Analysis of B2 vitamins and pyridixic acid in plasma, tissues, and urine using HPLC // Nutr. Res. - 1989. - Vol. 9. -
Р. 259-263.
Shich E., Demidova O., Litvak N., Krasnyh L. The examination of watersoluble vitamins concentration in patients with chronic cardiovascular and respiratory disease: Abstracts of the joint meeting of 3rd Congress of the European Association for Clinical Pharmacology and Therapeutics //
Br. J. Clin. Pharmacol. - 1999. - Р. 438.